文档内容
年下学期高三期末质量检测化学
2024
参考答案、提示及评分细则
石油是不可再生能源 大力开采加速能源危机 不利于实现碳中和 应加快开发高效 洁净新能源
1.D , , , 、 .
选项乙炔的 键是极性键 共用电子对偏向 原子 通过头碰头形成 键 碳原子电子云密度大
2.C A C-Hσ , C , σ , ,
故 键示意图不对称 选项 的价电子对数为 故 模型为平面三角形 选项双分子膜是头向
σ ;B SO2 3, VSEPR ;D
外 尾向内的结构
, .
选项由于电负性 故氢键的键能 的沸点高于 是由于水分子中
3.A A F>O, :O-HO<F-HF,H2O HF
氢键的数目多于
HF.
选项工业中冶炼金属镁是电解熔融态的无水
4.B B MgCl2.
选项 醋酸为弱酸 离子方程式书写不能拆 而且弱酸电离是吸热的 小于强碱的中和热
-1
5.D A , , , , 57.3kJmol ;B
选项铅酸蓄电池的正极反应是 得电子 发生还原反应 选
2- + -
:PbO2+SO4 +4H +2e PbSO4+2H2O, , ;C
项苯酚钠与 的反应 产物都是 与 的用量无关 选项水解呈酸性 能溶解镁产生 故
-
CO2 , HCO3 , CO2 ;D , H2,
选
D.
选项实验室制 固体与固体加热制取气态 试管口应略向下倾斜 选项 与 在加热条件
6.B A NH3, , ;C Cl2 NaOH
下产生 不能制取 消毒液 选项用新制的 检验乙醛 应该往 的 溶
NaClO3, “84” ;D Cu(OH)2 , 2mL10% NaOH
液中滴加 滴 溶液
5 5%CuSO4 .
选项化合物 的分子式为 选项产物 是苯甲酸和水 选项 中含有酯基 酮羰基
7.B A F C10H10O4;C M、N ;D G 、 、
醚键和碳碳双键 种官能团 而且没有手性碳原子 故没有对映异构体
4 , , .
依据题意可知五种短周期元素 原子序数依次增大 是 元素 与 不在同一周期 故 是 元素
8.D , ,Y C 、X M , X H ,
核外未成对电子数为 则 是 元素 则 是 或者 元素 是 元素 选项 的 电子云更弥
1, M F , Z N O ,Q Al .A Y 2s
散 选项 与 形成的简单化合物是 与 形成的简单化合物是 或者 其键角 选
;B Y X CH4,Z X NH3 H2O, :Y>Z;C
项 与 形成的化合物是 或者 其中 离子键百分数是 离子键百分数是依据电负性差
Q Z AlN Al2O3, Al2O3 41%,
值计算的 故离子键百分数 低于 都小于
, AlN Al2O3, 50%.
选项氨水受热不稳定 不能采取高温条件 选项经过焙烧 滤渣主要成分是 选项灼烧
9.D A , ;B , Fe2O3、SiO2,C
固体 仪器应用坩埚 不用蒸发皿
, , .
依据装置图可知 极产生 为阴极 极为阳极 还原器中 和 在催化剂的作用下发
3- -
10.B :a H2, ,b , [Fe(CN)6] OH
催化剂
生反应释放出 其发生反应的离子方程式
3- - 4-
O2, :4[Fe(CN)6] +4OH 4[Fe(CN)6] +O2↑+
则 极中有大量的 流入还原器中参与反应 故为阴离子交换膜 选项依据得失电子守恒 装置
-
2H2O, b OH , ;D ,
中生成 时 外电路转移 电子
0.5molH2 , 1mol .
依据反应 的正反应是气体体积增大的反应 可知增大压
11.D :2CHCl3(g)+O2(g)2COCl2(g)+2HCl(g) ,
强平衡逆向移动 则 正确 T 时 平衡转化率b a 则b点对应的压强小 即体积V V
, C ;1℃ CHCl3(g) > , , 1> 2,A
正确 升高温度 平衡转化率下降 则平衡常数 K K K 项正确ab点 平衡转
; CHCl3(g) , : a = b < c,B ;、 CHCl3(g)
化率分别为 列三段法可得 达平衡时体系总物质的量na nb 依据阿伏
60%、70%, , :()=3.6mol,()=3.7mol,
加德罗定律的推论pV
=
nRT
,
体系气体压强之比pa
∶
pb
=36
V
1∶37
V
2,D
错误
,
符合题意
,
故选
D.
高三化学试题参考答案 第 页 共 页
【 1 ( 4 )】依据晶胞的结构可知 该储氢合金通过与 大量结合形成金属氢化物来储氢的 晶胞重复的结构单元
12.C , H2 ,
无缝并置排列 故与 原子最近且距离相等的 原子有 个 该晶胞中 之间相互连接形成的笼状结构
, La Ba 4 ; ,H
有 个面 选项根据均摊法计算可知 个 原子处于体心位置 原子处于上下底面棱心和z轴心 原子
14 ;D :1 Ba ,La ,
32
个数为 1 原子共 个 即一个晶胞的化学式为 则晶体的密度为5.94×10 -3
12× =3;H 40 , BaLa3H40, N a3 gcm .
4 A
选项氯水溶液中能氧化 的还可能是 不能说明溶液中还有 剩余 选项不知道两种溶液
13.D A KI HClO, Cl2 ;B
的浓度 测定溶液的 不能比较水解程度大小 选项苯酚与 溶液的显色反应 生成的产物不是紫色
, pH ;C FeCl3 ,
沉淀
.
根据两种酸的K 可知 没有加入氢氧化钠溶液 二氯乙酸电离出来的氢离子抑制了乙酸的电离 故乙酸的
14.C a , , ,
分布分数为 二氯乙酸的分布分数为 二氯乙酸根离子的分布分数为 加入氢氧化钠溶液与二
100%, 50%, 50%,
氯乙酸反应 二氯乙酸的分布分数下降 而二氯乙酸的分布分数增大 故 表示二氯乙酸根离子的分布分数
, , , Ⅱ ,A
项错误 由 点 可知 加入氢氧化钠溶液体积 得到c c - 那么也一
; a (10,98.7) , 10mL, (CH3COOH)= (CHCl2COO ),
c +c - c +c -
定有c - c 根据K (H )(CH3COO )K (H )(CHCl2COO )两式
(CH3COO )= (CHCl2COOH), a1= c 、 a2= c ,
(CH3COOH) (CHCl2COOH)
相乘得K K c2 + c + -1.8 -4.76 -3.28 其数量级为 -4 项错误 加入氢
a1 a2= (H ). (H )= 10 ×10 =1.0×10 , 10 ,B ;
氧化 钠 溶 液 体 积 时 根 据 物 料 守 恒 有c c - -1
10 mL , (CH3COOH)+ (CH3COO )=0.05molL ;
c c - -1c + -1 再根据电荷守恒c +
(CHCl2COOH)+ (CHCl2COO )=0.05molL ;(Na )=0.05molL , :(Na )+
c + c - c - c - 将c c - c + 代入电荷守
(H )= (OH )+ (CH3COO )+ (CHCl2COO ), (CH3COOH)+ (CH3COO )= (Na )
恒关系式可得c c + c - c - 项正确 若将c
:(CH3COOH)+ (H )= (OH )+ (CHCl2COO ),C ; (CHCl2COOH)+
c - c + 代入电荷守恒关系式可得c c + c - c -
(CHCl2COO )= (Na ) :(CHCl2COOH)+ (H )= (OH )+ (CH3COO );
二氯乙酸被氢氧化钠溶液完全中和 二氯乙酸根离子的分布分数没有变 故不考虑其水解 由 点可知
, , , b
c c - 故c + -4.76 溶液显酸性 即c + c - 根据电荷守恒
(CH3COOH)= (CH3COO ), (H )=10 , . (H )> (OH ), :
c + c - c - 故c + c c - 项错误
(Na )< (CH3COO )+ (CHCl2COO ), (Na )< (CH3COOH)+ (CHCl2COO ),D .
除特殊标注外 每空 分 共 分
15.( , 2 , 15 )
蒸发皿 分
(1) (1 )
或 写成 或 也给分
- -
(2)Na[Cr(OH)4] NaCrO2( [Cr(OH)4] CrO2 )
降低
2- 3+ -
(3)3H2O2+10CH3COOH+2CrO4 2Cr +10CH3COO +3O2↑+8H2O
2- 2+ +
(4)Cr2O7 +2Pb +H2O2PbCrO4↓+2H
滴入最后半滴 溶液蓝色褪去 且半分钟内不恢复 或者滴入最后半滴 溶液蓝色褪
(5)① Na2S2O3, , ( Na2S2O3,
去变为亮绿色 且半分钟内不复色
, )
②93.67 ③BC
【解析】 步骤 中若没有将 煮沸去除 则黄色溶液含 酸性条件下 在步骤 中 会发生
2-
(3) Ⅱ H2O2 , CrO4 , , Ⅲ H2O2
氧化还原反应 会导致铬酸铅
2- 3+ -
:3H2O2+10CH3COOH+2CrO4 2Cr +10CH3COO +3O2↑+8H2O,
的产率降低
.
依据测定的步骤 实验中 与足量的 发生氧化还原反应 关系式
(5)② :0.3000g PbCrO4 KI , :2PbCrO4~6KI~3I2,
生成的 再用 标准溶液滴定 反应的关系式 则计算 的纯度关系式
I2 Na2S2O3 , :I2~2Na2S2O3, PbCrO4 :PbCrO4
代入数据计算得 的纯度为
~3Na2S2O3, PbCrO4 93.67%.
导致测得 纯度数值偏低 即消耗的 溶液体积偏小 选项用 溶液酸化样
③ PbCrO4 , Na2S2O3 .A HNO3-NaCl
高三化学试题参考答案 第 页 共 页
【 2 ( 4 )】品溶液 则加入足量的 反应时 生成的 的量偏大 使测定结果偏高 选项滴定前有气泡 终点时气泡消
, KI , I2 , ;D ,
失 则实际消耗的 溶液体积偏大 导致测定结果偏高
, Na2S2O3 , .
除特殊标注外 每空 分 共 分
16.( , 2 , 14 )
分
1 2
(1)3d4s(1 )
少答且答对给 分 答错不给分
(2)TiO2、SiO2( 1 , )
少答且答对给 分 答错不给分
(3)65℃、2%( 1 , )
高温
(4)2Sc2(C2O4)3+3O22Sc2O3+12CO2
+ 分 + + - b 30-3 a
(5)ScF2 (1 ) ScF2 +3NH3H2OSc(OH)3+3NH4 +2F ×10
a
3
(6)
4
【解析】 原子序数为 位于周期表第四周期第 族 价层电子为
1 2
(1)Sc 21, ⅡB , 3d4s.
酸浸 过程中 不溶于盐酸 所以滤渣成分为
(2)“ ” TiO2、SiO2 , TiO2、SiO2.
根据流程 萃取 环节要将 溶液与目标元素 分离 萃取出的 元素越多越好 在 时
(3) ,“ ” FeCl3、AlCl3 Sc , Sc , 65℃
分离系数 最高 分离效果最佳 萃取剂浓度为 时 铁的萃取率最低 钪的萃取率又高 体系分相也比较
β
, , 2% , , ,
容易 所以选择条件最佳为
, 65℃、2%.
加入 时形成 经过草酸将沉淀转化为 达到富集目的 在焙烧时草酸根被氧
(4) NaOH Sc(OH)3, Sc2(C2O4)3 ,
高温
化成 发生反应
CO2, 2Sc2(C2O4)3+3O22Sc2O3+12CO2.
根据信息要求 浓度和图示横坐标 找到元素 主要存在方式为 若在氨水调 时 氨
- +
(5) F pH=5, Sc ScF2 ; pH ,
水过多 根据图像 变化 会转变成 发生反应
+ +
, pH ,ScF2 Sc(OH)3, :ScF2 +3NH3H2OSc(OH)3+
+ - 已知K b 图中 ac - a -14 K c 3+ c - 3
3NH4 +2F ; sp[Sc(OH)3]= , pH= ,(OH )=10 , sp[ScF3]= (Sc )× (F )=
b -4 3
×( a 10 -14 3 ) = b ×10 30-3 a .
(10 )
a
晶胞参数为a 与 最近距离为体对角线的1 即 3
(6) ,Ag Al , nm.
4 4
每空 分 共 分
17.( 2 , 14 )
高温
(1)3AlCl(g)2Al(l)+AlCl3(g)
(2)0.06
先升温至T 以上 反应 的 G 反应 自发占主导 再降温至T 以下 反应 的 G 反应 自
(3) 2 , Ⅰ Δ <0, Ⅰ ; 1 , Ⅱ Δ <0, Ⅱ
发占主导 并保持较高温度 收集液态
, , Al
-4.8 6.6
(4)①> ②10 ③5×10 ④A
【解析】 依据题给信息和图 从热力学角度分析得到铝的具体操作为 先升温至T 以上 反应 的 G
(3) 1, : 2 , Ⅰ Δ <
反应 自发占主导 再降温至T 以下 反应 的 G 反应 自发占主导 并保持较高温度 收集液
0, Ⅰ ; 1 , Ⅱ Δ <0, Ⅱ , ,
态
Al.
p
由图 可知 反应 减低温度时 平衡使 (CO2)的值增大 即该平衡逆向移动 故 H
(4)① 2 , Ⅴ , lgp , , Δ >0.
(CO)
p
依据a点对应的温度为 (CO2) 将p 代入p
-4.8
② 1674K,lgp =-6.8, (CO)=100Pa ,(CO2)=10 .
(CO)
高三化学试题参考答案 第 页 共 页
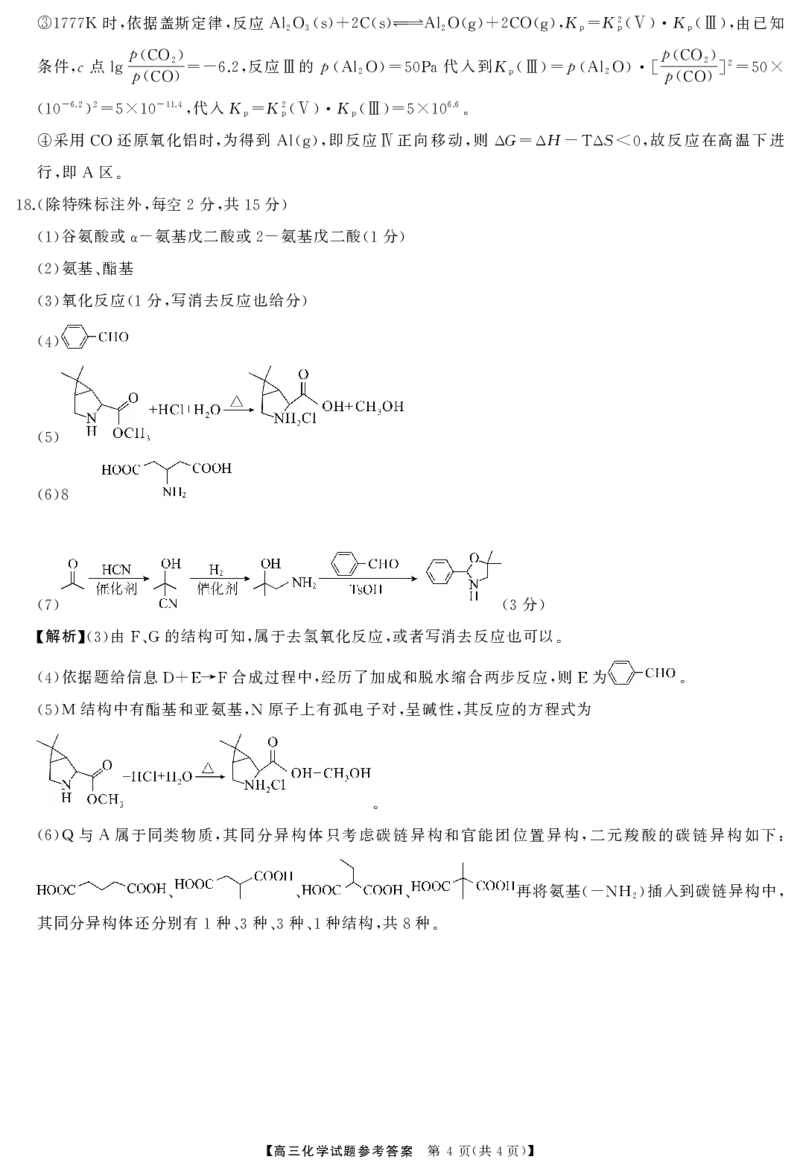
【 3 ( 4 )】时 依据盖斯定律 反应 K K2 K 由已知
③1777K , , Al2O3(s)+2C(s)Al2O(g)+2CO(g), p= p(Ⅴ) p(Ⅲ),
p p
条件c点 (CO2) 反应 的p 代入到K p (CO2) 2
, lgp =-6.2, Ⅲ (Al2O)=50Pa p(Ⅲ)= (Al2O)[p ]=50×
(CO) (CO)
-6.2 2 -11.4 代入K K2 K 6.6
(10 )=5×10 , p= p(Ⅴ) p(Ⅲ)=5×10 .
采用 还原氧化铝时 为得到 即反应 正向移动 则 G H S 故反应在高温下进
④ CO , Al(g), Ⅳ , Δ =Δ -TΔ <0,
行 即 区
, A .
除特殊标注外 每空 分 共 分
18.( , 2 , 15 )
谷氨酸或 氨基戊二酸或 氨基戊二酸 分
(1) α- 2- (1 )
氨基 酯基
(2) 、
氧化反应 分 写消去反应也给分
(3) (1 , )
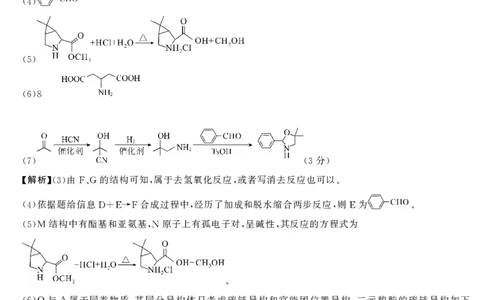
(4)
(5)
(6)8
分
(7) (3 )
【解析】 由 的结构可知 属于去氢氧化反应 或者写消去反应也可以
(3) F、G , , .
依据题给信息 合成过程中 经历了加成和脱水缩合两步反应 则 为
(4) D+E→F , , E .
结构中有酯基和亚氨基 原子上有孤电子对 呈碱性 其反应的方程式为
(5)M ,N , ,
.
与 属于同类物质 其同分异构体只考虑碳链异构和官能团位置异构 二元羧酸的碳链异构如下
(6)Q A , , :
再将氨基 插入到碳链异构中
、 、 、 (-NH2) ,
其同分异构体还分别有 种 种 种 种结构 共 种
1 、3 、3 、1 , 8 .
高三化学试题参考答案 第 页 共 页
【 4 ( 4 )】