文档内容
2024 年新课标卷理科综合化学试题
一、单选题
1.文房四宝是中华传统文化的瑰宝。下列有关叙述错误的是
A.羊毛可用于制毛笔,主要成分为蛋白质
B.松木可用于制墨,墨的主要成分是单质碳
C.竹子可用于造纸,纸的主要成分是纤维素
D.大理石可用于制砚台,主要成分为硅酸盐
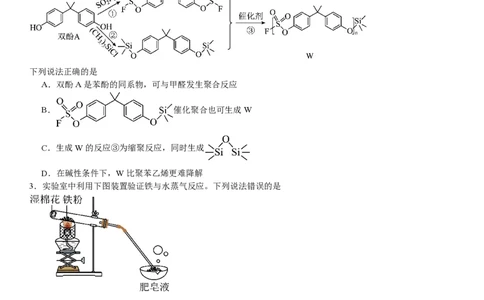
2.一种点击化学方法合成聚硫酸酯(W)的路线如下所示:
下列说法正确的是
A.双酚A是苯酚的同系物,可与甲醛发生聚合反应
B. 催化聚合也可生成W
C.生成W的反应③为缩聚反应,同时生成
D.在碱性条件下,W比聚苯乙烯更难降解
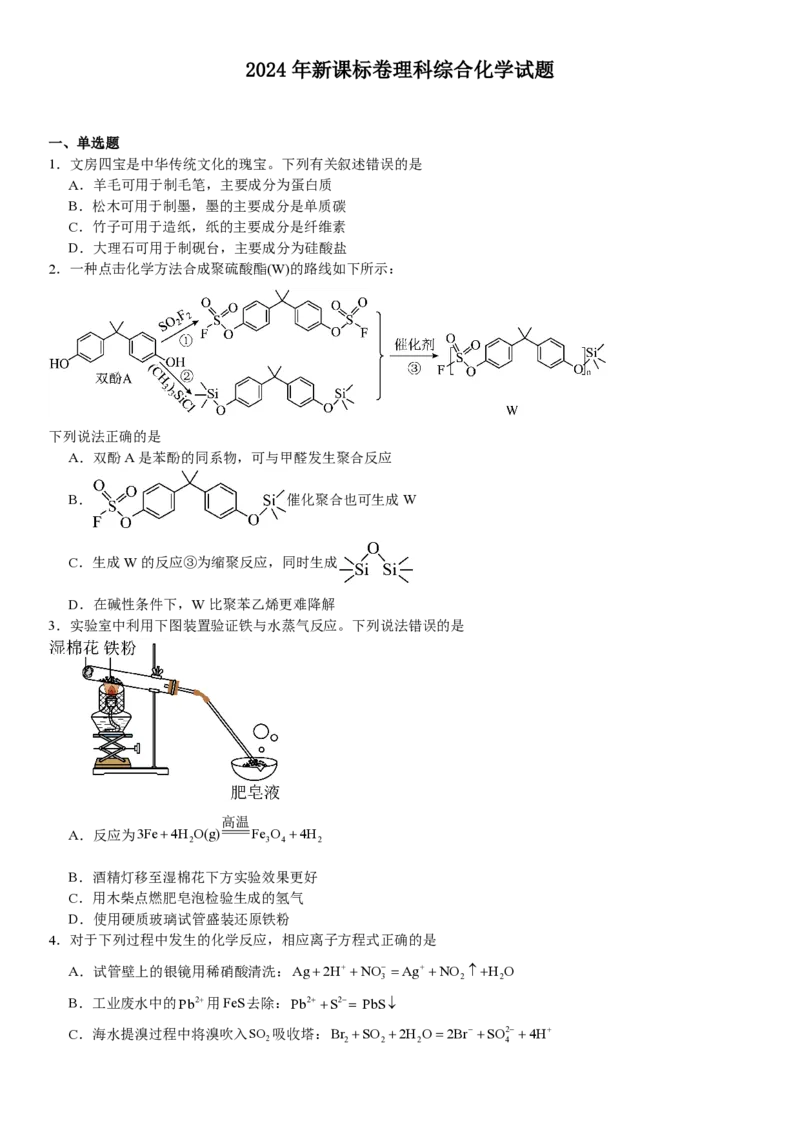
3.实验室中利用下图装置验证铁与水蒸气反应。下列说法错误的是
高温
A.反应为3Fe+4H O(g) Fe O +4H
2 3 4 2
B.酒精灯移至湿棉花下方实验效果更好
C.用木柴点燃肥皂泡检验生成的氢气
D.使用硬质玻璃试管盛装还原铁粉
4.对于下列过程中发生的化学反应,相应离子方程式正确的是
A.试管壁上的银镜用稀硝酸清洗:Ag+2H+ +NO− =Ag+ +NO ↑+H O
3 2 2
B.工业废水中的Pb2+用FeS去除:Pb2+ +S2−= PbS↓
C.海水提溴过程中将溴吹入SO 吸收塔:Br +SO +2H O=2Br−+SO2−+4H+
2 2 2 2 4D.用草酸标准溶液测定高锰酸钾溶液的浓度:2MnO−+5C O2−+16H+ =2Mn2+ +10CO ↑+8H O
4 2 4 2 2
5.我国科学家最近研究的一种无机盐Y [ Z(WX) ] 纳米药物具有高效的细胞内亚铁离子捕获和抗氧化能力。W、X、
3 6 2
Y、Z的原子序数依次增加,且W、X、Y属于不同族的短周期元素。W的外层电子数是其内层电子数的2倍,X
和Y的第一电离能都比左右相邻元素的高。Z的M层未成对电子数为4。下列叙述错误的是
A.W、X、Y、Z四种元素的单质中Z的熔点最高
B.在X的简单氢化物中X原子轨道杂化类型为sp3
C.Y的氢氧化物难溶于NaCl溶液,可以溶于NH Cl溶液
4
D.Y [ Z(WX) ] 中WX−提供电子对与Z3+形成配位键
3 6 2
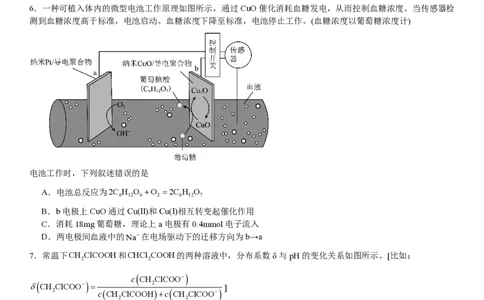
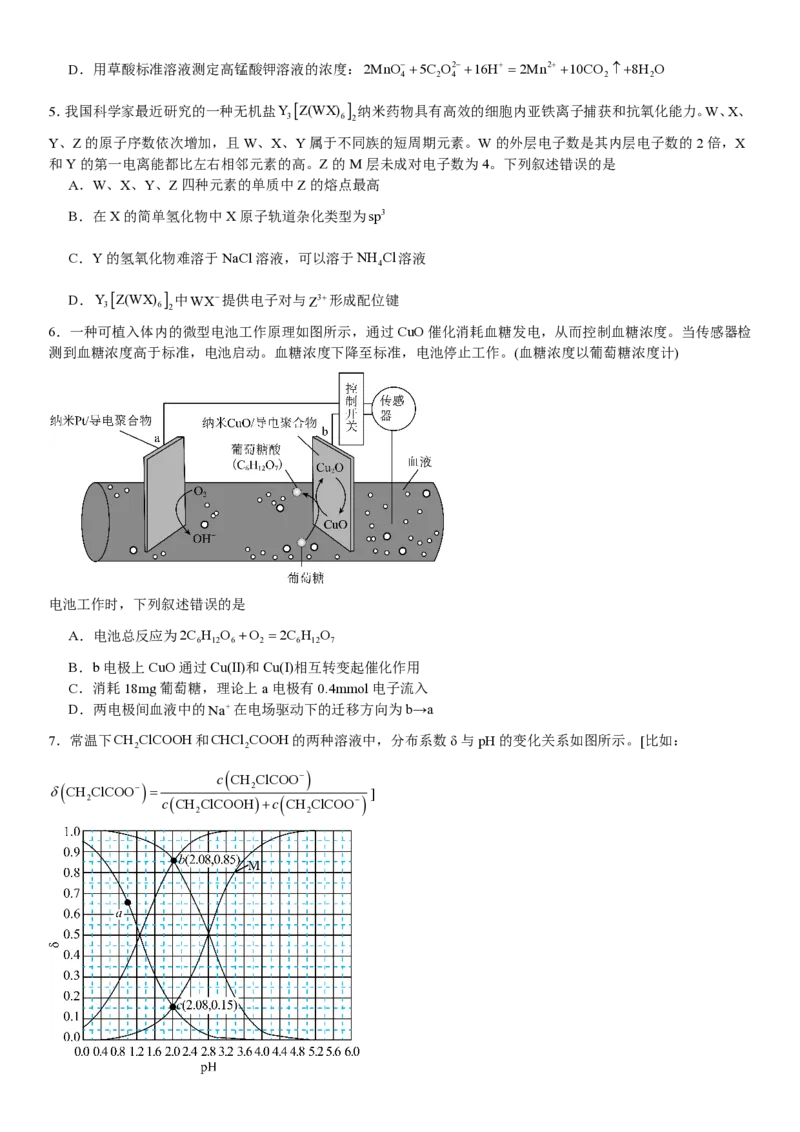
6.一种可植入体内的微型电池工作原理如图所示,通过CuO催化消耗血糖发电,从而控制血糖浓度。当传感器检
测到血糖浓度高于标准,电池启动。血糖浓度下降至标准,电池停止工作。(血糖浓度以葡萄糖浓度计)
电池工作时,下列叙述错误的是
A.电池总反应为2C H O +O =2C H O
6 12 6 2 6 12 7
B.b电极上CuO通过Cu(Ⅱ)和Cu(Ⅰ)相互转变起催化作用
C.消耗18mg葡萄糖,理论上a电极有0.4mmol电子流入
D.两电极间血液中的Na+在电场驱动下的迁移方向为b→a
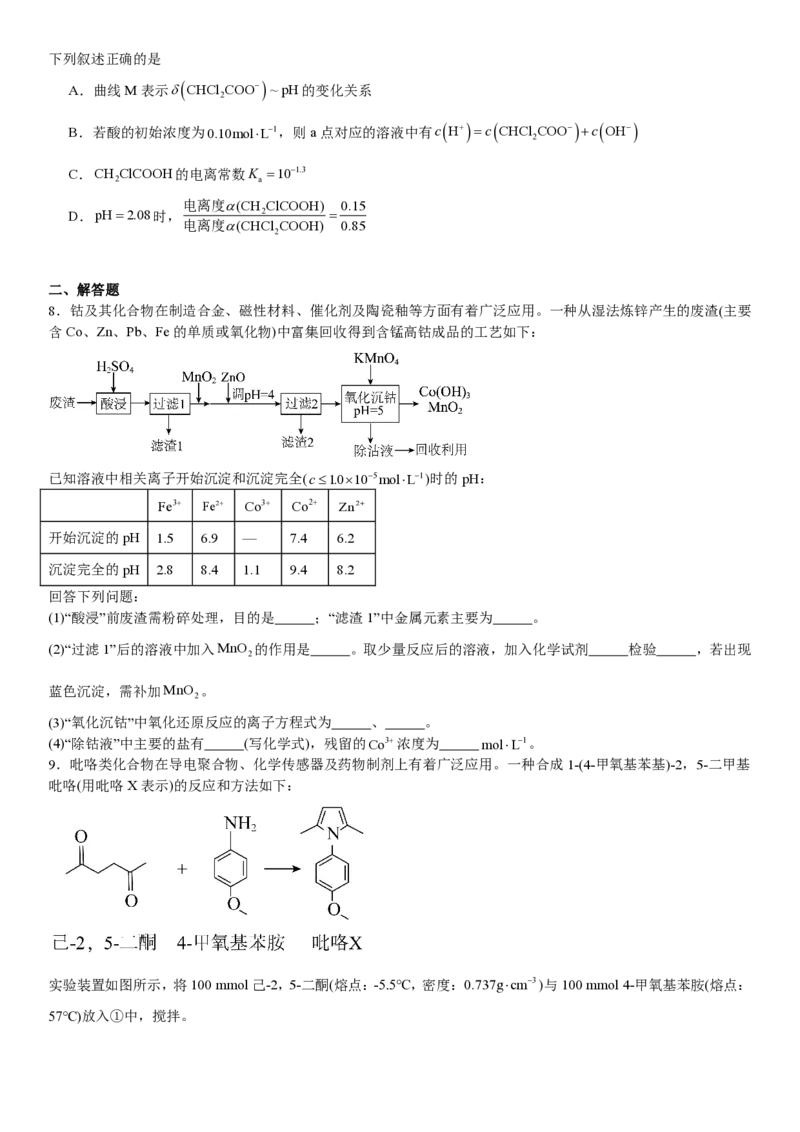
7.常温下CH ClCOOH和CHCl COOH的两种溶液中,分布系数δ与pH的变化关系如图所示。[比如:
2 2
c
(
CH
ClCOO−)
δ ( CH ClCOO−) = 2 ]
2 c(CH ClCOOH)+c ( CH ClCOO−)
2 2下列叙述正确的是
A.曲线M表示δ
(
CHCl
COO−)
~pH的变化关系
2
B.若酸的初始浓度为0.10mol⋅L−1,则a点对应的溶液中有c
( H+)
=c
(
CHCl
COO−)
+c
( OH−)
2
C.CH ClCOOH的电离常数K =10−1.3
2 a
电离度α(CH ClCOOH) 0.15
D.pH=2.08时, 2 =
电离度α(CHCl COOH) 0.85
2
二、解答题
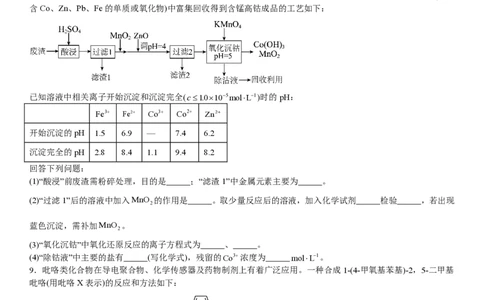
8.钴及其化合物在制造合金、磁性材料、催化剂及陶瓷釉等方面有着广泛应用。一种从湿法炼锌产生的废渣(主要
含Co、Zn、Pb、Fe的单质或氧化物)中富集回收得到含锰高钴成品的工艺如下:
已知溶液中相关离子开始沉淀和沉淀完全(c≤1.0×10−5mol⋅L−1)时的pH:
Fe3+ Fe2+ Co3+ Co2+ Zn2+
开始沉淀的pH 1.5 6.9 — 7.4 6.2
沉淀完全的pH 2.8 8.4 1.1 9.4 8.2
回答下列问题:
(1)“酸浸”前废渣需粉碎处理,目的是 ;“滤渣1”中金属元素主要为 。
(2)“过滤1”后的溶液中加入MnO 的作用是 。取少量反应后的溶液,加入化学试剂 检验 ,若出现
2
蓝色沉淀,需补加MnO 。
2
(3)“氧化沉钴”中氧化还原反应的离子方程式为 、 。
(4)“除钴液”中主要的盐有 (写化学式),残留的Co3+浓度为 mol⋅L−1。
9.吡咯类化合物在导电聚合物、化学传感器及药物制剂上有着广泛应用。一种合成1-(4-甲氧基苯基)-2,5-二甲基
吡咯(用吡咯X表示)的反应和方法如下:
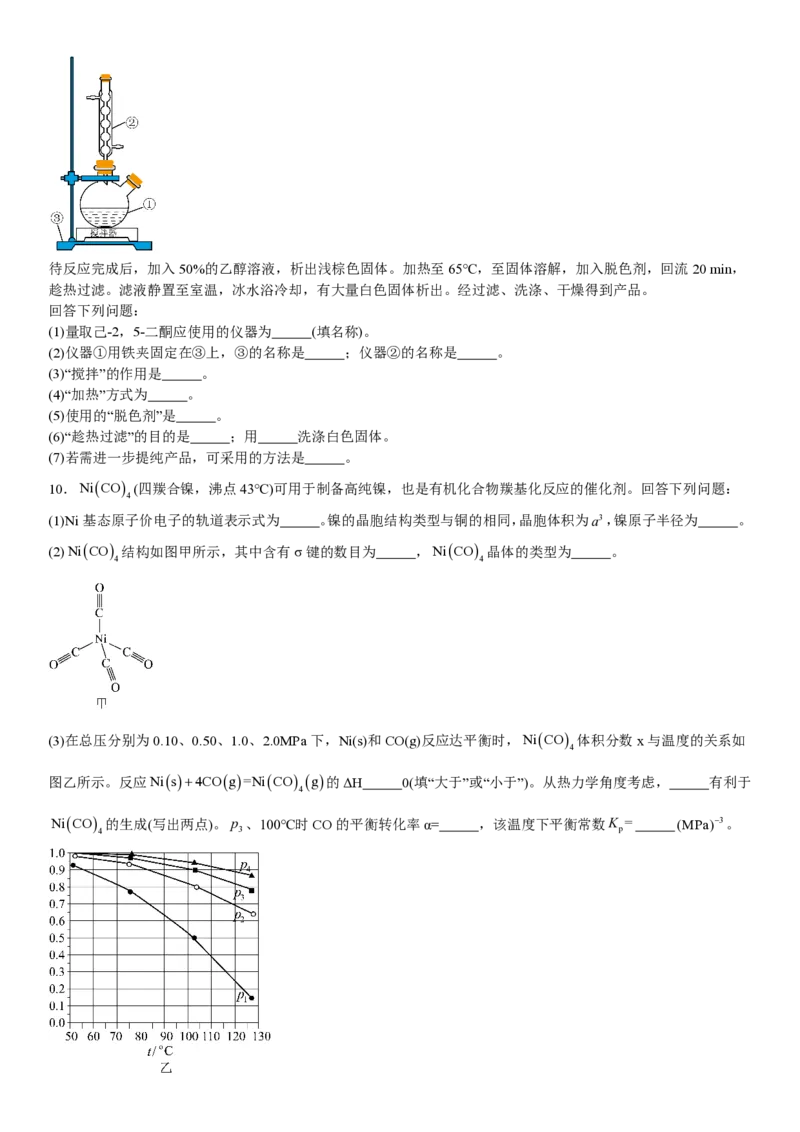
实验装置如图所示,将100 mmol己-2,5-二酮(熔点:-5.5℃,密度:0.737g⋅cm−3)与100 mmol 4-甲氧基苯胺(熔点:
57℃)放入①中,搅拌。待反应完成后,加入50%的乙醇溶液,析出浅棕色固体。加热至65℃,至固体溶解,加入脱色剂,回流20 min,
趁热过滤。滤液静置至室温,冰水浴冷却,有大量白色固体析出。经过滤、洗涤、干燥得到产品。
回答下列问题:
(1)量取己-2,5-二酮应使用的仪器为 (填名称)。
(2)仪器①用铁夹固定在③上,③的名称是 ;仪器②的名称是 。
(3)“搅拌”的作用是 。
(4)“加热”方式为 。
(5)使用的“脱色剂”是 。
(6)“趁热过滤”的目的是 ;用 洗涤白色固体。
(7)若需进一步提纯产品,可采用的方法是 。
10.Ni(CO) (四羰合镍,沸点43℃)可用于制备高纯镍,也是有机化合物羰基化反应的催化剂。回答下列问题:
4
(1)Ni基态原子价电子的轨道表示式为 。镍的晶胞结构类型与铜的相同,晶胞体积为a3,镍原子半径为 。
(2)Ni(CO) 结构如图甲所示,其中含有σ键的数目为 ,Ni(CO) 晶体的类型为 。
4 4
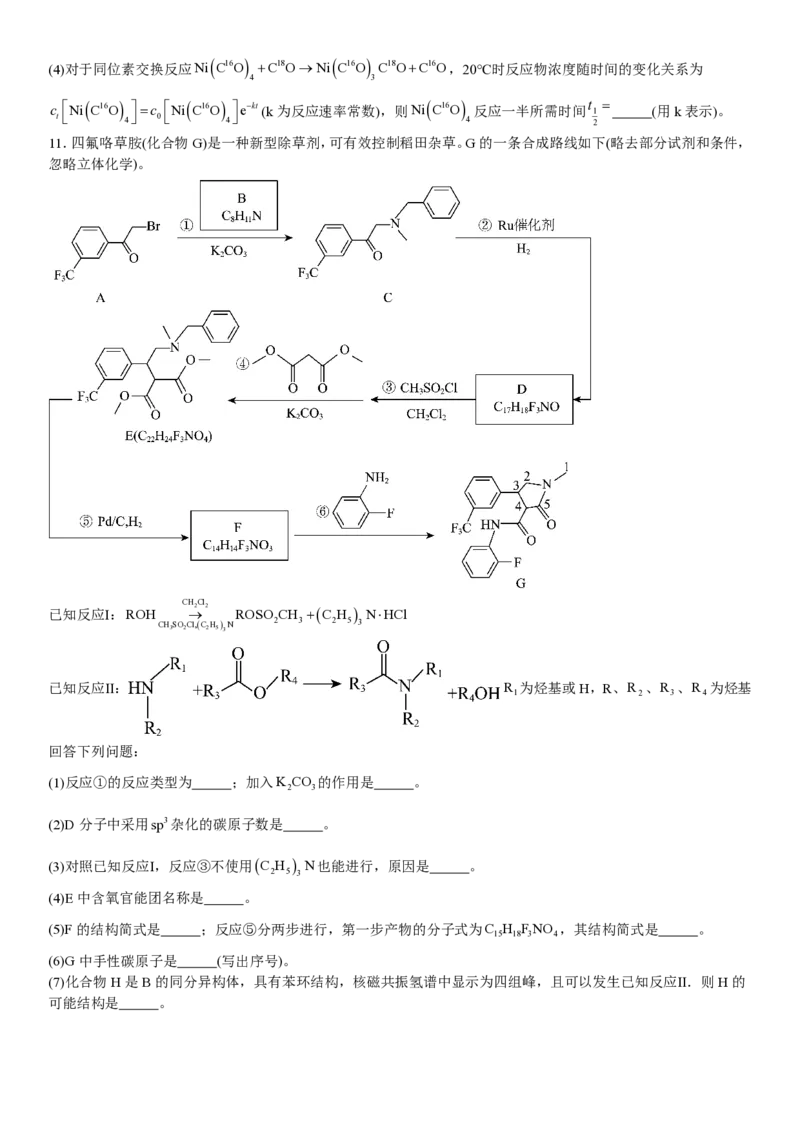
(3)在总压分别为0.10、0.50、1.0、2.0MPa下,Ni(s)和CO(g)反应达平衡时,Ni(CO) 体积分数x与温度的关系如
4
图乙所示。反应Ni(s)+4CO(g)=Ni(CO) (g)的ΔH 0(填“大于”或“小于”)。从热力学角度考虑, 有利于
4
Ni(CO) 的生成(写出两点)。p 、100℃时CO的平衡转化率α= ,该温度下平衡常数K = (MPa)−3。
4 3 p(4)对于同位素交换反应Ni ( C16O ) +C18O→Ni ( C16O ) C18O+C16O,20℃时反应物浓度随时间的变化关系为
4 3
c Ni ( C16O ) =c Ni ( C16O ) e−kt(k为反应速率常数),则Ni ( C16O ) 反应一半所需时间 t 1 = (用k表示)。
t 4 0 4 4 2
11.四氟咯草胺(化合物G)是一种新型除草剂,可有效控制稻田杂草。G的一条合成路线如下(略去部分试剂和条件,
忽略立体化学)。
已知反应Ⅰ:ROH
CH
→
2Cl2
ROSO CH +(C H ) N⋅HCl
CH3SO2Cl,(C2H5 )
3
N 2 3 2 5 3
已知反应Ⅱ: R 为烃基或H,R、R 、R 、R 为烃基
1 2 3 4
回答下列问题:
(1)反应①的反应类型为 ;加入K CO 的作用是 。
2 3
(2)D分子中采用sp3杂化的碳原子数是 。
(3)对照已知反应Ⅰ,反应③不使用(C H ) N也能进行,原因是 。
2 5 3
(4)E中含氧官能团名称是 。
(5)F的结构简式是 ;反应⑤分两步进行,第一步产物的分子式为C H FNO ,其结构简式是 。
15 18 3 4
(6)G中手性碳原子是 (写出序号)。
(7)化合物H是B的同分异构体,具有苯环结构,核磁共振氢谱中显示为四组峰,且可以发生已知反应Ⅱ.则H的
可能结构是 。