文档内容
【赢在高考·黄金 8 卷】备战 2024 年高考化学模拟卷(新高考七省专用)
黄金卷 08
(考试时间:75分钟 试卷满分:100分)
可能用到的相对原子质量:Al 27 Cl 35.5 Mn 55 Ni 59 Ga 70
第Ⅰ卷
一、选择题:本题共14小题,每小题3分,共42分。在每小题给出的四个选项中,只有一项是符合题目
要求的。
1.下列说法不正确的是
A.德国化学家维勒合成了尿素,开创了人工合成有机化合物的新时代
B.铝合金密度低、强度高,可用于航空工业
C.氨基酸之间通过氢键作用形成蛋白质的一级结构
D.制玻璃、水泥和炼铁过程中均须使用石灰石
2.下列有关物质的性质与用途说法不正确的是
A.碳酸钠和碳酸氢钠水溶液显碱性,可用作工业用碱或食用碱
B.常温下用铝制容器盛装浓硝酸,是因为铝很稳定不与浓硝酸反应
C.利用高纯单质硅的半导体性能,可以制成光电池
D.自来水厂用氯气杀菌消毒,是因为氯气可与水反应形成次氯酸具有强氧化性
3.已知:2NO
2
(g)+NaCl(s)NaNO3(s)+ClNO(g) H0,下列说法正确的是
cNaNO cClNO
A.该反应的平衡常数可表达为K= 3
c2NO cNaCl
2
微信公众号:【高中精品资料君】全网最全电子讲义以及最全网课,有需要的联系微信:xygewx002B.该反应一定能自发进行
C.降温有利于提高NO 的平衡转化率
2
D.NaCl晶胞(如图所示)中每个Na周围与其距离最近的Na有6个
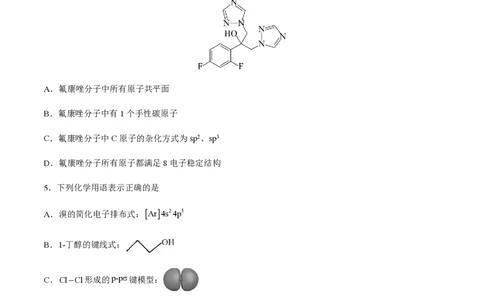
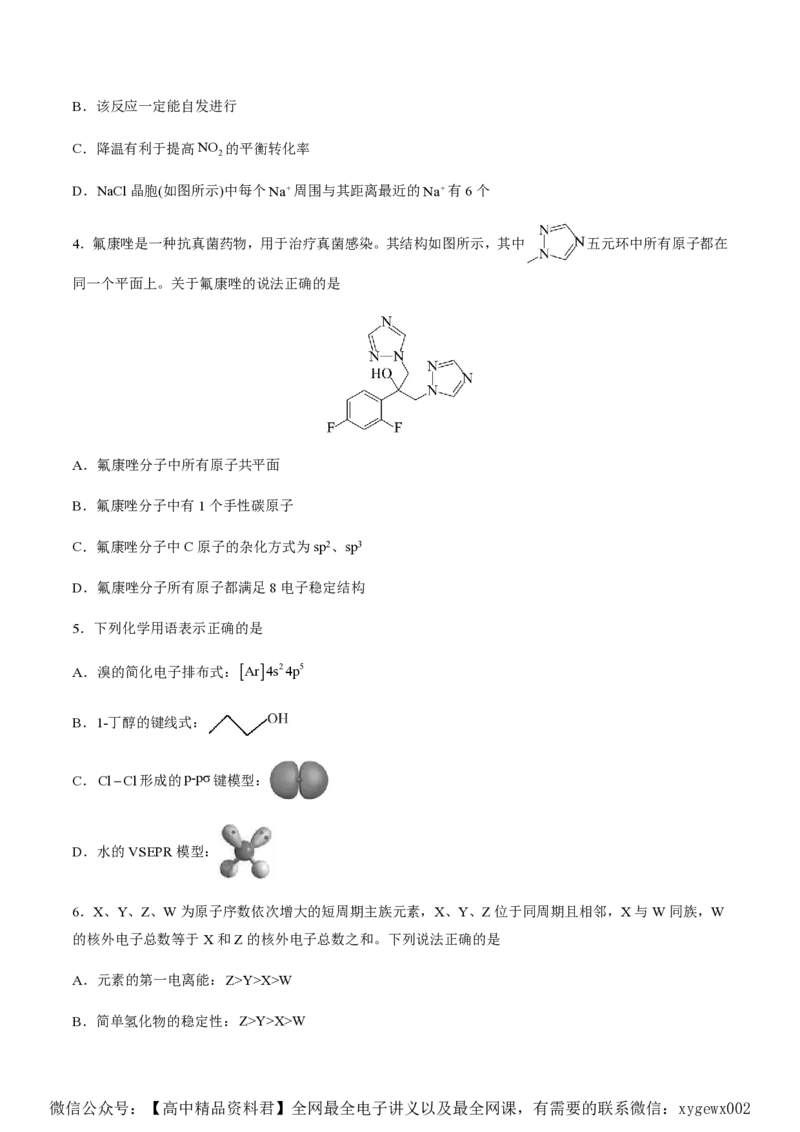
4.氟康唑是一种抗真菌药物,用于治疗真菌感染。其结构如图所示,其中 五元环中所有原子都在
同一个平面上。关于氟康唑的说法正确的是
A.氟康唑分子中所有原子共平面
B.氟康唑分子中有1个手性碳原子
C.氟康唑分子中C原子的杂化方式为sp2、sp3
D.氟康唑分子所有原子都满足8电子稳定结构
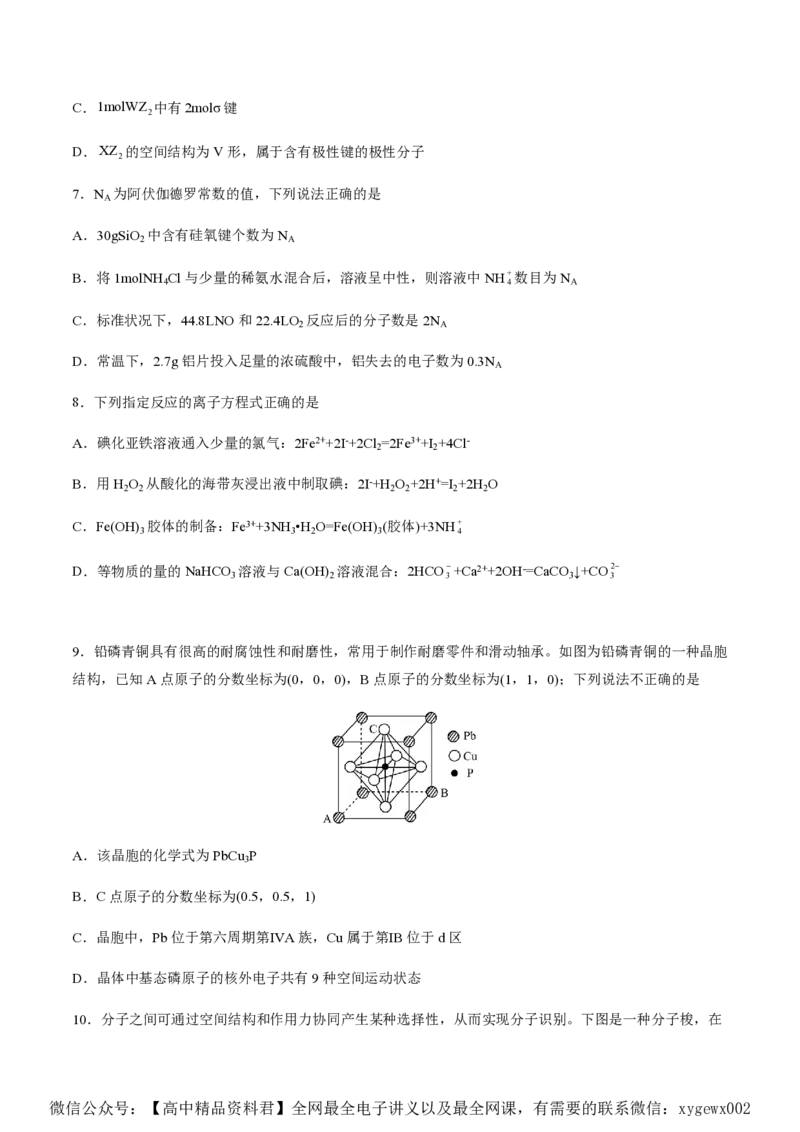
5.下列化学用语表示正确的是
A.溴的简化电子排布式:Ar4s24p5
B.1-丁醇的键线式:
C.ClCl形成的p-pσ键模型:
D.水的VSEPR模型:
6.X、Y、Z、W为原子序数依次增大的短周期主族元素,X、Y、Z位于同周期且相邻,X与W同族,W
的核外电子总数等于X和Z的核外电子总数之和。下列说法正确的是
A.元素的第一电离能:Z>Y>X>W
B.简单氢化物的稳定性:Z>Y>X>W
微信公众号:【高中精品资料君】全网最全电子讲义以及最全网课,有需要的联系微信:xygewx002C.1molWZ 中有2molσ键
2
D.XZ 的空间结构为V形,属于含有极性键的极性分子
2
7.N 为阿伏伽德罗常数的值,下列说法正确的是
A
A.30gSiO 中含有硅氧键个数为N
2 A
B.将1molNH Cl与少量的稀氨水混合后,溶液呈中性,则溶液中NH数目为N
4 4 A
C.标准状况下,44.8LNO和22.4LO 反应后的分子数是2N
2 A
D.常温下,2.7g铝片投入足量的浓硫酸中,铝失去的电子数为0.3N
A
8.下列指定反应的离子方程式正确的是
A.碘化亚铁溶液通入少量的氯气:2Fe2++2I-+2Cl =2Fe3++I +4Cl-
2 2
B.用H O 从酸化的海带灰浸出液中制取碘:2I-+H O +2H+=I +2H O
2 2 2 2 2 2
C.Fe(OH) 胶体的制备:Fe3++3NH •H O=Fe(OH) (胶体)+3NH
3 3 2 3 4
D.等物质的量的NaHCO 溶液与Ca(OH) 溶液混合:2HCO+Ca2++2OH-=CaCO ↓+CO2
3 2 3 3 3
9.铅磷青铜具有很高的耐腐蚀性和耐磨性,常用于制作耐磨零件和滑动轴承。如图为铅磷青铜的一种晶胞
结构,已知A点原子的分数坐标为(0,0,0),B点原子的分数坐标为(1,1,0);下列说法不正确的是
A.该晶胞的化学式为PbCu P
3
B.C点原子的分数坐标为(0.5,0.5,1)
C.晶胞中,Pb位于第六周期第ⅣA族,Cu属于第ⅠB位于d区
D.晶体中基态磷原子的核外电子共有9种空间运动状态
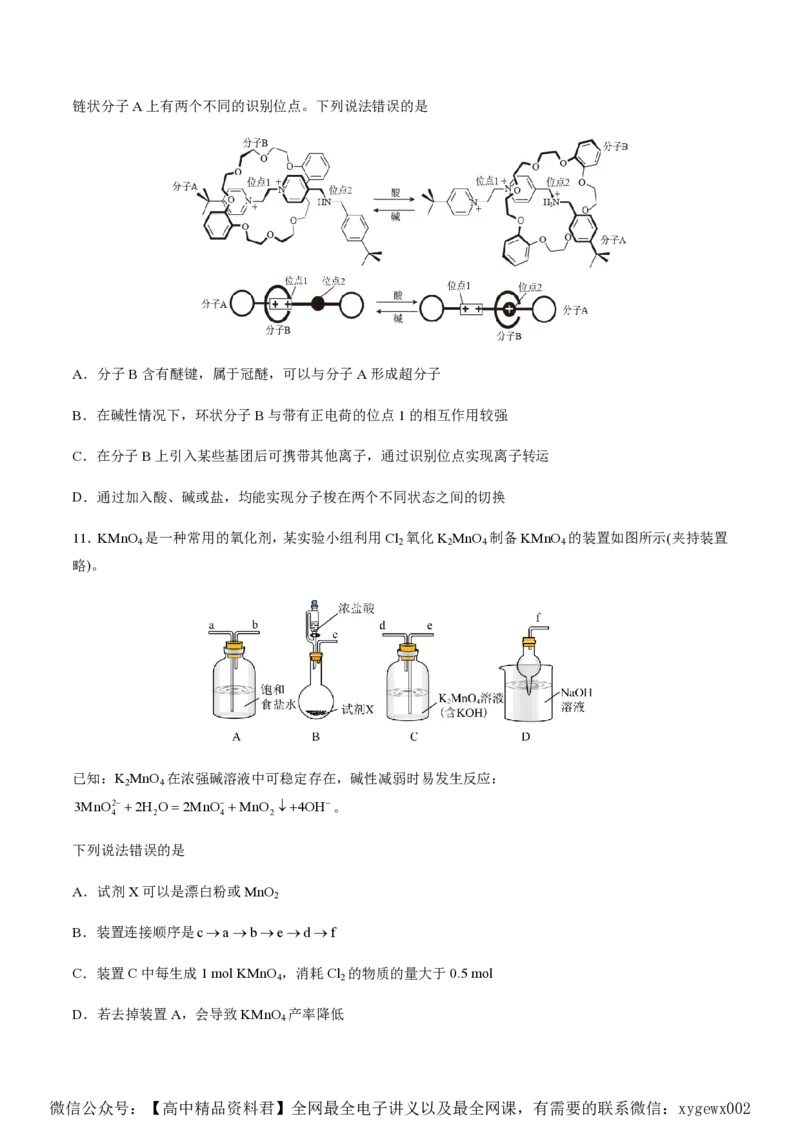
10.分子之间可通过空间结构和作用力协同产生某种选择性,从而实现分子识别。下图是一种分子梭,在
微信公众号:【高中精品资料君】全网最全电子讲义以及最全网课,有需要的联系微信:xygewx002链状分子A上有两个不同的识别位点。下列说法错误的是
A.分子B含有醚键,属于冠醚,可以与分子A形成超分子
B.在碱性情况下,环状分子B与带有正电荷的位点1的相互作用较强
C.在分子B上引入某些基团后可携带其他离子,通过识别位点实现离子转运
D.通过加入酸、碱或盐,均能实现分子梭在两个不同状态之间的切换
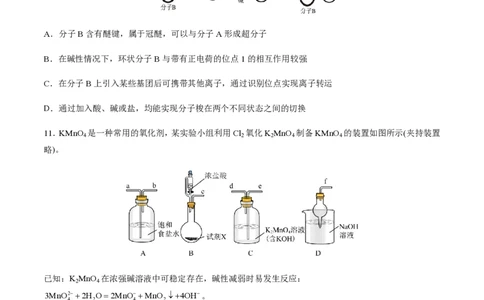
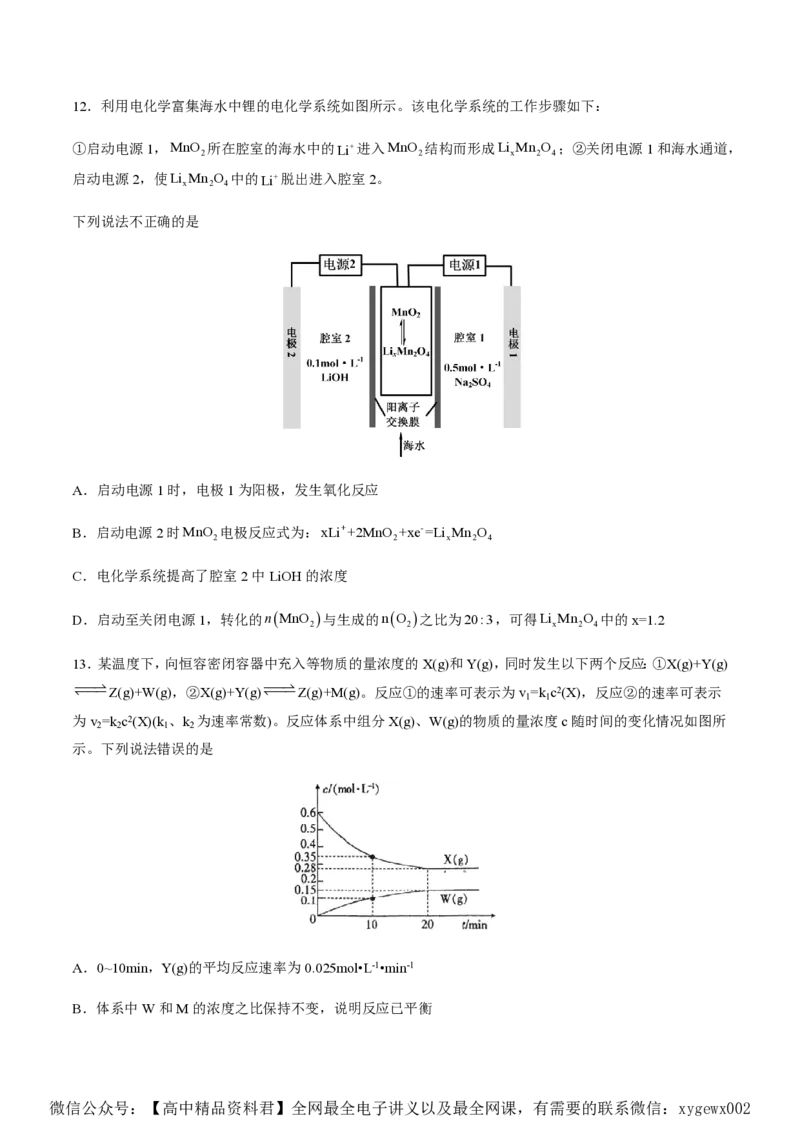
11.KMnO 是一种常用的氧化剂,某实验小组利用Cl 氧化K MnO 制备KMnO 的装置如图所示(夹持装置
4 2 2 4 4
略)。
已知:K MnO 在浓强碱溶液中可稳定存在,碱性减弱时易发生反应:
2 4
3MnO22H O2MnOMnO 4OH。
4 2 4 2
下列说法错误的是
A.试剂X可以是漂白粉或MnO
2
B.装置连接顺序是cabedf
C.装置C中每生成1 mol KMnO ,消耗Cl 的物质的量大于0.5 mol
4 2
D.若去掉装置A,会导致KMnO 产率降低
4
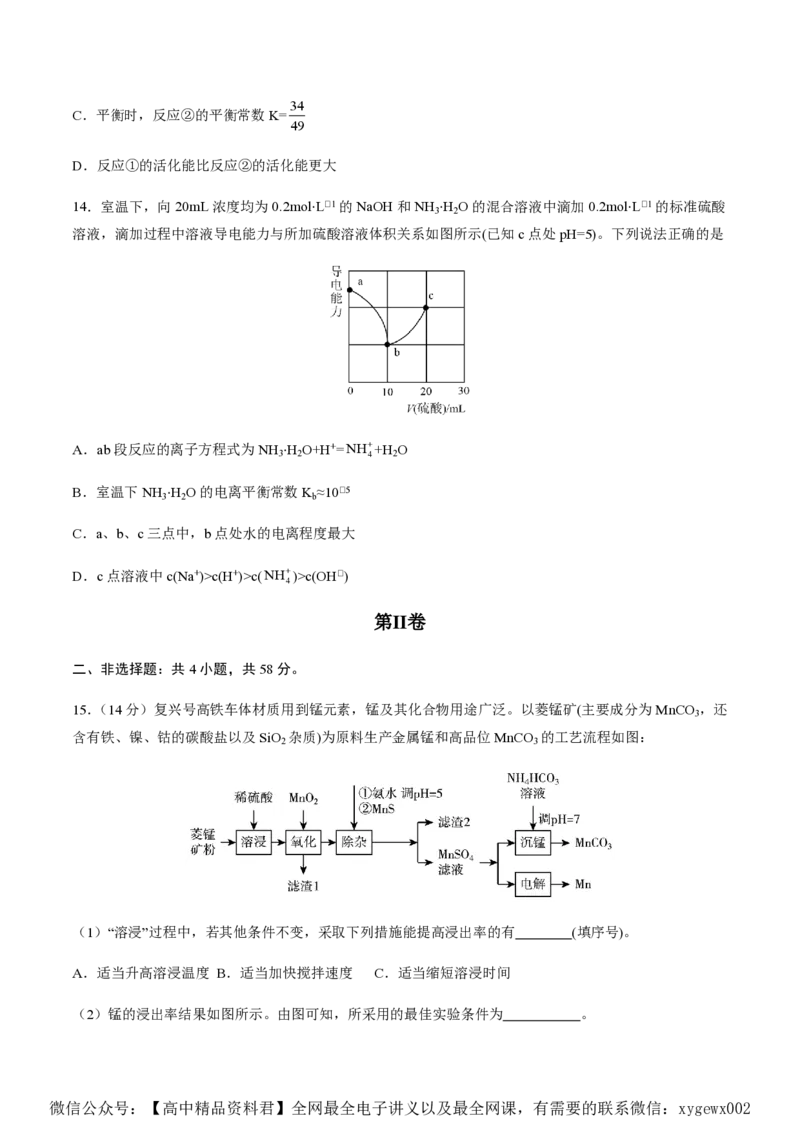
微信公众号:【高中精品资料君】全网最全电子讲义以及最全网课,有需要的联系微信:xygewx00212.利用电化学富集海水中锂的电化学系统如图所示。该电化学系统的工作步骤如下:
①启动电源1,MnO 所在腔室的海水中的Li进入MnO 结构而形成Li Mn O ;②关闭电源1和海水通道,
2 2 x 2 4
启动电源2,使Li Mn O 中的Li脱出进入腔室2。
x 2 4
下列说法不正确的是
A.启动电源1时,电极1为阳极,发生氧化反应
B.启动电源2时MnO 电极反应式为:xLi++2MnO +xe-=Li Mn O
2 2 x 2 4
C.电化学系统提高了腔室2中LiOH的浓度
D.启动至关闭电源1,转化的nMnO 与生成的nO 之比为20:3,可得Li Mn O 中的x=1.2
2 2 x 2 4
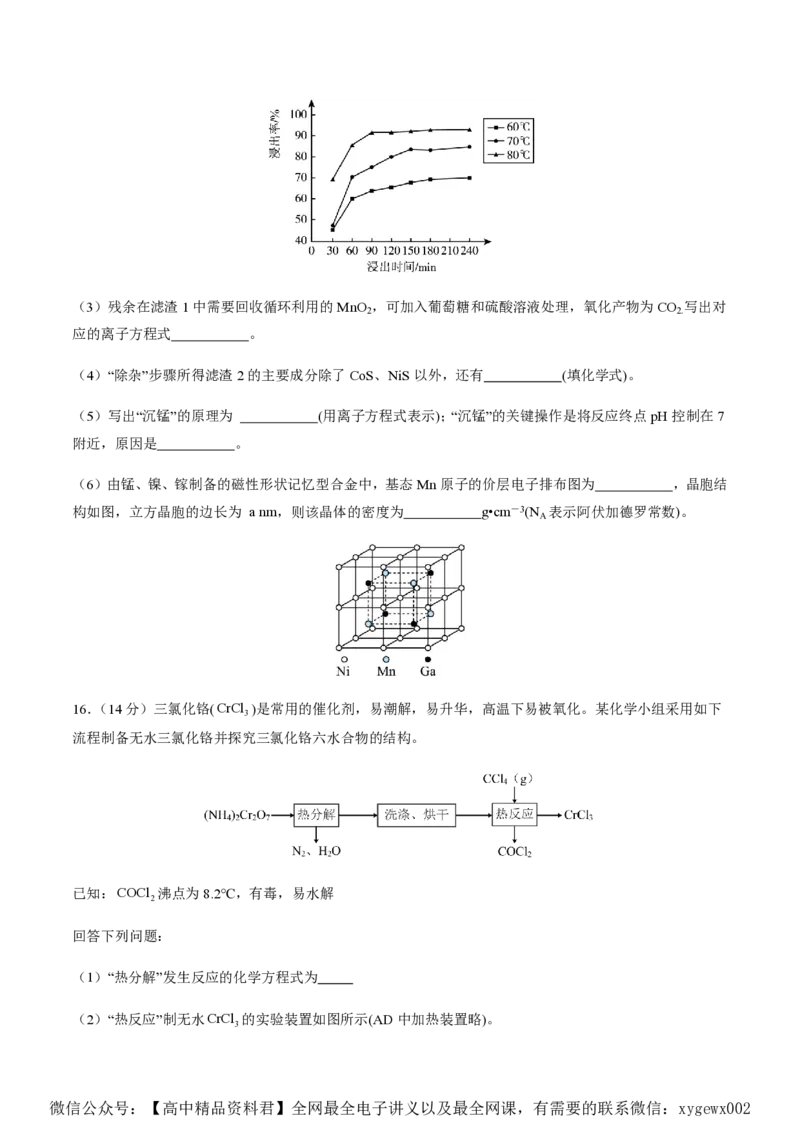
13.某温度下,向恒容密闭容器中充入等物质的量浓度的X(g)和Y(g),同时发生以下两个反应:①X(g)+Y(g)
Z(g)+W(g),②X(g)+Y(g)Z(g)+M(g)。反应①的速率可表示为v
1
=k
1
c2(X),反应②的速率可表示
为v =k c2(X)(k 、k 为速率常数)。反应体系中组分X(g)、W(g)的物质的量浓度c随时间的变化情况如图所
2 2 1 2
示。下列说法错误的是
A.0~10min,Y(g)的平均反应速率为0.025mol•L-1•min-1
B.体系中W和M的浓度之比保持不变,说明反应已平衡
微信公众号:【高中精品资料君】全网最全电子讲义以及最全网课,有需要的联系微信:xygewx00234
C.平衡时,反应②的平衡常数K=
49
D.反应①的活化能比反应②的活化能更大
14.室温下,向20mL浓度均为0.2mol⋅L﹣1的NaOH和NH ⋅H O的混合溶液中滴加0.2mol⋅L﹣1的标准硫酸
3 2
溶液,滴加过程中溶液导电能力与所加硫酸溶液体积关系如图所示(已知c点处pH=5)。下列说法正确的是
A.ab段反应的离子方程式为NH ⋅H O+H+=NH++H O
3 2 4 2
B.室温下NH ⋅H O的电离平衡常数K ≈10﹣5
3 2 b
C.a、b、c三点中,b点处水的电离程度最大
D.c点溶液中c(Na+)>c(H+)>c(NH+)>c(OH﹣)
4
第Ⅱ卷
二、非选择题:共4小题,共58分。
15.(14分)复兴号高铁车体材质用到锰元素,锰及其化合物用途广泛。以菱锰矿(主要成分为MnCO ,还
3
含有铁、镍、钴的碳酸盐以及SiO 杂质)为原料生产金属锰和高品位MnCO 的工艺流程如图:
2 3
(1)“溶浸”过程中,若其他条件不变,采取下列措施能提高浸出率的有 (填序号)。
A.适当升高溶浸温度 B.适当加快搅拌速度 C.适当缩短溶浸时间
(2)锰的浸出率结果如图所示。由图可知,所采用的最佳实验条件为 。
微信公众号:【高中精品资料君】全网最全电子讲义以及最全网课,有需要的联系微信:xygewx002(3)残余在滤渣1中需要回收循环利用的MnO ,可加入葡萄糖和硫酸溶液处理,氧化产物为CO 写出对
2 2.
应的离子方程式 。
(4)“除杂”步骤所得滤渣2的主要成分除了CoS、NiS以外,还有 (填化学式)。
(5)写出“沉锰”的原理为 (用离子方程式表示);“沉锰”的关键操作是将反应终点pH控制在7
附近,原因是 。
(6)由锰、镍、镓制备的磁性形状记忆型合金中,基态Mn原子的价层电子排布图为 ,晶胞结
构如图,立方晶胞的边长为 a nm,则该晶体的密度为 g•cm-3(N 表示阿伏加德罗常数)。
A
16.(14分)三氯化铬(CrCl )是常用的催化剂,易潮解,易升华,高温下易被氧化。某化学小组采用如下
3
流程制备无水三氯化铬并探究三氯化铬六水合物的结构。
已知:COCl 沸点为8.2℃,有毒,易水解
2
回答下列问题:
(1)“热分解”发生反应的化学方程式为
(2)“热反应”制无水CrCl 的实验装置如图所示(AD中加热装置略)。
3
微信公众号:【高中精品资料君】全网最全电子讲义以及最全网课,有需要的联系微信:xygewx002①实验装置连接顺序为 。
b→_____,_____→_____,_____→_____,_____→_____(填仪器接口字母)
②加热反应前通N 的目的是 。
2
③A中仪器x的名称是 ,其作用是 。
④E中收集的物质含有 (写化学式)。
⑤尾气经 处理后可循环使用。
(3)已知CrCl 6H O配合物(Mr=266.5,配位数为6)有多种异构体,不同条件下析出不同颜色的晶体,如
3 2
CrH O ClCl H O晶体为淡绿色。将CrCl 溶于水,一定条件下结晶析出暗绿色晶体。称取5.33g该暗
2 5 2 2 3
绿色晶体溶于水配成暗绿色溶液,加入足量的AgNO 溶液,得到2.87g白色沉淀。
3
①CrH O ClCl H O中存在的化学键有 (填序号)。
2 5 2 2
a.配位键 b.氢键 c.离子键 d.金属键
②该暗绿色晶体的化学式为 。
17.(15分)甲酸甲酯(HCOOCH )是一种重要的有机合成中间体,可通过甲醇催化脱氢法制备,其工艺过
3
程包含以下反应:
反应Ⅰ:2CH OH(g)=HCOOCH (g)+2H (g) K ,△H =+51.2kJ•mol-1
3 3 2 1 1
反应Ⅱ:CH OH(g)=CO(g)+2H (g) K ,△H =+90.1kJ•mol-1
3 2 2 2
回答下列问题:
(1)反应HCOOCH (g)=2CO(g)+2H (g)的△H = kJ•mol-1,K = (用K 、K 表示)。
3 2 3 3 1 2
(2)对于反应Ⅰ:增大压强,平衡 移动(填“向左”“向右”或“不”)。保持压强不变,要缩短反应达到
平衡的时间,可采取的措施是 、 。
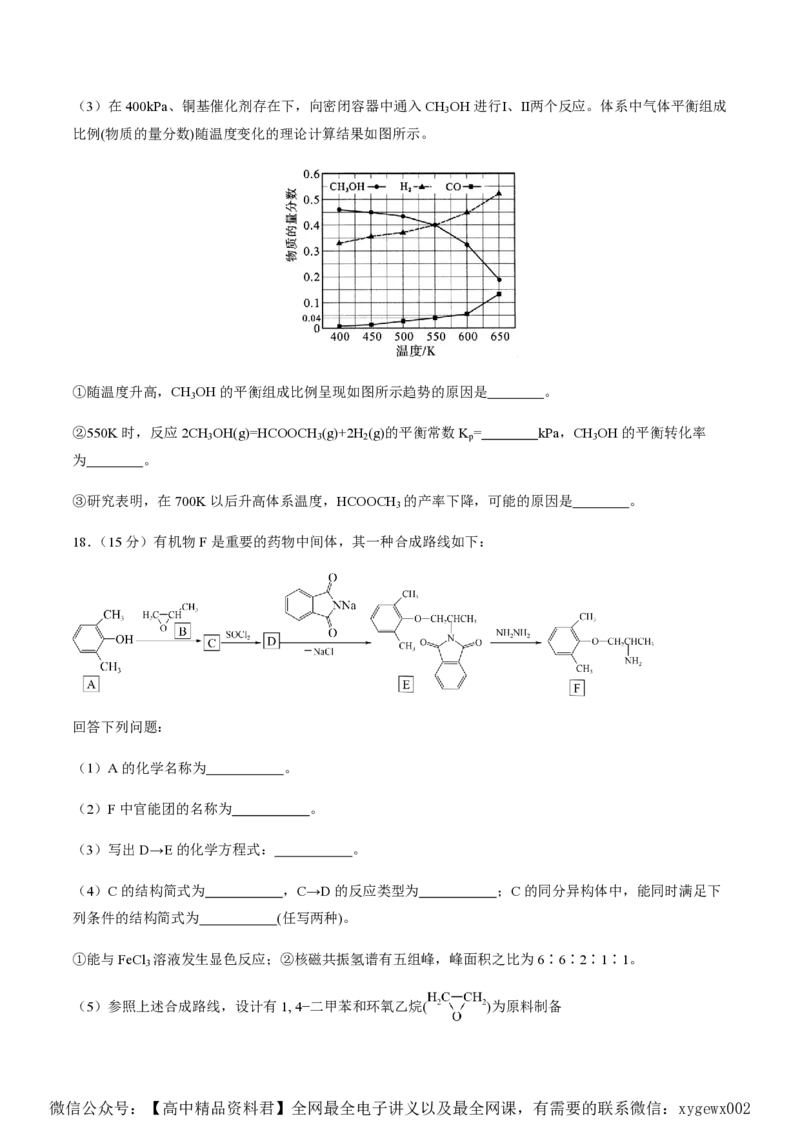
微信公众号:【高中精品资料君】全网最全电子讲义以及最全网课,有需要的联系微信:xygewx002(3)在400kPa、铜基催化剂存在下,向密闭容器中通入CH OH进行Ⅰ、Ⅱ两个反应。体系中气体平衡组成
3
比例(物质的量分数)随温度变化的理论计算结果如图所示。
①随温度升高,CH OH的平衡组成比例呈现如图所示趋势的原因是 。
3
②550K时,反应2CH OH(g)=HCOOCH (g)+2H (g)的平衡常数K = kPa,CH OH的平衡转化率
3 3 2 p 3
为 。
③研究表明,在700K以后升高体系温度,HCOOCH 的产率下降,可能的原因是 。
3
18.(15分)有机物F是重要的药物中间体,其一种合成路线如下:
回答下列问题:
(1)A的化学名称为 。
(2)F中官能团的名称为 。
(3)写出D→E的化学方程式: 。
(4)C的结构简式为 ,C→D的反应类型为 ;C的同分异构体中,能同时满足下
列条件的结构简式为 (任写两种)。
①能与FeCl 溶液发生显色反应;②核磁共振氢谱有五组峰,峰面积之比为6∶6∶2∶1∶1。
3
(5)参照上述合成路线,设计有1, 4−二甲苯和环氧乙烷( )为原料制备
微信公众号:【高中精品资料君】全网最全电子讲义以及最全网课,有需要的联系微信:xygewx002的合成路线: (其他无机试剂任选)。
微信公众号:【高中精品资料君】全网最全电子讲义以及最全网课,有需要的联系微信:xygewx002