文档内容
扬州市 2024 届高三上学期期初考试模拟试题
化学学科
可能用到的相对原子质量:H-1 Li-7 C-12 N-14 O-16 Mg-24 S-32 Cl-35.5
一、单项选择题:共13题,每题3分,共39分。每题只有一个选项最符合题意。
1.我国提出在2060年前完成“碳中和”的目标,下列有关低碳生活的说法正确的是
A.杜绝化石燃料等传统能源的使用
B.在一定条件下,选择合适的催化剂将CO 氧化为甲酸
2
C.推广使用煤液化技术,可减少二氧化碳的排放
D.开发太阳能、风能、生物质能等新能源是践行低碳生活的有效途径
2.反应3Cl +8NH =6NH Cl+N 常用来检验输送氯气的管道是否漏气。下列说法正确的是
2 3 4 2
A.NH 是非极性分子 B.Cl原子结构示意图为
3
C.N 的电子式为 D.NH Cl中既含有离子键又含有共价键
2 4
3.实验室制备和收集氨气时,下列装置能达到相应实验目的的是
A.制备氨气 B.干燥氨气 C.收集氨气 D.吸收尾气
A.A B.B C.C D.D
4.CrSi、Ge—GaAs、ZnGeAs 和碳化硅都是重要的半导体化合物,下列说法错误的是
2
A.基态铬原子的价电子排布式为3d54s1
B.Ge—GaAs中元素Ge、Ga、As的第一电离能由大到小的顺序为As>Ga>Ge
C.ZnGeAs 中元素Zn、Ge、As的电负性由大到小的顺序为As>Ge>Zn
2
D.碳化硅属于原子晶体,其熔沸点均大于晶体硅
第1页,共9页
学科网(北京)股份有限公司5.卤族元素单质及其化合物应用广泛。CN 具有与卤素单质相似的化学性质。F 在常温下能与Cu反应
2 2
生成致密的氟化物薄膜,还能与熔融的Na SO 反应生成硫酰氟(SO F )。CaF 与浓硫酸反应可制得HF,
2 4 2 2 2
常温下,测得氟化氢的相对分子质量约为37.SO 通入KClO 酸性溶液中可制得黄绿色气体ClO ,该气体常
2 3 2
用作自来水消毒剂。工业用Cl 制备TiCl 的热化学方程式为TiO s2Cl g2Csƒ TiCl g
2 4 2 2 4
2COg H 49kJmol1。下列说法不正确的是
A.CN 是由极性键构成的极性分子 B.ClO、SO2中心原子的杂化方式均为sp3
2 3 4
C.常温下,氟化氢可能以HF 分子的形式存在
2
D.F 与熔融Na SO 反应时一定有氧元素化合价升高
2 2 4
6.化学方程式是化学转化过程的符号语言描述,不仅表示物质的转化,有的还揭示转化的本质,有的还
表示出物质转化过程中的能量变化,下列叙述正确的是
A.碳酸氢铵溶液中滴加足量NaOH溶液:NH HCO2OH NH H OCO2H O
4 3 3 2 3 2
B.H O 一种绿色氧化剂,但遇到酸性高锰酸钾时,只能表现出还原性,其反应的方程式:
2 2
3H O 3H SO 2KMnO =K SO 2MnSO 4O 6H O
2 2 2 4 4 2 4 4 2 2
C.SO 通入漂白粉溶液中产生白色浑浊:SO Ca2 2ClO H OCaSO 2HClO
2 2 2 3
D.H 的标准燃烧热是285.8kJmol1,其燃烧的热化学方程式可以表示为2H (g)O (g)2H O(g)
2 2 2 2
H571.6kJmol1。
7.卤族元素单质及其化合物应用广泛。CN 具有与卤素单质相似的化学性质。F 在常温下能与Cu反应
2 2
生成致密的氟化物薄膜,还能与熔融的Na SO 反应生成硫酰氟(SO F )。CaF 与浓硫酸反应可制得HF,
2 4 2 2 2
常温下,测得氟化氢的相对分子质量约为37。SO 通入KClO 酸性溶液中可制得黄绿色气体ClO ,该气体
2 3 2
常用作自来水消毒剂。工业用Cl 制备TiCl 的热化学方程式为TiO s2Cl g2Csƒ TiCl g
2 4 2 2 4
2COg H 49kJmol1。下列物质性质与用途具有对应关系的是
A.铜单质化学性质不活泼,可用于制作储存F 的容器 B.ClO 呈黄绿色,可用于自来水消毒
2 2
C.SO 具有还原性,可用于与KClO 反应制ClO
2 3 2
第2页,共9页
学科网(北京)股份有限公司D.浓硫酸具有强氧化性,可用于与CaF 反应制HF
2
8.氯及其化合物应用广泛。氯的单质Cl 可由MnO 与浓盐酸共热得到,Cl 能氧化Br-,可从海水中提取
2 2 2
Br ;氯的氧化物ClO 可用于自来水消毒,ClO 是一种黄绿色气体,易溶于水,与碱反应会生成ClO- 与
2 2 2 2
ClO-,在稀硫酸和NaClO 的混合溶液中通入SO 气体可制得ClO ;漂白液和漂白粉的有效成分是次氯酸
3 3 2 2
盐,可作棉、麻的漂白剂。下列含氯物质的转化正确的是
A.漂白粉 过量CO 2HClO(aq) 光照 Cl (g) B.MgCl (aq) 加热无水MgCl 电解 Mg
2 2 2
C.NaCl(aq) 通电 Cl (g) Fe FeC1 D.NaCl(aq) 过量CO 2NaHCO (aq) Na CO (s)
2 点燃 3 3 2 3
9.五倍子是一种常见的中草药,其有效成分为X。在一定条件下X可分别转化为Y、Z。
下列说法不正确的是
A.Z中含氧官能团有三种:羟基、羧基、酯基
B.Y在浓硫酸做催化剂加热条件下发生消去反应
C.Z在酸性条件下水解生成两种有机物,1mol Z最多能与8mol NaOH 发生反应
D.可以用FeC1 溶液检验X是否完全转化为Y
3
10.用活性炭与NO 反应:为2C(s)+2NO (g)⇌2CO (g)+N (g) H0来消除氮氧化物产生的空气污染。下
2 2 2 2
列说法正确的是
c2CO cN
A.该反应只在高温条件下能自发进行 B.该反应平衡常数的表达式为K 2 2
c2NO c2(C)
2
C.该反应中消耗1molNO ,转移电子的数目为46.021023
2
D.该反应到达平衡后,升高温度,正反应速率减慢,逆反应速率加快
11.下列实验探究方案能达到探究目的的是
选
探究方案 探究目的
项
A 向FeCl 溶液中滴加氯水,观察溶液颜色变化 氯水中含有HClO
3
第3页,共9页
学科网(北京)股份有限公司取5mL 0.1molL1 FeCl 溶液,向其中加入1mL 0.1molL1 KI溶 2Fe3 2I 2Fe2 I 是可
3 2
B
液,振荡,向上层清液滴加3~4滴KSCN溶液,观察溶液颜色变化 逆反应
C 用pH计测定Na CO 、Na SiO 溶液的pH,比较溶液pH大小 C的非金属性比Si强
2 3 2 3
将NaClO溶液分别滴入品红溶液和滴加醋酸的品红溶液中,观察品
D pH对ClO氧化性的影响
红溶液颜色变化
A.A B.B C.C D.D
12.硫代硫酸钠(Na S O )的制备和应用相关流程如图所示。
2 2 3
已知:25℃时,H SO 的K 1.4102,K 6.0108;H CO 的K 4.5107,K 5.01011
2 3 a1 a2 2 3 a1 a2
下列说法正确的是
A.步骤1过程中pH=8时,c
SO2
c
CO2
0.03c
HSO
c
HCO
3 3 3 3
B.步骤1所得的溶液中:c Na 2cH SO c HSO c SO2
2 3 3 3
C.步骤3所得的清液中:c Ag c Br K AgBr
sp
D.步骤3的离子方程式为:Ag 2S O2 AgS O 3
2 3 2 3 2
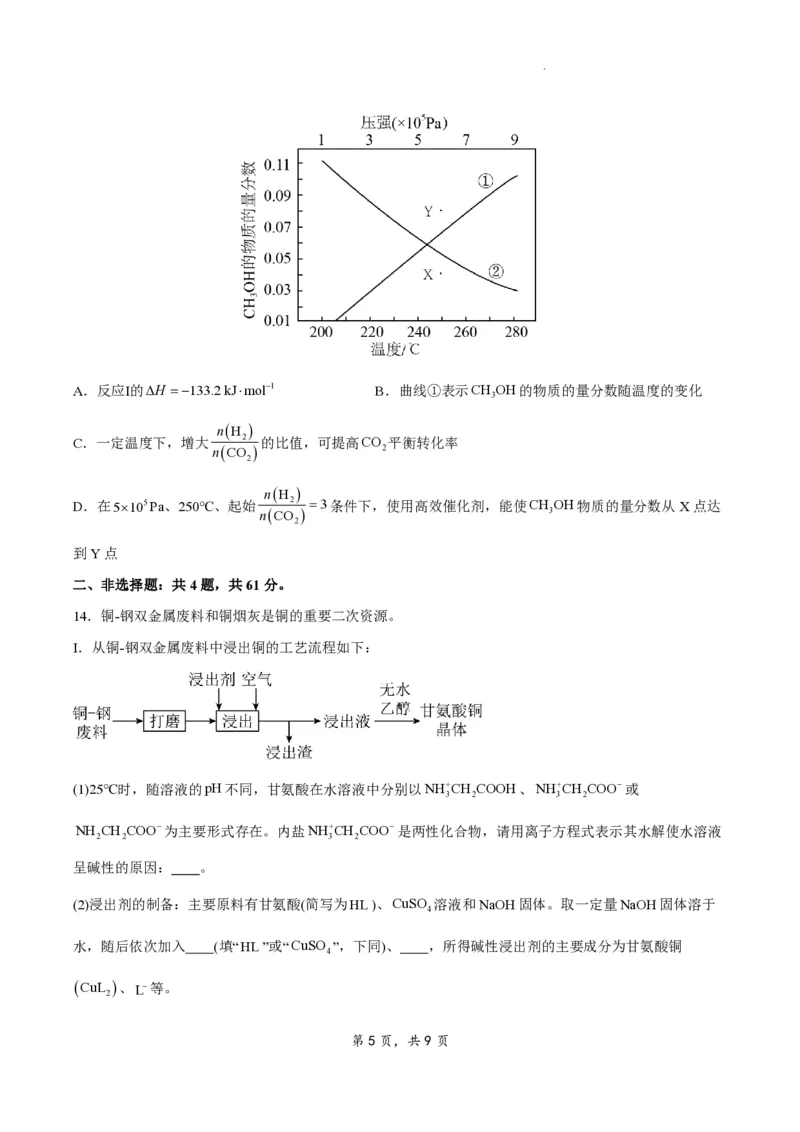
13.通过反应Ⅰ:CO g3H gƒ CH OHgH Og可以实现CO 捕获并资源化利用。密闭容器中,
2 2 3 2 2
nH
反应物起始物质的量比 2 3时,在不同条件下(分别在温度为250℃下压强变化和在压强为5105Pa
nCO
2
下温度变化)达到平衡时CH OH物质的量分数变化如图所示。主要反应有:
3
反应Ⅱ:CO gH gCOgH Og H 42.5kJmol1
2 2 2
反应Ⅲ:COg2H gCH OHg H 90.7kJmol1
2 3
下列说法正确的是
第4页,共9页
学科网(北京)股份有限公司A.反应Ⅰ的H 133.2kJmol1 B.曲线①表示CH OH的物质的量分数随温度的变化
3
nH
C.一定温度下,增大 2 的比值,可提高CO 平衡转化率
nCO 2
2
nH
D.在5105Pa、250℃、起始 2 3条件下,使用高效催化剂,能使CH OH物质的量分数从X点达
nCO 3
2
到Y点
二、非选择题:共4题,共61分。
14.铜-钢双金属废料和铜烟灰是铜的重要二次资源。
Ⅰ.从铜-钢双金属废料中浸出铜的工艺流程如下:
(1)25℃时,随溶液的pH不同,甘氨酸在水溶液中分别以NHCH COOH、NHCH COO或
3 2 3 2
NH CH COO为主要形式存在。内盐NHCH COO是两性化合物,请用离子方程式表示其水解使水溶液
2 2 3 2
呈碱性的原因: 。
(2)浸出剂的制备:主要原料有甘氨酸(简写为HL)、CuSO 溶液和NaOH固体。取一定量NaOH固体溶于
4
水,随后依次加入 (填“HL”或“CuSO ”,下同)、 ,所得碱性浸出剂的主要成分为甘氨酸铜
4
CuL 、L等。
2
第5页,共9页
学科网(北京)股份有限公司(3)浸出:将经打磨的铜钢废料投入浸出剂,控制温度50℃,通入空气,并搅拌。浸出剂不与钢作用,但
与铜反应,最终铜全部转化为CuL 进入溶液,从而实现铜、钢分离。
2
①浸出时发生的反应过程为CuL Cu2L 2CuL、 。
2 2
②其它条件不变时,空气流量对铜浸出速率的影响如图1所示。当空气流量超过1.0Lmin1时,铜浸出速
率急剧下降的可能原因是 。
Ⅱ.从铜烟灰(主要成分为Cu(OH)Cl、FeO、Fe O、Zn PO )中回收铜的主要步骤为:酸浸→萃取→反
2 3 3 4 2
萃取→电解。
已知:Zn PO 溶于无机酸。
3 4 2
(4)酸浸:将铜烟灰用硫酸浸出,控制其他条件相同,铜浸出率与温度的变化关系如图2所示。随温度升
高,铜浸出率先增大后减小的可能原因是 。
(5)萃取、反萃取:向浸出液(Cu2浓度为7g/L)中加入有机萃取剂(RH)萃取,其原理可表示为:Cu2(水
层)2RH(有机层)ƒ R Cu(有机层)2H(水层)。
2
向萃取所得有机相中加入硫酸,反萃取得到水相(Cu2浓度达40g/L)。该工艺中设计萃取、反萃取的目的
是 。
15.F是一种抗血小板凝聚的药物,其人工合成路线如图:
(1)D分子中采取sp3杂化的碳原子数目是 。
(2)B的一种同分异构体同时满足下列条件,写出该同分异构体的结构简式: 。
第6页,共9页
学科网(北京)股份有限公司①分子中有4种不同化学环境的氢原子;
②苯环上有2个取代基,能发生银镜反应。
(3)E→F中有一种相对分子质量为60的产物生成,该产物的结构简式为 ,实验室中如需确定此
产物中含有的官能团,通常使用的分析仪器设备名称为 。
(4)A→B的反应需经历 的
过程,中间体Y的分子式为C H NF,X→Y的反应类型为 。
11 12
(5)已知: ,写出以 、(CH CO) O、
3 2
和NBS为原料制备 的合成路线流程图 (无机
试剂和有机溶剂任用,合成路线示例见本题题干)。
16.以硫酸烧渣(主要成分为Fe O 和少量Fe O 、Al O 、SiO 等)为原料制备氧化铁红的工艺流程如下:
2 3 3 4 2 3 2
已知:Fe3 3H C O FeC O 36H,Fe2 H C O FeC O 2H。
2 2 4 2 4 3 2 2 4 2 4
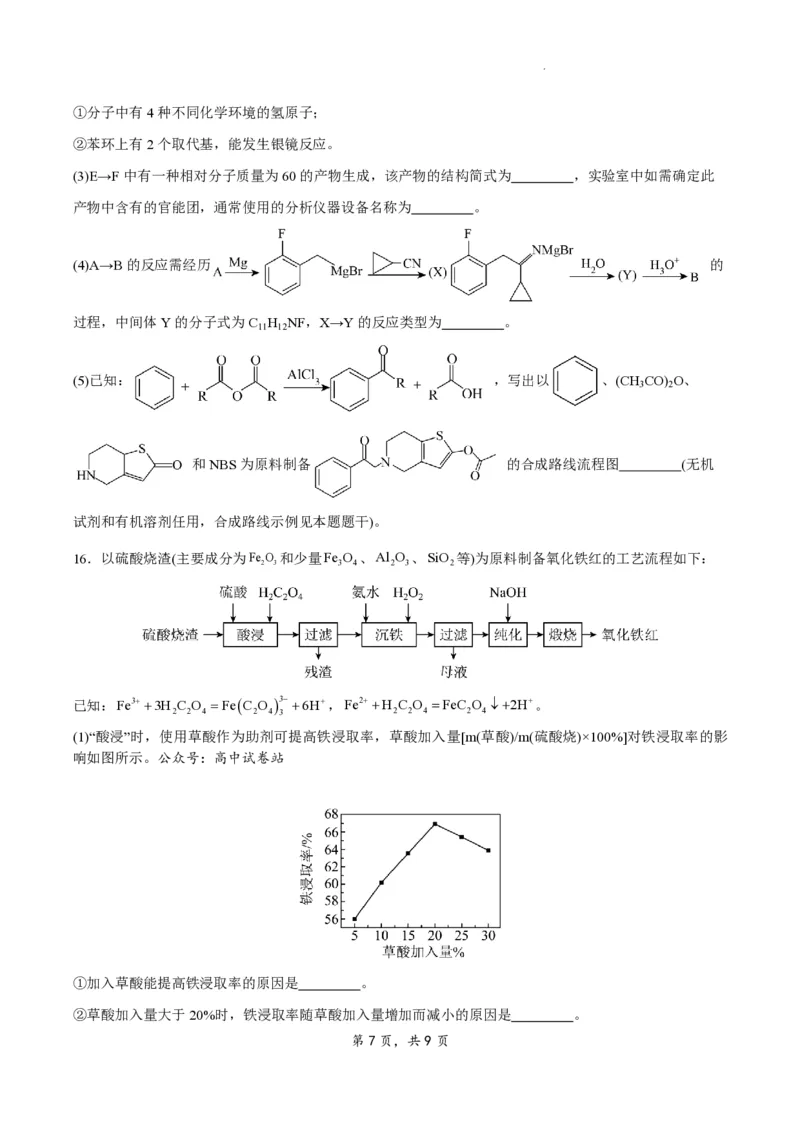
(1)“酸浸”时,使用草酸作为助剂可提高铁浸取率,草酸加入量[m(草酸)/m(硫酸烧)×100%]对铁浸取率的影
响如图所示。公众号:高中试卷站
①加入草酸能提高铁浸取率的原因是 。
②草酸加入量大于20%时,铁浸取率随草酸加入量增加而减小的原因是 。
第7页,共9页
学科网(北京)股份有限公司(2)“沉铁”时,反应温度对铁回收率的影响如图所示。
①FeSO 转化为FeOH 的离子方程式为 。
4 3
②反应温度超过
第8页,共9页
学科网(北京)股份有限公司
35℃时,铁回收率下降的原因是 。
③“沉铁”后过滤所得“母液”中含有的主要成分为硫酸铵和 。
(3)“纯化”时,加入 NaOH 溶液的目的是 。
17.研发二氧化碳利用技术、降低空气中二氧化碳含量成为研究热点。
(1)减少碳排放的方法有很多,CO
2
转化成有机化合物可有效实现碳循环,如下反应:
a 光合作用 6CO +6H O C H O . +6O
2 2 6 12 6 2
b 催化剂 CO +3H CH OH+H . O
2 2 加热 3 2
c 催化剂 2CO +6H CH =CH +4H . O
2 2 加热 2 2 2
上述反应中原子利用率最高的是 (填编号)。
(2) CO
2
在固体催化表面加氢合成甲烷过程中发生以下两个反应:
主反应: ˆ ˆ CO
2
(g)+4H
2
(g) ‡ ˆ†ˆ CH
4
(g)+2H O(g)
2
Δ H
1
=-156.9kJ mol-1
副反应: ˆ ˆ CO
2
(g)+H
2
(g) ‡ ˆ†ˆ CO(g)+H O(g)
2
ΔH
2
=+41.1kJ mol-1
已知: 2H
2
(g)+O
2
(g)=2H O(g)
2
ΔH
3
=-395.6kJ mol-1 ,
则
CH
4 燃烧的热化学方程式
CH
4
(g)+2O
2
(g)=CO
2
(g)+2H O(g)
2
ΔH=
。公众号:高中试卷
站
(3)利用电化学方法通过微生物电催化将CO 有效地转化为H C O ,装置如图1所示。阴极区电极反应式
2 2 2 4
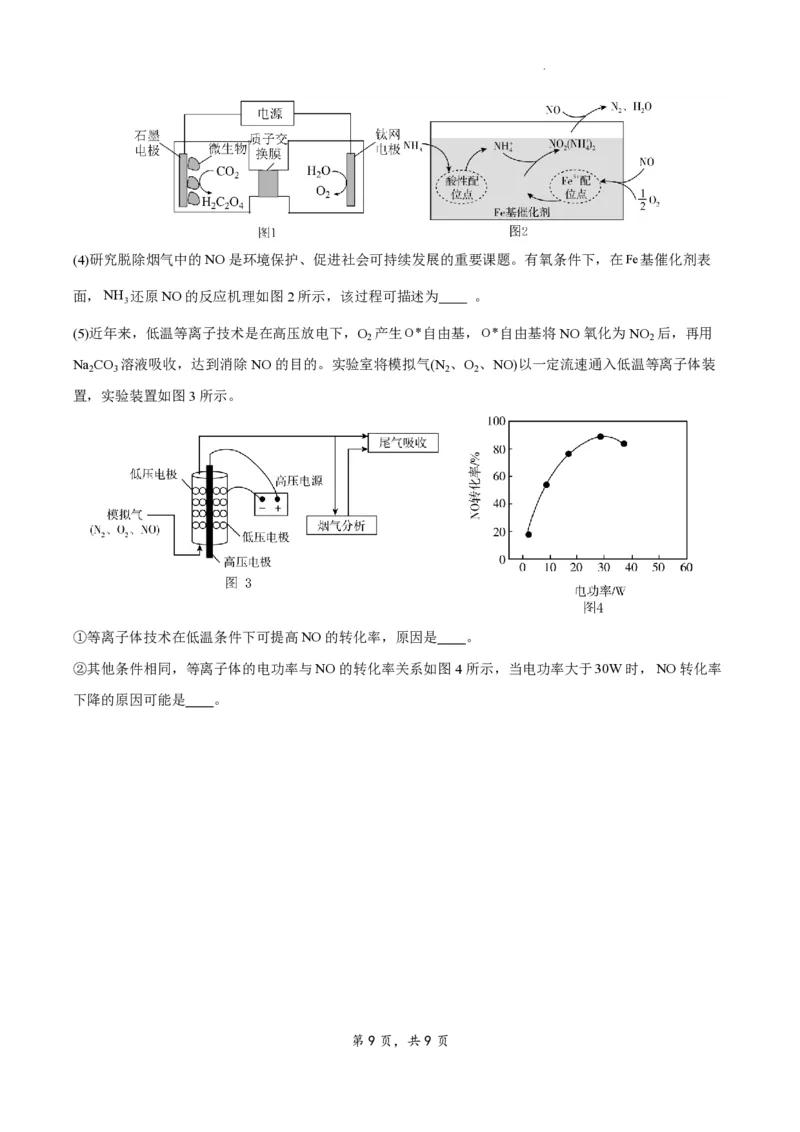
为 ;当体系的温度升高到一定程度,电极反应的速率反而迅速下降,其主要原因是 。(4)研究脱除烟气中的NO是环境保护、促进社会可持续发展的重要课题。有氧条件下,在Fe基催化剂表
面,NH 还原NO的反应机理如图2所示,该过程可描述为 。
3
(5)近年来,低温等离子技术是在高压放电下,O 产生O*自由基,O*自由基将NO氧化为NO 后,再用
2 2
Na CO 溶液吸收,达到消除NO的目的。实验室将模拟气(N 、O 、NO)以一定流速通入低温等离子体装
2 3 2 2
置,实验装置如图3所示。
①等离子体技术在低温条件下可提高NO的转化率,原因是 。
②其他条件相同,等离子体的电功率与NO的转化率关系如图4所示,当电功率大于30W时,NO转化率
下降的原因可能是 。
第9页,共9页
学科网(北京)股份有限公司