文档内容
平许济洛 2023—2024 学年高三第一次质量检测
化 学
注意事项:
1.答题前,考生务必将自己的姓名、考号、考试科目涂写在答题卡上。
2.考试结束,将答题卡交回。
可能用到的相对原子质量 H 1 C 12 N 14 O 16 Si 28 Ca 40 Ni 58.7
一、选择题:本题共10小题,每小题2分,共20分。在每小题给出的四个选项中,只有一项是符合
题目要求的。
1.中原文化源远流长,化学与文化传承密不可分。下列说法错误的是
A.冬凌草中含有谷氨酸等,可合成人体所需蛋白质
B.玛瑙是汝瓷的主要原料之一,其主要成分为二氧化硅
C.为减轻酸雨对龙门石窟的腐蚀,应采取措施改善周边能源结构
D.制作传统手工蚕丝绒球所用的原料是蚕丝,其主要成分为纤维素
2.下列消毒剂的有效成分属于盐的是
A.高锰酸钾溶液 B.过氧乙酸溶液 C.双氧水 D.医用酒精
3.下列各组物质中,属于弱电解质的是
A. NaOH B. CH₃COOH C. BaSO₄ D. C₂H₅OH
4.下列物质中,既含有氯离子,又含有氯分子的是
A.液氯 B.氯化钠溶液 C.新制氯水 D.漂白粉
5.下列应用中涉及到氧化还原反应的是
A.使用苏打去除碗筷油污 B.雪天道路上撒盐融雪
C.食品包装袋内放置一小包铁粉 D.霓虹灯发出五颜六色的光
6.下列反应中生成H₂的速率最快的是
金属 酸溶液 温度
A Mg 0.5 mol·L⁻' H₂SO₄ 20 ℃
B Fe 1m ol·L⁻¹ HCl 20 ℃
C Zn 2m ol·L⁻¹ HCl 20 ℃
D Mg 1 mol·L⁻¹ H₂SO₄ 30 ℃
7.下列反应的离子方程式错误的是
A.将氨气通入水中: N H +H O=N H++OH−
3 2 4
B.盐酸中滴加 Na₂SiO₃溶液: SiO2−+2H+=H SiO ↓
3 2 3
C. Al₂O₃溶于 NaOH溶液: Al O +2OH−+3H O=2Al(OH) −
2 3 2 4
D.将少量铜屑放入浓硝酸中: Cu+4H++2NO−=Cu2++2NO ↑+2H O
3 2 2
8.将lg氯气完全分解为氮气、氢气时,吸收2.72 kJ的热量,下列热化学方程式正确的是
①N₂(g)+3H₂(g)===2NH₃(g) △H= -46.2 kJ/mol
②N₂(g)+3H₂(g)===2NH₃(g) ΔH=-92.4 kJ/mol
学科网(北京)股份有限公司1 3
N H (g)= N (g)+ H (g) ΔH= +46.2 kJ/mol
1 2 2 2 2
④2NH₃(g)===N₂(g)+3H₂(g) ΔH= -92.4 kJ/mol
A.①② B.①②③ C.②③ D.全部
9.关于1.5m ol H₂O₂,下列说法正确的是
A、摩尔质量是34 g B.含有3 mol H
C.含氧原子数目约为 1.806×10²³个 D.含有15 mol 电子
10.在恒容密闭容器中发生反应: 3FeO(s)+H O(g)600KFe O (s)+H (g),下列能说明该条件
2 3 4 2
下反应已达到化学平衡的是
B.容器内的压强不再变化 A.v (H O)=v (H )
iE 2 iE 2
C.混合气体总的物质的量不再变化
D.单位时间内断裂H—O键个数是断裂H—H键个数的2倍
二、选择题:本题共10小题,每小题3分,共30分。在每小题给出的四个选项中,只有一项是符合
题目要求的。
11.氚管是一种应用在深海夜光手表中的发光装置。其主要结构是在一个密闭玻璃管中充入氚气,
由氚在β衰变时释放出的电子射中涂在玻璃管内部的荧光粉,发出荧光。下列说法错误的是
A.氚原子核内中子数为2 B.β衰变属于化学变化
C.|H、D、T互为同位素 D.含有氚的废水具有放射性
12.维生素C又称抗坏血酸(Ascorbic Acid),因其具有直接的肺保护作用,可增加肺泡上皮的屏障
功 能 , 上 海 等 地 将 维 生 素 C 列 为 新 冠 肺 炎 预 防 药 品 。 已 知 25 ℃ 时 , 维 生 素 C 的
Kₐₓ=6.76×10⁻⁵,H₂CO₃的 K =4.5×10−7。下列说法错误的是
a
1
A.分子中含有3种官能团
B.与五元环相连的三个氧原子不在同一平面上C.位置1、2的羟基易被氧化生成脱氢抗坏血酸
D.向盛有 NaHCO₃ 粉末的试管中加入维生素 C溶液,可观察到粉末逐渐消失,并有气泡产生
13. NA为阿伏伽德罗常数的值,下列说法正确的是
A.342g蔗糖完全水解生成葡萄糖的分子数为 2N
A
B.标准状况下,22.4 L单质溴中含溴原子数为2N
A
C.44g环氧乙烷(分子式为C₂H₄O)含C―O键数目为N
A
D.1m ol Fe 与足量含 HCl的FeCl₃溶液充分反应,转移电子数为2N
A
14.用如图所示装置进行下列实验:将①中液休滴入②中,预测的现象与实际相符的是
选项 ①中物质 ②中物质 预测②中的现象
固体逐渐变黑,产生刺激性气
A 浓硫酸 蔗糖
味气体
B 浓盐酸 二氧化锰 产生黄绿色气体
Fe粉、Cu 粉混合
C 稀醋酸 产生气泡,溶液逐渐变蓝
物
D AlCl₃溶液 浓氨水 无明显现象
学科网(北京)股份有限公司15.短周期主族元素X、Y、Z、W原子序数依次增大,基态X原子s轨道上的电子数和p轨道上的电
子数相等,Y是迄今发现的非金属性最强的元素,Z的3s轨道半充满,W与X属于同一主族。下列说法正
确的是
A.元素X、W的简单阴离子具有相同的电子层结构
B.由Y、Z两种元素组成的化合物是离子化合物
C.简单气态氢化物的热稳定性:W>Y
D.原子半径:r(X) ol⋅L⁻¹(列出计算式即可)。
m
(5)“沉镍”时的离子方程式为 。
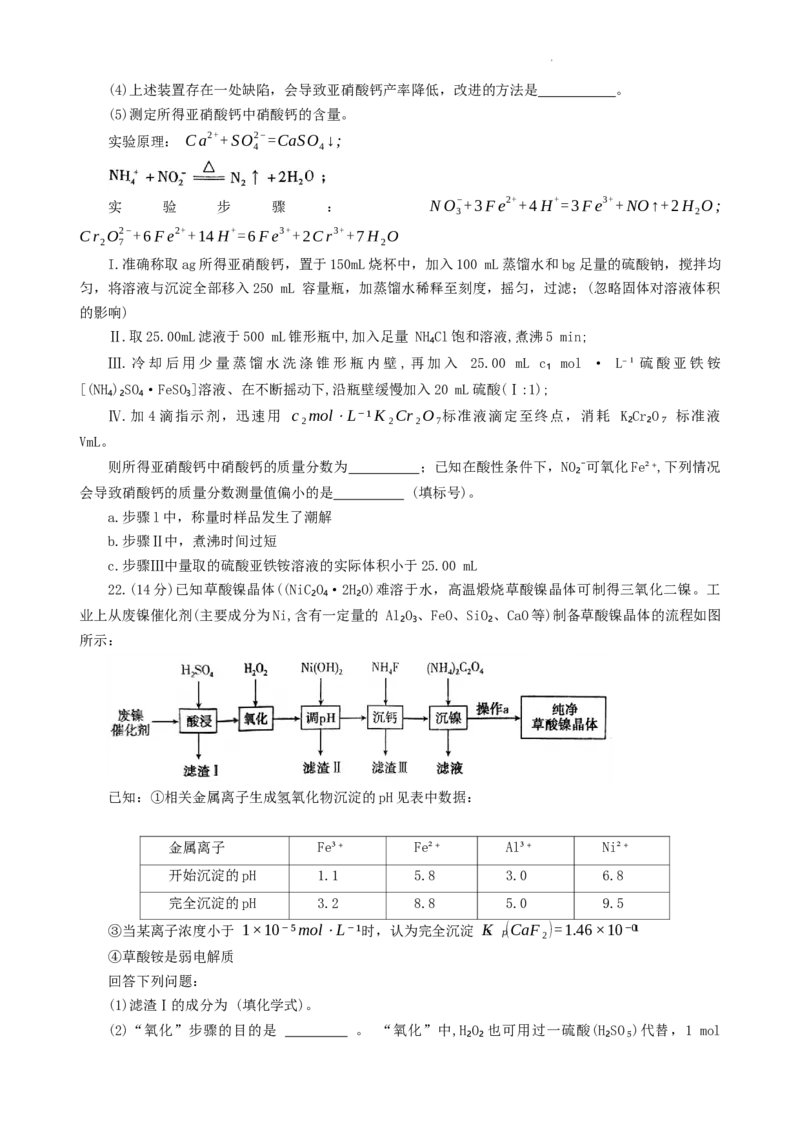
(6)操作a包含过滤、用乙醇洗涤、110 ℃下烘干等步骤,其中用乙醇洗涤的目的是洗去杂质和
。
(7)NiC₂O₄·2H₂O(式量为182.7)高温煅烧制取三氧化二镍的热重曲线如图所示,则温度为 T₂时,固
体产物化学式为 。
23、(12 分)重铬酸钾(K₂Cr₃O₇)又名红矾钾,是化学实验室中的一种重要分析试剂,在工业上用途
广泛。已知水溶液中存在平衡:(С 。 请 回 答 下
列问题:
(1)复分解法制备重铬酸钾
以Na₂CrO₄溶液为原料,步骤如下:
①先向 Na₂CrO₄溶液中加入酸调节溶液pH,其目的是 。
②再向①的溶液中加入适量KCl,搅拌溶解、蒸发浓缩、冷却结晶,抽滤得到 K₂Cr₂O₇粗产品。则相
同温度时的溶解度:Na₂Cr₂O₇ K₂Cr₂O₇(填“﹥”“﹤”或“=”)。
(2)电化学法制备重铬酸钾
以净化后的铬酸钾(K₂CrO₄)为原料,用电化学法制备重铬酸钾的实验装置如图所示。
①不锈钢电极的电极反应式为 。
②阳极区能得到重铬酸钾溶液的原因是 。
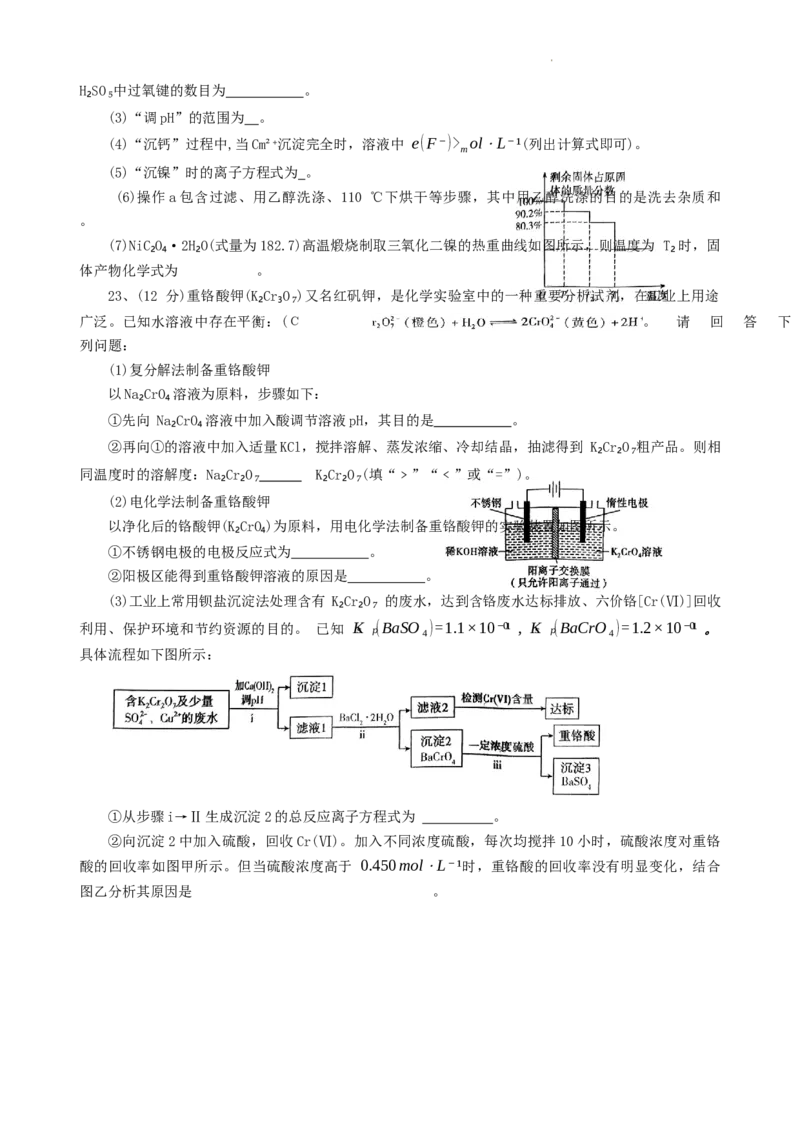
(3)工业上常用钡盐沉淀法处理含有 K₂Cr₂O₇ 的废水,达到含铬废水达标排放、六价铬[Cr(Ⅵ)]回收
利用、保护环境和节约资源的目的。 已知 Kₛ ₚ(BaSO₄)=1.1×10⁻⁰¹ , Kₛ ₚ(BaCrO₄)=1.2×10⁻⁰¹ 。
具体流程如下图所示:
①从步骤i→Ⅱ生成沉淀2的总反应离子方程式为 。
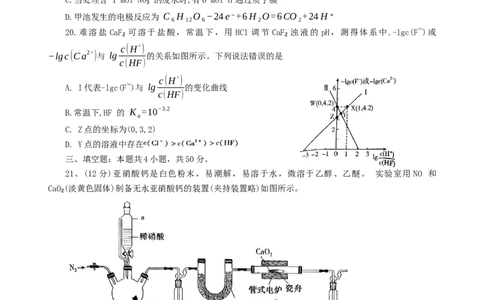
②向沉淀2中加入硫酸,回收Cr(Ⅵ)。加入不同浓度硫酸,每次均搅拌10小时,硫酸浓度对重铬
酸的回收率如图甲所示。但当硫酸浓度高于 0.450mol⋅L⁻¹时,重铬酸的回收率没有明显变化,结合
图乙分析其原因是 。
学科网(北京)股份有限公司24.(12 分)氮氧化物对环境及人类活动影响日趋严重,如何消除大气污染物中的氮氧化物成为人们
关注的主要问题之一。
Ⅰ.利用 NH₃的还原性可以消除氮氧化物的污染,其中除去 NO 的主要反应如下:
已知:N₂(g)+O₂(g)===2NO(g) ΔH₁= +182.4 kJ·mol⁻¹
4NH₃(g)+4NO(g)+O₂(g)===4N₂(g)+6H₂O(l) ΔH₃
(1)ΔH₃= 。
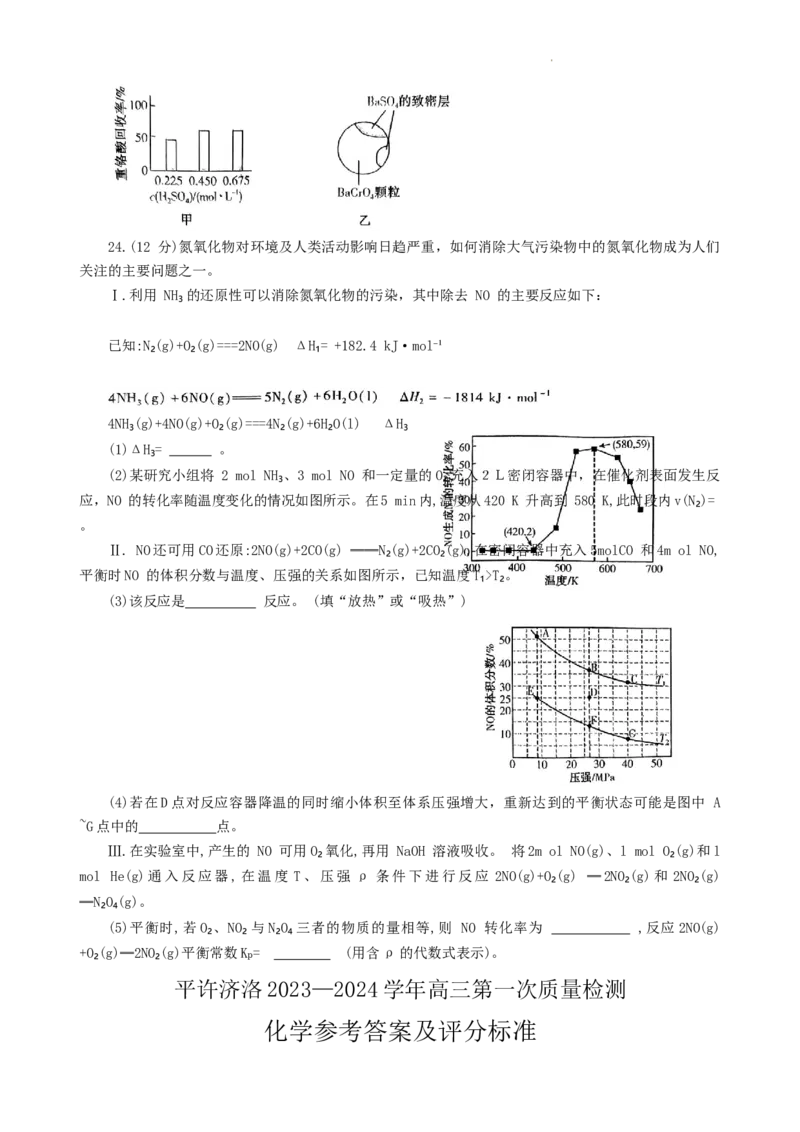
(2)某研究小组将 2 mol NH₃、3 mol NO 和一定量的O₂充入2L密闭容器中,在催化剂表面发生反
应,NO 的转化率随温度变化的情况如图所示。在5 min内,温度从420 K 升高到 580 K,此时段内v(N₂)=
。
Ⅱ. NO还可用CO还原:2NO(g)+2CO(g) ══N₂(g)+2CO₂(g),在密闭容器中充入5molCO 和4m ol NO,
平衡时NO 的体积分数与温度、压强的关系如图所示,已知温度T₁>T₂。
(3)该反应是 反应。 (填“放热”或“吸热”)
(4)若在D点对反应容器降温的同时缩小体积至体系压强增大,重新达到的平衡状态可能是图中 A
~G点中的 点。
Ⅲ.在实验室中,产生的 NO 可用O₂氧化,再用 NaOH 溶液吸收。 将2m ol NO(g)、l mol O₂(g)和l
mol He(g)通入反应器,在温度 T、压强 ρ 条件下进行反应 2NO(g)+O₂(g) ═2NO₂(g)和 2NO₂(g)
═N₂O₄(g)。
(5)平衡时,若O₂、NO₂与N₂O₄三者的物质的量相等,则 NO 转化率为 ,反应2NO(g)
+O₂(g)═2NO₂(g)平衡常数Kₚ= (用含ρ的代数式表示)。
平许济洛 2023—2024 学年高三第一次质量检测
化学参考答案及评分标准
学科网(北京)股份有限公司评卷说明:1.简答题学生只要回答出最核心的要点即可给分。学生多答只要无错误不扣分。
2.方程式化学式正确给1分,配平给1分,条件和状态符号不占分。
一、选择题(每小题2分,共20分)
题号 1 2 3 4 5 6 7 8 9 10
答案 D A B C C D A C B D
二、选择题(每小题3分,共30分)
题号 11 12 13 14 15 16 17 18 19 20
答案 B B D A B A D D C D
三、填空题(共50分)
21.(12分,每空2分)
(1)平衡滴液漏斗与三颈烧瓶中的压强,便于液体顺利流下
(2)2NO+3H O 2H++2NO−+2H O
2 2 3 2
(3)排出装置内残留的氮的氧化物,防止污染空气。(或:加速无水亚硝酸钙的冷却)
(4)在装置D、E之间加装盛有浓硫酸的洗气瓶(答案合理即可)
82(25c −6c V)
(5) 1 2 %;a
3a
22.(14 分)
(1)SiO₂、CaSO₄(2分,写对一个给1分)
(2)将 Fe²⁺全部氧化为Fe³⁺,以便于除去。(1分) N (或 6.02×10²³)(1分)
A
(3)5.0≤pH<6.8(2分)
√1.46×10−10
(4) (或 √14.6×10−3 )(2分)
1.0×10−5
(5)Ni2++(N H ) C O +2H O=∋C O ⋅2H O↓+2N H+(2分)
4 2 2 4 2 2 4 2 4
(6)便于快速干燥(已知草酸镍晶体难溶于水,若只从减少溶质损失角度答0分)(2分)
(7)NiC₂O₄(2分)
23.(12分,每空2分)
(1)①将 Na₂CrO₄转化为 Na₂Cr₂O₇ ② >
② 阳极上 H₂O 放电,溶液中H⁺浓度增大,使 CrO2−转化为 Cr O2−,部分K⁺通过阳离子交
4 2 7
换膜移动到阴极区,使阳极区溶液的主要溶质变为K₂Cr₂O₇ (2)2H₂O+2e⁻=2OH⁻+H₂↑
(3)①Cr O2−+2OH−+2Ba2+=2BaCrO ↓+H O[Ca(OH) 不拆也给分]
2 7 4 2 2
②生成的 BaSO₄难溶于水,会覆盖在 BaCrO₄固体的表面,阻碍反应的进行。
学科网(北京)股份有限公司24.(12分,每空2分)
(3)放热 (1)−1631.6kJ⋅mol⁻¹ (2)0.171mol⋅L⁻¹⋅min⁻¹
(4)G
15
(5)60%
8p
学科网(北京)股份有限公司