文档内容
2.1 第二课时 钠的几种化合物 练习(解析版)
1.下列叙述正确的是 ( )。
A.Na O与Na O 都能与水反应生成碱,它们都是碱性氧化物
2 2 2
B.Na CO 溶液和NaHCO 溶液都能与CaCl 溶液反应得到白色沉淀
2 3 3 2
C.钠在常温下不容易被氧化
D.Na O 可作供氧剂,而Na O不行
2 2 2
解析 Na O 不属于碱性氧化物,A错;B项NaHCO 与CaCl 溶液不反应,得不到白色沉
2 2 3 2
淀;C项Na在常温下很容易被空气中的O 氧化。
2
答案 D
2.有两个无标签的试剂瓶,分别装有Na CO 和NaHCO ,有4位同学为鉴别它们采用了以下
2 3 3
不同的方法,其中不可行的是 ( )。
A.分别配成溶液,再加入澄清石灰水
B.分别配成溶液,再加入CaCl 溶液
2
C.分别加热,再检验是否有使澄清石灰水变浑浊的气体产生
D.分别取固体样品,滴加同浓度盐酸,观察产生气泡的快慢
解析 A项中的石灰水与Na CO 和NaHCO 皆能发生反应产生CaCO 沉淀;B项中CaCl
2 3 3 3 2
与NaHCO 不反应,与 Na CO 反应产生CaCO 沉淀;C项加热时,只有 NaHCO 受热分
3 2 3 3 3
解,2NaHCO =====Na CO +H O+CO ↑,产生的CO 能使澄清石灰水变浑浊,故可用
3 2 3 2 2 2
来鉴别;D项NaHCO 与盐酸反应速率比Na CO 快。
3 2 3
答案 A
3.对于反应:2Na O +2H O===4NaOH+O ↑,下列说法中正确的是 ( )。
2 2 2 2
A.Na O 是氧化剂,H O是还原剂
2 2 2
B.Na O 既是氧化剂,又是还原剂
2 2
C.该反应中电子转移的数目为4e-
D.氧气是还原产物
解析 略
答案 B
4. (1)Na CO 固体中混有少量 NaHCO 固体,除去杂质的方法是________,化学方程式是
2 3 3
___________________________________。
(2)NaHCO 固体中混有少量 Na CO 固体,除杂方法是________,化学方程式是
3 2 3________________________________________________________。
(3)NaOH 固体中混有少量 Na CO 固体,除杂方法是________,反应的离子方程式是
2 3
_______________________________________________________。
答案 (1)加热 2NaHCO =====Na CO +H O+CO ↑
3 2 3 2 2
(2)配成溶液,通入CO 后常温风干 Na CO +CO +H O===2NaHCO
2 2 3 2 2 3
(3)加适量石灰水,过滤,蒸发滤液 Ca2++CO===CaCO ↓
3
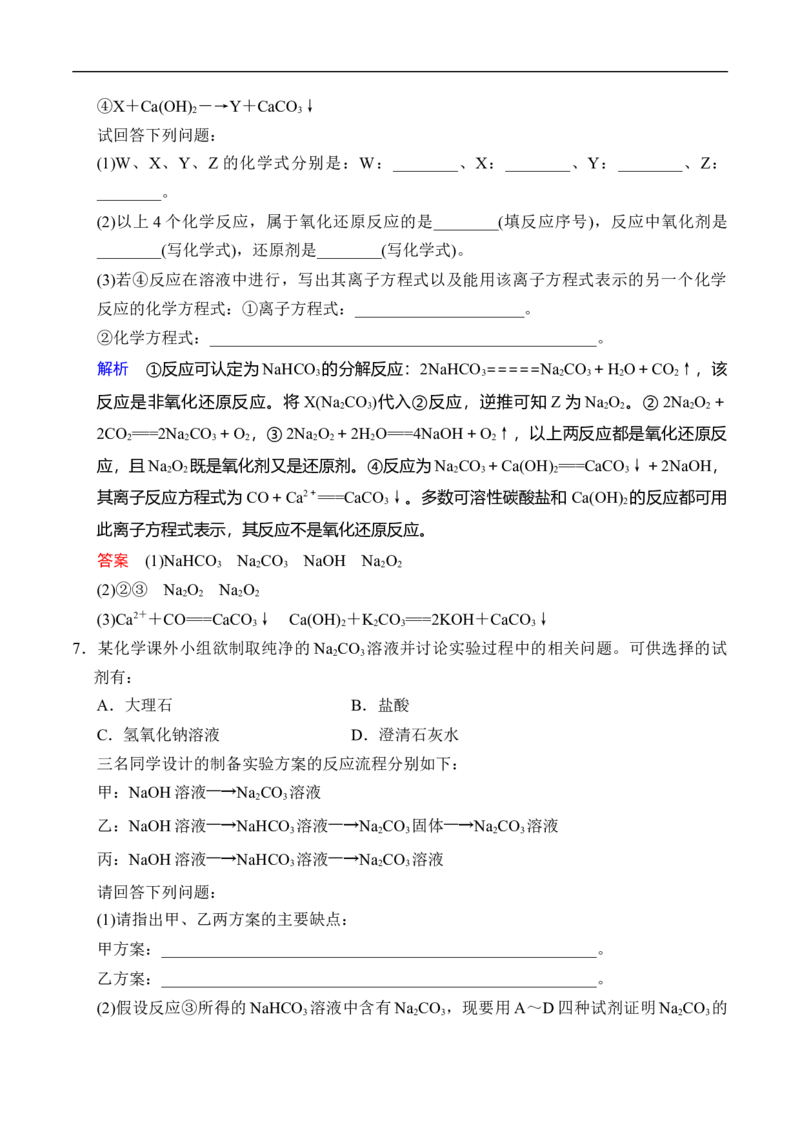
5.为了制取纯净干燥的气体A,可用如图所示装置,生成A的速度可通过滴入液体B的速度
控制,已知A是一种无色、无味、不能使酸碱指示剂变色、也不会在空气中燃烧的气体,
但能使带火星的木条复燃。
(1)A是________。
(2)若C是一种淡黄色固体,则烧瓶中发生反应的化学方程式是___________。
(3)若C是一种黑色粉末,则B物质是________,C物质的作用是___________。
(4)洗气瓶(广口瓶)中装的试剂D是________,其作用是________________。所制得的气体
用________法收集。
解析 无色、无味且不燃烧的气体主要有O 、N 、稀有气体,而能使带火星的木条复燃
2 2
的气体只能是氧气。可用淡黄色固体(Na O )与水反应制得O ,也可由黑色固体(MnO )和
2 2 2 2
液体(H O )作用制得。由于上述方法制得的氧气都是在水溶液中制得的,所以要得到干燥
2 2
纯净的O 则应干燥后再收集。
2
答案 (1)O
2
(2)2Na O +2H O===4NaOH+O ↑
2 2 2 2
(3)H O 催化剂
2 2
(4)浓硫酸 除去O 中的水蒸气 向上排空气
2
6.(11分)有4种钠的化合物W、X、Y、Z它们之间存在如下关系:
①W――→X+H O+CO ↑
2 2
②Z+CO ―→X+O
2 2
③Z+H O―→Y+O ↑
2 2④X+Ca(OH) ―→Y+CaCO ↓
2 3
试回答下列问题:
(1)W、X、Y、Z 的化学式分别是:W:________、X:________、Y:________、Z:
________。
(2)以上4个化学反应,属于氧化还原反应的是________(填反应序号),反应中氧化剂是
________(写化学式),还原剂是________(写化学式)。
(3)若④反应在溶液中进行,写出其离子方程式以及能用该离子方程式表示的另一个化学
反应的化学方程式:①离子方程式:_____________________。
②化学方程式:________________________________________________。
解析 ①反应可认定为NaHCO 的分解反应:2NaHCO =====Na CO +H O+CO ↑,该
3 3 2 3 2 2
反应是非氧化还原反应。将 X(Na CO )代入②反应,逆推可知 Z 为 Na O 。② 2Na O +
2 3 2 2 2 2
2CO ===2Na CO +O ,③2Na O +2H O===4NaOH+O ↑,以上两反应都是氧化还原反
2 2 3 2 2 2 2 2
应,且Na O 既是氧化剂又是还原剂。④反应为Na CO +Ca(OH) ===CaCO ↓+2NaOH,
2 2 2 3 2 3
其离子反应方程式为CO+Ca2+===CaCO ↓。多数可溶性碳酸盐和 Ca(OH) 的反应都可用
3 2
此离子方程式表示,其反应不是氧化还原反应。
答案 (1)NaHCO Na CO NaOH Na O
3 2 3 2 2
(2)②③ Na O Na O
2 2 2 2
(3)Ca2++CO===CaCO ↓ Ca(OH) +K CO ===2KOH+CaCO ↓
3 2 2 3 3
7.某化学课外小组欲制取纯净的 Na CO 溶液并讨论实验过程中的相关问题。可供选择的试
2 3
剂有:
A.大理石 B.盐酸
C.氢氧化钠溶液 D.澄清石灰水
三名同学设计的制备实验方案的反应流程分别如下:
甲:NaOH溶液――→Na CO 溶液
2 3
乙:NaOH溶液――→NaHCO 溶液――→Na CO 固体――→Na CO 溶液
3 2 3 2 3
丙:NaOH溶液――→NaHCO 溶液――→Na CO 溶液
3 2 3
请回答下列问题:
(1)请指出甲、乙两方案的主要缺点:
甲方案:______________________________________________________。
乙方案:______________________________________________________。
(2)假设反应③所得的NaHCO 溶液中含有Na CO ,现要用A~D四种试剂证明Na CO 的
3 2 3 2 3存在,你所选择的试剂有________________。
解析 (1)NaOH与CO 反应时两者量不同,产物不同,2OH-+CO ===CO+H O,OH-+
2 2 2
CO ===HCO,甲不能控制通入CO 的物质的量,也就不能控制产物为纯净的Na CO 。乙
2 2 2 3
的操作程序复杂。丙应将NaOH溶液分成两等份,一份通入足量 CO ,加热赶出其中溶解
2
的CO ,再将另一份NaOH溶液与NaHCO 溶液混合即可得到纯净的Na CO 溶液。
2 3 2 3
(2)检验NaHCO 溶液中含有Na CO ,应向溶液中加入BaCl 或CaCl ,所以应选盐酸和澄
3 2 3 2 2
清石灰水,二者生成CaCl 再检验。
2
答案 (1)由于难以控制CO 的量,故很难得到纯净的Na CO 原料利用率低,程序复杂
2 2 3
(2)BD