文档内容
2.2.2 氯气的制取 练习(解析版)
1.下列叙述正确的是( )
A.氯气的性质很活泼,它与氢气混合后立即发生爆炸
B.可以用氢氧化钙溶液吸收实验室制取氯气时多余的氯气
C.检验Cl 中是否混有HCl方法是将气体通入硝酸银溶液
2
D.除去Cl 中的HCl气体,可将气体通入饱和食盐水
2
【答案】D
【解析】氯气与氢气混合只有点燃或强光照射才会发生反应甚至爆炸,A项错误;由于氢氧化钙的溶
解度比较小,所以实验室制取氯气时,多余的氯气不用氢氧化钙溶液吸收,而是用氢氧化钠溶液吸收,B
项错误;Cl 溶于水也会产生Cl-,所以C项错误;HCl气体易溶于水,也易溶于饱和食盐水,而Cl 在饱
2 2
和食盐水中的溶解度极小,D项正确。
2.下列离子方程式错误的是( )
A.实验室制Cl:MnO +4H++2Cl- Mn2++Cl↑+2HO
2 2 2 2
B.在NaCl溶液中滴入AgNO 试液:Ag++Cl-===AgCl↓
3
C.Cl 溶于水:Cl+HO===2H++Cl-+ClO-
2 2 2
D.用NaOH溶液吸收Cl∶Cl+2OH-===Cl-+ClO-+HO
2 2 2
【答案】C
【解析】本题中HClO是弱电解质应写成分子形式,C项错误。
3.检验某未知溶液中是否含有氯离子(Cl-),正确的操作是( )
A.向未知溶液中加入AgNO 溶液,有白色沉淀产生
3
B.向未知溶液中加入AgNO 溶液,有白色沉淀产生, 加入盐酸,沉淀不消失
3
C.向未知溶液中加入稀硝酸酸化后,再加入AgNO 溶液,有白色沉淀产生
3
D.向未知溶液中加入稀盐酸酸化后,再加入AgNO 溶液,有白色沉淀产生
3
【答案】C
【解析】A操作不正确,它不能排除CO的干扰;B操作不正确,因为Ag CO 跟HCl反应时,生成的
2 3
AgCl仍是白色沉淀;C操作正确;D操作用盐酸酸化,加入了Cl-,无法确定原溶液中是否有Cl-。
4.某同学用下列装置制备并进行有关Cl 的实验。
2下列说法中正确的是( )
A.Ⅰ图中:如果MnO 过量,浓盐酸就可全部消耗
2
B.Ⅱ图中:闻Cl 的气味
2
C.Ⅲ图中:生成蓝色的烟
D.Ⅳ图中:若气球干瘪,证明Cl 可与NaOH反应
2
【答案】B
【解析】MnO 与浓盐酸反应时,会出现酸变稀而导致反应中止的情况,因此 A中浓盐酸不可能全部
2
消耗;Cl 有毒,闻其气味时应用手轻轻在瓶口扇动,仅使极少量气体飘入鼻中;Cu丝在Cl 中燃烧生成棕
2 2
黄色烟;若Cl 能与NaOH溶液反应,瓶内压强减小,气球就会鼓起。
2
5.下列关于实验室用MnO 制取Cl 的叙述不正确的是( )
2 2
A.MnO 与浓盐酸共热
2
B.缓慢加热反应
C.用向下排空气法收集Cl
2
D.多余氯气常用较浓的碱液吸收
【答案】C
【解析】由于浓盐酸易挥发,故必须缓慢加热以减少HCl的挥发;Cl 的密度比空气的密度大,故应用
2
向上排空气法收集Cl;Cl 极易与碱反应:Cl+2NaOH===NaCl+NaClO+HO,故应用较浓的碱液吸收多
2 2 2 2
余的Cl。
2
6.氯仿(CHCl )可用作麻醉剂,常因保存不慎而被空气氧化产生剧毒物质 COCl (光气)和氯化氢,为防
3 2
止事故发生,使用前要检验氯仿是否变质,应选用的检验试剂是( )
A.水 B.AgNO 溶液
3
C.NaOH溶液 D.KI溶液
【答案】B
【解析】氯仿氧化后生成COCl (光气)和HCl,因此,用AgNO 溶液检验HCl中Cl-的存在即可判断氯
2 3
仿是否变质。
7.实验室制氯气时有如下操作,操作顺序正确的是( )
①连接好装置,检查气密性;②缓缓加热;③在烧瓶中加入少量的MnO ,向分液漏斗中加入浓盐酸;
2④通过分液漏斗慢慢向烧瓶中注入浓盐酸;⑤将多余氯气用浓NaOH溶液吸收;⑥当有连续气泡出现时,
开始用向上排空气法收集氯气。
A.①②③④⑤⑥ B.③④②①⑥⑤
C.①④③②⑥⑤ D.①③④②⑥⑤
【答案】D
【解析】实验室制取氯气的实验步骤为:先连接好装置,检查装置的气密性,加试剂(先固体后液体),
缓缓加热,收集气体,尾气处理。
8.在未知液中加入AgNO 溶液有白色沉淀生成,加入稀硝酸后,沉淀部分溶解,有无色无味的气体
3
生成,将气体通入澄清石灰水中,澄清石灰水变浑浊,由此判断未知液中含有( )
A.Cl-、SO B.Cl-、NO
C.Cl-、CO D.Cl-、OH-
【答案】C
【解析】能使澄清石灰水变浑浊的无色无味气体应是CO ,又因为加入稀HNO 后沉淀部分溶解,故
2 3
原溶液中除含有CO外,还有Cl-。
9.已知KMnO 与浓盐酸在常温下反应生成Cl 。若用如图所示的实验装置来制备纯净、干燥的Cl ,
4 2 2
并试验它与金属的反应。每个虚线框表示一个单元装置,其中有错误的是( )
A.①和②处 B.②处
C.②和③处 D.②③④处
【答案】D
【解析】②中的NaOH溶液与Cl 反应,Cl 被吸收;③中的内部左边的导气管过短,右边的导气管过
2 2
长,这样Cl 不能通过该瓶;④中试管中只有进气管没有出气管,Cl 不能进入试管,且缺少加热装置酒精
2 2
灯。
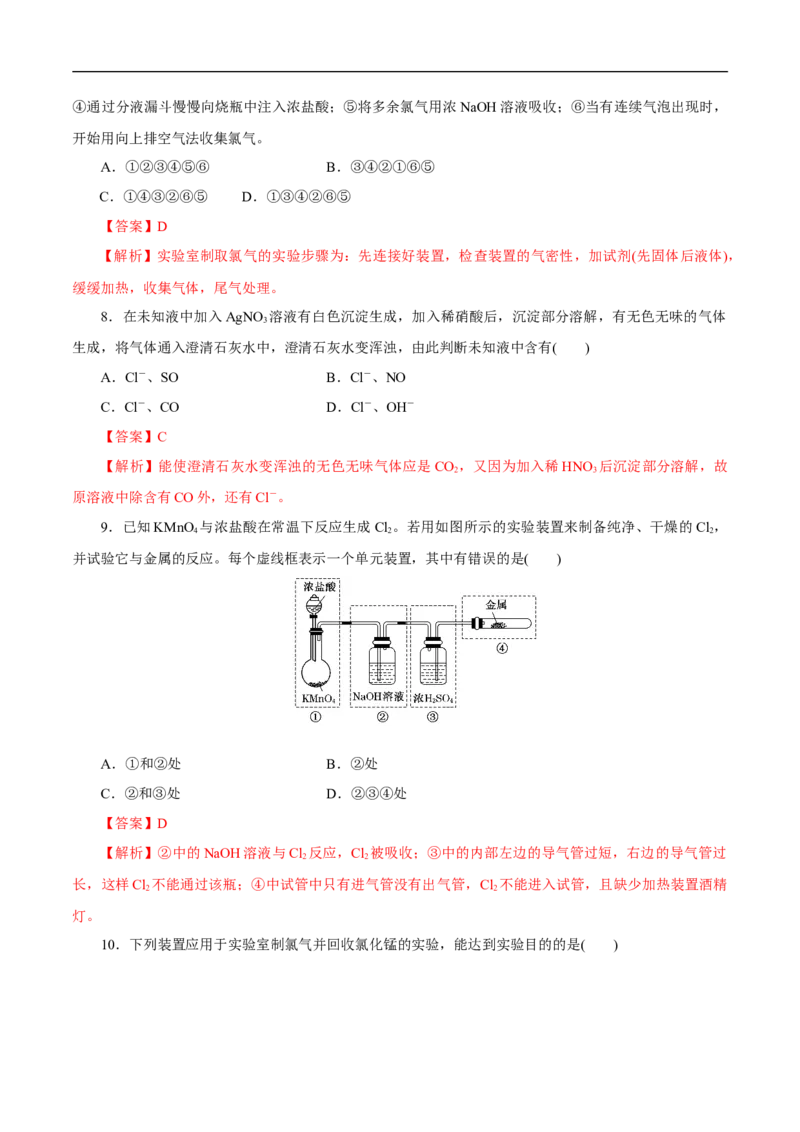
10.下列装置应用于实验室制氯气并回收氯化锰的实验,能达到实验目的的是( )A.用装置甲制取氯气
B.用装置乙除去氯气中混有的少量氯化氢
C.用装置丙分离二氧化锰和氯化锰溶液
D.用装置丁蒸干氯化锰溶液制MnCl ·4H O
2 2
【答案】C
【解析】A项,二氧化锰和浓盐酸制备氯气需要加热,甲装置没有加热仪器,错误;B项,饱和碳酸
氢钠溶液能吸收氯气,但NaHCO 和HCl反应能生成CO ,引入新的杂质气体,所以吸收试剂应该为饱和
3 2
食盐水,并且洗气瓶气体流向为长导气管进短导气管出,错误;C项,二氧化锰不溶于水,氯化锰易溶于
水,因此分离二氧化锰和氯化锰溶液需要过滤,正确;D项,若蒸干氯化锰溶液可能得不到MnCl ·4H O,
2 2
错误。
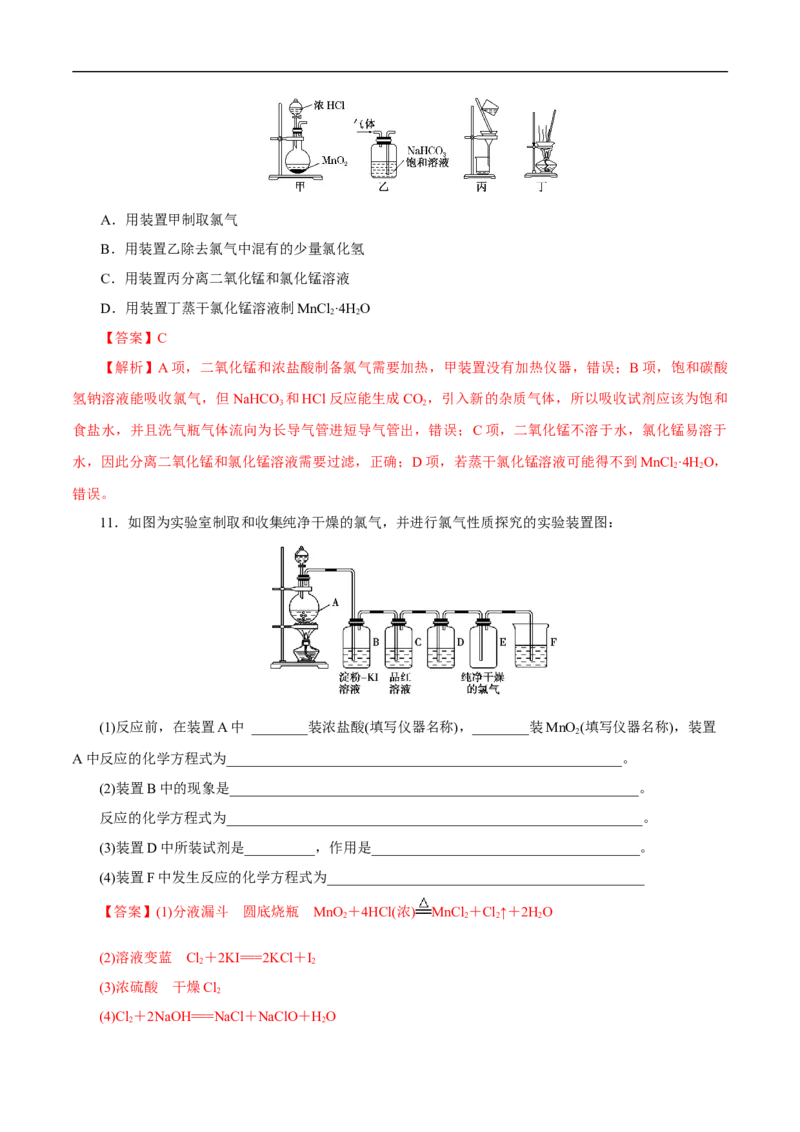
11.如图为实验室制取和收集纯净干燥的氯气,并进行氯气性质探究的实验装置图:
(1)反应前,在装置A中 ________装浓盐酸(填写仪器名称),________装MnO (填写仪器名称),装置
2
A中反应的化学方程式为________________________________________________________。
(2)装置B中的现象是__________________________________________________________。
反应的化学方程式为___________________________________________________________。
(3)装置D中所装试剂是__________,作用是______________________________________。
(4)装置F中发生反应的化学方程式为_____________________________________________
【答案】(1)分液漏斗 圆底烧瓶 MnO +4HCl(浓) MnCl +Cl↑+2HO
2 2 2 2
(2)溶液变蓝 Cl+2KI===2KCl+I
2 2
(3)浓硫酸 干燥Cl
2
(4)Cl +2NaOH===NaCl+NaClO+HO
2 2【解析】(1)实验室中常用MnO 与浓盐酸在加热条件下制取Cl,其中MnO 放入圆底烧瓶中,浓盐酸
2 2 2
放入分液漏斗中,反应的化学方程式为MnO +4HCl(浓) MnCl +Cl↑+2HO。
2 2 2 2
(2)Cl 与KI发生反应Cl+2KI===2KCl+I,淀粉遇I 变蓝色。
2 2 2 2
(3)干燥Cl 应用浓硫酸作干燥剂。
2
(4)多余Cl 一般用NaOH溶液吸收。
2
12.某溶液中可能含有K+、Na+、CO、Cl-中的一种或几种,为鉴别其中所含离子,现进行如下实验:
序号 实验操作及现象
步骤① 取原溶液,进行焰色反应,显黄色,透过蓝色钴玻璃观察无紫色
步骤② 取原溶液,向溶液中加入盐酸,有气体产生
请回答下列问题:
(1)原溶液中一定存在的离子是________(填离子符号,下同),一定不存在的离子是________,可能存
在的离子是________。
(2)为进一步确定原溶液中可能存在的离子是否存在,应进行的实验操作及判断依据是
________________________________________________________________________
【答案】(1)Na+、CO K+ Cl-
(2)取原溶液,向溶液中加入AgNO 溶液,有白色沉淀生成,再加入足量稀HNO ,若白色沉淀不消失,
3 3
则原溶液中存在Cl-,若白色沉淀消失,则原溶液中不存在Cl-
【解析】由步骤①确定原溶液中含有Na+不含有K+,由步骤②确定原溶液中含有CO。但不能判断原
溶液中是否含有Cl-,需要用AgNO 和稀HNO 检验Cl-的存在。
3 3
13.实验室里用如图所示仪器和药品来制取纯净的无水氯化铜(Cu+Cl CuCl )。图中A、B、C、
2 2
D、E、F表示玻璃管接口,接口的弯曲和伸长等部分未画出。根据要求填写下列各小题空白。
(1)如果所制气体从左向右流向时,上述各仪器装置的正确连接顺序是(填各装置的序号)( )接(
)接( )接( )接( )接( ),其中②与④装置相连时,玻璃管接口(用装置中字母表示)应
是________接________。
(2)装置②的作用是_______________________________________________________;装置④的作用是__________________________________________________________。
(3)实验开始时,应首先检验装置的________,实验结束时,应先熄灭________处的酒精灯。
(4)在装置⑤的烧瓶中,发生反应的化学方程式为________________________________
【答案】(1)③ ⑤ ④ ② ① ⑥ C B
(2)除去Cl 中的水蒸气 除去Cl 中的HCl气体
2 2
(3)气密性 ①
(4)MnO +4HCl(浓) MnCl +Cl↑+2HO
2 2 2 2
【解析】制取纯净的无水CuCl ,应由Cu和纯净的Cl 加热制得,欲制得纯净的氯气需③和⑤组合制
2 2
得Cl ,再经④洗去Cl 中的氯化氢,经过②除去水蒸气,最后排出的尾气用碱液吸收以防止多余的 Cl 污
2 2 2
染环境。