文档内容
3.1.1 强电解质和弱电解质 弱电解质的电离平衡
练习(解析版)
1.下列属于强电解质的是( )
A.H SO B.NH Cl C.CH COOH D.Cu
2 3 4 3
【答案】B
【解析】A.H SO 属于弱酸,在水溶液中部分电离的电解质,属于弱电解质,故A错误;
2 3
B.NH Cl是盐,在水溶液中能完全电离的电解质,属于强电解质,故B正确;
4
C.醋酸属于弱酸,在水溶液中部分电离的电解质,属于弱电解质,故C错误;
D.铜是单质,不是电解质,故D错误;故选:B。
2.下列物质中,属于弱电解质的是( )
A.CH COOH B.Na CO C.H SO D.NaOH
3 2 3 2 4
【答案】A
【解析】A、CH COOH属于弱酸,在水溶液里能部分电离,所以是弱电解质,故A正确;
3
B、Na CO 在水溶液里完全电离,所以是强电解质,故B错误;
2 3
C、H SO 属于强酸,在水溶液里完全电离,所以是强电解质,故C错误;
2 4
D、NaOH属于强碱,在水溶液里完全电离,所以是强电解质,故D错误。故选:A。
3.下列有关表述正确的是( )
A.HClO是弱酸,所以NaClO是弱电解质
B.向溶有氨气的CaCl 溶液中通SO 能看到白色沉淀
2 2
C.室温下,AgCl在水中的溶解度小于在食盐水中的溶解度
D.Na O、Na O 组成元素相同,所以与CO 反应产物也相同
2 2 2 2
【答案】B
【解析】A.两种物质的类别不同,相同条件下电离程度不同,NaClO是钠盐完全电离是强电解质,
故A错误;
B.因为有氨气,所以可以发生:2NH +H O+CaCl +SO =2NH Cl+CaSO ↓,故B正确;
3 2 2 2 4 3
C.根据同离子效应,相同离子可以降低该物质的溶解度,AgCl在水中的溶解度大于在食盐水中的
溶解度 故C错误;
D.Na O与CO 反应生成碳酸钠,Na O 与CO 反应生成碳酸钠和氧气,故D错误;故选:B。
2 2 2 2 2
4.下列有关电解质的说法正确的是( )
A.强电解质一定是离子化合物
B.易溶性强电解质的稀溶液中不存在溶质分子C.强电解质溶液的导电能力一定比弱电解质强
D.由于硫酸钡难溶于水,所以硫酸钡是弱电解质
【答案】B
【解析】A.强电解质不一定为离子化合物,如硫酸、硝酸等共价化合物属于强电解质,故A错误;
B.由于强电解质完全电离,则易溶性强电解质的稀溶液中不会存在溶质分子,故B正确;
C.由于溶液导电性与导电离子浓度大小有关,则强电解质溶液的导电能力不一定比弱电解质强,
故C错误;
D.硫酸钡难溶于水,但溶于水的硫酸钡完全电离,则硫酸钡属于强电解质,故 D错误;故选:
B。
5.下列电离方程式中正确的是( )
A.Fe(OH) Fe3++3OH﹣ B.H CO H++CO 2﹣
3 2 3 3
C.NaHCO N⇌a++H++CO 2﹣ D.Na SO⇌ SO 2﹣+2Na+
3 3 2 3 3
【答案】A ⇌ ⇌
【解析】A.氢氧化铁是多元弱碱,电离方程式为:Fe(OH) Fe3++3OH﹣,故A正确;
3
B.碳酸是二元弱酸,分步电离,以第一步电离为主,电离方程⇌式为:H CO H++HCO ﹣,HCO ﹣
2 3 3 3
H++CO 2﹣,故B错误; ⇌
3
⇌C.碳酸氢钠溶液中电离生成钠离子和碳酸氢根离子,电离方程式为:NaHCO =Na++HCO ﹣,故
3 3
C错误;
D.亚硫酸钠是盐,完全电离出钠离子和亚硫酸根离子,电离方程式为:Na SO =SO 2﹣+2Na+,故
2 3 3
D错误;故选:A。
6.下列电离方程式中,错误的是( )
A.Al (SO ) ═2Al3++3SO 2﹣
2 4 3 4
B.HCO ﹣+H O CO 2﹣+H O+
3 2 3 3
C.HI H++I﹣ ⇌
D.Cu⇌(OH) Cu2++2OH﹣
2
【答案】C ⇌
【解析】A.硫酸铝属于盐,在水中或熔融状态下完全电离出铝离子和硫酸根离子,电离方程式为:
Al (SO ) ═2Al3++3SO 2﹣,故A正确;
2 4 3 4
B.碳酸氢根离子属于弱酸碳酸的酸式盐的酸根部分,部分电离,电离方程式为: HCO ﹣
3
+H O CO 2﹣+H O+,或HCO ﹣ CO 2﹣+H+,故B正确;
2 3 3 3 3
C.H⇌I是强酸,完全电离,电离⇌方程式为HI═H++I﹣,故C错误;
D.氢氧化铜为弱碱,电离方程式:Cu(OH) Cu2++2OH﹣,故D正确;故选:C。
2
⇌7.能证明乙酸是弱酸的实验事实是( )
A.CH COOH溶液与Zn反应放出H
3 2
B.1mol•L﹣1CH COONa溶液的pH大于7
3
C.CH COOH溶液与Na CO 反应生成CO
3 2 3 2
D.0.1mol•L﹣1CH COOH溶液可使紫色石蕊变红
3
【答案】B
【解析】A.醋酸和Zn反应生成氢气说明醋酸为酸,不能说明醋酸部分电离,则不能证明醋酸是
弱酸,故A错误;
B.0.1mol/LCH COONa溶液的PH值大于7,该盐水溶液显碱性,由于NaOH是强碱,故可以证明乙
3
酸是弱酸,故B正确;
C.CH COOH溶液与Na CO 反应生成CO ,可以证明乙酸的酸性比碳酸强,但是不能证明其酸性
3 2 3 2
强弱,故C错误;
D.0.1mol/LCH COOH溶液可使紫色石蕊变红,可以证明乙酸具有酸性,但是不能证明其酸性强弱,
3
故D错误。故选:B。
8.下列事实能说明某一元酸HA是强电解质的是( )
A.常温下NaA溶液的pH=7
B.HA溶液能使紫色石蕊试液变红
C.用HA溶液和NaCl溶液做导电性实验,灯泡亮度相同
D.等体积、等物质的量浓度的HA与NaOH溶液两者恰好完全反应
【答案】A
【解析】A.常温下NaA溶液的pH=7,溶液呈中性,说明NaA是强酸强碱盐,则HA是强电解质,
故A正确;
B.HA溶液能使紫色石蕊试液变红色,说明HA电离出氢离子而使溶液呈酸性,但是不能说明HA
完全电离,所以不能说明HA是强电解质,故B错误;
C.溶液导电性强弱与离子浓度有关,与电解质强弱无关,两种溶液浓度相对大小未知,所以无法
判断HA是强电解质,故C错误;
D.等体积、等物质的量浓度的HA与NaOH溶液两者恰好完全反应说明HA是一元酸,不能说明
HA是强电解质,故D错误;故选:A。
9.能证明硅酸的酸性弱于碳酸酸性的实验事实是( )
A.CO 溶于水形成碳酸,SiO 难溶于水
2 2
B.高温下SiO 与碳酸盐反应生成CO
2 2
C.HCl通入可溶性碳酸盐溶液中放出气体,通入可溶性硅酸盐溶液中生成沉淀D.CO 通入可溶性硅酸盐中析出硅酸沉淀
2
【答案】D
【解析】A.不能根据CO 、SiO 的水溶性比较酸性强弱,故A错误;
2 2
B.比较强酸制取弱酸时在溶液中进行的反应,则在高温下固体之间的反应不能得到酸性强弱的结
论,故B错误;
C.HCl通入可溶性碳酸盐溶液中放出气体,通入可溶性硅酸盐溶液中生成沉淀,证明酸性:盐酸
>碳酸、盐酸>硅酸,无法比较碳酸和硅酸的酸性强弱,故C错误;
D . CO 通 入 可 溶 性 硅 酸 盐 中 析 出 硅 酸 沉 淀 , 发 生 反 应 为 : Na SiO +H O+CO =
2 2 3 2 2
Na CO +H SiO ↓,该反应为强酸制弱酸,可证明碳酸比硅酸酸性强,故D正确;故选:D。
2 3 2 3
二.解答题(共5小题)
10.Ⅰ.现有下列物质: NaCl晶体 BaSO 熔融K SO Na CO 溶液 液态氯化氢 醋
4 2 4 2 3
酸溶液 石灰水 石墨① NH •H O ②酒精 ③CO NaOH溶④液. ⑤ ⑥
3 2 2
请将序⑦号分别填入⑧下面的⑨横线处: ⑩ ⑪ ⑫
(1)上述状态下可导电的是________________________。
(2)属于强电解质的是____________。
Ⅱ.写出下列物质在水溶液中的电离方程式。
(3)Ca(OH) :_____________;
2
(4)NaHCO :_____________;
3
(5)KAl(SO ) :________________________;
4 2
(6)NH •H O:___________。
3 2
【答案】Ⅰ.(1) ;
(2) ;③④⑥⑦⑧⑫
Ⅱ.(3①)②Ca(③O⑤H)
2
=Ca2++2OH﹣;
(4)NaHCO =Na++HCO ﹣;
3 3
(5)KAl(SO ) =K++Al3++2SO 2﹣ ;
4 2 4
(6)NH 3•H
2
O NH
4
++OH﹣。
【解析】Ⅰ. ⇌NaCl晶体不含自由电子,也不含自由移动的离子,不导电;水溶液中或者熔融状态
下能完全电离①,属于强电解质;
BaSO 不含自由电子,也不含自由移动的离子,不导电;熔融状态下能完全电离,属于强电解质;
4
②熔融K
2
SO
4
含自由移动的离子,导电;水溶液中或者熔融状态下能完全电离,属于强电解质;
③Na
2
CO
3
溶液,含自由移动的离子,导电;是混合物,不是电解质;
④液态氯化氢,不含自由电子,也不含自由移动的离子,不导电;水溶液中能完全电离,属于强
⑤电解质;
醋酸溶液含自由移动的离子,导电;是混合物,不是电解质;
⑥石灰水含自由移动的离子,导电;是混合物,不是电解质;
⑦石墨是单质,含有自由电子,能导电;不是电解质;
⑧NH
3
•H
2
O,不含自由电子,也不含自由移动的离子,不导电;水溶液能部分电离产生自由移动
⑨的离子,属于弱电解质;
酒精,不含自由电子,也不含自由移动的离子,不导电;是非电解质;
⑩CO
2
不含自由电子,也不含自由移动的离子,不导电;是非电解质;
⑪NaOH溶液,含自由移动的离子,导电;是混合物,不是电解质;
⑫所以:(1)上述状态下可导电的是: ,
故答案为: ; ③④⑥⑦⑧⑫
(2)属于强③电④解⑥质的⑦是⑧:⑫ ,
故答案为: ; ①②③⑤
Ⅱ.(3)氢①氧②化③钙⑤为强电解质,完全电离产生钙离子、氢氧根离子,电离方程式:Ca(OH)
2
=
Ca2++2OH﹣,
故答案为:Ca(OH) =Ca2++2OH﹣;
2
(4)碳酸氢钠为强电解质,水溶液中完全电离产生钠离子、碳酸氢根离子,电离方程式:NaHCO
3
=Na++HCO ﹣,
3
故答案为:NaHCO =Na++HCO ﹣;
3 3
(5)硫酸铝钾为强电解质,水溶液中完全电离产生钾离子、铝离子、硫酸根离子,电离方程式:
KAl(SO ) =K++Al3++2SO 2﹣,
4 2 4
故答案为:KAl(SO ) =K++Al3++2SO 2﹣;
4 2 4
(6)一水合氨为弱电解质,水溶液中部分电离生成铵根离子、氢氧根离子,电离方程式:
NH 3•H
2
O NH
4
++OH﹣,
故答案为⇌:NH 3•H
2
O NH
4
++OH﹣。
11.现有6种物质:⇌ NaCl晶体 液态SO
3
液态的醋酸 汞 BaSO
4
固体 酒精. 请
用序号回答下列问①题: ② ③ ④ ⑤ ⑥
(1)属于强电解质的是_____________;
(2)属于弱电解质的是_____________;
(3)属于非电解质的是_____________.
【答案】(1) ; (2) ; (3) .
【解析】 Na①Cl⑤晶体在水溶液里③或熔融状态②下能⑥完全电离出自由离子而导电,属于强电解质;
①液态SO 本身不能电离,是化合物,属于非电解质;
3
②液态的醋酸在水溶液里只能部分电离出自由离子而导电,属于弱电解质;
③汞是单质,既不是电解质,也不是非电解质;
④BaSO
4
固体在水溶液里或熔融状态下能完全电离出自由离子而导电,属于强电解质;
⑤酒精在水溶液里和熔融状态下都不能导电的化合物,属于非电解质;
⑥所以:1)属于强电解质的是 ;
(2)属于弱电解质的是 ;①⑤
(3)属于非电解质的是③ ;
故答案为:(1) ;② ⑥ (2) ; (3) .
12.现有十种物质①:⑤ 水 石墨③ 氯气 ②⑥硫酸钡晶体 醋酸 二氧化碳 氨水
氯化钠固体 ①熔化的②氯化钠 ③ 氯化④钠溶液. ⑤ ⑥ ⑦
⑧请用序号按要求填⑨空: ⑩
(1)其中能导电的是________________;
(2)属于强电解质的是________________,属于弱电解质的是________________;
(3)属于非电解质的是________________;
(4)既不是电解质也不是非电解质的是_________________.
【答案】(1) ;(2) ; ;(3) ;(4) .
【解析】(1)②⑦石墨⑨ ⑩氨水 熔④化⑧的⑨氯化①钠⑤氯化钠溶⑥液中均有自②由③移⑦动⑩的离子,所以能导电;
故答案为: ② ;⑦ ⑨ ⑩
(2)强电解②质⑦,⑨包括⑩强酸、强碱、大部分盐, 硫酸钡晶体 氯化钠固体 熔化的氯化钠属于强
电解质,弱电解质再水溶液中部分电离,包括弱④酸、弱碱和水⑧, 水 醋⑨酸属于弱电解质,故答
案为: ; ; ① ⑤
(3)非④电⑧解⑨质包括①一⑤些非金属氧化物、氨气、大多数有机物(如蔗糖、酒精等), 二氧化碳属
于非电解质,故答案为: ; ⑥
(4)根据电解质、非电解⑥质的定义分析,二者必须是化合物的范畴,单质和混合物都不符合,
石墨 氯气属于单质, 氨水 氯化钠溶液属于混合物,既不是电解质也不是非电解质,故答②案
为:③ . ⑦ ⑩
13.②山西③老⑦陈⑩醋是山西省的汉族传统名产,属于中国四大名醋之一,其主要成分是醋酸。请回答下
列问题:
(1)下列说法正确的是________________。
A.向某温度下的醋酸溶液中通入HCl气体,醋酸的电离常数K会增大B.向0.1 mol•L﹣1醋酸溶液中通入HCl气体或加入 CH COONa固体,溶液中 均
3
会增大
C.山西老陈醋加水稀释过程中酸味不变
D.相同体积相同浓度的醋酸溶液和盐酸分别与足量 NaHCO 反应,放出的气体体积(相同状况
3
下)相等
(2)25℃时,醋酸、碳酸和亚硫酸的电离常数如表所示。
酸 电离常数
醋酸 K=1.75×10﹣5
碳酸 K =4.30×10﹣7K =5.61×10﹣11
1 2
亚硫酸 K =1.54×10﹣2K =1.02×10﹣7
1 2
碳酸第一步电离的电离常数表达式为________________。
①在相同条件下,试比较 H
2
CO
3
、HCO
3
﹣和 HSO
3
﹣的酸性强弱:________________>
②_______________>________________。
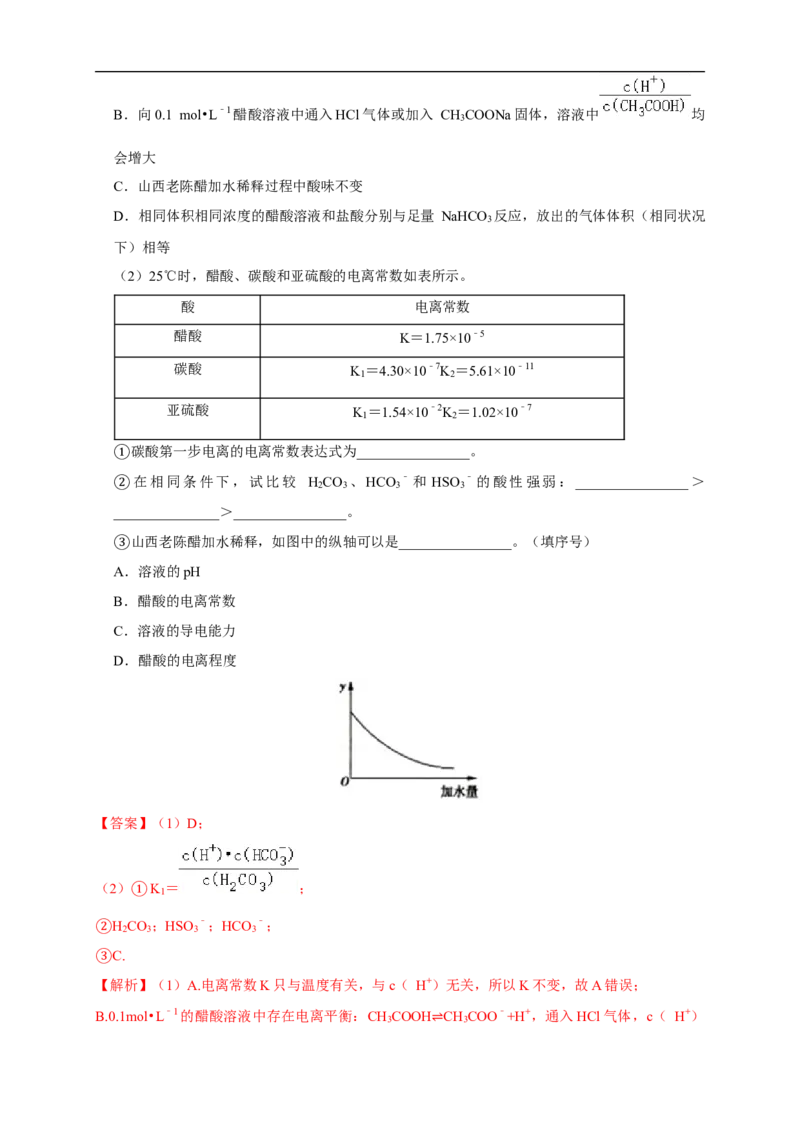
山西老陈醋加水稀释,如图中的纵轴可以是________________。(填序号)
③A.溶液的pH
B.醋酸的电离常数
C.溶液的导电能力
D.醋酸的电离程度
【答案】(1)D;
(2) K = ;
1
H C ① O ;HSO ﹣;HCO ﹣;
2 3 3 3
②C.
③【解析】(1)A.电离常数K只与温度有关,与c( H+)无关,所以K不变,故A错误;
B.0.1mol•L﹣1的醋酸溶液中存在电离平衡:CH COOH CH COO﹣+H+,通入HCl气体,c( H+)
3 3
⇌增大,平衡左移,c( CH COOH)增大的程度,所以 增大,加入 CH COONa固体,
3 3
c(CH COO﹣)增大,平衡左移,c( H+)减小,c( CH COOH)增大,所以 减小,
3 3
故B错误;
C.山西老陈醋加水稀释过程中,c( CH COOH)和c( H+)降低,酸味变淡,故C错误;
3
D.CH COOH和HCl都是一元酸,二者的溶液体积和浓度相同时,消耗的 NaHCO 的量相同,放出
3 3
的 CO 体积(相同状况下)也相等,故D正确。
2
故答案为:D;
(2) H CO 第一步电离的方程式为H CO HCO ﹣+H+,K = ,故答案为:
2 3 2 3 3 1
① ⇌
K = ;
1
相同条件下,酸的的电离常数越大,则酸性越强,故酸性强弱:H CO >HSO ﹣>HCO ﹣,故答
2 3 3 3
②案为:H CO >HSO ﹣>HCO ﹣;
2 3 3 3
老陈醋加水稀释,CH COOH电离程度增大,n( H+)增大,但c( H+)减小,因此pH增大,
3
③A、D错误;电离常数只与温度有关,因此稀释时电离常数不变,B错误;加水稀释时溶液中离子
浓度减小,溶液的导电能力降低,C正确,
故答案为:C。
14.在一定温度下,向醋酸中加水稀释,溶液导电能力变化情况如图所示,回答下列问题。
(1)“O”点时液体不能导电,说明醋酸中_______________(填“含有”或“不含”)离子键。
(2)a、b、c三点醋酸电离程度由大到小的顺序为_______________;a、b、c三点对应的溶液
中 H+浓度最大的是_______________。
(3)将等体积的a、b、c三点所对应的溶液用1mol•L﹣1氢氧化钠溶液中和,消耗氢氧化钠溶液
体积由大到小的顺序为_______________。
(4)要使 c 点溶液中 CH COO﹣浓度增大而 H+浓度减小,可采取的两种措施是
3
_______________。
(5)若实验测得c点处溶液中c(CH COOH)=0.1mol•L﹣1,c(CH COO﹣)=0.001mol•L﹣
3 3
1,则该条件下CH COOH的电离常数K=_____________________________。
3【答案】(1)不含;
(2)c>b>a;b;
(3)a>b>c;
(4)加入Zn,NaOH或CH COONa;
3
(5)1×10﹣5mol•L﹣1。
【解析】(1)“O”点时液体不能导电,说明液态条件下醋酸没有发生电离,则醋酸中没有离子
键,故答案为:不含;
(2)溶液浓度越小,电离程度越大;离子浓度越大,导电能力越强,则 a、b、c三点醋酸电离程
度由大到小的顺序为c>b>a;a、b、c三点对应的溶液中 H+浓度最大的是b,故答案为:c>b>
a;b;
(3)等体积的酸溶液浓度越大,中和时所需要的碱越多,则将等体积的a、b、c三点所对应的溶
液用1mol•L﹣1氢氧化钠溶液中和,消耗氢氧化钠溶液体积由大到小的顺序为a>b>c,故答案为:
a>b>c;
(4)要使醋酸根离子浓度增大,c(H+)减少,可以采用消耗氢离子的方法使电离平衡向正方向移
动,故可以加入Zn,NaOH等;或者增加醋酸根浓度使电离向逆方向移动,故可加CH COONa等,
3
故答案为:加入Zn,NaOH或CH COONa;
3
(5)c(CH COOH)=0.1mol•L﹣1,c(CH COO﹣)=0.001mol•L﹣1,由 CH COOH的电离方程
3 3 3
式 知 c ( H+ ) = c ( CH COO﹣ ) = 0.001mol• L﹣ 1 , 则 K = =
3
mol•L﹣1=1×10﹣5mol•L﹣1,故答案为:1×10﹣5mol•L﹣1。