文档内容
第三章 晶体结构与性质
第三节 金属晶体与离子晶体
第2课时 过渡晶体与混合型晶体、晶体类型的比较
培优第一阶——基础过关练
1.(2022·福建·莆田第十五中学高二期中)下列叙述正确的是
A.分子晶体中的每个分子内一定含有共价键
B.共价晶体中的相邻原子间只存在非极性共价键
C.离子晶体中可能含有共价键
D.金属晶体的熔点和沸点都很高
【答案】C
【详解】A.由单原子形成的分子晶体不含共价键,如稀有气体,故A错误;
B.共价晶体指原子晶体,其相邻原子间也可能是极性共价键,如SiC,故B错误;
C.离子晶体中一定含有离子键,可能含有共价键,故C正确;
D.金属晶体的熔沸点不一定都很高,如K、Na等,故D错误;
故选C。
2.(2022·浙江省杭州第九中学高二期中)下列说法不正确的是
A.Al O 是偏向离子晶体的过渡晶体,当作离子晶体来处理:SiO 是偏向共价晶体的过渡晶体,当作共价
2 3 2
晶体来处理
B.NaO 中离子键的百分数为62%,则NaO不是纯粹的离子晶体,是离子晶体与共价晶体之间的过渡晶
2 2
体
C.NaO通常当作离子晶体来处理,因为NaO是偏向离子晶体的过渡晶体,在许多性质上与纯粹的离子
2 2
晶体接近
D.分子晶体、共价晶体、金属晶体和离子晶体都有过渡型
【答案】A
【详解】A.Al O 和SiO 都是偏向共价晶体的过渡晶体,当作共价晶体来处理,故A错误;
2 3 2
B.NaO 中离子键的百分数为62%,说明NaO中存在共价键,则NaO不是纯粹的离子晶体,是离子晶
2 2 2
体与共价晶体之间的过渡晶体,故B正确;
C.离子键和共价键的本质区别是形成两元素电负性的差值,差值大为离子键,差值小为共价键,NaO通
2
常当作离子晶体来处理,因为NaO是偏向离子晶体的过渡晶体,在许多性质上与纯粹的离子晶体接近,
2
故C正确;
D.根据微粒间的作用力分析,分子晶体、共价晶体、金属晶体和离子晶体都有过渡型,故D正确;
故选A。
3.(2022·福建·莆田砺志学校高二期中)2010年诺贝尔物理学奖所指向的是碳的又一张奇妙脸孔:人类已
知的最薄材料——石墨烯。下列说法中,正确的是
A.固态时,碳的各种单质的晶体类型相同 B.石墨烯具有导电性
C.从石墨剥离得石墨烯需要破坏化学键 D.石墨烯含有极性键
【答案】B
【详解】A.碳各种单质的晶体类型不相同,如金刚石属于原子晶体,足球烯属于分子晶体,故A错误;
B.石墨烯中含有自由移动的电子,所以具有导电性,故B正确;
C.石墨中层与层间存在分子间作用力,所以从石墨剥离得到石墨烯需要破坏分子间作用力,故C错误;
D.石墨烯中碳原子间含有非极性键,故D错误;
故选:B。
4.(2022·湖北·南漳县第二中学高二阶段练习)下面的排序不正确的是
A.晶体熔点由低到高:CFMg>Al
C.硬度由大到小:金刚石>碳化硅>晶体硅
D.离子键由强到弱:MgO>CaO>NaF>NaCl
【答案】B
【详解】A.四种物质都形成分子晶体,相对分子质量越大,熔点越高,则熔点由低到高为:
CFMg >Na,则熔点由高到低为:Al>Mg >Na,故
B错误;
C.三种物质形成共价晶体,共价键的键能,C-C>C-Si>Si-Si,则硬度由大到小为:金刚石>碳化硅>晶体硅,
故C正确;
D.四种物质形成离子晶体,离子所带电荷Mg2+=Ca2+>Na+,O2->F-=Cl-,离子半径Ca2+>Na+>Mg2+,Cl->O2-
>F-,则离子键由强到弱为:MgO>CaO>NaF>NaCl,故D正确;
答案选B。
5.(2022·福建·莆田一中高二期末)下列各组物质熔化或升华时,所克服的粒子间作用属于同种类型的是
A.MgO和SiC B.Fe和S C.CO 和SiO D.碘和干冰升华
2 2
【答案】D
【详解】A.MgO是离子晶体,熔化克服离子键,SiC是共价晶体,熔化克服共价键,A错误;
B.铁是金属晶体,熔化克服金属键,硫是分子晶体,熔化克服分子间作用力,B错误;C.SiO 是共价晶体,熔化克服共价键,CO 是分子晶体,熔化克服分子间作用力,C错误;
2 2
D.碘和干冰都是分子晶体,其升华均是克服分子间作用力,D正确;
故选D。
6.下列有关化学键、氢键和范德华力的叙述中,不正确的是
A.金属键是金属阳离子与“自由电子”之间的较强作用,金属键无方向性和饱和性
B.共价键是相邻原子之间通过共用电子形成的化学键,共价键有方向性和饱和性
C.范德华力是分子间存在的一种作用力,分子的极性越大,范德华力越大
D.氢键不是化学键,而是一种分子间作用力,所以氢键只存在于分子与分子之间
【答案】D
【详解】A.金属键是化学键的一种,主要在金属中存在,由自由电子及排列成晶格状的金属离子之间的
静电吸引力组合而成,因为电子的自由运动金属键没有固定的方向,所以A选项是正确的;
B.共价键是原子之间强烈的相互作用共价键,有方向性和饱和性,所以B选项是正确的;
C.范德华力是分子间作用力,相对分子质量越大分子间作用力越大极性越大,分子间作用力越强,所以
C选项是正确的;
D.氢键是一种分子间作用力比范德华力强但是比化学键要弱,氢键既可以存在于分子间(如水、乙醇、甲
醇等),又可以存在于分子内(如 ),故D错误;
故选D。
7.(2022·甘肃·兰州一中高二期中)下列物质所属晶体类型分类正确的是
A B C D
原子晶
石墨 生石灰 碳化硅 金刚石
体
分子晶
冰 固态氨 氯化铯 干冰
体
离子晶
氮化硼 食盐 明矾 石膏
体
金属晶
铜 汞 铝 铁
体
【答案】D
【详解】A.生石灰是离子晶体,故A错误;
B.氯化铯是离子晶体,故B错误;
C.氮化硼为原子晶体,故C错误;D.铜、汞、铝、铁都为金属晶体,故D正确。
综上所述,答案为D。
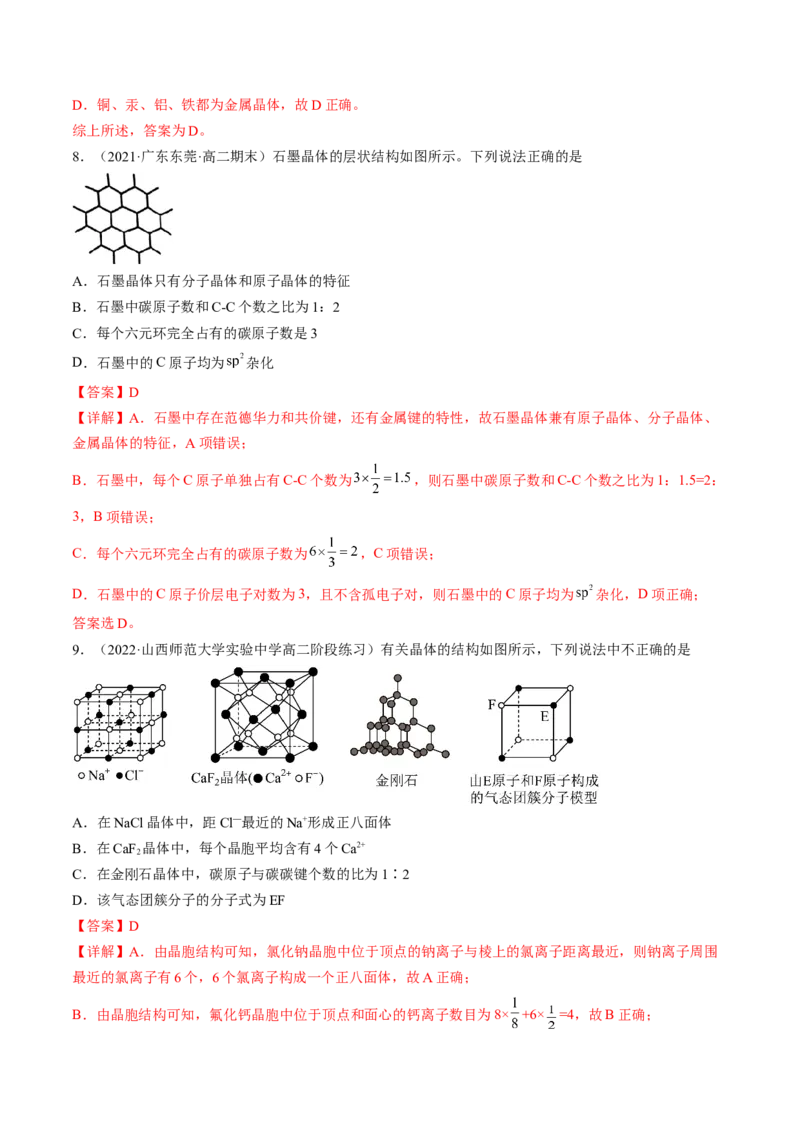
8.(2021·广东东莞·高二期末)石墨晶体的层状结构如图所示。下列说法正确的是
A.石墨晶体只有分子晶体和原子晶体的特征
B.石墨中碳原子数和C-C个数之比为1:2
C.每个六元环完全占有的碳原子数是3
D.石墨中的C原子均为 杂化
【答案】D
【详解】A.石墨中存在范德华力和共价键,还有金属键的特性,故石墨晶体兼有原子晶体、分子晶体、
金属晶体的特征,A项错误;
B.石墨中,每个C原子单独占有C-C个数为 ,则石墨中碳原子数和C-C个数之比为1:1.5=2:
3,B项错误;
C.每个六元环完全占有的碳原子数为 ,C项错误;
D.石墨中的C原子价层电子对数为3,且不含孤电子对,则石墨中的C原子均为 杂化,D项正确;
答案选D。
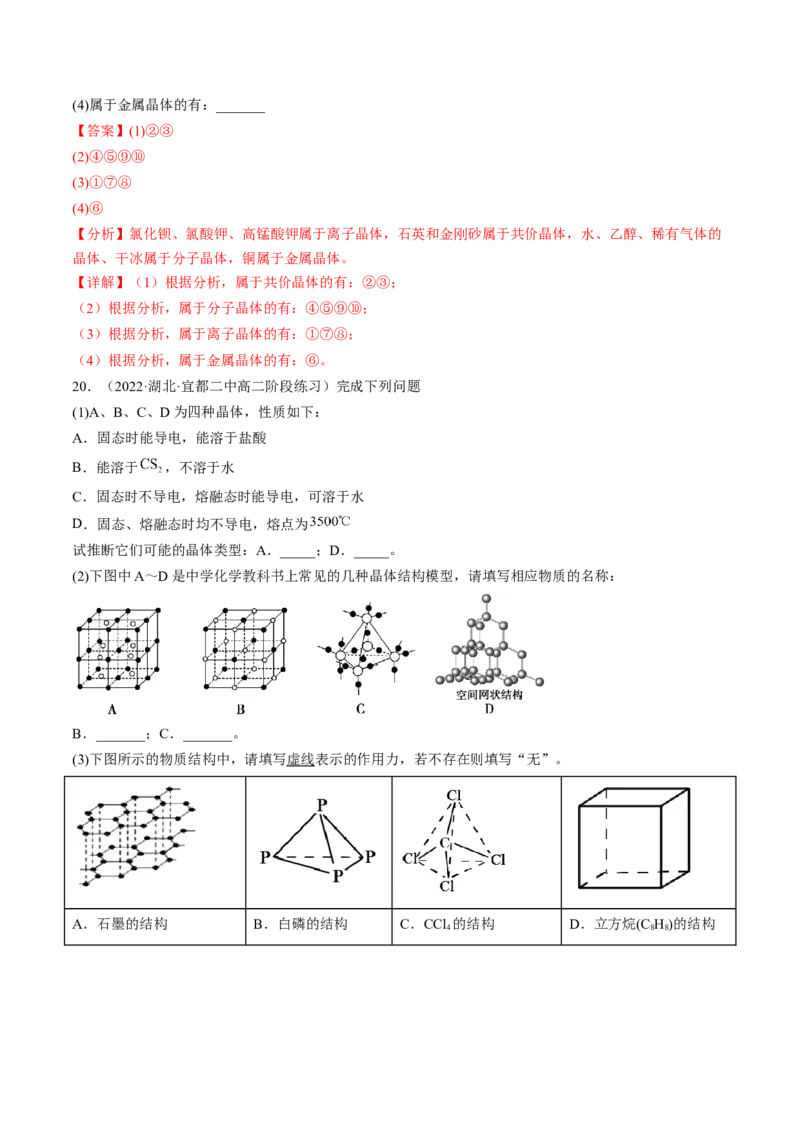
9.(2022·山西师范大学实验中学高二阶段练习)有关晶体的结构如图所示,下列说法中不正确的是
A.在NaCl晶体中,距Cl—最近的Na+形成正八面体
B.在CaF 晶体中,每个晶胞平均含有4个Ca2+
2
C.在金刚石晶体中,碳原子与碳碳键个数的比为1∶2
D.该气态团簇分子的分子式为EF
【答案】D
【详解】A.由晶胞结构可知,氯化钠晶胞中位于顶点的钠离子与棱上的氯离子距离最近,则钠离子周围
最近的氯离子有6个,6个氯离子构成一个正八面体,故A正确;
B.由晶胞结构可知,氟化钙晶胞中位于顶点和面心的钙离子数目为8× +6× =4,故B正确;C.由图可知,金刚石晶体中每个碳原子形成4个共价键,每两个碳原子形成一个共价键,则每个碳原子
形成的共价键平均为4× =2,则晶体中碳原子与碳碳键个数的比为1∶2,故C正确;
D.气态团簇分子不同于晶胞,气态团簇分子中含有4个E原子,4个F原子,则分子式为EF 或FE,故
4 4 4 4
D错误;
故选D。
10.(2022·新疆·乌鲁木齐市第三十一中学高二期中)下列有关离子晶体的数据大小比较中不正确的是
A.晶格能: B.晶格能:
C.阴离子的配位数: D.硬度:
【答案】A
【详解】A.离子半径 ,离子半径越小,所带电荷数越大,晶格能越大,故A错误;
B.离子半径 ,离子半径越小,所带电荷数越大,晶格能越大,故B正确;
C. 、 、 中阴离子的配位数分别为 、 、 ,故C正确;
D.离子半径 ,晶格能: 则硬度: ,故D正确;
故选A
11.(2022·湖北·浠水县实验高级中学高二阶段练习)下列关于物质特殊聚集状态结构的叙述中,错误的
是
纳米氧化锌晶体的晶胞结构
A.液晶具有液体的流动性,在某些物理性质方面具有类似晶体的各向异性
B.氧化镁晶体中离子键的百分数为50%,氧化镁晶体是一种过渡晶体
C.如图氧化锌纳米晶体的晶胞中锌离子与氧离子的个数比为1∶1
D.等离子体的基本构成粒子只有阴、阳离子
【答案】D
【详解】A.液晶是介于液态和晶态之间的物质状态,既具有液体的流动性、粘度等,又具有晶体的某些
物理性质,如导热性等表现出类似晶体的各向异性,故A正确;
B.MgO中离子键的百分数为50%,不是纯粹的离子键,也不是纯粹的共价晶体,是离子晶体和共价晶体
之间的过渡晶体,故B正确;
C.在此六棱柱晶胞中取,位于顶角有12个小球,位于面心的有2个小球,位于内部的有3个小球,则属
于此晶胞的小球有 个;6个大球位于棱上,4个大球位于内部,则属于此晶胞的大球有个。则锌离子与氧离子的个数比为1∶1,故C正确;
D.等离子体是由电子、阳离子和电中性粒子组成的整体上呈电中性的物质聚集体。因此等离子体的基本
构成粒子不是阴、阳离子,故D错误;
答案选D。
培优第二阶——拓展培优练
12.(2022·山西英才学校高二期中)泽维尔研究发现,当用激光脉冲照射NaI使Na+和I-的核间距为
1.0~1.5nm时,呈共价键。根据泽维尔的研究成果能得出的结论是
A.NaI晶体是离子晶体和分子晶体的混合物
B.离子晶体可能含有共价键
C.NaI晶体中既有离子键,又有共价键
D.共价键和离子键没有绝对的界限
【答案】D
【详解】A.NaI晶体是离子化合物,如改变离子的核间距,可能为共价化合物,但为纯净物,不是混合物,
A错误;
B.NaOH晶体中就有离子键和共价键,但不是泽维尔的研究成果,B错误;
C.NaI晶体中当Na+和I-的核间距为1.0~1.5nm时,呈现共价键,但不存在既有离子键,又有共价键的情
形,C错误;
D.NaI为离子晶体,钠离子和碘离子之间是离子键,但是当Na+和I-的核间距为1.0~1.5nm时,呈现共价
键,故共价键和离子键没有绝对的界限,D正确;
故选D。
13.(2022·广东·福田外国语高中高三阶段练习)下列描述不正确的是
A.熔点由高到低:金刚石>SiC>晶体硅
B.DNA分子的两条长链中的碱基以氢键互补配对形成双螺旋结构
C.水晶和干冰的熔化需克服相同类型的作用力
D.石墨层与层间的主要作用力为范德华力,易发生相对滑移,因此石墨可用作润滑剂
【答案】C
【详解】A.金刚石、SiC、晶体硅都属于共价晶体,原子之间以共价键结合形成立体网状结构。形成共价
键的原子半径越小,形成的该共价键就越强,断裂该共价键消耗的能量就越高,物质的熔沸点就越高。原
子半径:C<Si,共价键的键长:C-C<C-Si<Si-Si,所以熔点由高到低:金刚石>SiC>晶体硅,A正确;
B.N元素的电负性较大,在DNA分子结构中,由于碱基之间的氢键具有固定的数目和DNA两条链之间
的距离保持不变,所以DNA中的碱基互补配对是通过氢键来实现的,B正确;
C.水晶是SiO,属于共价晶体,原子之间以共价键结合形成立体网状结构,物质熔化需断裂共价键,其
2
熔点较高;干冰是固态CO,CO 分子之间以分子间作用力结合形成分子晶体,物质熔化需断裂分子间作
2 2
用力,而分子间作用力比共价键弱很多,因此物质的熔沸点比较低,可见二者熔化需克服不同类型的作用
力,C错误;D.石墨属于混合型晶体,在石墨的层内C原子之间以共价键结合;在层与层间的主要作用力为范德华力,
范德华力比较弱,层与层之间易发生相对滑移,因此石墨可用作润滑剂,D正确;
故合理选项是C。
14.(2022·云南·曲靖市马龙区第一中学高二阶段练习)下列数据是对应物质的熔点(℃):
BCl Al O NaO NaCl AlF AlCl 干冰 SiO
3 2 3 2 3 3 2
﹣107 2073 920 801 1291 190 ﹣57 1723
据此做出的下列判断中错误的是A.铝的化合物的晶体中有的不是分子晶体
B.表中只有BCl 和干冰是分子晶体
3
C.同族元素的氧化物可形成不同类型的晶体
D.不同族元素的氧化物可形成相同类型的晶体
【答案】B
【详解】A.由表格数据可知,氯化铝为熔点低的分子晶体,氧化铝和氟化铝为熔点高的离子晶体,则铝
的化合物的晶体中有的不是分子晶体,故A正确;
B.由表格数据可知,除三氯化硼和干冰是熔点低的分子晶体,氯化铝也是熔点低的分子晶体,故B错误;
C.由表格数据可知,二氧化硅熔点高为原子晶体,而二氧化碳的熔点较低为分子晶体,则同族元素的氧
化物可形成不同类型的晶体,故C正确;
D.钠元素是IA元素,铝元素是IIIA元素,氧化钠和氧化铝都属于离子晶体,所以不同族元素的氧化物可
形成相同类型的晶体,故D正确;
故选B。
15.(2022·山东省郓城第一中学高二阶段练习)下列说法中正确的有
①含有离子的晶体一定是离子晶体;
②离子键是阴、阳离子间的相互吸引作用;
③金属晶体的导电性、导热性均与自由电子有关;
④共价键的强弱决定分子晶体熔、沸点的高低;
⑤共价晶体中一定含有共价键;
⑥分子晶体的熔点一定比金属晶体低;
⑦NaCl晶体中,阴离子周围紧邻的阳离子数为6;
⑧硬度由大到小:金刚石>碳化硅>晶体硅
A.2个 B.3个 C.4个 D.5个
【答案】C
【详解】①金属晶体含有金属阳离子,故含有离子的晶体不一定是离子晶体,故错误;
②离子键是阴、阳离子间的静电作用力,包括吸引力和排斥力,故错误;
③金属晶体的导电性、导热性均与自由电子有关,故正确;
④分子晶体熔、沸点的高低由分子间作用力决定,故错误;
⑤共价晶体是原子通过共价键结合而成,所以共价晶体含有共价键,故正确;⑥分子晶体的熔点不一定比金属晶体低,如汞在常温下为液体,碘是分子晶体,常温下为固体,故错误;
⑦NaCl晶体中,阴离子周围紧邻的阳离子数为6,故正确;
⑧金刚石、碳化硅、晶体硅均为原子晶体,键能越大,硬度越大,原子半径:C>Si,键长:C-C>C-Si>
Si-Si,键能:C-C>C-Si>Si-Si,故硬度由大到小:金刚石>碳化硅>晶体硅,故正确;综上所述,共4个
正确;
故选C。
16.(2022·江苏省包场高级中学高二开学考试)氮化硼(BN)晶体有多种相结构。它们的两种晶体结构如图
所示。关于这两种晶体的说法,不正确的是
A.六方相氮化硼含有BN小分子
B.六方相氮化硼层间作用力小,所以质地软
C.立方氮化硼中熔点高、硬度大
D.六方相氮化硼晶体其结构与石墨相似却不导电,原因是没有可以自由移动的电子
【答案】A
【详解】A.六方相氮化硼中存在共价键和分子间作用力,空间结构与石墨类似,属于混合晶体,不含BN
小分子,故A错误;
B.六方相氮化硼层与层之间存在分子间作用力,分子间作用力比较小,所以其质地较软,故B正确;
C.立方相氮化硼空间结构为网状结构,与金刚石类似,属于共价晶体,所以其熔点高、硬度大,故C正
确;
D.晶体中存在可以自由移动的电子能导电,六方相氮化硼晶体中没有可以自由移动的电子,所以不导电,
故D正确;
故答案选A。
17.(2021·宁夏·银川一中高二期末)碳元素的单质有多种形式,下图依次是C 、石墨和金刚石的结构图:
60
下列说法正确的是
A.三种单质的晶体中C 晶体熔点最低
60
B.假设金刚石晶体中最近碳原子相切,则晶胞的空间利用率为74%C.均为原子晶体
D.C原子杂化方式均为sp3
【答案】A
【详解】A.C 为分子晶体,石墨烯为混合键晶体,金刚石为原子晶体,三种单质的晶体中C 晶体熔点
60 60
最低,A正确;
B.晶胞中只有体对角线上的原子是密置的,体对角线与晶胞边长a的关系是根号3 倍的a 等于8r,顶点
两个原子,里面对角线上三个,这样找到a与r的关系,算出来的空间利用率是34.01%,B错误;
C.C 为分子晶体,C错误;
60
D.金刚石中碳原子与4个碳原子形成4个共价键,即sp3杂化,石墨烯和C 的碳原子为sp2杂化,D错误;
60
答案选A。
18.(2022·辽宁·沈阳市第一二〇中学高三阶段练习)下表是常见晶胞结构,下列说法正确的是
金刚石 干冰
A.金刚石是共价晶体,熔点关系为:金刚石>晶体硅>碳化硅
B. 晶胞中, 位于 所构成的八面体空隙中
C. 是金属晶体,与 距离最近的 有6个
D.干冰是分子晶体,由于分子间作用力弱,所以干冰熔点低
【答案】D
【详解】A.碳化硅中的Si-C键长比晶体硅中Si-Si键长短,键能更大,熔点高,所以熔点:碳化硅>晶体
硅,金刚石中C-C键比Si-C键长短,所以熔点:金刚石>碳化硅,综上熔点:金刚石>碳化硅>晶体硅,故
A错误;
B.如图,ZnS晶胞中, 位于ZnS晶胞面心,所以 位于 所构成的八面体空隙中,故B错误;
C.如图,从Fe的晶胞中可以看出,每个Fe原子周围与Fe原子最近的Fe原子有8个,故C错误;
D.干冰属于分子晶体,且只存在分子间作用力,由于分子间作用力弱,所以干冰熔点低,故D正确;
故选D。
19.(2022·海南·儋州川绵中学高二阶段练习)按构成晶体的粒子和粒子间作用力的不同,将以下晶体进
行分类:
①氯化钡、②石英、③金刚砂、④水、⑤乙醇、⑥铜、⑦氯酸钾、⑧高锰酸钾、⑨稀有气体的晶体、⑩干
冰
(1)属于共价晶体的有:_______
(2)属于分子晶体的有:_______
(3)属于离子晶体的有:_______(4)属于金属晶体的有:_______
【答案】(1)②③
(2)④⑤⑨⑩
(3)①⑦⑧
(4)⑥
【分析】氯化钡、氯酸钾、高锰酸钾属于离子晶体,石英和金刚砂属于共价晶体,水、乙醇、稀有气体的
晶体、干冰属于分子晶体,铜属于金属晶体。
【详解】(1)根据分析,属于共价晶体的有:②③;
(2)根据分析,属于分子晶体的有:④⑤⑨⑩;
(3)根据分析,属于离子晶体的有:①⑦⑧;
(4)根据分析,属于金属晶体的有:⑥。
20.(2022·湖北·宜都二中高二阶段练习)完成下列问题
(1)A、B、C、D为四种晶体,性质如下:
A.固态时能导电,能溶于盐酸
B.能溶于 ,不溶于水
C.固态时不导电,熔融态时能导电,可溶于水
D.固态、熔融态时均不导电,熔点为
试推断它们可能的晶体类型:A._____;D._____。
(2)下图中A~D是中学化学教科书上常见的几种晶体结构模型,请填写相应物质的名称:
B._______;C._______。
(3)下图所示的物质结构中,请填写虚线表示的作用力,若不存在则填写“无”。
A.石墨的结构 B.白磷的结构 C.CCl 的结构 D.立方烷(C H)的结构
4 8 8F.水和甲醇的相互溶
E.干冰的结构 G.邻羟基苯甲醛 H.氟化钙的晶胞结构
解
A._______;B._______;C._______;F. _______。
【答案】(1) 金属晶体 共价晶体
(2) 氯化钠 二氧化硅
(3) 范德华力 共价键 无 氢键
【解析】(1)溶液导电的原因是存在自由移动的离子,金属导电的原因是存在自由移动的电子;A固态时
能导电,能溶于盐酸,则A为活泼金属,属于金属晶体;D固态、熔融态时均不导电,熔点为 ,熔
点很高且不能电离出离子,则为共价晶体;
(2)由晶体图可知,B为氯化钠、C为二氧化硅;
(3)A为石墨,石墨层与层之间的作用力为范德华力;B为白磷结构,磷原子之间使用共价键相结合;C
中虚线只是表示4个氯形成正四面体,不是化学键;F表示的是水分子和甲醇分子之间的氢键。
21.完成下列问题。
(1)石墨晶体由层状石墨“分子”按ABAB……方式堆积而成,如图甲所示,图中用虚线标出了石墨的一个
六方晶胞。该晶胞中含有的碳原子数为_______。
(2)石墨烯是一种由单层碳原子构成的平面结构新型碳材料,如图乙所示。设N 为阿伏加德罗常数的值,
A
1mol石墨烯中含有的六元环个数为_______。下列有关石墨烯的说法正确的是_______(填字母)。
a.晶体中碳原子间全部是单键
b.石墨烯中所有碳原子可以处于同一个平面
c.从石墨中剥离得到石墨烯需克服分子间作用力(3)石墨烯可转化为 , 的结构如图丙所示,该分子是由五边形和六边形构成的球体,其中五边形有
12个,则六边形有_______个(注:简单多面体的顶点数V、面数F及棱数E间的关系为 )。
(4)金刚石晶胞如图丁所示,则金刚石晶胞中原子的配位数为_______。
【答案】(1)4
(2) abc
(3)20
(4)4
【解析】(1)由题图甲可知,六方晶胞中处于顶点的8个碳原子分为两种,其中4个被6个晶胞所共有,
4个被12个晶胞所共有;处于棱上的4个碳原子也分为两种,其中2个被3个晶胞所共有,2个被6个晶胞
所共有;处于面上的2个碳原子分别被2个晶胞所共有;晶胞内还有1个碳原子,所以每个六方晶胞中含
有的碳原子数为 ;
(2)a.由题图乙可知,石墨烯中6个碳原子组成1个环,每个碳原子被3个环共有,相当于2个碳原子
组成1个环,1mol碳原子组成的环的个数为 。根据碳原子成键特点可知,每个碳原子与周围三个碳
原子形成3个单键,a正确;
b.石墨烯中所有碳原子可以处于同一个平面,b正确;
c.从石墨中剥离得到石墨烯需克服分子间作用力,c正确;
故选:abc;
(3)设 中六边形、五边形的个数分别为x、y。则有: 、 ,解得
, ;
(4)由金刚石晶胞结构可知原子的配位数为4。
22.(2022·上海交大附中高二开学考试)现有几组物质的熔点(℃)数据:
A组 B组 C组 D组金刚石:3550℃ Li:181℃ HF:-83℃ NaCl:801℃
硅晶体:1410℃ Na:98℃ HCl:-115℃ KCl:776℃
硼晶体:2300℃ K:64℃ HBr:-89℃ RbCl:718℃
二氧化硅:1723℃ Rb:39℃ HI:-51℃ CsCl:645℃
据此回答下列问题:
(1)A组属于_______晶体,其熔化时克服的微粒间的作用力是_______。
(2)B组晶体共同的物理性质是_______(填序号)。
①有金属光泽 ②导电性 ③导热性 ④延展性
(3)C组中自HCl至HI熔点依次升高,原因是_______。
(4)D组晶体可能具有的性质是_______(填序号)。
①硬度小 ②水溶液能导电 ③固体能导电 ④熔融状态能导电
(5)D组晶体的熔点由高到低的顺序为NaCl>KCl>RbCl>CsCl,其原因为_______。
【答案】(1) 原子晶体 共价键
(2)①②③④
(3)含有分子间氢键,增加了分子之间的吸引力,使物质熔化、气化需消耗更高的能量,因此其熔点反常
(4)②④
(5)这些都属于离子晶体,熔点与晶格能有关,由于离子半径:r(Na+)<r(K+)<r(Rb+)<r(Cs+),在离子所
带电荷数相同的情况下,半径越小,晶格能越大,熔点就越高。
【解析】(1)A组熔点很高,为原子晶体,构成微粒是原子,原子晶体是由原子通过共价键形成的,熔化
时克服的是共价键;
(2)B组为金属晶体,根据金属晶体的特征可知,B组金属晶体具有①②③④四条共性;
(3)HF的分子之间除存在范德华力外,分子之间还含有分子间氢键,增加了分子之间的吸引力,使物质
熔化、气化需消耗更高的能量,因此其熔点反常;
(4)D组属于离子晶体,离子晶体的构成微粒是阴、阳离子,离子之间通过离子键结合,离子键是一种比
较强的相互作用,具有一定的硬度;一般能够溶于水,在水分子作用下电离产生自由移动的离子,因而能
够导电;在固体时离子之间通过离子键结合,不能自由移动,因此固态时不能导电;在熔融状态时断裂离
子键,产生自由移动的离子,因此在熔融状态下也可以导电,故②④两个性质符合;
(5)D组属于离子晶体,其熔点与离子键键能有关。离子半径越小,离子之间作用力越强,离子键的键能
越大,晶格能越大,物质的熔沸点就越高。由于离子半径:r(Na+)<r(K+)<r(Rb+)<r(Cs+),在离子所带电
荷数相同的情况下,半径越小,晶格能越大,熔点就越高。