文档内容
第3章 晶体结构与性质
3.3.2 过渡晶体与混合型晶体
一.选择题(共11小题)
1.下列有关石墨晶体的说法正确的是 ( )
A.由于石墨晶体导电,所以它是金属晶体
B.由于石墨的熔点很高,所以它是共价晶体
C.由于石墨质软,所以它是分子晶体
D.石墨晶体是一种混合晶体
2.中科院的科学家已研制出一种高性能超级电容器电极材料——氮掺杂有序介孔石墨烯。该材料可用作电动
车的“超强电池”:充电只需7秒钟,即可续航35公里。相关研究成果已于2015年12月18日发表在世界顶
级期刊美国《Science》上。下面有关石墨晶体说法不正确的是
A.石墨晶体内既有共价键又有分子间作用力
B.石墨晶体熔沸点很高,硬度很大
C.石墨晶体内每个六边形平均含完整碳原子2个
D.石墨晶体中,每个C原子连接3个六元环
3.2015年03月02日,全球首批3万部石墨烯手机在渝发布,石墨烯是从石墨材料中剥离出来、由碳原子组成
的只有一层原子厚度的二维晶体。有关石墨烯的说法不正确的是
A.金刚石、富勒烯、石墨烯互为碳元素的同素异形体。
B.石墨烯中每一层内碳原子排列成平面正六边形
C.由于同素异形体是同种元素组成,所以石墨转化为金刚石属于物理变化
D.金刚石属于共价晶体,由C 构成的晶体属于分子晶体
60
4.碳有多种同素异形体,其中石墨烯与金刚石的晶体结构如图所示,下列说法错误的是()
A.在石墨烯晶体中,每个C原子连接3个六元环
B.石墨烯晶体中的化学键全部是碳碳单键
C.在金刚石晶体中,C原子采用sp3杂化
D.在金刚石晶体中,六元环中最多有4个C原子在同一平面5.从严格意义上讲石墨属于
A.分子晶体 B.原子晶体 C.金属晶体 D.混合型晶体
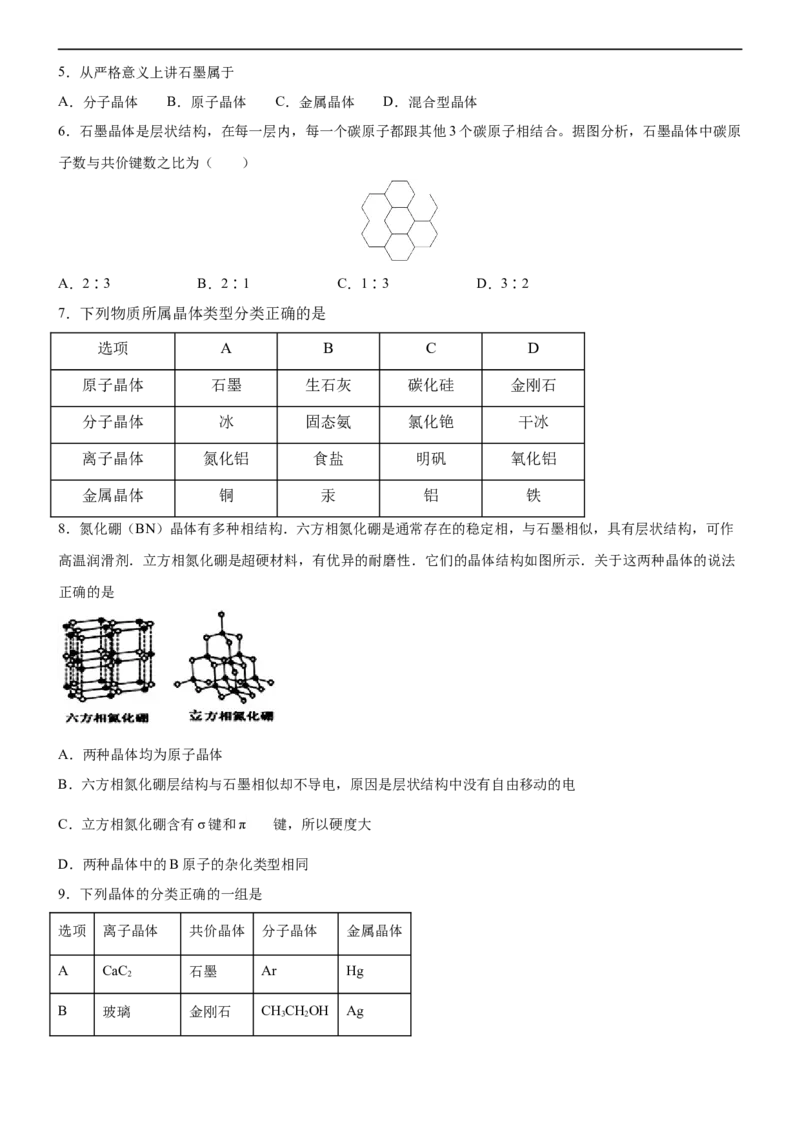
6.石墨晶体是层状结构,在每一层内,每一个碳原子都跟其他3个碳原子相结合。据图分析,石墨晶体中碳原
子数与共价键数之比为( )
A.2∶3 B.2∶1 C.1∶3 D.3∶2
7.下列物质所属晶体类型分类正确的是
选项 A B C D
原子晶体 石墨 生石灰 碳化硅 金刚石
分子晶体 冰 固态氨 氯化铯 干冰
离子晶体 氮化铝 食盐 明矾 氧化铝
金属晶体 铜 汞 铝 铁
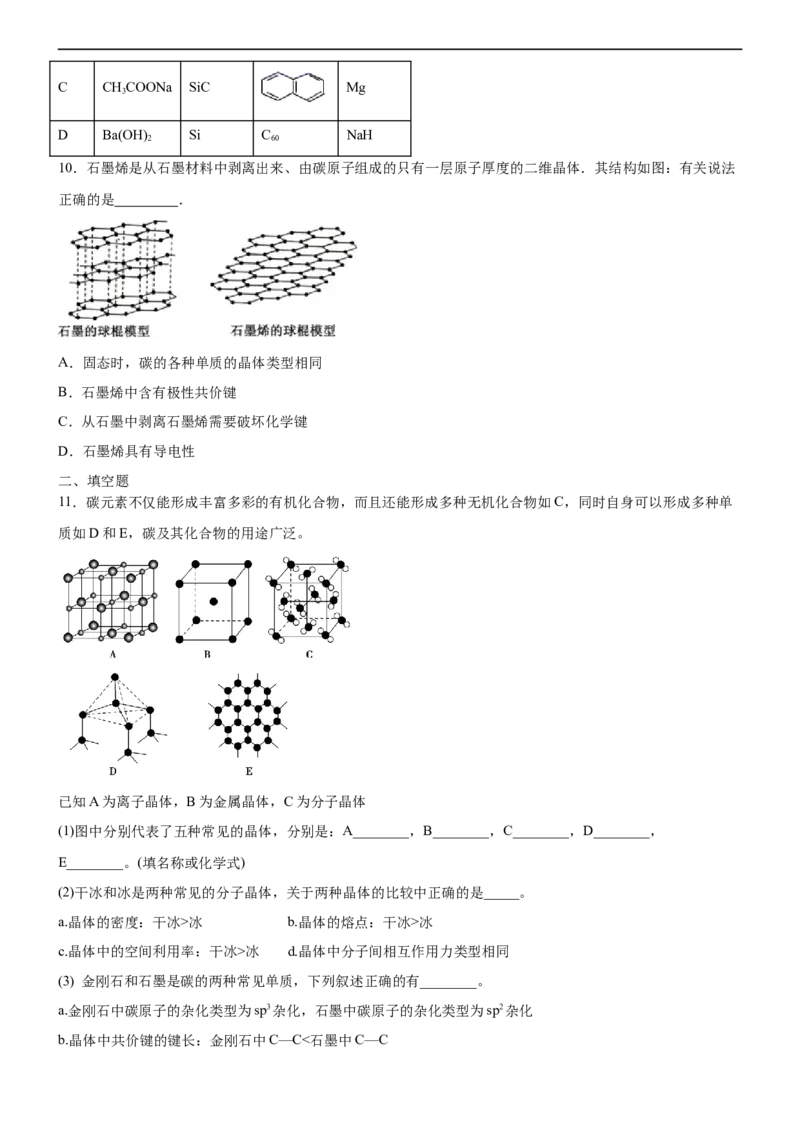
8.氮化硼(BN)晶体有多种相结构.六方相氮化硼是通常存在的稳定相,与石墨相似,具有层状结构,可作
高温润滑剂.立方相氮化硼是超硬材料,有优异的耐磨性.它们的晶体结构如图所示.关于这两种晶体的说法
正确的是
A.两种晶体均为原子晶体
B.六方相氮化硼层结构与石墨相似却不导电,原因是层状结构中没有自由移动的电
C.立方相氮化硼含有σ键和π 键,所以硬度大
D.两种晶体中的B原子的杂化类型相同
9.下列晶体的分类正确的一组是
选项 离子晶体 共价晶体 分子晶体 金属晶体
A CaC 石墨 Ar Hg
2
B 玻璃 金刚石 CHCHOH Ag
3 2C CHCOONa SiC Mg
3
D Ba(OH) Si C NaH
2 60
10.石墨烯是从石墨材料中剥离出来、由碳原子组成的只有一层原子厚度的二维晶体.其结构如图:有关说法
正确的是 .
A.固态时,碳的各种单质的晶体类型相同
B.石墨烯中含有极性共价键
C.从石墨中剥离石墨烯需要破坏化学键
D.石墨烯具有导电性
二、填空题
11.碳元素不仅能形成丰富多彩的有机化合物,而且还能形成多种无机化合物如C,同时自身可以形成多种单
质如D和E,碳及其化合物的用途广泛。
已知A为离子晶体,B为金属晶体,C为分子晶体
(1)图中分别代表了五种常见的晶体,分别是:A________,B________,C________,D________,
E________。(填名称或化学式)
(2)干冰和冰是两种常见的分子晶体,关于两种晶体的比较中正确的是_____。
a.晶体的密度:干冰>冰 b.晶体的熔点:干冰>冰
c.晶体中的空间利用率:干冰>冰 d.晶体中分子间相互作用力类型相同
(3) 金刚石和石墨是碳的两种常见单质,下列叙述正确的有________。
a.金刚石中碳原子的杂化类型为sp3杂化,石墨中碳原子的杂化类型为sp2杂化
b.晶体中共价键的键长:金刚石中C—C<石墨中C—Cc.晶体的熔点:金刚石>石墨
d.晶体中共价键的键角:金刚石>石墨
e.金刚石晶体中只存在共价键,石墨晶体中则存在共价键、金属键和范德华力
f.金刚石和石墨的熔点都很高,所以金刚石和石墨都是原子晶体
(4)金刚石晶胞结构如图,一个晶胞中的C原子数目为 ________。
(5)C与孔雀石共热可以得到金属铜,金属铜采用面心立方最密堆积,已知Cu单质的晶体密度为ρ g/cm3,Cu的
相对原子质量为M,阿伏加德罗常数为N ,则Cu的原子半径为 __________cm。
A
12.金刚石、石墨、C 和石墨烯都是碳的同素异形体,其结构示意图如下:
60
(1)石墨晶体中存在的作用力有________________________________
(2)金刚石质硬但脆,金刚石能被砸碎的原因是___________________________;金刚石、石墨、C 的熔点由
60
高到低的顺序是________________________。
(3)C 晶体的堆积方式为______________;晶体中C 的配位数为_________。
60 60
(4)石墨烯具有神奇的特性,两位科学家由于对石墨烯研究做出重大贡献而获得了2010年诺贝尔物理学奖。
石墨烯即单层石墨。石墨烯中碳原子的杂化轨道类型为_______________;碳碳键的键角是_________;碳原子
和碳碳键的个数比是_______;12g石墨烯中含有________个六元环。
(5)碳化硅的结构与金刚石类似,设碳化硅的密度为a g/cm3,碳化硅晶体内碳硅键的键长为______pm(用N
A
表示阿伏加德罗常数的值,列表达式即可)。