文档内容
第二节 化学反应的速率与限度
(第2课时 化学反应的限度及反应条件的控制)
一、选择题(共12题)
1.化学反应速率和化学反应的限度是化工生产研究的主要问题之一,下列对化学反应速率和反应限度的
认识正确的是
A.决定化学反应速率的主要因素是光照、超声波、压强和催化剂等
B.化学反应速率理论是研究怎样提高原料转化率的
C.可逆反应到一定程度时,会出现正、逆反应速率相等,各物质浓度相等的现象
D.化学限度(即平衡)理论,是研究怎样改变反应条件,提高产品的产率
【答案】D
【解析】
A. 决定化学反应速率的主要因素是反应物本身的性质,A错误;B. 化学反应速率是研究反应快慢的,化学
反应的限度理论是研究怎样提高原料转化率的,B错误;C. 可逆反应到一定程度时,会出现正、逆反应速
率相等的现象,但各物质浓度不一定相等,C错误;D. 化学限度(即平衡)理论,是研究怎样改变反应条
件,提高产品的产率,D正确,答案选D。
2.一定温度下,在恒容密闭容器中发生反应: 。当 、 、
、 的浓度不再变化时,下列说法正确的是
A. 和 全部转化为 和
B.该反应已达到化学平衡
C.正、逆反应速率相等且等于零
D. 、 、 、 的浓度一定相等
【答案】B
【解析】
A.可逆反应有限度,转化率不可能为100%,故A错误;
学科网(北京)股份有限公司B.该反应是可逆反应, 、 、 、 的浓度不再变化时,说明达到平衡状态,故B正确;
C.根据B分析可知该反应达到平衡,正、逆反应速率相等但不等于零,故C错误;
D. 、 、 、 的浓度不再变化时,但浓度不一定相等,故D错误;
综上所述,答案为B。
3.T℃时,在 2 L 的密闭容器中,气体 X、Y 和 Z 三种物质的物质的量随时间变化的曲线如图所示,下
列描述正确的是
A.容器中化学反应为 X(g)+Y(g) Z(g)
B.0~10 s,X 表示的平均化学反应速率为 0.04 mol/(L·s)
C.使用催化剂只能加快 0~10 s 间的反应速率
D.0~4 s 的平均反应速率小于 0~10 s 的平均反应速率
【答案】B
【解析】
A. 由图像可知反应在10s时达到化学平衡,此时X、Y分别减少了0.8mol、0.8mol,Z增加了1.6mol,所以
反应的化学方程式为:X(g)+Y(g) 2Z(g),故A错误;B. 0~10 s,X表示的平均化学反应速率为
(0.8mol÷2L÷10s)=0.04 mol/(L·s),故B正确;C.使用催化剂不仅加快0~10s间的反应速度,平衡后的速率
也加快,故C错误;D.随着反应进行反应物浓度减小,速率减小,所以0~4s的平均反应速率大于0~10s
时平均反应速率,故D错误;答案选B。
4.一定温度下,向一恒容密闭容器中充入 和 ,在催化剂作用下发生反比应:
,下列有关说法错误的是
A.温度升高,可以加快反应速率
B.使用催化剂是为了加快反应速率,提高生产效率
学科网(北京)股份有限公司C.达到化学平衡时,生成 的物质的量为
D.若单位时间内消耗 ,同时生成 ,则反应达到平衡状态
【答案】C
【解析】
A.升高温度,可以加快反应速率,A正确;
B.使用催化剂是为了加快反应速率,缩短到达平衡所需要的时间,提高生产效率,B正确;
C.达到化学平衡时,由于转化率不可能是100%,因此生成 的物质的量小于 ,C错误;
D.若单位时间内消耗 ,同时生成 ,说明正逆反应速率相等,则反应达到平衡状态,D
正确;
答案选C。
5.2SO +O 2SO ∆H<0。实验发现,一定条件下向一密闭容器中充入SO 和18O ,反应一段时
2 2 3 2 2
间后,核素18O存在于SO 、O 、SO 中。下列分析不正确的是
2 2 3
A.18O 与O 的化学性质基本相同
2 2
B.断裂2molSO +1molO 中的共价键的能量小于断裂2molSO 中的共价键的能量
2 2 3
C.化合反应与分解反应可同时发生,说明反应存在可逆性
D.平衡时,18O 初始浓度c (18O )与平衡时各组分浓度c之间一定存在:2c (18O )=2c(S18O )+3c(S18O )+2c(18O )
2 0 2 0 2 2 3 2
【答案】D
【解析】
A.18O 与O 的结构相同,化学性质基本相同,故A正确;
2 2
B.该反应为放热反应,反应物的键能和小于生成物的键能和,故B正确;
C.该反应正向为化合反应,逆向为分解反应,在相同的条件下,反应既可以正向进行,也可以逆向进行,
可说明反应存在可逆性,故C正确;
D.在反应过程中还可能存在只含一个18O原子的二氧化硫,只含一个18O原子的三氧化硫等分子,故D错
误;
故选:D。
学科网(北京)股份有限公司6.甲烷消除NO 的污染原理为: 。在一定温度下,向恒容
2
密闭容器中充入一定量的CH 和NO 进行上述反应。下列表述能用来判断该反应达到化学平衡状态的是
4 2
A.v (CH )=2v (NO )
正 4 逆 2
B.容器中混合气体的平均密度不再变化
C.容器中混合气体的平均摩尔质量不再发生变化
D.单位时间内,消耗1molCH 同时生成1molCO
4 2
【答案】C
【解析】
A.v (CH )=2v (NO )不满足化学计量数关系,说明没有达到平衡状态,故A不选;
正 4 逆 2
B.该反应前后都是气体,气体总质量、容器容积为定值,则混合气体密度始终不变,因不能根据混合气
体密度判断平衡状态 ,故B不选;
C.该反应为正向是气体体积增大的反应,气体的平均摩尔质量为变量,当容器中混合气体平均摩尔质量
不再发生变化时,表明正逆反应速率相等,达到平衡状态 ,故C选;
D.单位时间内,消耗1molCH 同时生成1molCO ,表示的都是正反应速率,无法判断是否达到平衡状态,
4 2
故D不选;
故选:C。
7.空气中久置的铝片5.0g投入盛有50mL0.5mol/L硫酸溶液的烧杯中,该铝片与硫酸反应产生氢气的速率
v与反应时间t可用如图所示的曲线来表示。下列推论错误的是
A.0→a段不产生氢气是因为表面的氧化物隔离了铝和硫酸溶液
B.b→c段产生氢气的速率增加较快的主要原因之一是温度升高
C.t=c时反应处于平衡状态,产率最大
D.t>c时,产生氢气的速率降低主要是因为溶液中c(H+)降低
【答案】C
学科网(北京)股份有限公司【解析】
由图可知,开始不生成氢气,为氧化铝与硫酸的反应,然后Al与硫酸反应生成氢气,开始温度较低,由于
反应放热,则温度升高反应速率加快,后来,氢离子浓度减小,则反应速率减小;
A.因铝的表面有一层致密的Al O 能与硫酸反应得到盐和水,无氢气放出,发生的反应为
2 3
Al O +3H SO =Al (SO ) +3H O,故A正确;
2 3 2 4 2 4 3 2
B.在反应过程中,浓度减小,反应速率减小,但反应放热,溶液温度升高,反应速率加快,且后者为主
要因素,故B正确;
C.t=c时反应反应没有停止,继续生成氢气,则产率不最大,故C错误;
D.随着反应的进行,溶液中的氢离子浓度逐渐降低,所以反应速率逐渐减小,故D正确;
故选:C。
8.一定温度和压强不变的条件下,发生可逆反应:A(g)+3B(g) 4C(g),下列叙述能作为该反应达到平衡
状态的标志的是 ⇌
①混合气体的平均摩尔质量不再变化 ②v(A)∶v(B)∶v(C)=1∶3∶4
③A、B、C的浓度不再变化 ④C的体积分数不再变化
⑤A、B、C的分子数之比为1∶3∶4 ⑥混合气体的密度不再变化
⑦单位时间消耗a mol A,同时生成3a mol B
A.②③④⑤⑥⑦ B.③④⑦
C.③④⑥⑦ D.①③⑤⑥⑦
【答案】B
【解析】
①反应前后气体体积不变,气体物质的量不变,质量守恒,所以混合气体的摩尔质量始终不变,不能据此
判断反应是否达到平衡状态,①错误;
②在任何情况下速率之比等于化学计量数之比,不能说明正、逆反应速率相等,因此不能据此判断反应是
否达到平衡状态,②错误;
③当混合气体中各组分浓度不变时,说明反应达到平衡状态,③正确;
④C的体积分数不变,说明正、逆反应速率相等,反应达到了平衡状态,④正确;
⑤平衡时各物质的分子数之比,决定于开始加入物质的多少和反应程度,与平衡状态无关,⑤错误;
⑥混合气体质量守恒,体积不变,密度始终不变,所以密度不变不能说明反应达到平衡状态,⑥错误;
⑦消耗a mol A,同时生成3a mol B,说明正、逆反应速率相等,反应达到了平衡状态,⑦正确;
可见能够判断反应达到平衡状态的叙述是③④⑦,故合理选项是B。
学科网(北京)股份有限公司9.一定温度和压强下,在2 L的密闭容器中合成氨气:N (g)+3H (g) 2NH (g) 。在反应过程中反应物和
2 2 3
生成物的物质的量随时间的变化如图所示。下列说法错误的是:
A.0~10 min内,以NH 表示的平均反应速率为0.005 mol • L-1• min-1
3
B.10~20 min内,NH 浓度变化的原因可能是加入催化剂或缩小容器体积
3
C.该反应在20 min时达到化学平衡状态
D.N 的平衡转化率与H 平衡转化率相等
2 2
【答案】D
【解析】
由图可知,该反应在20 min时各物质浓度不变,说明反应达到化学平衡状态,10 min时改变条件的瞬间各
物质的物质的量不变,反应速率加快,可能是加入催化剂或缩小容器体积导致。
A项、0~10 min内,生成NH 的物质的量为0.1 mol,浓度为0.05mol • L-1,则以NH 表示的平均反应速率
3 3
为 = =0.005 mol • L-1• min-1,故A正确;
B项、10 min时改变条件的瞬间各物质的物质的量不变,10~20min内反应速率加快,则10~20 min内,
NH 浓度变化的原因可能是加入催化剂或缩小容器体积导致,故B正确;
3
C项、由图可知,该反应在20 min时各物质浓度不变,说明反应达到化学平衡状态,故C正确;
D项、反应达到平衡时,N 的平衡转化率为 100%=37.5%,H 平衡转化率
2 2
×
100%=75%,两者转化率不同,故D错误。
×
故选D。
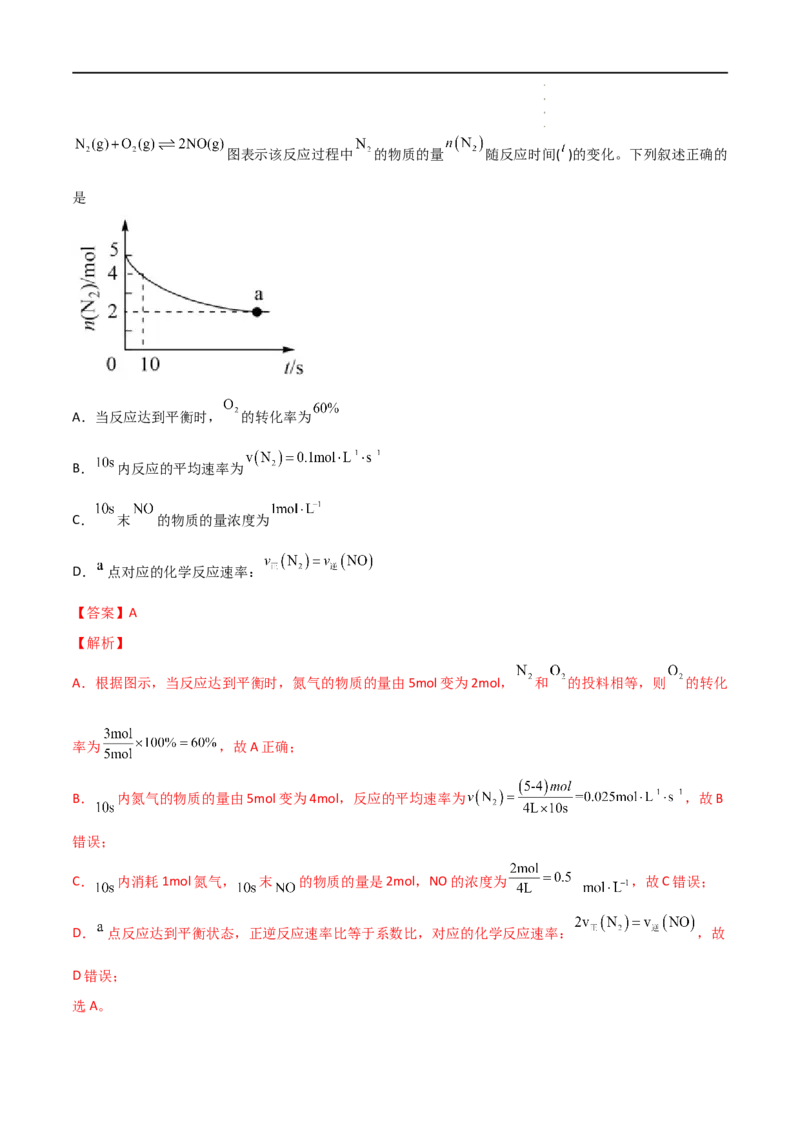
10.一定条件下,等物质的量的 和 在容积为 的恒容密闭容器中发生如下反应:
学科网(北京)股份有限公司图表示该反应过程中 的物质的量 随反应时间( )的变化。下列叙述正确的
是
A.当反应达到平衡时, 的转化率为
B. 内反应的平均速率为
C. 末 的物质的量浓度为
D. 点对应的化学反应速率:
【答案】A
【解析】
A.根据图示,当反应达到平衡时,氮气的物质的量由5mol变为2mol, 和 的投料相等,则 的转化
率为 ,故A正确;
B. 内氮气的物质的量由5mol变为4mol,反应的平均速率为 ,故B
错误;
C. 内消耗1mol氮气, 末 的物质的量是2mol,NO的浓度为 ,故C错误;
D. 点反应达到平衡状态,正逆反应速率比等于系数比,对应的化学反应速率: ,故
D错误;
选A。
学科网(北京)股份有限公司11.在一定温度下的定容容器中,有反应 。当下列的物理量不再发生变化
时,表明已达到平衡状态的是
A.混合气体的密度 B.混合气体的压强
C.气体的总物质的量 D.物质A的物质的量浓度
【答案】A
【解析】
A.因为A为固体,所以反应中气体的总质量一直在变化,当混合气体的密度不变,说明气体的质量不变,
反应达平衡状态,故A正确;
B.方程式两边气体的计量数相等,所以混合气体的压强一直不变,故B错误;
C.混合气体的总物质的量一直不变,故C错误;
D.A为纯固体、物质的量浓度是常数,故D正确;
答案:A
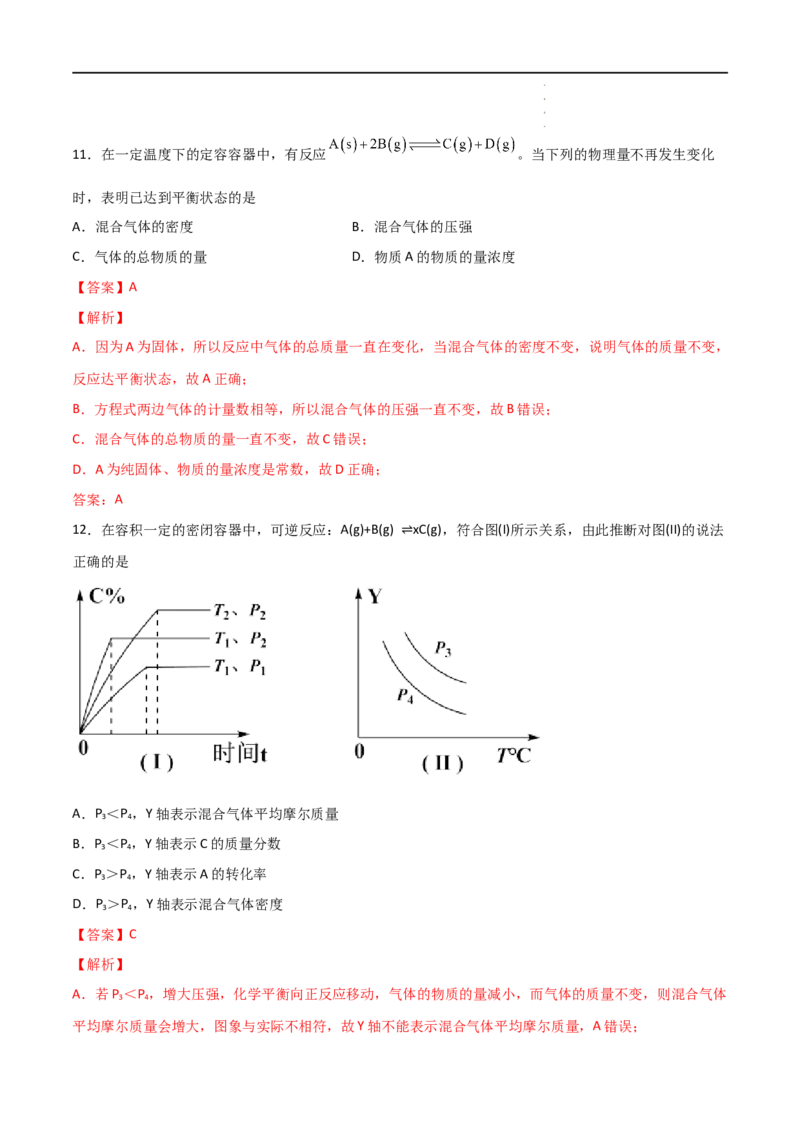
12.在容积一定的密闭容器中,可逆反应:A(g)+B(g) xC(g),符合图(I)所示关系,由此推断对图(II)的说法
正确的是 ⇌
A.P <P ,Y轴表示混合气体平均摩尔质量
3 4
B.P <P ,Y轴表示C的质量分数
3 4
C.P >P ,Y轴表示A的转化率
3 4
D.P >P ,Y轴表示混合气体密度
3 4
【答案】C
【解析】
A.若P <P ,增大压强,化学平衡向正反应移动,气体的物质的量减小,而气体的质量不变,则混合气体
3 4
平均摩尔质量会增大,图象与实际不相符,故Y轴不能表示混合气体平均摩尔质量,A错误;
学科网(北京)股份有限公司B.若P <P ,增大压强,化学平衡向正反应移动,C的物质的量及质量增大,C的质量分数也会增加,图
3 4
象与实际不相符,故Y轴不能表示C的质量分数,B错误;
C.若P >P ,在相同温度下增大压强,化学平衡向正反应方向移动,A的转化率会增大;同时升高温度化
3 4
学平衡向吸热的逆反应方向移动,导致A的转化率降低,图象与实际符合,故Y轴表示A的转化率,C正
确;
D.若P >P ,由于混合气体的总质量不变,反应在恒容密闭容器中进行,容器的体积不变,混合气体的密
3 4
度不变,因此Y轴不能表示混合气体密度,D错误;
故合理选项是C。
二、非选择题(共3题)
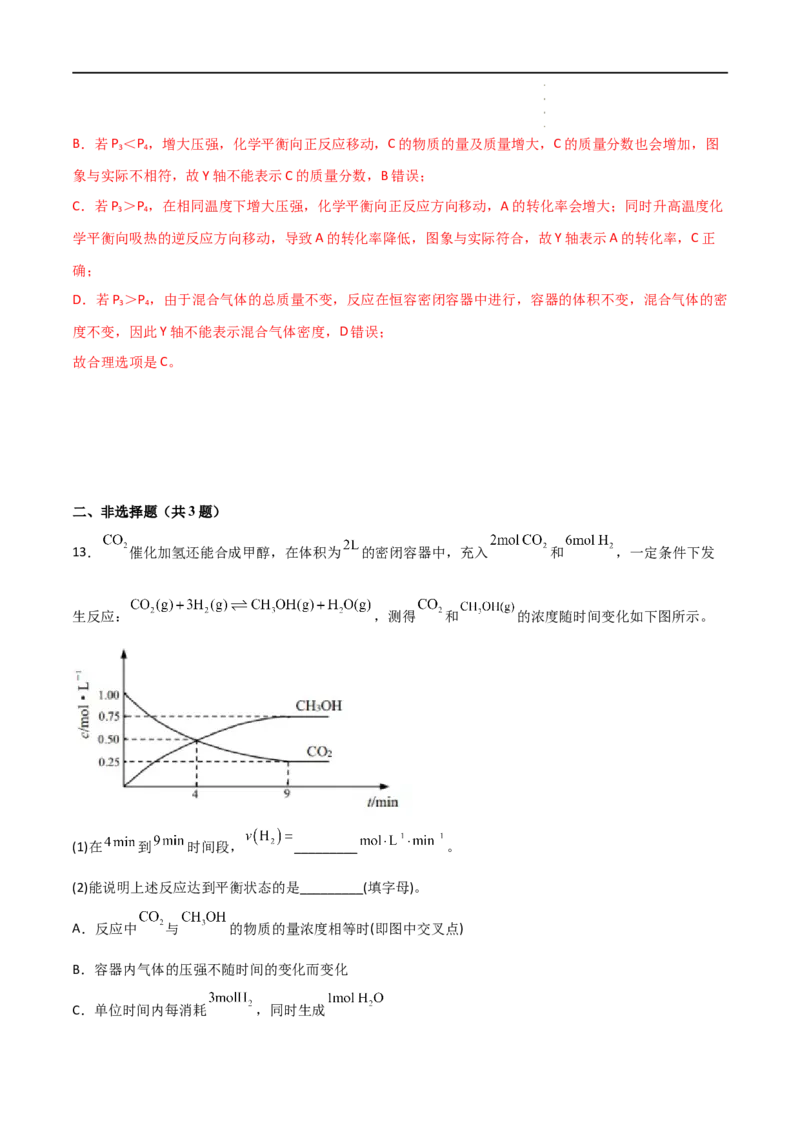
13. 催化加氢还能合成甲醇,在体积为 的密闭容器中,充入 和 ,一定条件下发
生反应: ,测得 和 的浓度随时间变化如下图所示。
(1)在 到 时间段, _________ 。
(2)能说明上述反应达到平衡状态的是_________(填字母)。
A.反应中 与 的物质的量浓度相等时(即图中交叉点)
B.容器内气体的压强不随时间的变化而变化
C.单位时间内每消耗 ,同时生成
学科网(北京)股份有限公司D. 的体积分数在混合气体中保持不变
(3)下列措施能增大反应速率的是_________(填字母)。
A.升高温度 B.扩大容器体积
C.充入一定量氦气 D.加入催化剂
(4)平衡时 的物质的量为_________。
【答案】(1) 0.15 (2) BD (3) AD (4)
【解析】
(1)在 到 时间段, ,由反应速率之比等于计量数之比,
则 3 ;
(2)A.由图可知反应中CO 与CH OH的物质的量浓度之比为1:1时,并未达到平衡状态,故A错误;
2 3
B.因反应前后气体分子数不相等,则压强是一变量,当容器内气体的压强不随时间的变化而变化,说明
达到平衡状态,故B正确;
C.无论是否达到平衡状态,都存在单位时间内每消耗3molH ,同时生成1molH O,故C错误;
2 2
D.CO 的体积分数在混合气体中保持不变,说明达到平衡状态,故D正确;
2
故答案为:BD;
(3)A.升高温度能增大反应速率,A正确;
B.扩大容器体积,浓度减小,反应速率减小,B错误;
C.由于体积不变,充入一定量氦气但浓度不变,反应速率不变,C错误;
D.加入催化剂可增大反应速率,D正确;
故选:AD;
(4)由图知平衡时n( )=cV=0.75mol/L×2=1.5mol,则消耗的n( )=3n( )=3×1.5mol=4.5mol,平
衡时 的物质的量为6-4.5=1.5mol。
14.某同学探究外界条件对H O 分解速率的影响
2 2
实验所用试剂:0.4 mol·L-1 H O 溶液、蒸馏水、MnO 粉末、Fe O 粉。
2 2 2 2 3
学科网(北京)股份有限公司实
收集112
验 H O 浓度 V(H O 溶
2 2 2 2 温度 催化剂 mLO 所需时
序 (mol·L-1) 液)(mL) 2
间(s)
号
几乎无气体
1 0.4 20 室温 无
产生
50℃水
2 0.4 20 无 296
浴
3 0.4 20 室温 0.5 g a 45
0.5 g
4 0.4 20 室温 100
MnO 粉末
2
5 0.4 b 室温 a >45
(1)实验1、2的目的是其他条件相同时,研究____对H O 分解速率的影响。
2 2
(2)表中a处所用试剂为_。对比实验3、4可得出的结论是__。
(3)实验3、5是其他条件相同时,探究浓度对该化学反应速率的影响。b处取用10 mL 0.4 mol·L-1 H O 溶液,
2 2
还应添加的试剂及用量为___。
(4)控制其他条件相同,印刷电路板的金属粉末用0.4 mol·L-1 H O 溶液和3.0 mol·L-1 H SO 溶液处理。
2 2 2 4
①请配平方程式:___
Cu + H O + H+— Cu2+ + H O
2 2 2
②某同学在不同温度下完成该实验,测得铜的平均溶解速率分别为:
温度(℃) 20 30 40 50 60 70 80
铜的平均溶解速率
7.34 8.01 9.25 7.98 7.24 6.73 5.76
(×10-3 mol·L-1·min-1)
当温度高于40℃时,铜的平均溶解速率随着反应温度的升高而下降,其主要原因是:______。
【答案】 (1) 温度
(2) Fe O 粉末 其他条件相同时,不同催化剂对H O 分解速率影响不同
2 3 2 2
(3) 10 mL蒸馏水
(4) ① 1 1 2 1 2 ② 温度高于40℃时,有较多H O 分解,反应物浓度降低,使铜的平均溶
2 2
解速率降低
学科网(北京)股份有限公司【解析】
(1)由控制变量法可知,实验1、2的目的是其他条件相同时,研究温度对H O 分解速率的影响;
2 2
(2) 实验3、4是Fe O 粉末相比MnO 粉末具有更高的催化效率,对比实验3、4可得出的结论是其他条件
2 3 2
相同时,不同催化剂对H O 分解速率影响不同;
2 2
(3)为了保持溶液体积相同,此处还应添加的试剂及用量为10 mL蒸馏水;
(4) ①由得失电子守恒,电荷守恒:Cu+H O +2H+=Cu2+ +2H O;②温度高于40℃后,随着温度的升高,
2 2 2
H O 的分解速率加快,使溶液中H O 的浓度降低的更快,对铜的溶解速率的影响超过了温度升高对铜溶解
2 2 2 2
速率的影响,所以铜的溶解速率逐渐减小。
15.回收利用硫和氮的氧化物是保护环境的重要举措。
(1)H S与CO 在高温下发生反应:H S(g)+CO (g) COS(g)+H O(g)。在610K时,将0.10molCO 与0.40molH S
2 2 2 2 2 2 2
充入2.5L的空钢瓶中,反应平衡后水的物质的量分数为0.02。H S的平衡转化率α =___%。
2 1
(2)在620K重复实验,平衡后水的物质的量分数为0.03,H S的转化率α __α ,该反应的ΔH__0。(填“>”“<”
2 2 1
或“=”)
(3)向反应器中再分别充入下列气体,能使H S转化率增大的是__(填标号)。
2
A.H S B.CO C.COS D.N
2 2 2
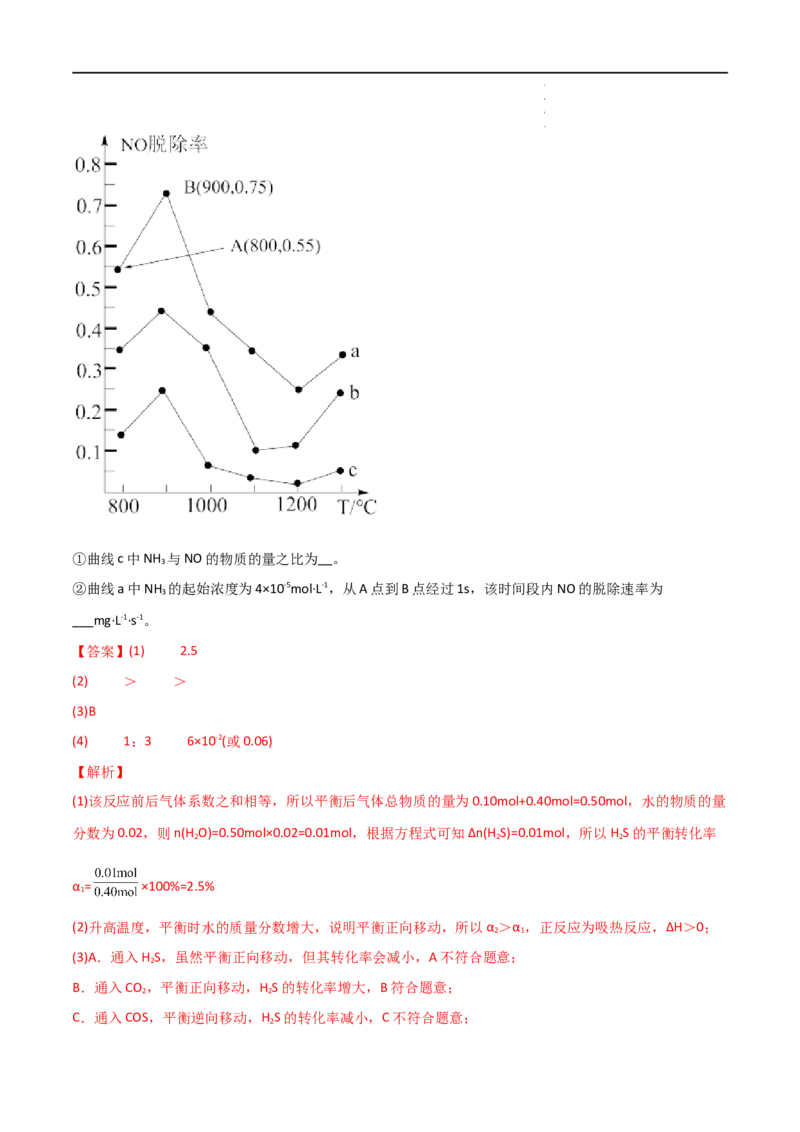
(4)用NH 消除NO污染的反应原理为:4NH (g)+6NO(g) 5N (g)+6H O(l) ΔH=-1807.98kJ·mol-1。不同温度条件
3 3 2 2
下,NH 与NO的物质的量之比分别为4∶1、3∶1、1∶3,得到NO脱除率曲线如图所示。
3
学科网(北京)股份有限公司①曲线c中NH 与NO的物质的量之比为__。
3
②曲线a中NH 的起始浓度为4×10-5mol·L-1,从A点到B点经过1s,该时间段内NO的脱除速率为
3
___mg·L-1·s-1。
【答案】(1) 2.5
(2) > >
(3)B
(4) 1:3 6×10-2(或0.06)
【解析】
(1)该反应前后气体系数之和相等,所以平衡后气体总物质的量为0.10mol+0.40mol=0.50mol,水的物质的量
分数为0.02,则n(H O)=0.50mol×0.02=0.01mol,根据方程式可知Δn(H S)=0.01mol,所以H S的平衡转化率
2 2 2
α = ×100%=2.5%
1
(2)升高温度,平衡时水的质量分数增大,说明平衡正向移动,所以α >α ,正反应为吸热反应,ΔH>0;
2 1
(3)A.通入H S,虽然平衡正向移动,但其转化率会减小,A不符合题意;
2
B.通入CO ,平衡正向移动,H S的转化率增大,B符合题意;
2 2
C.通入COS,平衡逆向移动,H S的转化率减小,C不符合题意;
2
学科网(北京)股份有限公司D.恒容通入N ,各物质的浓度不改变,平衡不移动,D不符合题意;
2
综上所述答案为B;
(4)①当NO的量一定时,通入NH 平衡正向移动,NO的脱除率增大,即NH 与NO的物质的量之比越大,
3 3
NO的脱除率越大,相同温度时,曲线c表示的NO脱除率最小,所以曲线c中NH 与NO的物质的量之比为
3
1:3;
②根据①的分析可知曲线a中NH 与NO的物质的量之比为4∶1,NH 的起始浓度为4×10-5mol·L-1,则NO的
3 3
起始浓度为1×10-5mol·L-1,从A到B,NO的脱除率由0.55变为0.75,所以该时间段内NO的脱除速率为
=6×10-2(或0.06) mg·L-1·s-1。
学科网(北京)股份有限公司学科网(北京)股份有限公司