文档内容
化学试题 第1页(共8页) 化学试题 第2页(共8页)
………………○………………线………………○………………订………………○………………装………………○………………外………………○………………
______________________:号考_______________:级班_____________:名姓______________:校学
…
………………○………………线………………○………………订………………○………………装………………○………………内………………○………………
绝密★启用前 电解
4.据报道,我国科学家研制出一种低压高效电催化还原CO 的新方法,其总反应为NaClCO NaClO
2 2
2024 届高三 1 月大联考考后强化卷(河北卷)
CO。设N 为阿伏加德罗常数的值,下列说法正确的是
A
化 学
A.1 mol CO 中含有的σ键数目为2N
2 A
B.标准状况下,11.2 L CO 和CO混合气体中含C原子数目为N
2 A
本卷满分100分,考试时间75分钟。
C.1 L 0.1 mol·L−1 NaClO溶液中含有的ClO−数目为0.1N
A
注意事项:
D.理论上,上述反应中若有22 g CO 被还原,则转移电子数目为2N
2 A
1.答卷前,考生务必将自己的姓名、准考证号等填写在答题卡和试卷指定位置上。
5.Z是医药工业和香料工业的重要中间体,其合成路线如图所示。下列说法正确的是
2.回答选择题时,选出每小题答案后,用铅笔把答题卡上对应题目的答案标号涂黑。如需改动,用橡皮
擦干净后,再选涂其他答案标号。回答非选择题时,将答案写在答题卡上。写在本试卷上无效。
3.考试结束后,将本试卷和答题卡一并交回。
可能用到的相对原子质量:H 1 B 11 C 12 N 14 O 16 Na 23
A.X和Y互为同系物
一、选择题:本题共14小题,每小题3分,共42分。在每小题给出的四个选项中,只有一项是符合题目要
B.X→Y属于取代反应
求的。
C.X苯环上的二氯代物有6种
1.2023年“文化和自然遗产日”非遗宣传展示活动主题是“加强非遗系统性保护,促进可持续发展”。下列说法
正确的是 D.Z与足量H 2 完全加成后分子中存在2个手性碳原子
A.龙泉青瓷的主要成分是石灰石 6.下列有关微粒的结构和性质的说法正确的是
B.狼毫毛笔的笔头主要成分是多糖 A.H O 和C H 的空间结构均为直线形
2 2 2 2
C.制作黑茶的发酵工艺中发生了化学变化
B.NH 和BF 的VSEPR模型均为平面三角形
3 3
D.非遗油纸伞中桐油(一种植物油)属于烃类
C.邻羟基苯甲酸沸点比对羟基苯甲酸沸点高
2.利用柠檬真菌青霉生成的前体可生产瑞舒伐他汀类药物,该类药物对降低胆固醇有积极作用,某种伐他汀
D.OF 和NCl 均是极性分子,且NCl 分子的键角较大
类药物结构如图,下列关于该物质的说法正确的是 2 3 3
7.近年我国在科技领域取得了举世瞩目的成就,下列成就所涉及的化学知识错误的是
A.蛟龙潜水器外壳的钛合金材料具有耐高压、耐腐蚀的特点
B.华龙一号核电站反应堆所用铀棒中含有的235U与238U互为同位素
92 92
C.长征七号运载火箭使用的液氢燃料具有高能、无污染的特点
D.北斗组网卫星所使用的光导纤维是一种有机高分子材料
8.一种由短周期主族元素组成的化合物(如图所示)具有良好的储氢性能,其中元素W、X、Y、Z的原子序数
A.含有五种官能团
依次增大,且原子序数之和为24,下列有关叙述正确的是
B.遇FeCl 溶液能发生显色反应
3
C.可发生氧化反应、水解反应
D.1 mol该物质最多消耗4 mol NaOH
3.下列说法正确的是
A.浓硫酸具有强氧化性,常温下不可用铝罐盛装
A.电负性大小顺序:YXW
B.碳单质具有还原性,高温下能将二氧化硅还原为硅
B.同周期中第一电离能处于X和Y之间的元素有3种
C.氧化铝的熔点很高,可用于制造熔融烧碱的坩埚
C.基态原子未成对电子数:WXY
D.侯氏制碱法的基本原理是向饱和NaCl溶液中依次通入过量CO 、NH ,析出沉淀
2 3 D.X的最高价氧化物对应的水化物为三元弱酸化学试题 第3页(共8页) 化学试题 第4页(共8页)
………………○………………内………………○………………装………………○………………订………………○………………线………………○………………
此
卷
只
装
订
不
密
封
………………○………………外………………○………………装………………○………………订………………○………………线………………○………………
9.下列操作、现象和结论均正确且有关联性的是
选项 操作及现象 结论
A 向品红溶液中通入氯气,品红溶液褪色 氯气有漂白性
B 向酸性KMnO 溶液中滴加乙醇,溶液褪色 乙醇表现还原性
4
C 在酚酞溶液中加入Na O 粉末,溶液先变红后褪色 Na O 表现碱性
2 2 2 2 c c
A.温度T下,0~40 s内v(N )= 0 1 molL1s1
2 40
D 在充满NO 的集气瓶中加入烘干的活性炭,气体颜色变浅 活性炭表现还原性
2
B.M点v (N )小于N点v (N )
正 2 逆 2
10.以炼铁厂锌灰(主要成分为ZnO,含少量的CuO、MnO 、Fe O )为原料制备ZnO的工艺流程如下。
2 2 3 C.曲线b对应的条件改变可能是充入氧气
D.若曲线b对应的条件改变是升高温度,则H 0
13.我国科研工作者通过研发新型催化剂,利用太阳能电池将工业排放的CO 转化为HCOOH,实现碳中和
2
目标,原理如图所示。下列说法正确的是
已知:浸取工序中ZnO、CuO分别转化为[Zn(NH ) ]2和[Cu(NH ) ]2。
3 4 3 4
下列说法正确的是
A.“浸取”采用较高温度更有利于提高浸取率
B.“滤渣①”经稀盐酸溶浸、过滤可获得MnO
2
C.“除杂”的主要目的是将铁元素从溶液中分离
D.“煅烧”时加入焦炭可提高ZnO的产率
11.一种铜的溴化物晶胞结构如图所示。下列说法正确的是
A.该过程中存在的能量转化形式只有太阳能→化学能
B.离子交换膜为阴离子交换膜
C.P极的电极反应式为CO 2e 2H=HCOOH
2
D.N极催化转化22.4LH 时,P极生成HCOOH的质量为46g
2
14.常温下,弱酸HA与弱碱MOH分别用强碱或强酸调节pH时,HA、A−、MOH和M+的分布分数δ(X)与
溶液pH的关系如图所示。
A.该化合物的化学式为CuBr
2
B.铜原子的配位数为12
C.与每个Br紧邻的Br有6个
1 1 1
D.由图中P点和Q点原子的分数坐标,可确定R点原子的分数坐标为( ,, )
4 4 4
12.汽车尾气中产生NO的反应为N 2 g+O 2 g 2NOg H 。一定条件下,等物质的量N 2 (g)和O 2 (g)
在恒容密闭容器中反应,曲线a表示该反应在温度T下c(N )随反应时间(t)的变化,曲线b表示该反应在
2
某一起始条件改变时c(N )随反应时间(t)的变化。下列叙述错误的是
2化学试题 第5页(共8页) 化学试题 第6页(共8页)
………………○………………线………………○………………订………………○………………装………………○………………外………………○………………
______________________:号考_______________:级班_____________:名姓______________:校学
…
………………○………………线………………○………………订………………○………………装………………○………………内………………○………………
c(HA) ③________________(填操作名称)后进行蒸馏,收集150~156 ℃的馏分。
已知:以HA分子为例,存在δ(HA)= 。下列说法正确的是
c(HA)+c(A)
(6)数据处理。反应开始时加入8.4 mL(0.08 mol)环己醇和过量的酸化的Na CrO 溶液。实验结束后收集
2 2 7
A.MA溶液中水的电离程度高于纯水
到产品0.06 mol,则该合成反应的产率为____________。
B.MOH的电离常数K (MOH)=10−9.25
b
16.(14分)我国铂族金属储量占世界储量的0.58%,而消费总量占世界消费总量的27%,因此从汽车废弃催
C.等物质的量浓度的HA和NaA的混合溶液中pH>7
化剂中回收铂族金属对可持续发展有重大意义。废弃催化剂中含有Pt,还含有少量的Fe O 、MgO、Al O 、
2 3 2 3
D.pH=7的HA与NaOH的混合溶液及HA与MOH的混合溶液中δ(HA)后者大于前者
SiO 。一种从汽车废弃催化剂中回收铂的流程如下:
二、非选择题:本题共4小题,共58分。 2
15.(15分)环己酮可作为涂料和油漆的溶剂。在实验室中以环己醇为原料制备环己酮的原理和装置如图所示
(夹持及加热装置略)。
已知:①长期使用的催化剂,表面会覆盖积碳和有机物;
②Pt溶于王水生成NO和氯铂酸,该酸的阴离子具有正八面体结构,其中Pt为正四价;
③该工艺条件下(常温),有关金属离子开始沉淀和沉淀完全时的pH见下表。
金属离子 Al3+ Mg2+ Fe3+
开始沉淀的pH 3.5 9.5 2.2
已知:环己醇、环己酮的部分物理性质如下表(括号中的沸点数据表示该有机物与水形成的具有固定组成
的恒沸混合物的沸点)。 沉淀完全(c=1.0× 10−5 mol·L−1)的pH 4.7 11.1 3.2
物质 沸点/(℃,1 atm) 密度/(g·cm−3) 溶解性 回答下列问题:
(1)粉碎废弃催化剂后,需进行预处理操作A,请写出操作A的名称 。
环己醇 161.1(97.8) 0.96 能溶于水,易溶于常见有机溶剂
(2)为了提高酸浸效率,温度不宜过高的原因是
环己酮 155.6(95) 0.94 微溶于水 。
回答下列问题: (3)酸浸工序中,铂发生的反应的化学方程式为 ,有同学提议,将王水换成
(1)仪器B的名称是______________________。 盐酸和过氧化氢的混合溶液,请分析优缺点:
(2)酸化Na CrO 溶液时不能选用盐酸,原因是_______________________________________________(用
。
2 2 7
(4)通过调节滤液的pH以回收其他金属,依次析出的金属离子为 ,当Al3+开始沉淀时,溶
离子方程式表示)。
液中的Fe3+浓度为 mol·L−1。
(3)该制备反应很剧烈,且放出大量的热。为控制反应体系温度在55~60 ℃范围内,可采取的措施一是
(5)铂的浸出率与不同加热方式、浸出时间及不同固液比的关系如下图所示:
加热方式选用_________________,二是在加入反应物时将__________________(填化学式)缓慢滴加
到其他试剂中。
(4)制备反应完成后,向混合物中加入适量水,蒸馏,收集95~100 ℃的馏分,得到主要含环己酮和水的
混合物。采用先加入适量水然后蒸馏而非直接蒸馏,原因是__________________________________。
(5)环己酮的提纯过程如下:
①在馏分中加NaCl固体至饱和,静置,分液,加NaCl的目的是______________________________。
②加入无水MgSO 块状固体,目的是__________________________________________________。 4 由图可知,Pt 浸出的最佳条件为 。化学试题 第7页(共8页) 化学试题 第8页(共8页)
………………○………………内………………○………………装………………○………………订………………○………………线………………○………………
此
卷
只
装
订
不
密
封
………………○………………外………………○………………装………………○………………订………………○………………线………………○………………
17.(14分)甲醇既是重要的化工原料,又可作为燃料。利用二氧化碳催化加氢制甲醇,有利于减少温室气体 n
A.温度为T 时,从反应开始到平衡,生成甲醇的平均速率为v(CH OH)= A mol·L-1·min-1
1 3 t
二氧化碳,发生反应:CO (g)+3H (g) CH OH(g)+H O(g)。
2 2 3 2 A
该反应一般认为通过以下步骤实现: B.该反应在T 时的平衡常数比T 时的小
1 2
①CO (g)+H (g) CO(g)+H O(g) ∆H =+41 kJ·mol−1 n(H )
2 2 2 1 C.处于A点的反应体系温度从T 变为T ,达到平衡时 2 增大
1 2 n(CH OH)
②CO(g)+2H (g) CH OH(g) ∆H =−90 kJ·mol−1 3
2 3 2
(1)总反应的∆H = kJ·mol−1;上述反应过程中的能量变化如图1所示,则反应 (填序号)决 D.v 正 (H 2 )=3v 逆 (CH 3 OH)时反应达到化学平衡状态
定了总反应的快慢。
②在T
1
温度时反应达到平衡后,若CO
2
转化率为a,则平衡后容器内的压强与起始压强之比为
。
18.(15分)化合物G是用于治疗充血性心力衰竭药品的合成中间体,其合成路线如下:
(2)在直接以甲醇为燃料的燃料电池中,电解质溶液为酸性,负极的电极反应式为 。
(3)反应②的化学平衡常数K的表达式为 ;图2中能正确反映反应②的平衡常数K随温
度变化关系的曲线为 (填曲线标记字母),其判断理由是
。
回答下列问题:
(1)A的名称为 。
(2)A→B所需的条件和试剂是 。
(3)C→D的化学方程式是 。
(4)D→E的反应类型为 。
(5)G中含氧官能团的名称为 。
(6)F有多种同分异构体,同时满足下列条件的结构共有 种(不考虑立体异构)。
(4)在容积为 2 L的密闭容器中充入 1 mol CO 和 3 mol H 发生反应 CO (g)+3H (g) CH OH(g) a.分子结构中含有苯环,且苯环上有三个取代基
2 2 2 2 3
+ H O(g),在其他条件不变的情况下,分析温度对反应的影响,实验结果如图3所示(注:T 、T 均 b.能发生银镜反应
2 1 2
大于300 ℃):
(7)设计以苯和 为原料合成 的合成路线 。(无机试剂任选)
①下列说法正确的是 (填序号)。2024 届高三 1 月大联考考后强化卷(河北卷)
化学·全解全析
1 2 3 4 5 6 7
C C B A C D D
8 9 10 11 12 13 14
B B B D B C A
1.C 【解析】瓷器是以黏土为主要原料烧制而成的无机非金属材料,主要成分为硅酸盐,A错误;“狼毫”
指的是黄鼠狼尾部的毛,毛的主要成分是蛋白质,B错误;制作黑茶的工艺中包含杀青、揉捻、渥堆等,
其中渥堆是指发酵工序,茶叶的发酵工序中,茶叶在空气中发生氧化还原反应,C正确;桐油的主要化
学成分是脂肪酸甘油三酯,不是烃类化合物,D错误。
2.C 【解析】此分子中含有酯基、碳碳双键、羟基三种官能团,A错误;该分子中不含酚羟基,不能与FeCl
3
溶液发生显色反应,B错误;此分子含有酯基,可发生水解反应,含有碳碳双键,可发生氧化反应,含
有羟基,可发生酯化反应、氧化反应,C正确;1 mol该物质中含有2 mol酯基,最多消耗2 mol NaOH,
D错误。
3.B 【解析】浓硫酸具有强氧化性,常温下与铝发生钝化,可以用铝制品盛放,A错误;单质碳具有还原
性,可将二氧化硅还原为单质硅,B正确;氧化铝与强碱反应,C错误;先向饱和食盐水中通入氨气,
增强溶液的碱性,以吸收更多的二氧化碳,D错误。
4.A 【解析】1个CO 分子中含有2个σ键,故1 mol CO 中含有的σ键数目为2N ,A正确;标准状况
2 2 A
下,11.2 L CO 和CO混合气体为0.5 mol,含C原子数目为0.5N ,B错误;ClO−是弱酸根离子,会发
2 A
生水解反应,故1 L 0.1 mol·L−1 NaClO溶液中含有的ClO−数目小于0.1N ,C错误;上述反应中每生成1
A
个CO分子,C的化合价降低2,转移2个电子,故若有22 g(0.5 mol)CO 被还原,转移电子数目为N ,
2 A
D错误。
5.C 【解析】由X和Y的结构简式可知,X只含酚羟基,Y既含有酚羟基又含有醇羟基,X和Y不是同
类物质,不可能互为同系物,A错误; 与甲醛发生加成反应生成 ,B错误;X苯环上的邻、
间、对二氯代物可以视作二氯苯分子中苯环上的氢原子被酚羟基取代所得结构,共有6种,C正确;Z
与足量氢气完全加成所得分子为结构对称的分子,分子中不存在连有4个不同原子或原子团的手性碳原
子,D错误。
6.D 【解析】H O 中氧原子为sp3杂化,空间结构不是直线形,C H 中碳原子为sp杂化,空间结构为直
2 2 2 2
线形,A错误;NH 中N原子的成键电子对数为3、孤对电子数为1,氮原子为sp3杂化,VSEPR模型
3
为四面体形,BF 中B原子的成键电子对数为3、孤对电子数为0,B原子为sp2杂化,VSEPR模型为平
3
面三角形,B错误;分子内氢键使物质熔沸点降低,分子间氢键使物质熔沸点升高,邻羟基苯甲酸存在
分子内氢键,对羟基苯甲酸存在分子间氢键,则邻羟基苯甲酸的沸点比对羟基苯甲酸的低,C错误;VSEPR
化学 全解全析 第1页(共6页)模型相同的分子,孤对电子数越多,孤对电子对成键电子对的排斥力越大,分子的键角越小,OF 中的
2
中心氧原子中孤对电子数为2,NCl 中的中心氮原子孤对电子数为1,则NCl 分子的键角大于OF 分子
3 3 2
的键角,D正确。
7.D 【解析】钛合金性能优越,具有强度大、耐腐蚀等特点,广泛用于航空、航天等领域,也用于制造潜
水器外壳,A正确;235U与238U为质子数相同,中子数不同的同种元素的不同核素,互为同位素,B正
92 92
确;液氢燃烧生成水,具有高能、无污染的特点,C正确;光导纤维是由二氧化硅制得,二氧化硅属于
无机非金属材料,D错误。
8.B 【解析】根据题目信息和题给物质结构推出W、X、Y、Z分别为H、B、N、Na。同周期元素从左到
右电负性逐渐增大,结合NaBH 中B显+3价,H显−1价知,电负性大小顺序为:NHB,A错误;
4
同周期元素中第一电离能处于B和N之间的元素有Be、C、O 3种,B正确;基态原子未成对电子数:
H=B<N,C错误;元素B的最高价氧化物对应的水化物H BO 为一元弱酸,D错误。
3 3
9.B 【解析】氯气没有漂白性,向品红溶液中通入氯气,品红溶液褪色,是因为氯气和水反应生成的次氯
酸具有漂白性,故A错误;向酸性KMnO 溶液中滴加乙醇,溶液褪色,说明高锰酸钾与乙醇发生氧化
4
还原反应,则乙醇表现还原性,故B正确;在酚酞溶液中加入Na O 粉末,溶液先变红是因为过氧化钠
2 2
和水反应生成的氢氧化钠具有碱性,后褪色是因为过氧化钠与水反应生成的中间产物H O 具有强氧化
2 2
性,故C错误;在充满NO 的集气瓶中加入烘干的活性炭,气体颜色变浅,是因为活性炭具有吸附性,
2
故D错误。
10.B 【解析】“浸取”时温度过高会导致碳酸氢铵和一水合氨分解,A错误;由分析可知,滤渣1的主要
成分为Fe O 和MnO ,用稀盐酸溶浸时Fe O 溶解,得到MnO ,B正确;加入过量锌粉发生的反应
2 3 2 2 3 2
为Zn+[Cu(NH ) ]2+=Cu+[Zn(NH ) ]2+,“除杂”的主要目的是将铜元素从溶液中分离出来,C错误;“煅
3 4 3 4
烧”时加入焦炭,ZnO会变为单质Zn,会降低ZnO的产率,D错误。
1 1
11.D 【解析】该晶胞中,溴原子位于8个顶点和6个面心,共有8 6 4个,铜原子位于晶胞内部,
8 2
共有4个,故该化合物的化学式为CuBr,A错误;1个铜原子连接4个溴原子,则铜原子的配位数是
4,B错误;溴原子位于晶胞的顶点和面心,与干冰结构类似,所以与每个Br紧邻的Br有12个,C错
1 1 1 1
误;R点原子在x、y、z三个坐标轴中的坐标均为 ,故坐标参数为( ,, ),D正确。
4 4 4 4
c c
12.B 【解析】温度T下,0~40 s内氮气的浓度从c mol·L−1减少到c mol·L−1,故v(N )= 0 1 molL1s1,
0 1 2 40
A正确;M点、N点反应均正向进行,且M点反应物浓度大,故M点氮气的正反应速率大于N点氮
气的逆反应速率,B错误;曲线b可能是充入氧气,反应速率加快,反应更快达到平衡,且平衡正向移
动,平衡时氮气的浓度比曲线a对应平衡时的小,C正确;若曲线b相对曲线a升温,则说明升温平衡
正向移动,则正反应为吸热反应,D正确。
13.C 【解析】光伏电池产生电能是太阳能→电能,光伏电池电解是电能→化学能,A错误;阴极(P极)
消耗氢离子,需要补充氢离子,则离子交换膜为阳离子交换膜或质子交换膜,B错误;P极的电极反应
化学 全解全析 第2页(共6页)式为CO 2e 2H=HCOOH,C正确;N极催化转化22.4LH 时,没有说明是标准状况下,无法计
2 2
算,D错误。
c(H)c(A)
14.A 【解析】由图可知,当c(HA)= c(A−)时,溶液pH为4.75,则K (HA)= = c(H+)=10−4.75;
a c(HA)
c(M)c(OH)
当c(MOH)= c(M+)时,溶液pH为9.25,则K (MOH)= = c(OH−)=10−4.75。MA属于弱酸弱
b c(MOH)
碱盐,M+和A−在溶液中都发生水解反应,促进水的电离,则MA溶液中水的电离程度高于纯水,A正
c(HA)c(OH)
确;由上述分析可知,MOH的电离常数K (MOH)=10−4.75,B错误;A−的水解常数K = =
b h c(A)
c(HA) c(H)c(OH) K 1014
= w = =10−9.25<K (HA),则等物质的量浓度的HA和NaA的
c(H)c(A) 1 K (HA) 104.75 a
a
混合溶液中HA的电离程度大于A−的水解程度,混合溶液pH<7,C错误;温度不变,电离平衡常数不
变,溶液pH相等时,分布分数δ(HA)相等,D错误。
15.(15分)
(1)分液漏斗(2分)
(2)CrO214H 6Cl=2Cr3 3Cl 7H O(2分)
2 7 2 2
(3)水浴(加热)(1分) Na CrO (1分)
2 2 7
(4)使环己醇溶于水中,同时使环己酮与水形成恒沸混合物被蒸馏出来,减少能耗(2分)
(5)①降低环己酮在水中的溶解度,增大水层的密度,便于分层(2分)
②除去有机物中的少量水(或干燥)(2分) ③过滤(1分)
(6)75%(2分)
【解析】(1)由装置图知,仪器B的名称是分液漏斗。
(2)盐酸和 Na CrO 能发生氧化还原反应,对应的离子方程式为 CrO2 14H 6Cl=2Cr3
2 2 7 2 7
3Cl 7H O,故酸化Na CrO 溶液时不能选用盐酸。
2 2 2 2 7
(3)为控制反应体系温度在55~60 ℃范围内,可采取水浴加热的方式,且在加入反应物时将Na CrO 溶
2 2 7
液缓慢滴加入其他试剂中,避免反应太过剧烈,短时间内放出大量热。
(4)制备反应完成后,向混合物中加入适量水,蒸馏,收集95~100 ℃的馏分,得到主要含环己酮和水
的混合物。由表格中信息知,采用先加入适量水然后蒸馏而非直接蒸馏,原因是使环己醇溶于水中,
同时使环己酮与水形成恒沸混合物被蒸馏出来,减少能耗。
(5)①提纯环己酮过程中,在馏分中加NaCl固体至饱和,可降低环己酮在水中的溶解度,增大水层的
密度,便于混合液分层而分出环己酮;②无水MgSO 块状固体是一种干燥剂,加入无水MgSO 块状固
4 4
体可除去有机物中的少量水;③过滤后进行蒸馏,收集150~155 ℃的馏分,即可得到环己酮。
(6)反应开始时加入了8.4 mL(0.08 mol)环己醇和过量的酸化的Na CrO 溶液,则理论上得到0.08 mol
2 2 7
0.06mol
环己酮,实验结束后实际收集到0.06 mol产品,则该合成反应的产率为 100%75%。
0.08mol
化学 全解全析 第3页(共6页)16.(14分)
(1)焙烧(或煅烧、灼烧等) (2分)
(2)HCl、HNO 均易挥发,且HNO 易分解(2分)
3 3
(3)3Pt + 4HNO + 18HCl=3H PtCl + 4NO↑+ 8H O(2分) 优点:避免生成氮的氧化物,污染空气;
3 2 6 2
缺点:温度过高(或由于Fe3+的存在),导致过氧化氢大量分解(2分)
(4)Fe3+、Al3+、Mg2+(2分) 10−5.9(2分)
(5)微波加热到109 ℃,约5分钟,固液比约为2(2分)
【解析】(1)长期使用的催化剂,表面会覆盖积碳和有机物,需要高温加热将有机物和C转化为CO
2
除去。
(2)酸浸溶解金属和金属氧化物,但HNO 和HCl均易挥发,且HNO 高温分解浪费原料。
3 3
(3)根据已知信息②,Pt溶于王水生成NO和氯铂酸,该酸的阴离子具有正八面体结构,其中Pt为正
四价,即Pt被氧化为H PtCl ,反应为3Pt + 4HNO + 18HCl=3H PtCl + 4NO↑+ 8H O。HNO 被还原成
2 6 3 2 6 2 3
NO,会造成污染,而H O 不会,但H O 稳定性差,易分解。
2 2 2 2
(4)从表格数据看金属离子开始沉淀的pH:Fe3+< Al3+<Mg2+,Fe3+先沉淀,然后是Al3+、Mg2+依次沉
淀。由Fe3+完全沉淀时pH=3.2计算得到K [Fe(OH) ]=(10−10.8)3×10−5=10−37.4。Al3+开始沉淀时的pH=3.5
sp 3
K [Fe(OH) ] 1037.4
即c(OH−)=10−10.5 mol·L−1,此时溶液中的Fe3+为 sp 3 = molL1=105.9molL1。
c3(OH) (1010.5)3
(5)从图看,微波加热短时间内浸出率较高,5 min时、固液比为2时浸出率接近100%。
17.(14分)
(1)−49(2分) ①(1分)
(2)CH OH+H O−6e− CO +6H+(2分)
3 2 2
c(CH OH)
(3) 3 (1分) a(2分) 反应②正反应为放热反应,平衡常数随温度升高而减
c(CO)c2(H )
2
小(2分)
(4)①CD(2分) ②(2−a)∶2(2分)
【解析】(1)①CO (g)+H (g) CO(g)+H O(g) ∆H =+41 kJ·mol−1,②CO(g)+2H (g) CH OH(g)
2 2 2 1 2 3
∆H =−90 kJ·mol−1,根据盖斯定律,①+②得CO (g)+3H (g) CH OH(g)+H O(g) ∆H =∆H +∆H =
2 2 2 3 2 1 2
+41 kJ·mol−1−90 kJ·mol−1=−49 kJ·mol−1,反应①的活化能较高,为慢反应,所以反应①决定了该反应的
快慢。
(2)原电池负极发生氧化反应,正极发生还原反应,甲醇在负极失去电子,酸性条件下生成二氧化碳,
由电荷守恒可知,还生成氢离子,负极的电极反应式为CH OH+H O−6e− CO +6H+。
3 2 2
c(CH OH)
(3)反应②CO(g)+2H (g) CH OH(g)的平衡常数表达式K= 3 ;由图1可知,反应②正
2 3 c(CO)c2(H )
2
反应为放热反应,升高温度,平衡向逆反应方向移动,平衡常数减小,曲线a能反映反应②的平衡常
数K随温度变化关系。
(4)根据题给图像分析可知,T 先达到平衡,则T >T ,由温度升高反应速率增大可知T 的反应速率
2 2 1 2
化学 全解全析 第4页(共6页)大于T ,又温度高时平衡状态CH OH的物质的量少,则说明可逆反应CO +3H CH OH+H O向
1 3 2 2 3 2
逆反应方向移动,故正反应为放热反应,则T 时的平衡常数比T 时的大。
1 2
①因为容器的容积为 2 L,温度为 T 时,从反应开始到平衡,生成甲醇的平均速率为 v(CH OH)=
1 3
n
A mol·L-1·min-1,A错误;总反应的正反应为放热反应,根据题给图像分析可知,T 温度下反应先
2t 2
A
达到平衡,则T >T ,升高温度,平衡向逆反应方向移动,该反应在T 时的平衡常数比T 时的大,B
2 1 1 2
错误;处于A点的反应体系温度从T 变为T ,温度升高,平衡向逆反应方向移动,达到平衡时,氢气
1 2
n(H )
物质的量增大、甲醇的物质的量减小,故 2 增大,C正确;v (H )=3v (CH OH)时正逆反应速
n(CH OH) 正 2 逆 3
3
率相等,说明反应达到化学平衡状态,D正确。
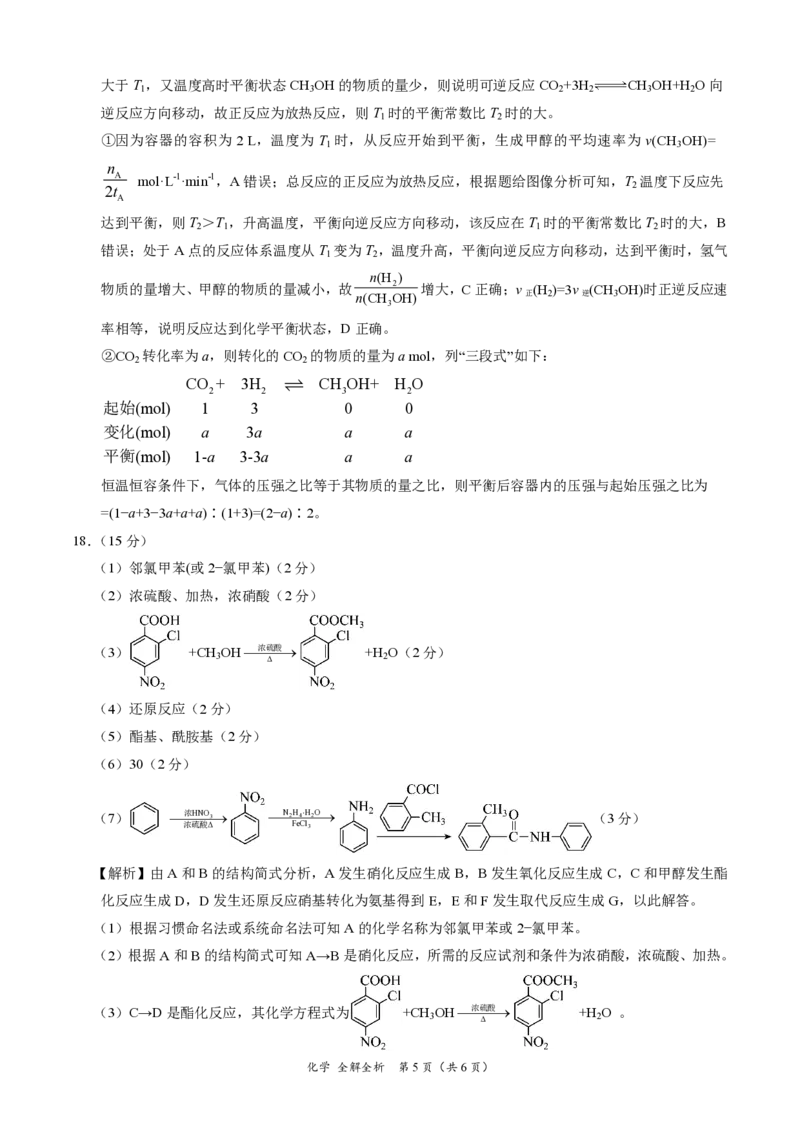
②CO 转化率为a,则转化的CO 的物质的量为a mol,列“三段式”如下:
2 2
CO + 3H CH OH+ H O
2 2 3 2
起始(mol) 1 3 0 0
变化(mol) a 3a a a
平衡(mol) 1-a 3-3a a a
恒温恒容条件下,气体的压强之比等于其物质的量之比,则平衡后容器内的压强与起始压强之比为
=(1−a+3−3a+a+a)∶(1+3)=(2−a)∶2。
18.(15分)
(1)邻氯甲苯(或2−氯甲苯)(2分)
(2)浓硫酸、加热,浓硝酸(2分)
(3) +CH OH浓硫酸 +H O(2分)
3 2
(4)还原反应(2分)
(5)酯基、酰胺基(2分)
(6)30(2分)
(7) 浓HNO3 N2H4H2O (3分)
浓硫酸Δ FeCl3
【解析】由A和B的结构简式分析,A发生硝化反应生成B,B发生氧化反应生成C,C和甲醇发生酯
化反应生成D,D发生还原反应硝基转化为氨基得到E,E和F发生取代反应生成G,以此解答。
(1)根据习惯命名法或系统命名法可知A的化学名称为邻氯甲苯或2−氯甲苯。
(2)根据A和B的结构简式可知A→B是硝化反应,所需的反应试剂和条件为浓硝酸,浓硫酸、加热。
(3)C→D是酯化反应,其化学方程式为 +CH OH浓硫酸 +H O 。
3 2
化学 全解全析 第5页(共6页)(4)D→E中“硝基”变为“氨基”,其反应类型为还原反应。
(5)G中含氧官能团的名称是酯基和酰胺基。
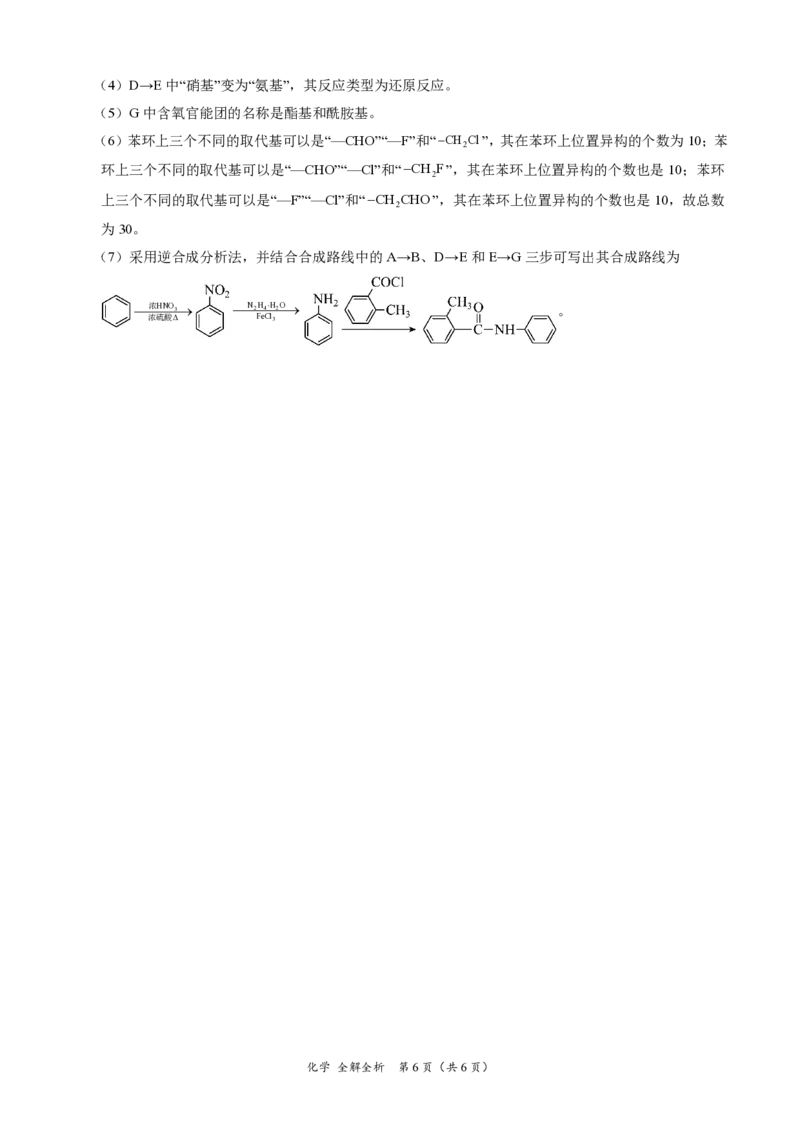
(6)苯环上三个不同的取代基可以是“—CHO”“—F”和“CH Cl”,其在苯环上位置异构的个数为10;苯
2
环上三个不同的取代基可以是“—CHO”“—Cl”和“CH F”,其在苯环上位置异构的个数也是10;苯环
2
上三个不同的取代基可以是“—F”“—Cl”和“CH CHO”,其在苯环上位置异构的个数也是10,故总数
2
为30。
(7)采用逆合成分析法,并结合合成路线中的A→B、D→E和E→G三步可写出其合成路线为
浓HNO3 N2H4H2O 。
浓硫酸Δ FeCl3
化学 全解全析 第6页(共6页)