文档内容
高一下学期第七单元达标检测卷
化 学(A)
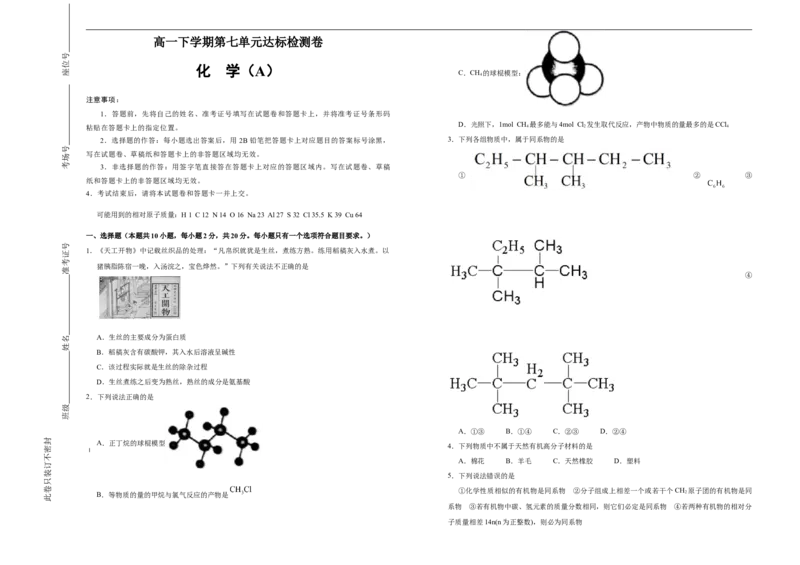
C.CH 的球棍模型:
4
注意事项:
1.答题前,先将自己的姓名、准考证号填写在试题卷和答题卡上,并将准考证号条形码
D.光照下,1mol CH 最多能与4mol Cl 发生取代反应,产物中物质的量最多的是CCl
粘贴在答题卡上的指定位置。 4 2 4
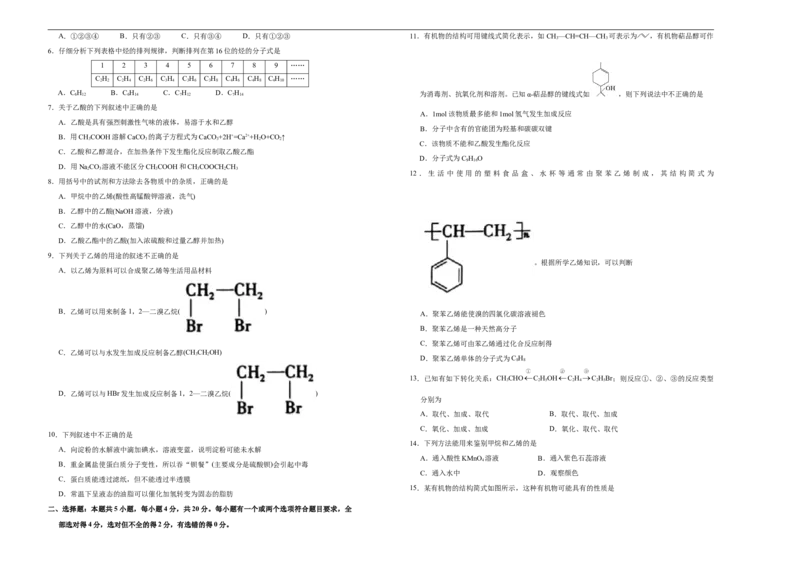
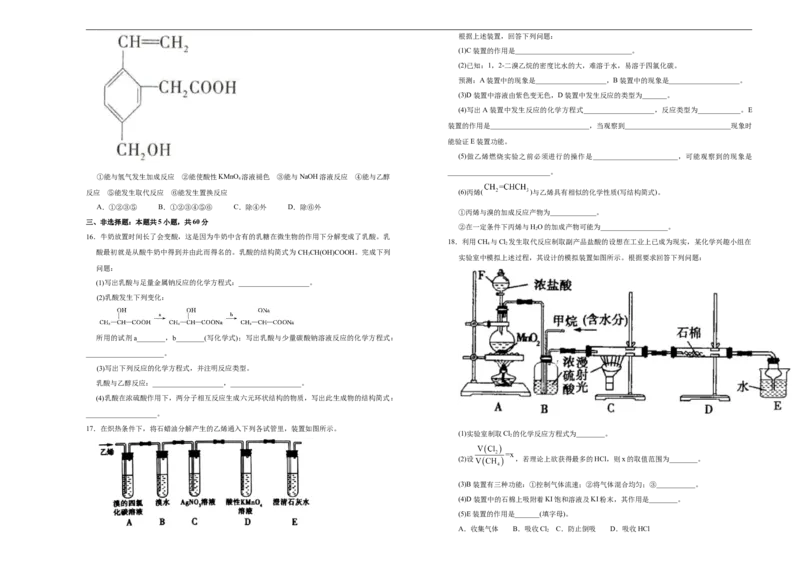
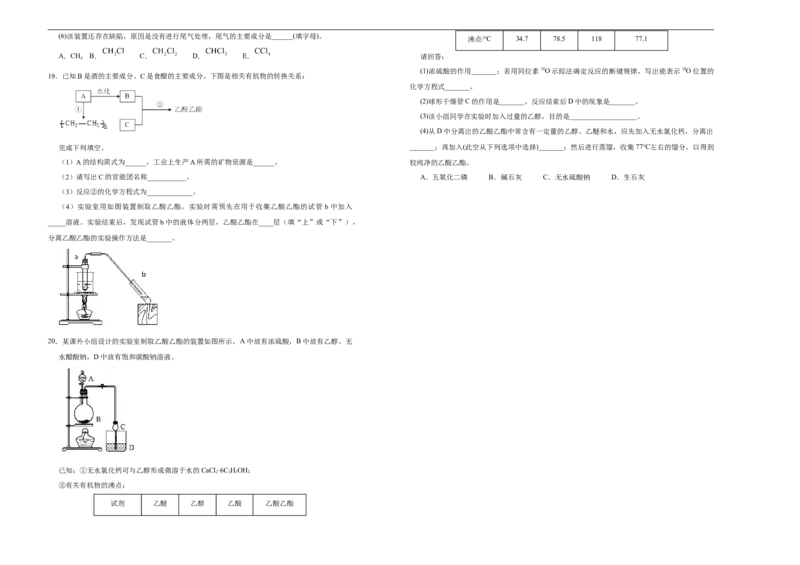
2.选择题的作答:每小题选出答案后,用 2B铅笔把答题卡上对应题目的答案标号涂黑, 3.下列各组物质中,属于同系物的是
写在试题卷、草稿纸和答题卡上的非答题区域均无效。
3.非选择题的作答:用签字笔直接答在答题卡上对应的答题区域内。写在试题卷、草稿
① ② ③
纸和答题卡上的非答题区域均无效。
4.考试结束后,请将本试题卷和答题卡一并上交。
可能用到的相对原子质量:H 1 C 12 N 14 O 16 Na 23 Al 27 S 32 Cl 35.5 K 39 Cu 64
一、选择题(本题共10小题,每小题2分,共20分。每小题只有一个选项符合题目要求。)
1.《天工开物》中记载丝织品的处理:“凡帛织就犹是生丝,煮练方熟。练用稻稿灰入水煮。以
猪胰脂陈宿一晚,入汤浣之,宝色烨然。”下列有关说法不正确的是
④
A.生丝的主要成分为蛋白质
B.稻稿灰含有碳酸钾,其入水后溶液呈碱性
C.该过程实际就是生丝的除杂过程
D.生丝煮练之后变为熟丝,熟丝的成分是氨基酸
2.下列说法正确的是
A.①③ B.①④ C.②③ D.②④
A.正丁烷的球棍模型
4.下列物质中不属于天然有机高分子材料的是
A.棉花 B.羊毛 C.天然橡胶 D.塑料
5.下列说法错误的是
①化学性质相似的有机物是同系物 ②分子组成上相差一个或若干个CH 原子团的有机物是同
B.等物质的量的甲烷与氯气反应的产物是 2
系物 ③若有机物中碳、氢元素的质量分数相同,则它们必定是同系物 ④若两种有机物的相对分
子质量相差14n(n为正整数),则必为同系物
封密不订装只卷此
号位座
号场考
号证考准
名姓
级班A.①②③④ B.只有②③ C.只有③④ D.只有①②③ 11.有机物的结构可用键线式简化表示,如CH—CH=CH—CH 可表示为 ,有机物萜品醇可作
3 3
6.仔细分析下列表格中烃的排列规律,判断排列在第16位的烃的分子式是
1 2 3 4 5 6 7 8 9 ……
C H C H C H C H C H C H C H C H C H ……
2 2 2 4 2 6 3 4 3 6 3 8 4 6 4 8 4 10
A.C 6 H 12 B.C 6 H 14 C.C 7 H 12 D.C 7 H 14 为消毒剂、抗氧化剂和溶剂。已知α-萜品醇的键线式如 ,则下列说法中不正确的是
7.关于乙酸的下列叙述中正确的是
A.1mol该物质最多能和1mol氢气发生加成反应
A.乙酸是具有强烈刺激性气味的液体,易溶于水和乙醇
B.分子中含有的官能团为羟基和碳碳双键
B.用CHCOOH溶解CaCO 的离子方程式为CaCO +2H+=Ca2++H O+CO↑
3 3 3 2 2
C.该物质不能和乙酸发生酯化反应
C.乙酸和乙醇混合,在加热条件下发生酯化反应制取乙酸乙酯
D.分子式为C H O
9 16
D.用NaCO 溶液不能区分CHCOOH和CHCOOCH CH
2 3 3 3 2 3
12 . 生 活 中 使 用 的 塑 料 食 品 盒 、 水 杯 等 通 常 由 聚 苯 乙 烯 制 成 , 其 结 构 简 式 为
8.用括号中的试剂和方法除去各物质中的杂质,正确的是
A.甲烷中的乙烯(酸性高锰酸钾溶液,洗气)
B.乙醇中的乙酸(NaOH溶液,分液)
C.乙醇中的水(CaO,蒸馏)
D.乙酸乙酯中的乙酸(加入浓硫酸和过量乙醇并加热)
9.下列关于乙烯的用途的叙述不正确的是
。根据所学乙烯知识,可以判断
A.以乙烯为原料可以合成聚乙烯等生活用品材料
B.乙烯可以用来制备1,2—二溴乙烷( )
A.聚苯乙烯能使溴的四氯化碳溶液褪色
B.聚苯乙烯是一种天然高分子
C.聚苯乙烯可由苯乙烯通过化合反应制得
C.乙烯可以与水发生加成反应制备乙醇(CHCHOH)
3 2
D.聚苯乙烯单体的分子式为C H
8 8
13.已知有如下转化关系:CHCHO C HOH C H C HBr;则反应①、②、③的反应类型
3 2 5 2 4 2 5
D.乙烯可以与HBr发生加成反应制备1,2—二溴乙烷( )
分别为
A.取代、加成、取代 B.取代、取代、加成
C.氧化、加成、加成 D.氧化、取代、取代
10.下列叙述中不正确的是
14.下列方法能用来鉴别甲烷和乙烯的是
A.向淀粉的水解液中滴加碘水,溶液变蓝,说明淀粉可能未水解
A.通入酸性KMnO 溶液 B.通入紫色石蕊溶液
4
B.重金属盐使蛋白质分子变性,所以吞“钡餐”(主要成分是硫酸钡)会引起中毒
C.通入水中 D.观察颜色
C.蛋白质能透过滤纸,但不能透过半透膜
15.某有机物的结构简式如图所示,这种有机物可能具有的性质是
D.常温下呈液态的油脂可以催化加氢转变为固态的脂肪
二、选择题:本题共5小题,每小题4分,共20分。每小题有一个或两个选项符合题目要求,全
部选对得4分,选对但不全的得2分,有选错的得0分。根据上述装置,回答下列问题:
(1)C装置的作用是_________________________________。
(2)已知:1,2-二溴乙烷的密度比水的大,难溶于水,易溶于四氯化碳。
预测:A装置中的现象是____________________,B装置中的现象是____________________。
(3)D装置中溶液由紫色变无色,D装置中发生反应的类型为_______。
(4)写出A装置中发生反应的化学方程式____________________,反应类型为____________。E
装置的作用是____________________________,当观察到______________________________现象时
能验证E装置功能。
(5)做乙烯燃烧实验之前必须进行的操作是________________________,可能观察到的现象是
_____________________________。
①能与氢气发生加成反应 ②能使酸性KMnO 溶液褪色 ③能与NaOH溶液反应 ④能与乙醇
4
反应 ⑤能发生取代反应 ⑥能发生置换反应 (6)丙烯( )与乙烯具有相似的化学性质(写结构简式)。
A.①②③⑤ B.①②③④⑤⑥ C.除④外 D.除⑥外
①丙烯与溴的加成反应产物为_____________。
三、非选择题:本题共5小题,共60分
②在一定条件下丙烯与HO的加成产物可能为___________________。
2
16.牛奶放置时间长了会变酸,这是因为牛奶中含有的乳糖在微生物的作用下分解变成了乳酸。乳
18.利用CH 与Cl 发生取代反应制取副产品盐酸的设想在工业上已成为现实,某化学兴趣小组在
4 2
酸最初就是从酸牛奶中得到并由此而得名的。乳酸的结构简式为 CHCH(OH)COOH。完成下列
3 实验室中模拟上述过程,其设计的模拟装置如图所示。根据要求回答下列问题:
问题:
(1)写出乳酸与足量金属钠反应的化学方程式:____________________。
(2)乳酸发生下列变化:
所用的试剂a________,b________(写化学式);写出乳酸与少量碳酸钠溶液反应的化学方程式:
______________________。
(3)写出下列反应的化学方程式,并注明反应类型。
乳酸与乙醇反应:____________________,____________________。
(4)乳酸在浓硫酸作用下,两分子相互反应生成六元环状结构的物质,写出此生成物的结构简式:
____________________。
17.在炽热条件下,将石蜡油分解产生的乙烯通入下列各试管里,装置如图所示。
(1)实验室制取Cl 的化学反应方程式为________。
2
(2)设 ,若理论上欲获得最多的HCl,则x的取值范围为________。
(3)B装置有三种功能:①控制气体流速;②将气体混合均匀;③___________。
(4)D装置中的石棉上吸附着KI饱和溶液及KI粉末,其作用是________。
(5)E装置的作用是_______(填字母)。
A.收集气体 B.吸收Cl C.防止倒吸 D.吸收HCl
2(6)该装置还存在缺陷,原因是没有进行尾气处理,尾气的主要成分是______(填字母)。
沸点/℃ 34.7 78.5 118 77.1
A.CH B. C. D. E. 请回答:
4
(1)浓硫酸的作用_______;若用同位素18O示踪法确定反应的断键规律,写出能表示18O位置的
19.已知B是酒的主要成分、C是食醋的主要成分。下图是相关有机物的转换关系:
化学方程式_______。
(2)球形干燥管C的作用是_______。反应结束后D中的现象是_______。
(3)该小组同学在实验时加入过量的乙醇,目的是___________________。
(4)从D中分离出的乙酸乙酯中常含有一定量的乙醇、乙醚和水,应先加入无水氯化钙,分离出
完成下列填空。 _______;再加入(此空从下列选项中选择)_______;然后进行蒸馏,收集77℃左右的馏分,以得到
(1)A的结构简式为______,工业上生产A所需的矿物资源是______。 较纯净的乙酸乙酯。
(2)请写出C的官能团名称___________。 A.五氧化二磷 B.碱石灰 C.无水硫酸钠 D.生石灰
(3)反应②的化学方程式为_____________。
(4)实验室用如图装置制取乙酸乙酯。实验时需预先在用于收集乙酸乙酯的试管 b中加入
_____溶液。实验结束后,发现试管b中的液体分两层,乙酸乙酯在____层(填“上”或“下”),
分离乙酸乙酯的实验操作方法是_______。
20.某课外小组设计的实验室制取乙酸乙酯的装置如图所示,A中放有浓硫酸,B中放有乙醇、无
水醋酸钠,D中放有饱和碳酸钠溶液。
已知:①无水氯化钙可与乙醇形成微溶于水的CaCl ·6C HOH;
2 2 5
②有关有机物的沸点:
试剂 乙醚 乙醇 乙酸 乙酸乙酯2020-2021 学年高一下学期第七单元达标检测卷
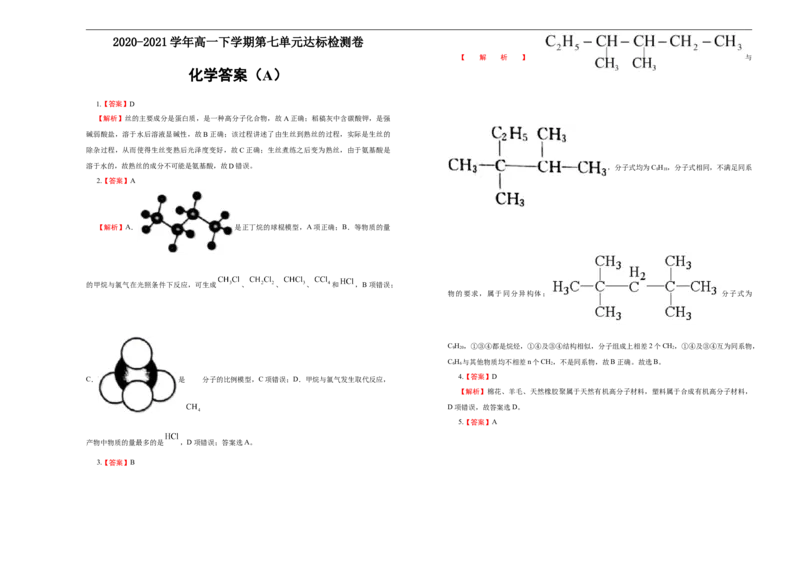
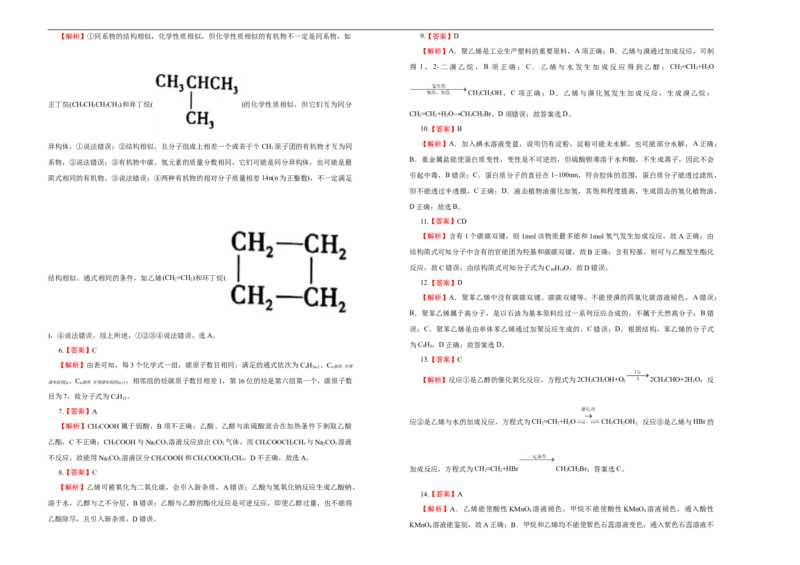
【 解 析 】 与
化学答案(A)
1.【答案】D
【解析】丝的主要成分是蛋白质,是一种高分子化合物,故A正确;稻稿灰中含碳酸钾,是强
碱弱酸盐,溶于水后溶液显碱性,故B正确;该过程讲述了由生丝到熟丝的过程,实际是生丝的
除杂过程,从而使得生丝变熟后光泽度变好,故C正确;生丝煮练之后变为熟丝,由于氨基酸是
溶于水的,故熟丝的成分不可能是氨基酸,故D错误。 ,分子式均为C H ,分子式相同,不满足同系
8 18
2.【答案】A
【解析】A. 是正丁烷的球棍模型,A项正确;B.等物质的量
的甲烷与氯气在光照条件下反应,可生成 、 、 、 和 ,B项错误;
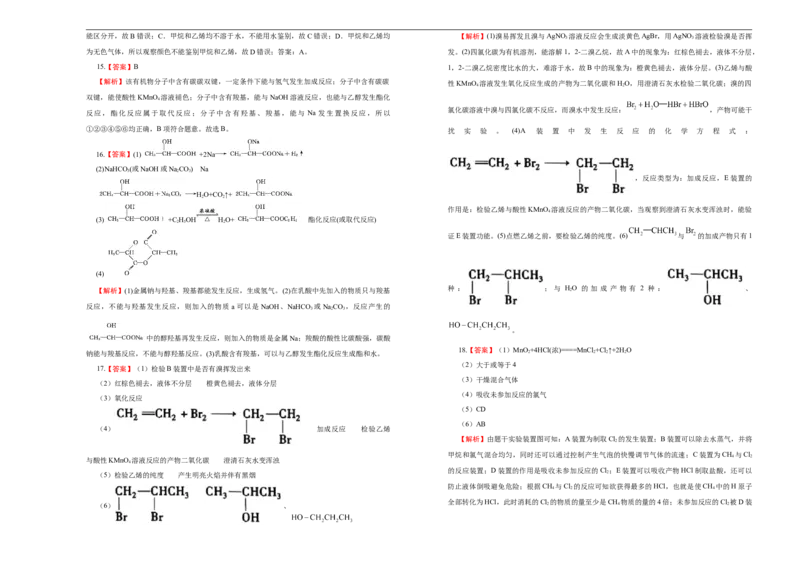
物的要求,属于同分异构体; 分子式为
C H ,①③④都是烷烃,①④及③④结构相似,分子组成上相差2个CH,①④及③④互为同系物,
9 20 2
C H 与其他物质均不相差n个CH,不是同系物,故B正确。故选B。
6 6 2
4.【答案】D
C. 是 分子的比例模型,C项错误;D.甲烷与氯气发生取代反应,
【解析】棉花、羊毛、天然橡胶聚属于天然有机高分子材料,塑料属于合成有机高分子材料,
D项错误,故答案选D。
5.【答案】A
产物中物质的量最多的是 ,D项错误;答案选A。
3.【答案】B【解析】①同系物的结构相似,化学性质相似,但化学性质相似的有机物不一定是同系物,如 9.【答案】D
【解析】A.聚乙烯是工业生产塑料的重要原料,A项正确;B.乙烯与溴通过加成反应,可制
得 1,2-二溴乙烷,B 项正确;C.乙烯与水发生加成反应得到乙醇:CH=CH +H O
2 2 2
CHCHOH,C 项正确;D.乙烯与溴化氢发生加成反应,生成溴乙烷:
3 2
正丁烷(CHCHCHCH)和异丁烷( )的化学性质相似,但它们互为同分
3 2 2 3
CH=CH +H O→CH CHBr,D项错误;故答案选D。
2 2 2 3 2
10.【答案】B
【解析】A.加入碘水溶液变蓝,说明仍有淀粉,淀粉可能未水解,也可能部分水解,A正确;
异构体,①说法错误;②结构相似,且分子组成上相差一个或若干个CH 原子团的有机物才互为同
2
B.重金属盐能使蛋白质变性,变性是不可逆的,但硫酸钡难溶于水和酸,不生成离子,因此不会
系物,②说法错误;③有机物中碳、氢元素的质量分数相同,它们可能是同分异构体,也可能是最
引起中毒,B错误;C.蛋白质分子的直径在1~100nm,符合胶体的范围,蛋白质分子能透过滤纸,
简式相同的有机物,③说法错误;④两种有机物的相对分子质量相差14n(n为正整数),不一定满足
但不能透过半透膜,C正确;D.液态植物油催化加氢,其饱和程度提高,生成固态的氢化植物油,
D正确;故选B。
11.【答案】CD
【解析】含有1个碳碳双键,则1mol该物质最多能和1mol氢气发生加成反应,故A正确;由
结构简式可知分子中含有的官能团为羟基和碳碳双键,故B正确;含有羟基,则可与乙酸发生酯化
反应,故C错误;由结构简式可知分子式为C H O,故D错误。
10 18
结构相似、通式相同的条件,如乙烯(CH=CH )和环丁烷(
2 2 12.【答案】D
【解析】A.聚苯乙烯中没有碳碳双键、碳碳双键等,不能使溴的四氯化碳溶液褪色,A错误;
B.聚苯乙烯属于高分子,是以石油为基本原料经过一系列反应合成的,不属于天然高分子,B错
误;C.聚苯乙烯是由单体苯乙烯通过加聚反应生成的,C错误;D.根据结构,苯乙烯的分子式
),④说法错误。综上所述,①②③④说法错误,选A。
为C H,D正确;故答案选D。
8 8
6.【答案】C
13.【答案】C
【解析】由表可知,每3个化学式一组,碳原子数目相同,满足的通式依次为C H 、C
n 2n-2 n错误: 引用
源未找到2n 、C n错误: 引用源未找到2n+2 ,相邻组的烃碳原子数目相差1,第16位的烃是第六组第一个,碳原子数 【解析】反应①是乙醇的催化氧化反应,方程式为2CH 3 CH 2 OH+O 2 2CH 3 CHO+2H 2 O;反
目为7,故分子式为C H 。
7 12
7.【答案】A
应②是乙烯与水的加成反应,方程式为CH=CH +H O CHCHOH;反应③是乙烯与HBr的
【解析】CHCOOH属于弱酸,B项不正确;乙酸、乙醇与浓硫酸混合在加热条件下制取乙酸 2 2 2 3 2
3
乙酯,C不正确;CHCOOH与NaCO 溶液反应放出CO 气体,而CHCOOCH CH 与NaCO 溶液
3 2 3 2 3 2 3 2 3
不反应,故能用NaCO 溶液区分CHCOOH和CHCOOCH CH,D不正确,故选A。
2 3 3 3 2 3
加成反应,方程式为CH=CH +HBr CHCHBr;答案选C。
8.【答案】C 2 2 3 2
【解析】乙烯可被氧化为二氧化碳,会引入新杂质,A错误;乙酸与氢氧化钠反应生成乙酸钠,
14.【答案】A
溶于水,乙醇与之不分层,B错误;乙酸与乙醇的酯化反应是可逆反应,即使乙醇过量,也不能将
【解析】A.乙烯能使酸性KMnO 溶液褪色,甲烷不能使酸性KMnO 溶液褪色,通入酸性
4 4
乙酸除尽,且引入新杂质,D错误。
KMnO 溶液能鉴别,故A正确;B.甲烷和乙烯均不能使紫色石蕊溶液变色,通入紫色石蕊溶液不
4能区分开,故B错误;C.甲烷和乙烯均不溶于水,不能用水鉴别,故C错误;D.甲烷和乙烯均 【解析】(1)溴易挥发且溴与AgNO 溶液反应会生成淡黄色AgBr,用AgNO 溶液检验溴是否挥
3 3
为无色气体,所以观察颜色不能鉴别甲烷和乙烯,故D错误;答案:A。 发。(2)四氯化碳为有机溶剂,能溶解1,2-二溴乙烷,故A中的现象为:红棕色褪去,液体不分层,
15.【答案】B 1,2-二溴乙烷密度比水的大,难溶于水,故B中的现象为:橙黄色褪去,液体分层。(3)乙烯与酸
【解析】该有机物分子中含有碳碳双键,一定条件下能与氢气发生加成反应;分子中含有碳碳 性KMnO 溶液发生氧化反应生成的产物为二氧化碳和 HO,用澄清石灰水检验二氧化碳;溴的四
4 2
双键,能使酸性KMnO 溶液褪色;分子中含有羧基,能与NaOH溶液反应,也能与乙醇发生酯化
4
氯化碳溶液中溴与四氯化碳不反应,而溴水中发生反应: ,产物可能干
反应,酯化反应属于取代反应;分子中含有羟基、羧基,能与 Na 发生置换反应,所以
①②③④⑤⑥均正确,B项符合题意。故选B。 扰 实 验 。 (4)A 装 置 中 发 生 反 应 的 化 学 方 程 式 :
16.【答案】(1) +2Na
(2)NaHCO (或NaOH或NaCO) Na
3 2 3
,反应类型为:加成反应,E装置的
HO+CO↑+
2 2
作用是:检验乙烯与酸性KMnO 溶液反应的产物二氧化碳,当观察到澄清石灰水变浑浊时,能验
4
(3) +C HOH HO+ 酯化反应(或取代反应)
2 5 2
证E装置功能。(5)点燃乙烯之前,要检验乙烯的纯度。(6) 与 的加成产物只有1
(4)
种 : ; 与 HO 的 加 成 产 物 有 2 种 : 、
【解析】(1)金属钠与羟基、羧基都能发生反应,生成氢气。(2)在乳酸中先加入的物质只与羧基 2
反应,不能与羟基发生反应,则加入的物质 a可以是NaOH、NaHCO 或NaCO ,反应产生的
3 2 3
。
中的醇羟基再发生反应,则加入的物质是金属Na;羧酸的酸性比碳酸强,碳酸
18.【答案】(1)MnO +4HCl(浓)====MnCl +Cl↑+2H O
钠能与羧基反应,不能与醇羟基反应。(3)乳酸含有羧基,可以与乙醇发生酯化反应生成酯和水。 2 2 2 2
(2)大于或等于4
17.【答案】(1)检验B装置中是否有溴挥发出来
(3)干燥混合气体
(2)红棕色褪去,液体不分层 橙黄色褪去,液体分层
(4)吸收未参加反应的氯气
(3)氧化反应
(5)CD
(6)AB
(4) 加成反应 检验乙烯
【解析】由题干实验装置图可知:A装置为制取Cl 的发生装置;B装置可以除去水蒸气,并将
2
甲烷和氯气混合均匀,同时还可以通过控制产生气泡的快慢调节气体的流速;C装置为CH 与Cl
4 2
与酸性KMnO 溶液反应的产物二氧化碳 澄清石灰水变浑浊
4
的反应装置;D装置的作用是吸收未参加反应的Cl ;E装置可以吸收产物HCl制取盐酸,还可以
(5)检验乙烯的纯度 产生明亮火焰并伴有黑烟 2
防止液体倒吸避免危险;根据CH 与Cl 的反应可知欲获得最多的HCl,也就是使CH 中的H原子
4 2 4
全部转化为HCl,此时消耗的Cl 的物质的量至少是CH 物质的量的4倍;未参加反应的Cl 被D装
(6) 、 2 4 2(4)乙醇 C
置吸收,生成的HCl被E装置吸收,取代产物 、 、 为液体,故该实验的尾气
【解析】酸与乙醇反应需浓硫酸作催化剂,该反应为可逆反应,浓硫酸吸水利于平衡向生成乙
酸乙酯方向移动,故浓硫酸的作用为催化剂、吸水剂;羧酸与醇发生的酯化反应中,羧酸中的羧基
主要有未参加反应的CH 和反应生成的 。(1)由实验装置图可知,A是实验室制备氯气的
4
提供-OH,醇中的-OH提供-H,相互结合生成水,其它基团相互结合生成酯,同时该反应可逆,反
装置,故发生的反应为:MnO +4HCl(浓)====MnCl +Cl↑+2H O;(2)氯气与甲烷发生取代反应
2 2 2 2
应的化学方程式为CHCOOH+CH CH18OH CHCO18OC H+H O;(2)圆底烧瓶受热不均,球
3 3 2 3 2 5 2
反应特点是1mol氯气可取代1mol H原子生成1mol HCl,设 =x,若理论上欲获得最多的 形干燥管的管口伸入液面下可能发生倒吸,球形干燥管体积大,可以防止倒吸;乙酸乙酯不溶于饱
和碳酸钠溶液,密度比水小,溶液分层,上层无色油体液体,乙酸和碳酸钠反应而使溶液红色变浅;
氯化氢,则x值应保证甲烷被完全取代,x应大于或等于4,故答案为:大于或等于4;(3)生成
故答案为:防止倒吸;溶液分层;上层无色油体液体,下层溶液颜色变浅。(3)增加乙醇的量有利
的氯气中含有水,B装置除具有控制气流速度、均匀混合气体外,因浓硫酸具有吸水性,还具有干
于反应向生成酯的方向移动,可以提高乙酸的转化率和提高酯的产率。(4)无水氯化钙可与乙醇形
燥作用,故答案为:干燥混合气体;(4)氯气具有氧化性,KI中-1价的碘能被氯气氧化,产物为
成难溶于水的CaCl ·6C HOH,用氯化钙除去少量乙醇,用无水硫酸钠除去少量的水,无水硫酸钠
2 2 5
氯化钾固体和碘单质,反应为Cl+2I−=2Cl−+I ,所以D装置的石棉中均匀混有KI粉末,能吸收过
2 2 吸水形成硫酸钠结晶水合物,不能选择五氧化二磷、碱石灰和生石灰等固体干燥剂,以防乙酸乙酯
量的氯气,故答案为:吸收过量的氯气;(5)装置中最后剩余的氯化氢气体需要吸收不能排放到
在酸性(五氧化二磷遇水生成酸)或碱性条件下水解,故答案为:乙醇;C。
空气中,氯化氢易溶于水需要防止倒吸;故答案为:CD;(6)反应生成的二氯甲烷、三氯甲烷、
四氯化碳均是油状的液体,只有一氯甲烷是气体,还可能有过量的甲烷,可能存在剩余的甲烷和生
成的一氯甲烷等气体,应进行尾气处理,故答案为:AB。
19.【答案】(1)CH =CH 石油
2 2
(2)羧基
(3)CH COOH+CH CHOH CHCOOCH CH+H O
3 3 2 3 2 3 2
(4)饱和碳酸钠 上 分液
【解析】B是酒的主要成分、C是食醋的主要成分,则B为CHCHOH、C为CHCOOH,B与
3 2 3
C 反应生成 CHCOOC H ,A 水化得到乙醇,则 A 为 CH=CH ;(1)A 为乙烯,其结构简式为
3 2 5 2 2
CH=CH ,工业上生产乙烯主要是通过对石油分馏产品的裂解得到;(2)C为乙酸,含有的官能团为
2 2
羧基;(3)反应②是乙酸乙醇在浓硫酸催化作用下生成乙酸乙酯,其反应方程式为
CHCOOH+CH CHOH CHCOOCH CH+H O;(4)为了除去乙酸乙酯中的杂质乙酸和乙
3 3 2 3 2 3 2
醇,一般要把乙酸乙酯蒸汽通入饱和碳酸钠溶液中;乙酸乙酯的密度比水小,则乙酸乙酯在上层,
水溶液在下层;分离互不相溶的液体混合物应选择分液操作。
20.【答案】(1)催化剂、吸水剂 CHCOOH+CH CH18OH CHCO18OC H+H O
3 3 2 3 2 5 2
(2)防止倒吸 溶液分层;上层无色油体液体,下层溶液颜色变浅
(3)增加乙醇的用量,提高乙酸的转化率和提高酯的产率