文档内容
南充高中 2024—2025 学年度上学期第一次月考
高 2024 级化学试题
(审命题:谢国春 马永生)
(考试时间:75分钟 试卷满分:100分)
注意事项:
1.答题前,务必将自己的姓名、班级、考号填写在答题卡规定的位置上。
2.答选择题时,必须使用2B铅笔将答题卡上对应题目的答案标号涂黑,如需改动,用橡皮擦
擦干净后,再选涂其它答案标号。
3.答非选择题时,将答案书写在答题卡相应位置上,写在本试卷上无效。
4.考试结束后将答题卡交回。
可能用到的相对原子质量:H1 C12 N14 O16 Cl35.5
第I卷(选择题共45分)
一、选择题:本题共15个小题,每小题3分,共45分。在每小题给出的四个选项中,只有一项是符合题
目要求的。
1.下列状态下能导电的电解质是( )
A.无水酒精 B.盐酸 C.液态二氧化硫 D.熔融氯化钾
2.分类是化学研究中常用的方法。下列分类方法正确的是( )
A.干冰、冰、胆矾都属于化合物 B.碱性氧化物都能与水化合生成碱
C.混合物一定含两种或两种以上的元素 D. 与 含相同元素,互为同素异形体
3.下列关于胶体的叙述错误的是( )
A.胶体与其他分散系的本质区别是分散质的微粒直径大小不同
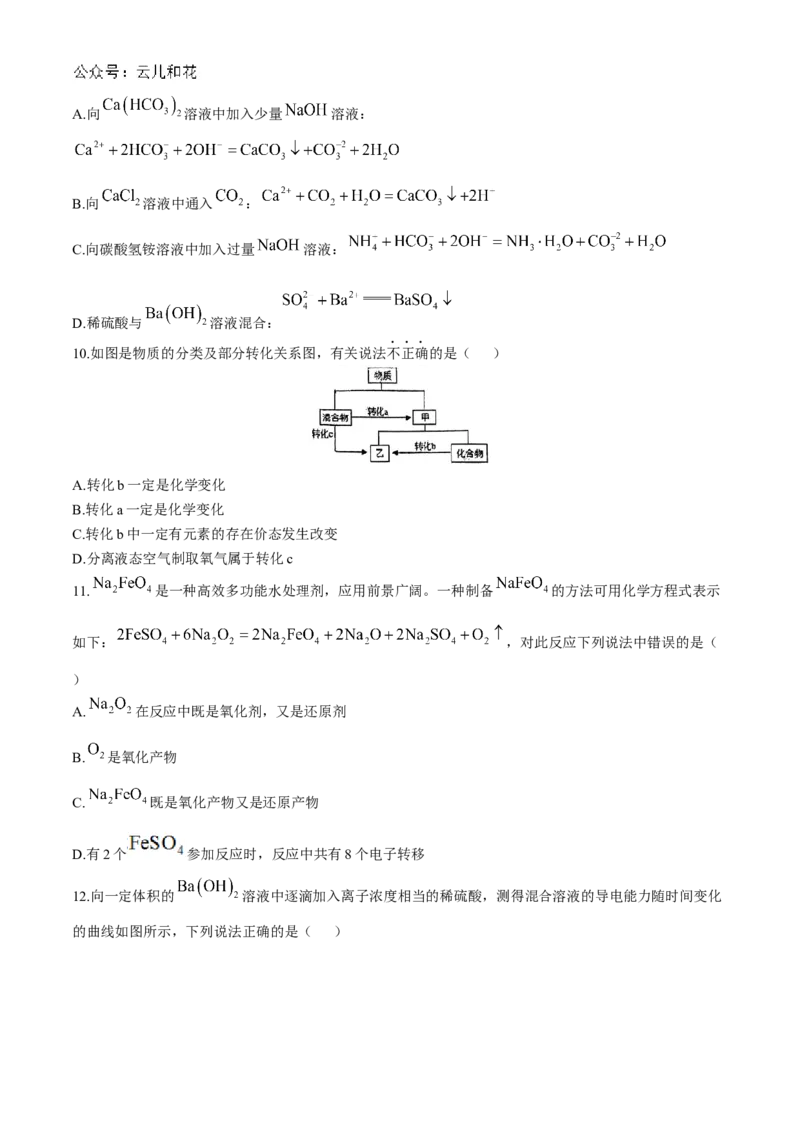
B. 胶体粒子能吸附阳离子,从而使 胶体带有一定电荷
C.用平行光照射 溶液和 胶体时,产生的现象不同
D. 胶体能够使水中悬浮的固体颗粒沉降,达到净水目的
4.NaC1在固体、熔融状态、溶于水三种状态下的导电实验,如图所示。
下列说法正确的是( )
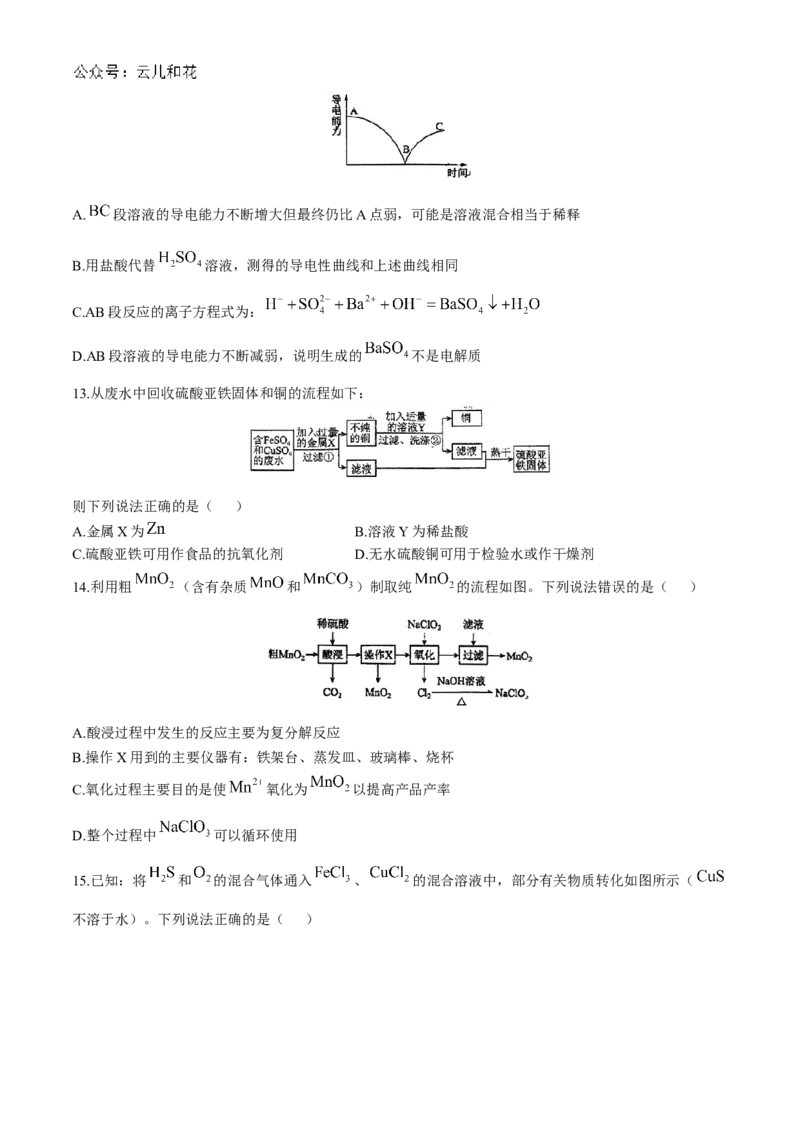
A.固体 中不存在离子,不能导电 B. 通电情况下才能电离C. 表示水合氯离子 D.工业上不能采用电解饱和 溶液制取
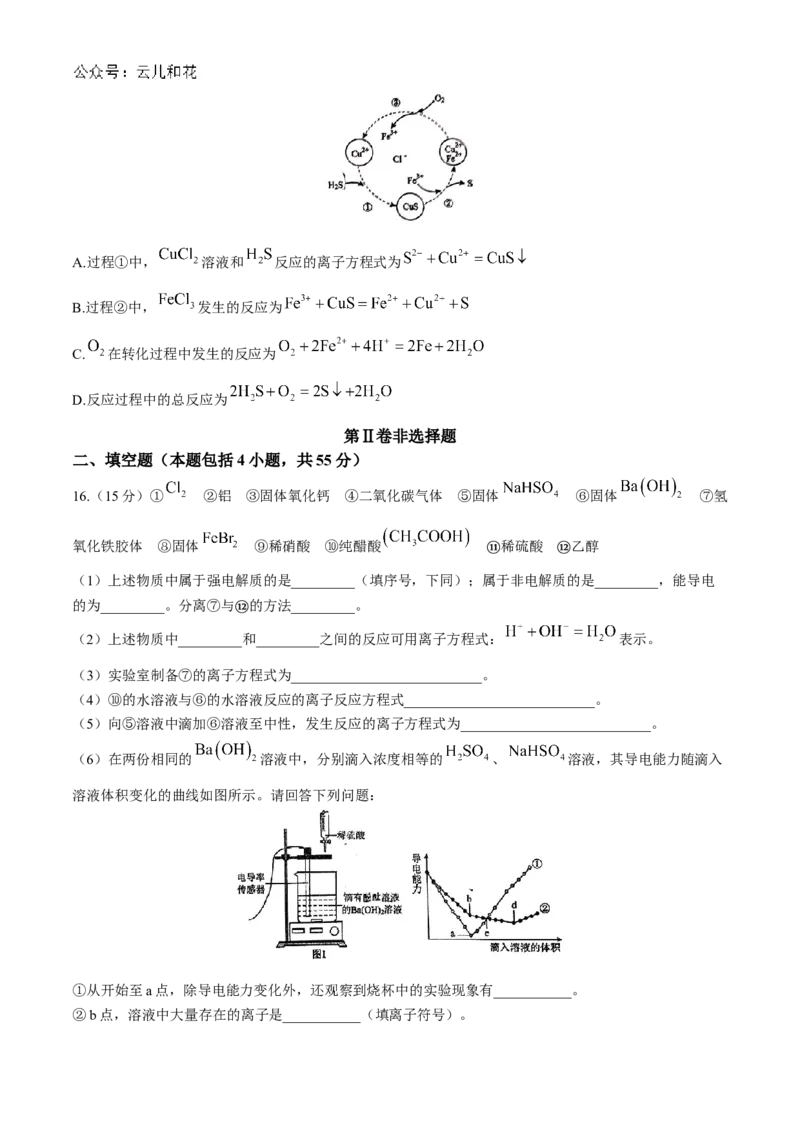
5.下列化学反应中电子转移的表示方法正确的是( )
A. B.
C. D.
6.下列说法正确的是( )
A.金属阳离子被还原一定得到金属单质
B.. 可表示所有的酸碱中和反应
C.失电子越多,还原性越强,得电子越多,氧化性越强
D. 个 与沸水完全反应转化为 胶体, 胶粒的数目少于 个
7.用下图表示的一些物质或概念之间的从属或包含关系中错误的是( )
X Y Z
A 溶液 分散系 混合物
B 碱性氧化物 金属氧化物 氧化物
C 强电解质 电解质 化合物
D 置换反应 氧化还原反应 离子反应
A.A B.B C.C D.D
8.下列溶液中的离子能够大量共存的一组是( )
A.所含溶质为 的溶液中: 、 、 、
B.使紫色石蕊呈红色的溶液中: 、 、 、
C.在澄清透明的溶液中: 、 、 、
D..无色酚酞试液呈红色的溶液中: 、 、 、
9.下列离子方程式与所述事实相符且正确的是( )A.向 溶液中加入少量 溶液:
B.向 溶液中通入 :
C.向碳酸氢铵溶液中加入过量 溶液:
D.稀硫酸与 溶液混合:
10.如图是物质的分类及部分转化关系图,有关说法不正确的是( )
A.转化b一定是化学变化
B.转化a一定是化学变化
C.转化b中一定有元素的存在价态发生改变
D.分离液态空气制取氧气属于转化c
11. 是一种高效多功能水处理剂,应用前景广阔。一种制备 的方法可用化学方程式表示
如下: ,对此反应下列说法中错误的是(
)
A. 在反应中既是氧化剂,又是还原剂
B. 是氧化产物
C. 既是氧化产物又是还原产物
D.有2个 参加反应时,反应中共有8个电子转移
12.向一定体积的 溶液中逐滴加入离子浓度相当的稀硫酸,测得混合溶液的导电能力随时间变化
的曲线如图所示,下列说法正确的是( )A. 段溶液的导电能力不断增大但最终仍比A点弱,可能是溶液混合相当于稀释
B.用盐酸代替 溶液,测得的导电性曲线和上述曲线相同
C.AB段反应的离子方程式为:
D.AB段溶液的导电能力不断减弱,说明生成的 不是电解质
13.从废水中回收硫酸亚铁固体和铜的流程如下:
则下列说法正确的是( )
A.金属X为 B.溶液Y为稀盐酸
C.硫酸亚铁可用作食品的抗氧化剂 D.无水硫酸铜可用于检验水或作干燥剂
14.利用粗 (含有杂质 和 )制取纯 的流程如图。下列说法错误的是( )
A.酸浸过程中发生的反应主要为复分解反应
B.操作X用到的主要仪器有:铁架台、蒸发皿、玻璃棒、烧杯
C.氧化过程主要目的是使 氧化为 以提高产品产率
D.整个过程中 可以循环使用
15.已知:将 和 的混合气体通入 、 的混合溶液中,部分有关物质转化如图所示(
不溶于水)。下列说法正确的是( )A.过程①中, 溶液和 反应的离子方程式为
B.过程②中, 发生的反应为
C. 在转化过程中发生的反应为
D.反应过程中的总反应为
第Ⅱ卷非选择题
二、填空题(本题包括4小题,共55分)
16.(15分)① ②铝 ③固体氧化钙 ④二氧化碳气体 ⑤固体 ⑥固体 ⑦氢
氧化铁胶体 ⑧固体 ⑨稀硝酸 ⑩纯醋酸 ⑪稀硫酸 ⑫乙醇
(1)上述物质中属于强电解质的是_________(填序号,下同);属于非电解质的是_________,能导电
的为_________。分离⑦与⑫的方法_________。
(2)上述物质中_________和_________之间的反应可用离子方程式: 表示。
(3)实验室制备⑦的离子方程式为___________________________。
(4)⑩的水溶液与⑥的水溶液反应的离子反应方程式___________________________。
(5)向⑤溶液中滴加⑥溶液至中性,发生反应的离子方程式为___________________________。
(6)在两份相同的 溶液中,分别滴入浓度相等的 、 溶液,其导电能力随滴入
溶液体积变化的曲线如图所示。请回答下列问题:
①从开始至a点,除导电能力变化外,还观察到烧杯中的实验现象有___________。
②b点,溶液中大量存在的离子是___________(填离子符号)。③曲线②中c点的溶质是___________,c点两溶液中含有相同量的哪种离子___________(填离子符号)。
17.(15分)科学家在研究化学物质时,常常对物质进行分类,属于同一类的物质具有相似性。请回答下
列问题:
(1)右图的分类方法是___________分类法。
(2)氢溴酸(气体溶于水形成的溶液)与盐酸属于同一类,预测下列反应不会发生的________(填序
号)。
A. B.
C. D.
(3)写出 与足量 反应的化学方程式_________________________。
(4)工业上次磷酸( )常用于化学镀银,发生如下反应,请配平:___________。
_______Ag+ +__________ +___ Ag↓ +_______________ ______
(5)某溶液中只可能大量含有 、 、 、 、 、 、 中的若干种,对其进行如
下实验:
i:取少量该溶液于试管中,加入过量BaCl 溶液,产生白色沉淀,过滤;
2
ii:向i中所得滤渣中加入足量盐酸,沉淀全部溶解,并有无色气体生成;
iii:向i中所得滤液中加入足量硝酸酸化后,再加入AgNO 溶液,有白色沉淀生成。回答下列问题:
3
①无需实验即可推断溶液中一定不会大量存在的离子为___________。
②通过实验i可知溶液中一定不会大量存在的离子为___________。
③由实验ii可知溶液中一定不会大量存在的离子为___________,一定大量存在的离子为__________;实
验ii中发生反应的离子方程式为______________________________。
④实验iii__________(填“能”或“不能”)说明该溶液中存在 ;若能请说明理由,若不能请简单设
计实验证明该溶液中是否存在 :__________18、(13分)双氧水( )和水都是极弱电解质,但 溶液显极弱酸性,医疗上利用它有杀菌消
毒作用来清洗伤口。请回答下列问题:
(1)若把 看成是二元弱酸,请写出它在水中的电离方程式:______________。
(2)鉴于 显弱酸性,它能同强碱作用形成“正盐”,在一定条件下也可形成“酸式盐”。请写出
与 作用形成的“正盐”的化学方程式:______________________。
(3)对于下列A~D涉及 的反应,填写空白:
A.
B.
C.
D.
E. (未配平)
① 仅体现还原性的反应是_____________(填代号)。
②上述反应说明 、 、 氧化性由弱剧强的顺序是_____________。
(4)在 的参与下, 可以与 反应制备 纳米颗粒。若 与 的个数之比为
,配平该反应的离子方程式:
_____ +_____ _____ _____ _____ _____ _____
(5)奥运会期间,由于工作人员将84消毒液 与双氧水混用,导致游泳池藻类快速生长,池水变
绿。一种可能的原因是 与 反应产生 促进藻类快速生长。该反应中氧化性:
________ (填“>”或“<”)。反应的离子反应方程式为__________________。
19.(12分)某小组通过实验探究氧化还原反应的规律。
已知:氧化还原反应电位传感器可以测量不同溶液的电位值,根据电位值大小可比较物质的氧化性/还原性
强弱;数值越大,氧化性越强;数值越小,还原性越强。测得几种物质的电位值如表所示。(注:实验中
进行酸化时均用稀硫酸)物质
(酸化) (酸化)
浓度
( 为物质的量浓度的单位)
171 1130 603 662 116 -361
电位值
根据表中数据,回答下列问题:
(1)浓度相同的下列三种溶液,氧化性由强到弱的顺序为__________(填序号)。
① ②酸性 ③酸性
(2)已知 与 不能共存,由此推测下列能大量共存的离子组是__________。
a. 、 b. 、 c. 、 、 d. 、 、
(3)向等浓度的 和 混合溶液滴加少量酸性 溶液(对应还原产物为 ),发生反应
的离子方程式为________________________________________。
(4)已知下列四种氧化剂(均可氧化 )对应的还原产物情况如下:
氧化剂
还原产物
请判断,等数量的四种氧化剂微粒分别与足量 作用,得到 最多的是__________。
(5)结合上述信息思考:对于 、 混合溶液,若控制性氧化 而不氧化 ,请提出两种合理的氧
化方案:①加入__________;②加入__________。
(6) 具有很强的氧化性(还原产物为 ),常被用作消毒剂,其消毒的效率(以单位质量得到的
电子数表示)是 的__________倍(保留两位有效数字)。参考答案
1、B 2、A 3、B 4.C 5.B 6.D 7、D 8.C 9.C 10.B 11.D 12.A 13.C 14.B 15.D
16.
(6)①有白色沉淀产生,溶液由红色变为无色 ②Na+ OH—
③NaOH NaSO SO 2—
2 4 4
17.(1)交叉分类法 (2)D(3)
(4)
(5)
18.19.