文档内容
第二节乙烯与有机高分子材料--课时训练 2022-2023学年高
一下学期化学人教版(2019)必修第二册
学校:___________姓名:___________班级:___________考号:___________
一、单选题
1.2019年7月1日起,上海、西安等地纷纷开始实行垃圾分类。这体现了我国保护环
境的决心,而环境保护与化学知识息息相关,下列有关说法正确的是( )
A.废旧电池中含有镍、镉等重金属,不可用填埋法处理,属于有害垃圾
B.各种玻璃制品的主要成分是硅酸盐,不可回收利用
C.废弃的聚乙烯塑料属于可回收垃圾,不易降解,能使溴水褪色
D.含棉、麻、丝、毛及合成纤维的废旧衣物燃烧处理时都只生成 CO 和HO
2 2
2.下列化学用语或图示表达不正确的是
A.N 的结构式:N≡N B.Na+的结构示意图:
2
C.CH 的球棍模型: D.CO 的电子式:
4 2
3.下列有关甲烷和乙烯的说法正确的是
A.两者都能发生氧化反应
B.两者互为同系物
C.两者分子中所有原子均共平面
D.两者都能使酸性高锰酸钾溶液褪色
4.化学与生活密切相关。下列说法中的因果关系正确的是
选
原因 结果
项
草酸钙是人体不能吸收的沉淀
A 卤水豆腐不可与菠菜一起煮
物
B 三氯化铁具有氧化性 三氯化铁可作净水剂
聚氯乙烯塑料稳定性比聚乙烯
C 用聚氯乙烯塑料袋来盛装食品
塑料强
燃气灶将天然气改为液化石油气时需增大空
D 天然气含碳量比液化石油气低
气进入量
A.A B.B C.C D.D5.下列化学用语描述不正确的是
A.中子数为18 的Cl 原子: Cl B. 的结构示意图:
C. 的电子式: D.HO的结构式:
2
6.某研究性小组为了探究石蜡油(液态烷烃混合物)的分解产物,设计了如下实验方案。
下列说法错误的是
A.石蜡油分解产物中含有烯烃,不含烷烃
B.试管乙、丙中溶液均褪色,分别发生氧化反应、加成反应
C.碎瓷片有催化和积蓄热量的作用
D.结束反应时,为防止倒吸,先撤出导管,再停止加热
7.采用下图装置制备乙烯并研究乙烯与溴水的反应。实验观察到溴水褪色,得到无色
透明的溶液。进一步分析发现反应产物主要为BrCHCHOH,含少量BrCHCHBr。下
2 2 2 2
列说法不正确的是
试卷第2页,共3页A.实验室制乙烯的方程式:CHCHOH CH=CH ↑+H O
3 2 2 2 2
B.除杂试剂A为NaOH溶液
C.乙烯与溴水反应后的溶液近乎中性
D.BrCHCHOH与HO之间存在氢键
2 2 2
8.下列有关化学用语表示正确的是
A.中子数为20的氯原子: B.对硝基苯酚的结构简式:
C.S2-的结构示意图: D.NH Cl的电子式:
4
9.硫酸是一种重要的化学试剂。某实验小组的同学利用浓硫酸和铜片等一些化学药品
和仪器制取二氧化硫。下列说法正确的是
A.装置a中先点燃酒精灯,再加入浓硫酸,以加快反应速率
B.可用b或c装置来收集产生的气体,不能用d装置
C.用装置e来吸收尾气,防止尾气泄漏
D.此实验浓硫酸表现强氧化性和酸性
10.实验是研究化学的基础,下图中所示的制备实验方法、装置或操作均正确的是(
)
A.可用装置甲制取氯气 B.可用装置乙制取氨气
C.可用装置丙制取并检验乙炔 D.可用装置丁制得金属锰11.《电石安全技术说明书》中对电石的描述为“…遇水或湿气能迅速产生高度易燃
的乙炔气体,应与氧化剂类物质分开存放…”。下列说法不合理的是( )
A.盛装电石的包装上贴有的危险化学品标志为(遇湿易燃)
B.电石与硝酸分开存放
C.运输电石的铁桶内可充入氮气
D.电石着火可用泡沫灭火器扑灭
12.有机物环丙叉环丙烷,由于其特殊的电导结构一直受到理论化学家的注意,其结
构如图所示。有关它的说法中错误的是( )
A.其二氯代物有4种 B.它所有的原子均在同一平面上
C.其分子式为C H D.它不可能是环丙烷的同系物
6 8
二、填空题
13.聚氯乙烯简称PVC,是当今世界上产量最大、应用最广的热塑性塑料之一。
(1)工业上以乙烯和氯气为原料合成PVC的流程如下:
乙烯 1,2-二氯乙烷(CHClCH Cl) 氯乙烯(CH=CHCl)
2 2 2
PVC
①氯乙烯的分子式为____。
②乙烯生成1,2-二氯乙烷的反应类型是____。
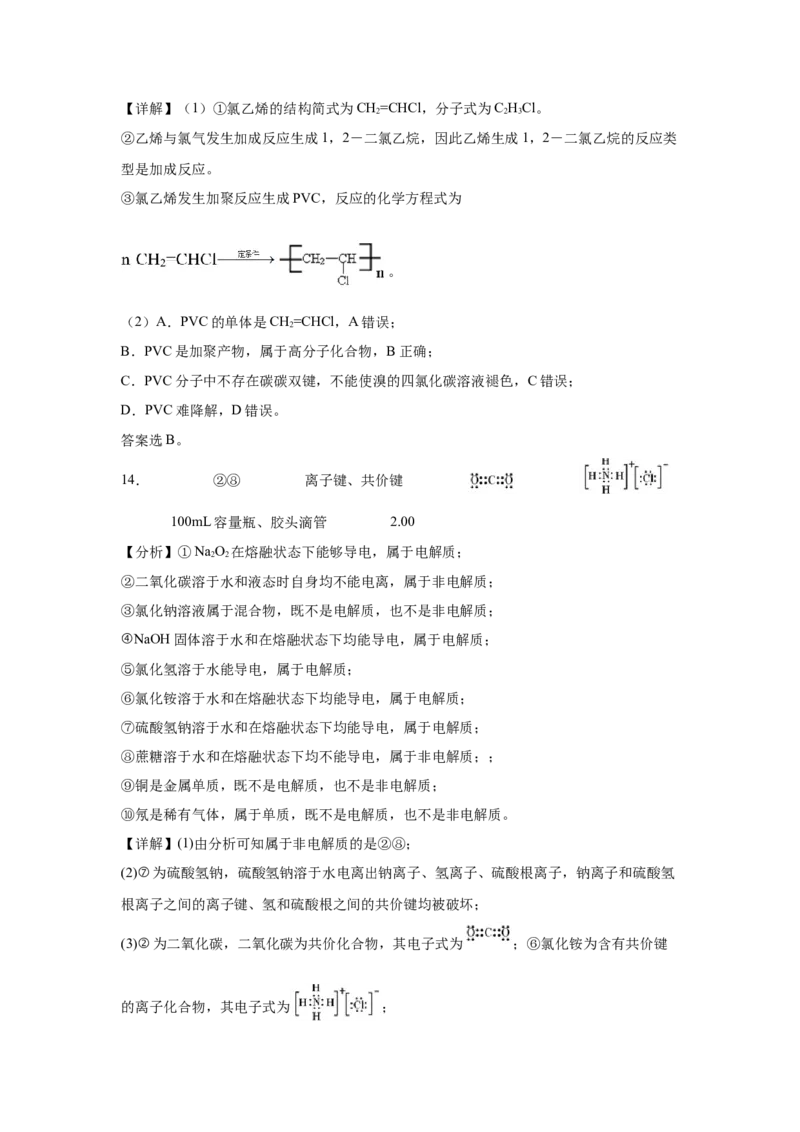
③氯乙烯生成PVC的化学方程式为____。
(2)下列有关PVC的说法正确的是___(填字母)。
A.PVC的单体是CHCHCl
3 2
B.PVC是高分子化合物
C.PVC能够使溴的四氯化碳溶液褪色
D.PVC易降解
14.以下十种物质 ①NaO;②二氧化碳;③氯化钠溶液;④NaOH固体;⑤氯化氢;
2 2
⑥氯化铵;⑦硫酸氢钠;⑧蔗糖;⑨铜; ⑩氖。
(1)以上属于非电解质的是_______ (填序号)
试卷第4页,共3页(2)⑦溶于水,被破坏的是_______。
(3)②的电子式为 _______;⑥的电子式为 _______
(4)配制90mL 0.500mol/L④的溶液,除烧杯、量筒、玻璃棒外还需的玻璃仪器是
_______,需要称量④的质量为_______g (保留三位有效数字)。
三、实验题
15.现以C H 为原料经裂解制得乙烯,进而制得1,2-二溴乙烷,根据如图所示装置,
8 18
结合有关知识回答问题:
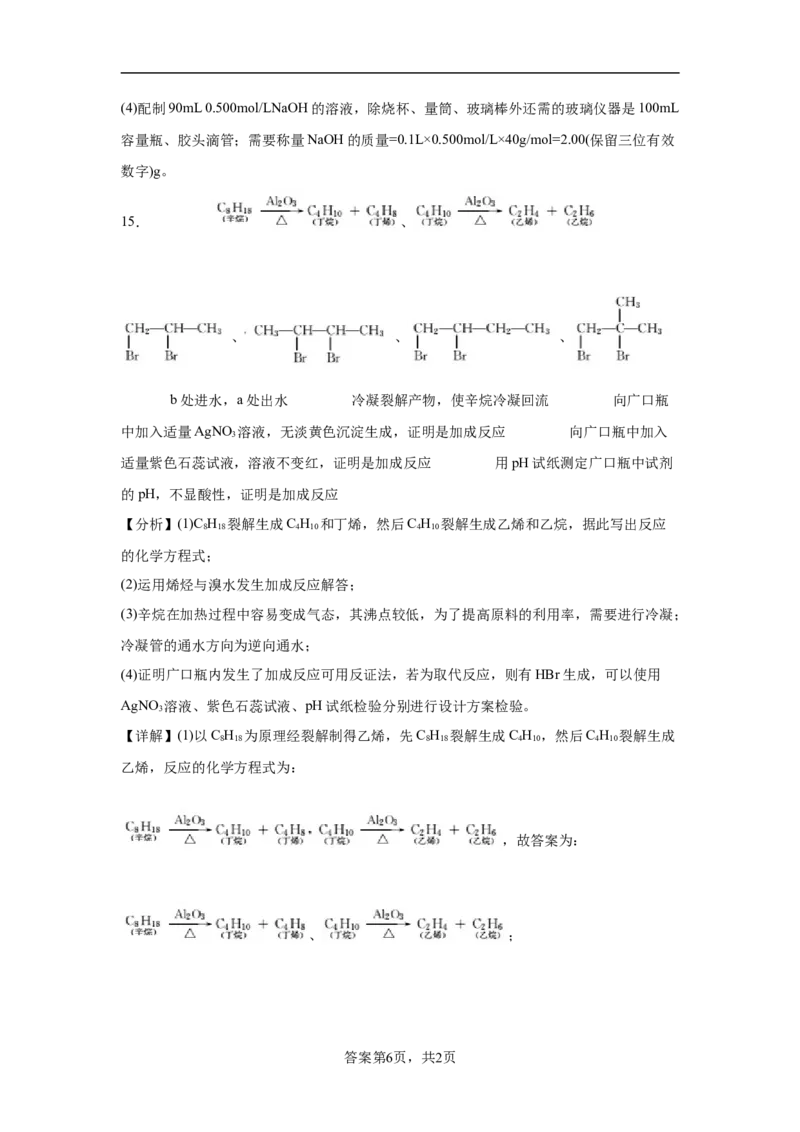
(1)制取乙烯的化学方程式为___。
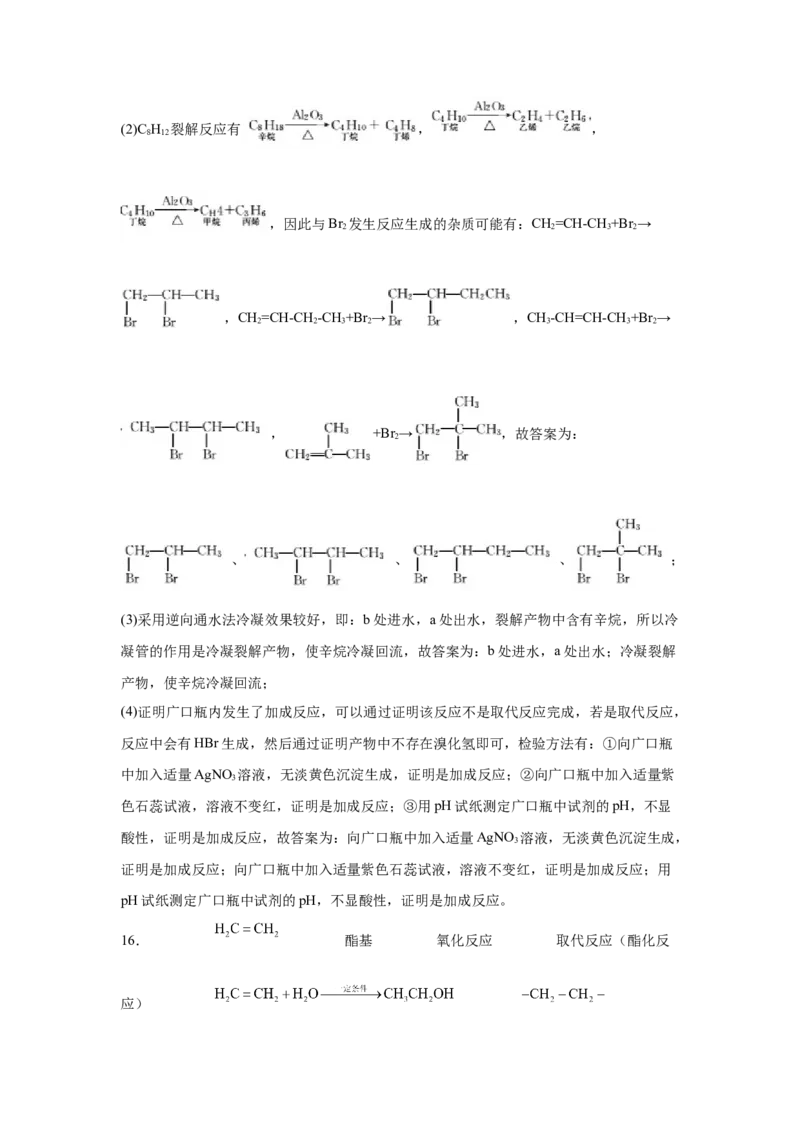
(2)制取的二溴乙烷可能混有一些杂质,这些杂质可能是___。
(3)冷凝管的进出水方向为___,使用冷凝管的目的是___。
(4)设计三种简单的实验证明广口瓶内发生的是加成反应而不是取代反应。
第一种___;
第二种___;
第三种___。
四、有机推断题
16.A、B、C、D、E为五种常见的有机物,它们之间的转化关系如图1所示。其中A
是一种可以使溴水及酸性 溶液褪色的气体,可作为水果的催熟剂。D分子的模
型如图2所示。请回答下列问题:
(1)A的结构简式为_____,E中的官能团名称为______。
(2)由B生成C的反应类型是_____,由B生成E的反应类型是___。
(3)A反应生成B的化学方程式为____。
(4)B在一定条件下可以生成某种高分子化合物,该高分子化合物的链节是_____。
(5)C物质存在一种同分异构体,该同分异构体属于有毒的一类致癌物,其别名为恶
烷,曾被广泛的用于洗涤,制药,印染等行业,试推测其结构简式_____。
( 结构不稳定)
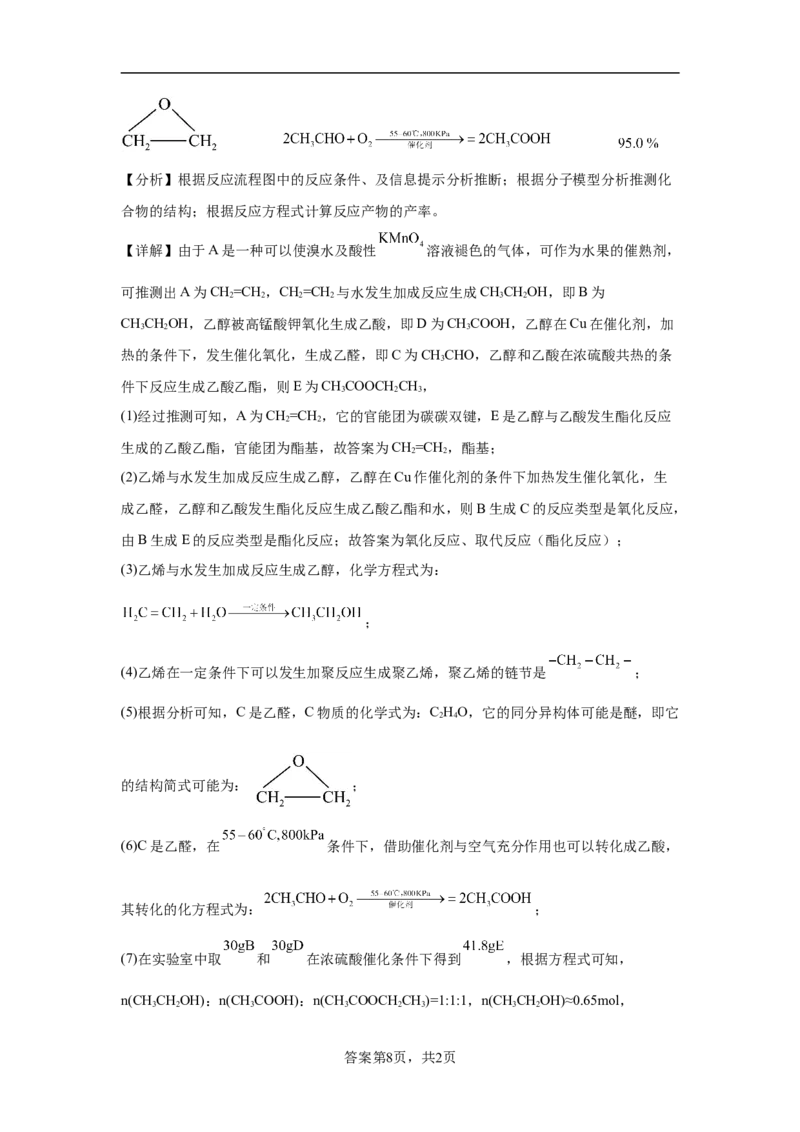
(6)C在 条件下,借助催化剂与空气充分作用也可以转化成D,其
转化的化方程式为_____。
(7)在实验室中取 和 在浓硫酸催化条件下得到 ,试计算该反应产物
的产率是______。(保留三位有效数字)
试卷第6页,共3页参考答案:
1.A
【详解】A.废旧电池若直接填埋,其中的Ni,Cd等重金属会渗漏到土壤中造成污染,因
此不能用填埋法处理,属于有害垃圾,A项正确;
B.废旧玻璃属于硅酸盐材料,可以回收利用,B项错误;
C.聚乙烯的结构中不含碳碳双键,不能使溴水褪色,C项错误;
D.棉和麻的主要成分是纤维素,燃烧后只产生CO 和水;丝和毛的主要成分是蛋白质,
2
蛋白质中含有C,H,O,N元素还可能含有S和其他元素,燃烧时不止生成CO 和水;合
2
成纤维的种类很多,除C和H元素外还可能含有其他元素,燃烧时也不止生成CO 和水,
2
D项错误;
答案选A。
2.D
【详解】A.N 分子以氮氮三键构成,其结构式为N≡N,A正确;
2
B.Na+的质子数为11,电子数为10,所以钠离子的结构示意图为: ,B正确;
C.CH 为正四面体结构,其中心C原子的半径略大于H原子的,所以其球棍模型为:
4
,C正确;
D.CO 分子中含2对碳氧双键,各原子满足8电子稳定结构,其电子式为: ,
2
D错误;
故选D。
3.A
【详解】A.甲烷和乙烯均能发生燃烧,均能发生氧化反应,故A正确;
B.甲烷属于饱和烃,乙烯属于不饱和烃,两者不是同系物,故B错误;
C.甲烷中的碳为饱和碳原子,分子呈四面体构型,故C错误;
D.甲烷结构稳定不能被高锰酸钾氧化,不能使其褪色,故D错误;
故选:A。4.A
【详解】A.豆腐中含有钙离子,菠菜中含有较多草酸,两者一起煮,生成草酸钙,草酸
钙是人体不能吸收的沉淀物,故A正确;
B.氯化铁可作净水剂,是利用Fe3+水解成氢氧化铁胶体,氢氧化铁胶体吸附凝聚水中悬浮
固体小颗粒,因此氯化铁作净水剂,与氯化铁的氧化性无关,故B错误;
C.在光照或加热条件下,聚氯乙烯塑料会释放出一些有毒的小分子,因此聚氯乙烯不能
用于制作食品包装袋,故C错误;
D.天然气、石油气均为碳氢化合物,一定质量的烃,烃的含碳量越小,完全燃烧消耗氧
气的量越多,因此燃气灶将天然气改为液化石油气时,需要减小空气进入量,故D错误;
答案为A。
5.A
【详解】A.左上角为质量数, 中子数为18 的Cl 原子其质量数为35:故核素符号错误,
A错误;
B. 的核电荷数为12、核外电子数为10,离子结构示意图正确,B正确;
C. 是共价分子、分子内每个氢原子和氧原子共用1对电子对、氧原子之间共用1对
电子,电子式正确,C正确;
D. HO分子呈V字形,分子内每个氢原子和氧原子共用1对电子对、结构式正确,D正
2
确;
答案选A。
6.A
【详解】A.石蜡油是液态烷烃混合物,石蜡油受热催化分解的产物中含烯烃和烷烃,故
A错误;
B.烯烃发生氧化反应使酸性KMnO 溶液褪色,烯烃与溴的四氯化碳溶液发生加成反应,
4
使溴的四氯化碳溶液褪色,故B正确;
C.在石蜡油分解反应中,碎瓷片的作用是催化和积蓄热量,故C正确;
D.实验结束,若先熄灭酒精灯,气体体积缩小易引起倒吸。为防止倒吸,实验结束时先
撤出导管,再停止加热,故D正确;
选A。
7.C
答案第2页,共2页【详解】A.实验室制乙烯用乙醇和浓硫酸在170℃下加热发生消去反应,A项正确;
B.此法制得的乙烯中可能会混有二氧化硫气体,二氧化硫也能使溴水褪色,因此应用氢
氧化钠溶液除去二氧化硫,B项正确;
C.乙烯与溴水发生加成反应的主要产物为BrCHCHOH,说明一定生成了HBr,而HBr
2 2
会使溶液呈酸性,C项错误;
D.BrCHCHOH与HO中都有O-H键,因此分子之间可以形成氢键,D项正确;
2 2 2
答案选C。
8.A
【详解】A.氯元素的质子数为17,中子数为20的氯原子的质量数=17+20=37,该氯原子
可以表示为: Cl,故A正确;
B、对硝基苯酚的结构简式为 ,硝基的书写形式错误,故B错误;
C.硫离子是硫原子得2个电子形成的,故硫离子的核外有18个电子,核电荷数为16,其
正确的结构示意图为 ,故C错误;
D.氯化铵的电子式中,阴阳离子都需要标出最外层电子及所带电荷,其正确的电子式为:
,故D错误;
故选A。
9.D
【详解】A. 装置a中先加入浓硫酸,再点燃酒精灯,制备二氧化硫,选项A错误;
B.二氧化硫可溶于水,不能用排水法收集,选项B错误;
C.若用装置e来吸收尾气,形成封闭的装置,不适合,选项C错误;
D.此实验反应后生成硫酸铜,溶液呈蓝色,产生二氧化硫,浓硫酸表现强氧化性和酸性,
选项D正确。
答案选D。
10.D
【详解】A.浓盐酸与二氧化锰反应需要加热,图中缺少酒精灯加热,故A错误;B.制备氨气时反应生成水,试管口不能向上,图中试管口应略向下倾斜,故B错误;
C.乙炔、HS等均能被高锰酸钾氧化,应先利用硫酸铜溶液除杂,再利用高锰酸钾溶液检
2
验乙炔,故C错误;
D.点燃镁条,引发铝热反应,Al与二氧化锰发生氧化还原反应可制得金属锰,故D正确;
答案选D。
11.D
【详解】A.电石与水发生反应的化学方程式为CaC +2H O→Ca(OH) +C H↑,生成易燃气体
2 2 2 2 2
乙炔(C H),乙炔遇明火发生爆炸生成二氧化碳和水,电石属于遇湿易燃物品,A合理;
2 2
B.浓硝酸易挥发、具有强氧化性,电石与挥发的水、硝酸接触,发生化学反应或引起燃烧,
保存时应与硝酸分开存放,B合理;
C.氮气性质稳定,运输电石的铁桶内可充入氮气,可防止电石遇潮易燃,C合理;
D.泡沫灭火器原理,在溶液中发生反应:Al3++3HCO-=Al(OH) ↓+3CO ↑,产生CO 灭火,
3 3 2 2
冲出的二氧化碳中含有水,电石与水反应生成的C H 继续燃烧,D不合理;
2 2
故合理选项是D。
12.B
【详解】A.该分子中只有4个碳原子上分别有2个H,如图所示 ,先
在1号碳上取代一个H,则取代第二个H有4种可能,故其二氯代物有4种 ,A正确;
B.由乙烯分子的6原子共面可知,它所有的碳原子可能在同一平面上,但是有氢原子的碳
原子全是饱和的碳原子,由甲烷的正四面体结构可知,8个氢原子不可能在同一平面上,B
不正确;
C.其分子式为C H,C正确;
6 8
D.该物质分子中有碳碳双键,故它不可能是环丙烷的同系物,D正确。
本题选B。
13. C HCl 加成反应
2 3
B
【分析】乙烯与氯气发生加成反应生成1,2-二氯乙烷,1,2-二氯乙烷发生消去反应生
成氯乙烯,氯乙烯发生加聚反应生成聚氯乙烯,据此解答。
答案第4页,共2页【详解】(1)①氯乙烯的结构简式为CH=CHCl,分子式为C HCl。
2 2 3
②乙烯与氯气发生加成反应生成1,2-二氯乙烷,因此乙烯生成1,2-二氯乙烷的反应类
型是加成反应。
③氯乙烯发生加聚反应生成PVC,反应的化学方程式为
。
(2)A.PVC的单体是CH=CHCl,A错误;
2
B.PVC是加聚产物,属于高分子化合物,B正确;
C.PVC分子中不存在碳碳双键,不能使溴的四氯化碳溶液褪色,C错误;
D.PVC难降解,D错误。
答案选B。
14. ②⑧ 离子键、共价键
100mL容量瓶、胶头滴管 2.00
【分析】①NaO 在熔融状态下能够导电,属于电解质;
2 2
②二氧化碳溶于水和液态时自身均不能电离,属于非电解质;
③氯化钠溶液属于混合物,既不是电解质,也不是非电解质;
④NaOH固体溶于水和在熔融状态下均能导电,属于电解质;
⑤氯化氢溶于水能导电,属于电解质;
⑥氯化铵溶于水和在熔融状态下均能导电,属于电解质;
⑦硫酸氢钠溶于水和在熔融状态下均能导电,属于电解质;
⑧蔗糖溶于水和在熔融状态下均不能导电,属于非电解质;;
⑨铜是金属单质,既不是电解质,也不是非电解质;
⑩氖是稀有气体,属于单质,既不是电解质,也不是非电解质。
【详解】(1)由分析可知属于非电解质的是②⑧;
(2)⑦为硫酸氢钠,硫酸氢钠溶于水电离出钠离子、氢离子、硫酸根离子,钠离子和硫酸氢
根离子之间的离子键、氢和硫酸根之间的共价键均被破坏;
(3)②为二氧化碳,二氧化碳为共价化合物,其电子式为 ;⑥氯化铵为含有共价键
的离子化合物,其电子式为 ;(4)配制90mL 0.500mol/LNaOH的溶液,除烧杯、量筒、玻璃棒外还需的玻璃仪器是100mL
容量瓶、胶头滴管;需要称量NaOH的质量=0.1L×0.500mol/L×40g/mol=2.00(保留三位有效
数字)g。
15. 、
、 、 、
b处进水,a处出水 冷凝裂解产物,使辛烷冷凝回流 向广口瓶
中加入适量AgNO 溶液,无淡黄色沉淀生成,证明是加成反应 向广口瓶中加入
3
适量紫色石蕊试液,溶液不变红,证明是加成反应 用pH试纸测定广口瓶中试剂
的pH,不显酸性,证明是加成反应
【分析】(1)C H 裂解生成C H 和丁烯,然后C H 裂解生成乙烯和乙烷,据此写出反应
8 18 4 10 4 10
的化学方程式;
(2)运用烯烃与溴水发生加成反应解答;
(3)辛烷在加热过程中容易变成气态,其沸点较低,为了提高原料的利用率,需要进行冷凝;
冷凝管的通水方向为逆向通水;
(4)证明广口瓶内发生了加成反应可用反证法,若为取代反应,则有HBr生成,可以使用
AgNO 溶液、紫色石蕊试液、pH试纸检验分别进行设计方案检验。
3
【详解】(1)以C H 为原理经裂解制得乙烯,先C H 裂解生成C H ,然后C H 裂解生成
8 18 8 18 4 10 4 10
乙烯,反应的化学方程式为:
,故答案为:
、 ;
答案第6页,共2页(2)C H 裂解反应有 , ,
8 12
,因此与Br 发生反应生成的杂质可能有:CH=CH-CH+Br →
2 2 3 2
,CH=CH-CH-CH+Br → ,CH-CH=CH-CH +Br →
2 2 3 2 3 3 2
, +Br → ,故答案为:
2
、 、 、 ;
(3)采用逆向通水法冷凝效果较好,即:b处进水,a处出水,裂解产物中含有辛烷,所以冷
凝管的作用是冷凝裂解产物,使辛烷冷凝回流,故答案为:b处进水,a处出水;冷凝裂解
产物,使辛烷冷凝回流;
(4)证明广口瓶内发生了加成反应,可以通过证明该反应不是取代反应完成,若是取代反应,
反应中会有HBr生成,然后通过证明产物中不存在溴化氢即可,检验方法有:①向广口瓶
中加入适量AgNO 溶液,无淡黄色沉淀生成,证明是加成反应;②向广口瓶中加入适量紫
3
色石蕊试液,溶液不变红,证明是加成反应;③用pH试纸测定广口瓶中试剂的pH,不显
酸性,证明是加成反应,故答案为:向广口瓶中加入适量AgNO 溶液,无淡黄色沉淀生成,
3
证明是加成反应;向广口瓶中加入适量紫色石蕊试液,溶液不变红,证明是加成反应;用
pH试纸测定广口瓶中试剂的pH,不显酸性,证明是加成反应。
16. 酯基 氧化反应 取代反应(酯化反
应)【分析】根据反应流程图中的反应条件、及信息提示分析推断;根据分子模型分析推测化
合物的结构;根据反应方程式计算反应产物的产率。
【详解】由于A是一种可以使溴水及酸性 溶液褪色的气体,可作为水果的催熟剂,
可推测出A为CH=CH ,CH=CH 与水发生加成反应生成CHCHOH,即B为
2 2 2 2 3 2
CHCHOH,乙醇被高锰酸钾氧化生成乙酸,即D为CHCOOH,乙醇在Cu在催化剂,加
3 2 3
热的条件下,发生催化氧化,生成乙醛,即C为CHCHO,乙醇和乙酸在浓硫酸共热的条
3
件下反应生成乙酸乙酯,则E为CHCOOCH CH,
3 2 3
(1)经过推测可知,A为CH=CH ,它的官能团为碳碳双键,E是乙醇与乙酸发生酯化反应
2 2
生成的乙酸乙酯,官能团为酯基,故答案为CH=CH ,酯基;
2 2
(2)乙烯与水发生加成反应生成乙醇,乙醇在Cu作催化剂的条件下加热发生催化氧化,生
成乙醛,乙醇和乙酸发生酯化反应生成乙酸乙酯和水,则B生成C的反应类型是氧化反应,
由B生成E的反应类型是酯化反应;故答案为氧化反应、取代反应(酯化反应);
(3)乙烯与水发生加成反应生成乙醇,化学方程式为:
;
(4)乙烯在一定条件下可以发生加聚反应生成聚乙烯,聚乙烯的链节是 ;
(5)根据分析可知,C是乙醛,C物质的化学式为:C HO,它的同分异构体可能是醚,即它
2 4
的结构简式可能为: ;
(6)C是乙醛,在 条件下,借助催化剂与空气充分作用也可以转化成乙酸,
其转化的化方程式为: ;
(7)在实验室中取 和 在浓硫酸催化条件下得到 ,根据方程式可知,
n(CHCHOH):n(CHCOOH):n(CHCOOCH CH)=1:1:1,n(CHCHOH)≈0.65mol,
3 2 3 3 2 3 3 2
答案第8页,共2页n(CHCOOH)=0.5mol,所以乙醇过量,需要用乙醇的物质的量计算,乙醇完全反应应该生
3
产0.5mol乙酸乙酯,即理论上应生成乙酸乙酯的质量为:88g/mol×0.5mol=44g,实际上生
成乙酸乙酯41.8g,则反应产物的产率是 ×100%=95%;故答案为95%。答案第10页,共2页