文档内容
人教版(2019)必修第二册第七章第三节乙醇与乙酸
课时训练三
学校:___________姓名:___________班级:___________考号:___________
一、单选题
1.下列反应中前者属于取代反应,后者属于加成反应的是
A.甲烷与氯气混合后光照后混合气体颜色变浅;乙烯使酸性高锰酸钾溶液褪色
B.乙烯与溴的四氯化碳溶液反应;苯( )与氢气在一定条件下反应生成环己烷(
)
C.CHCHOH与浓盐酸反应制取氯乙烷(CHCHCl); 乙烯与氯化氢反应制取氯乙烷
3 2 3 2
D.在苯中滴入溴水,溴水褪色;乙烯自身生成聚乙烯的反应
2.下列实验操作能完成实验目的的是
选
实验操作 实验目的
项
将乙醇和浓硫酸混合,迅速加热到170℃,产生的气 验证乙醇消去反应的产
A
体通入溴的四氯化碳溶液中,观察是否褪色 物是乙烯
过量的铁粉加入氯化亚铁和氯化铜的混合溶液中,观 验证还原性:
B
察到溶液的颜色由蓝色变成浅绿色
试管中加入3~5mL硅酸钠溶液,滴入1~2滴酚酞,再
C 逐滴加入稀盐酸,边加边振荡,至溶液红色接近消失 制备硅酸胶体
时停止,静置
向100g质量分数42%的乙二酸溶液中,加绿豆粒大小 验证乙二酸中含羧基数
D
的金属钠,观察产生气泡的快慢 目
A.A B.B C.C D.D
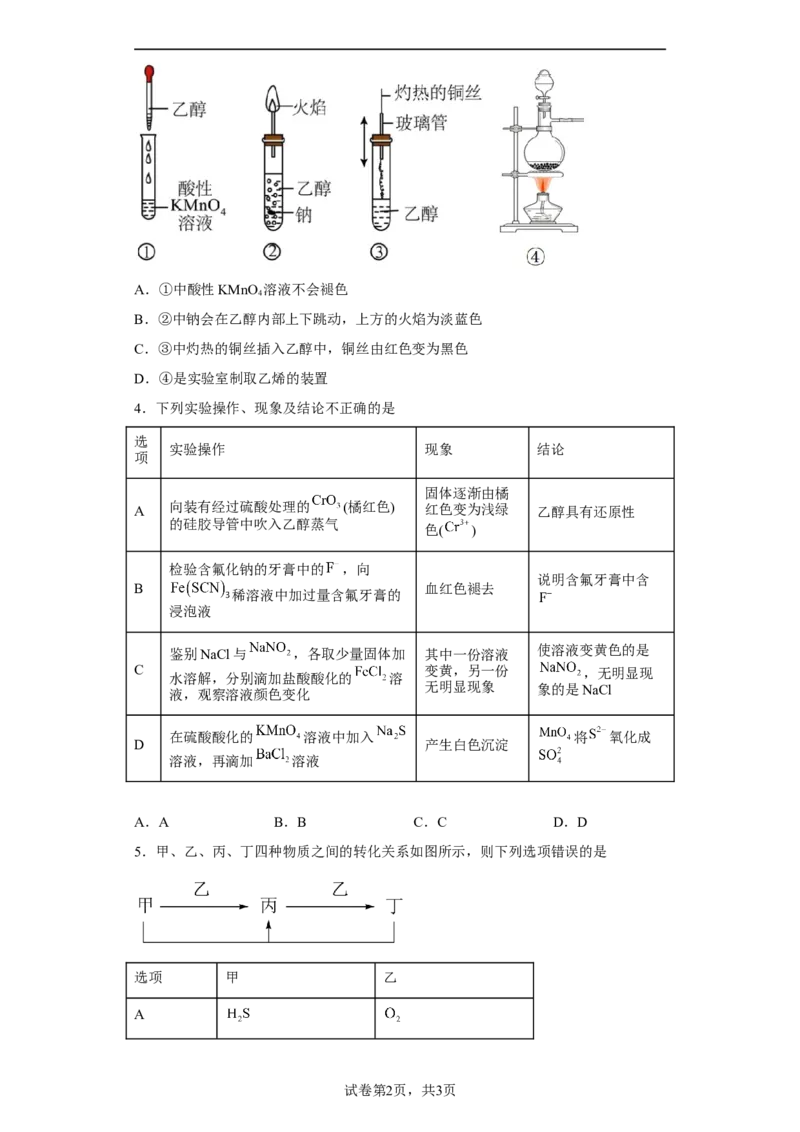
3.乙醇是生活中常见的有机物,下列有关乙醇的实验操作或实验现象正确的是A.①中酸性KMnO 溶液不会褪色
4
B.②中钠会在乙醇内部上下跳动,上方的火焰为淡蓝色
C.③中灼热的铜丝插入乙醇中,铜丝由红色变为黑色
D.④是实验室制取乙烯的装置
4.下列实验操作、现象及结论不正确的是
选
实验操作 现象 结论
项
固体逐渐由橘
A 向装有经过硫酸处理的 (橘红色) 红色变为浅绿 乙醇具有还原性
的硅胶导管中吹入乙醇蒸气
色( )
检验含氟化钠的牙膏中的 ,向
说明含氟牙膏中含
B 血红色褪去
稀溶液中加过量含氟牙膏的
浸泡液
鉴别NaCl与 ,各取少量固体加 其中一份溶液 使溶液变黄色的是
C 变黄,另一份 ,无明显现
水溶解,分别滴加盐酸酸化的 溶
液,观察溶液颜色变化
无明显现象 象的是NaCl
在硫酸酸化的 溶液中加入 将 氧化成
D 产生白色沉淀
溶液,再滴加 溶液
A.A B.B C.C D.D
5.甲、乙、丙、丁四种物质之间的转化关系如图所示,则下列选项错误的是
选项 甲 乙
A
试卷第2页,共3页B
C 溶液
D 溶液 稀盐酸
A.A B.B C.C D.D
6.N 是阿伏加德罗常数的值,下列说法正确的是
A
A.1L 0.1 mol∙L−1醋酸中含醋酸分子数为0.1N
A
B.1.0mol CH 与1molCl 在光照下充分反应生成的CHCl分子数为1.0N
4 2 3 A
C.78.0g苯中含有 键的数目为3N
A
D.0.1mol乙烯与乙醇的混合物完全燃烧所消耗的氧分子数为0.3N
A
7.下列各组粒子在指定溶液中能大量共存的是
A.0.1mol/LNaOH溶液中: 、 、 、
B.0.1mol/L 溶液中: 、 、 、
C.0.1mol/L 溶液中: 、 、 、
D.0.1mol/L酸性 溶液中: 、 、 、
8.下列由实验得出的结论不正确的是
实验 结论
A 将乙烯通入溴的四氯化碳溶液,溶液最终变为 生成的1,2-二溴乙烷为无
. 无色透明 色液体,可溶于四氯化碳
B 将一小块钠分别投入盛有水和乙醇的小烧杯 乙醇羟基中的氢原子不如水分
. 中,钠与乙醇反应要平缓得多 子中的氢原子活泼
C 在催化剂存在的条件下,石蜡油加强热生成的
石蜡油的分解产物中含有烯烃
. 气体通入溴的四氯化碳溶液中,溶液褪色
D 甲烷与氯气在光照下反应后的混合气体能使
生成的氯甲烷具有酸性
. 湿润的石蕊试纸变红
A.A B.B C.C D.D
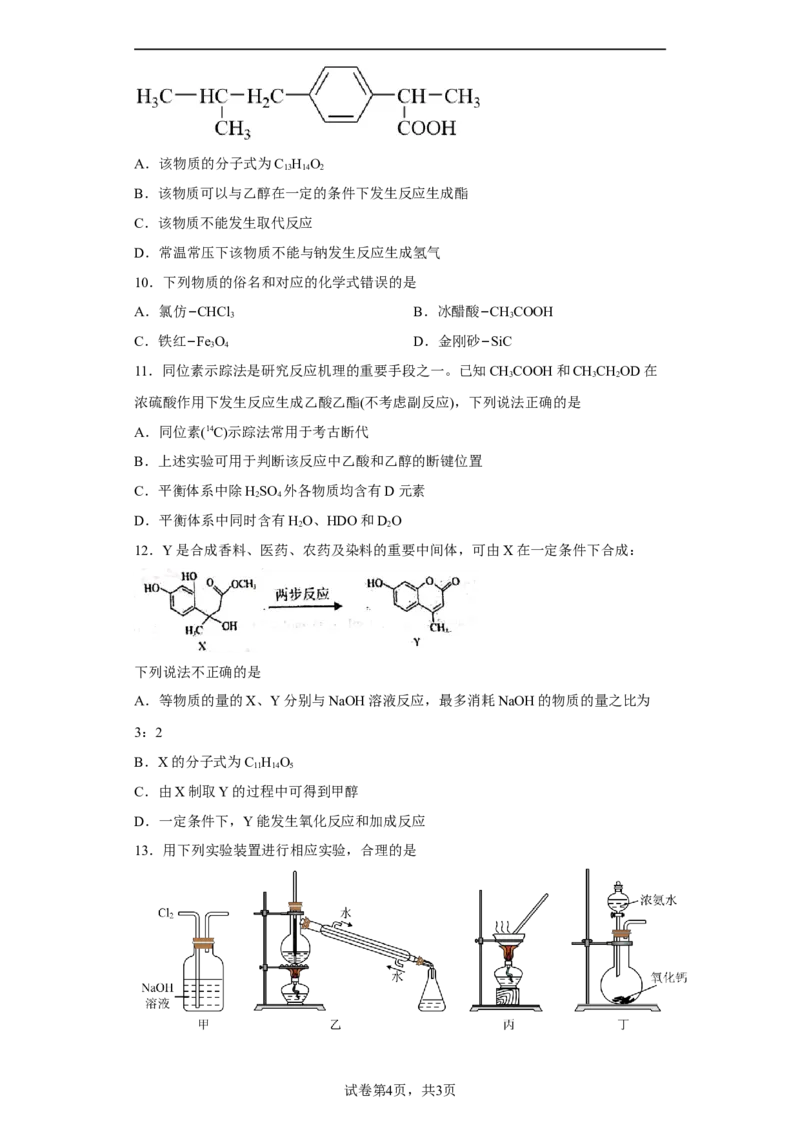
9.芬必得是一种具有解热、镇痛、抗生素作用的药物。芬必得主要成分的结构简式如
图所示。下列有关该物质说法正确的是A.该物质的分子式为C H O
13 14 2
B.该物质可以与乙醇在一定的条件下发生反应生成酯
C.该物质不能发生取代反应
D.常温常压下该物质不能与钠发生反应生成氢气
10.下列物质的俗名和对应的化学式错误的是
A.氯仿−CHCl B.冰醋酸−CHCOOH
3 3
C.铁红−Fe O D.金刚砂−SiC
3 4
11.同位素示踪法是研究反应机理的重要手段之一。已知CHCOOH和CHCHOD在
3 3 2
浓硫酸作用下发生反应生成乙酸乙酯(不考虑副反应),下列说法正确的是
A.同位素(14C)示踪法常用于考古断代
B.上述实验可用于判断该反应中乙酸和乙醇的断键位置
C.平衡体系中除HSO 外各物质均含有D元素
2 4
D.平衡体系中同时含有HO、HDO和DO
2 2
12.Y是合成香料、医药、农药及染料的重要中间体,可由X在一定条件下合成:
下列说法不正确的是
A.等物质的量的X、Y分别与NaOH溶液反应,最多消耗NaOH的物质的量之比为
3:2
B.X的分子式为C H O
11 14 5
C.由X制取Y的过程中可得到甲醇
D.一定条件下,Y能发生氧化反应和加成反应
13.用下列实验装置进行相应实验,合理的是
试卷第4页,共3页A.图甲是除去 中含有的少量
B.图乙是蒸干 饱和溶液制备无水 固体
C.图丙是分离饱和 溶液和乙酸乙酯的混合物
D.图丁是制备氨气
14.下列有关金属钠在水中和在乙醇中的反应情况对比正确的是。
A.钠能置换出水中所有的氢,却只能置换出乙醇里羟基中的氢
B.钠都要浮在水面上或乙醇液体表面
C.钠无论与水反应还是与乙醇反应都要放出热量
D.钠在乙醇中反应更剧烈,是因为乙醇分子中含有的氢原子比水分子中的多
15.可以证明乙醇分子中有一个氢原子与另外的氢原子不同的方法是
A.1 mol乙醇完全燃烧生成3 mol水
B.乙醇可以被酸性高锰酸钾溶液氧化为乙酸
C.1 mol乙醇跟足量的Na作用得到0.5 mol H
2
D.1 mol乙醇可以生成1 mol乙醛
二、填空题
16.有下列3种有机化合物:A. 、 B. 、C. 。
(1)写出化合物A、C中官能团的名称_______、_______;
(2)3种化合物中能使溴的四氯化碳溶液褪色的是_______(写名称);反应的化学方程式
为:_______;具有特殊气味、常做有机溶剂的是_______(写结构简式)。
(3)3种化合物中能与乙醇发生酯化反应的是_______(写名称) 。
17.乙酸乙酯广泛用于药物、染料、香料等工业,其合成路线如图所示:(1)实验室制乙烯的方程式是_______。反应③的化学方程式_______,反应类型是
_______。反应④的化学方程式_______。
(2)实验室可利用反应⑥制备乙酸乙酯,写出反应⑥的化学方程式_____,加入浓硫酸的
作用是_____,试管G中应加入的溶液是_____,G中导管不能伸入液面以下的原因是
______。
18.填空
(1)乙醇分子中不同的化学键可表示为 ,在乙醇和钠反应时,
_______键断裂,在 催化和加热条件下,_______键、_______键断裂。
(2)乙酸中不同的化学键可表示为 :在乙酸和钠反应时,
_______键断裂;在其和 反应时,_______键断裂。
(3)乙酸和乙醇发生酯化反应时,乙醇中的_______键断裂,乙酸中的_______键断裂。
19.按要求填空
Ⅰ.黑火药爆炸的化学方程式为: 。回答下列问题:
(1)硫元素在周期表的位置是_______。氨气的电子式_______。
(2)用电子式表示化合物 的形成过程为_______。
(3)硫酸钾在水溶液中的电离方程式为_______。
(4)在加热条件下木炭与浓硫酸反应的化学方程式为_______。
Ⅱ.某些烃分子的模型如图所示,回答下列问题:
试卷第6页,共3页(5)丁的分子式是_______,写出戊的结构简式_______
(6)写出乙完全燃烧的化学方程式_______
Ⅲ.烃可以通过化学反应制得烃的衍生物,例如由丙烯可以制得丙烯酸
(CH=CHCOOH)、乳酸( )等。
2
(7)丙烯酸中含氧官能团的名称是_______
(8)工业上用乙烯与水在一定条件下反应可制得乙醇,该反应的化学方程式为_______
(9)木糖醇[ ]是一种天然甜味剂,在人体中的代谢不受胰岛素
调节,可作为糖尿病人的热能源。请预测木糖醇的一种化学性质:_______
20.回答下列问题:
(1)从能量的角度看,断开化学键要________能量(填“吸收”或“释放”,下同),形
成化学键要________能量。化学反应是释放能量还是吸收能量取决于________。当反
应物的总能量高于生成物时,该反应为________反应。
(2)纯净的锌与稀HSO 反应制氢气,反应速率较小。为了增大反应速率,可以向稀硫
2 4
酸中加入少量某盐,该盐是________,能增大化学反应速率的原因是________。
(3)乙醇是重要的化学试剂。完成以下问题:
a.乙醇分子中的官能团名称:________。
b.乙醇与金属钠反应的化学方程式:________。
c.乙醇在空气中完全燃烧的化学方程式:________。
d.乙醇在铜作催化剂条件下被氧气氧化为乙醛化学方程式:________。
三、实验题
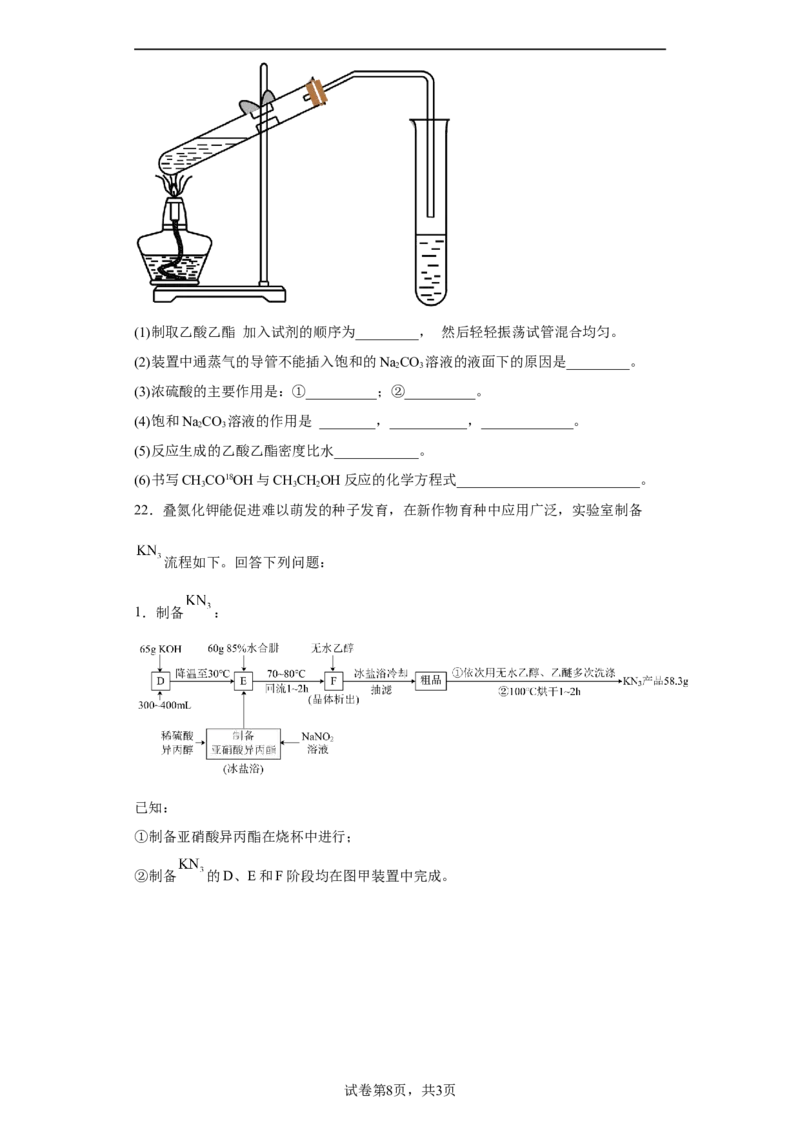
21.实验室用如图所示的装置制取乙酸乙酯。(1)制取乙酸乙酯 加入试剂的顺序为_________, 然后轻轻振荡试管混合均匀。
(2)装置中通蒸气的导管不能插入饱和的NaCO 溶液的液面下的原因是_________。
2 3
(3)浓硫酸的主要作用是:①__________;②__________。
(4)饱和NaCO 溶液的作用是 ________,___________,_____________。
2 3
(5)反应生成的乙酸乙酯密度比水____________。
(6)书写CHCO18OH与CHCHOH反应的化学方程式__________________________。
3 3 2
22.叠氮化钾能促进难以萌发的种子发育,在新作物育种中应用广泛,实验室制备
流程如下。回答下列问题:
1.制备 :
已知:
①制备亚硝酸异丙酯在烧杯中进行;
②制备 的D、E和F阶段均在图甲装置中完成。
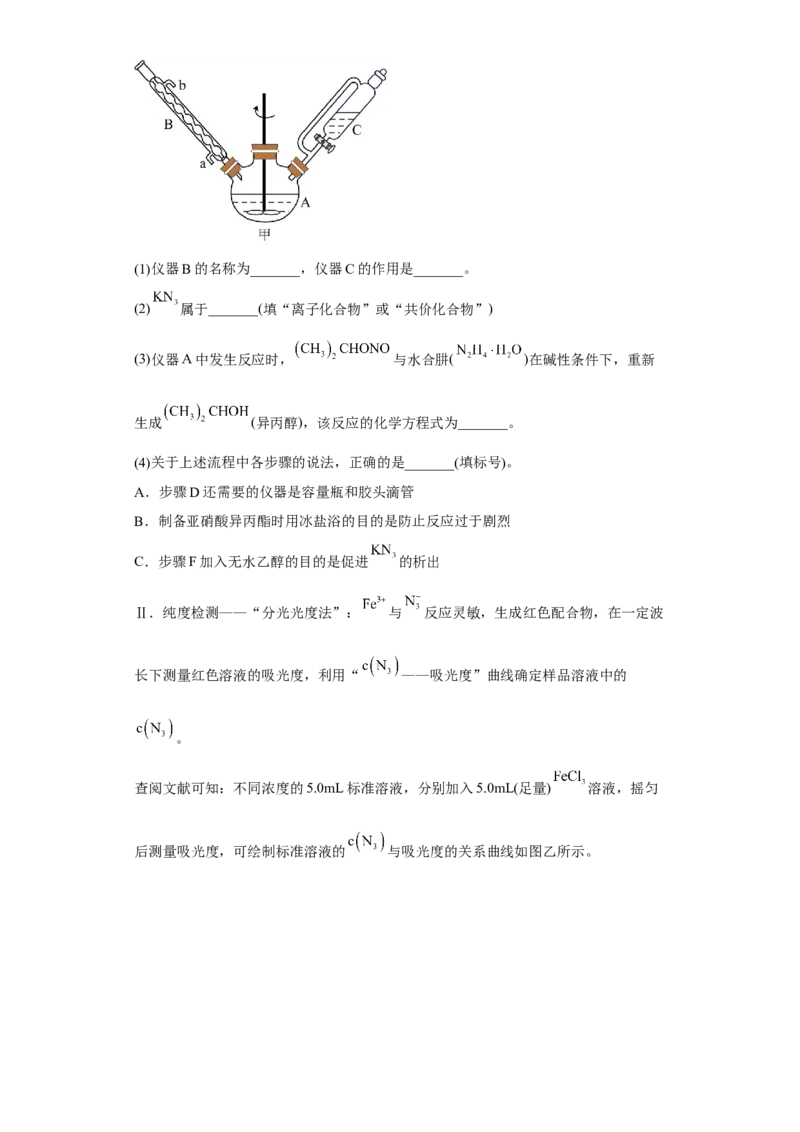
试卷第8页,共3页(1)仪器B的名称为_______,仪器C的作用是_______。
(2) 属于_______(填“离子化合物”或“共价化合物”)
(3)仪器A中发生反应时, 与水合肼( )在碱性条件下,重新
生成 (异丙醇),该反应的化学方程式为_______。
(4)关于上述流程中各步骤的说法,正确的是_______(填标号)。
A.步骤D还需要的仪器是容量瓶和胶头滴管
B.制备亚硝酸异丙酯时用冰盐浴的目的是防止反应过于剧烈
C.步骤F加入无水乙醇的目的是促进 的析出
Ⅱ.纯度检测——“分光光度法”: 与 反应灵敏,生成红色配合物,在一定波
长下测量红色溶液的吸光度,利用“ ——吸光度”曲线确定样品溶液中的
。
查阅文献可知:不同浓度的5.0mL标准溶液,分别加入5.0mL(足量) 溶液,摇匀
后测量吸光度,可绘制标准溶液的 与吸光度的关系曲线如图乙所示。纯度检测步骤如下:
①准确称 晶体,配制 标准液(与文献浓度一致)。
②准确称取0.72g样品,配制成100mL溶液,取5.0mL待测溶液,向其中加入
(足量)标准液,摇匀后测得吸光度为0.6。
(5)配制 溶液需要用到容量瓶,使用容量瓶的第一步操作是_______。
(6)步骤②中取用 标准液 _______mL,样品的质量分数为_______。
试卷第10页,共3页参考答案:
1.C
【详解】A.甲烷与氯气混合后光照后混合气体颜色变浅,原理为CH+Cl
4 2
CHCl+HCl发生取代反应;乙烯使酸性高锰酸钾溶液褪色是发生氧化反应,A不合题意;
3
B.乙烯与溴的四氯化碳溶液反应:CH=CH +Br BrCHCHBr,发生加成反应,苯(
2 2 2 2 2
)与氢气在一定条件下反应生成环己烷( ), +3H 发生
2
加成反应,B不合题意;
C.CHCHOH与浓盐酸反应制取氯乙烷(CHCHCl),CHCHOH+HCl
3 2 3 2 3 2
CHCHCl+H O,发生取代反应,乙烯与氯化氢反应制取氯乙烷:CH=CH +HCl
3 2 2 2 2
CHCHCl,发生加成反应,C符合题意;
3 2
D.在苯中滴入溴水,溴水褪色是萃取过程未发生化学反应;乙烯自身生成聚乙烯的反应
为加聚反应,D不合题意;
故答案为:C。
2.C
【详解】A.将乙醇和浓硫酸混合,迅速加热到170℃,产生的二氧化硫也能使溴的四氯化
碳溶液褪色,故A错误;
B.过量的铁粉加入氯化亚铁和氯化铜的混合溶液中,观察到溶液的颜色由蓝色变成浅绿
色,说明发生反应 ,则氧化性: ,即还原性 ,无
法证明还原性: ,故B错误;
C.试管中加入3~5mL硅酸钠溶液,滴入1~2滴酚酞,溶液呈红色,再逐滴加入稀盐酸,
边加边振荡,至溶液红色接近消失时得到硅酸胶体,故C正确;
D.向100g质量分数42%的乙二酸溶液中,加绿豆粒大小的金属钠,因金属钠的量未知,
且水也能与金属钠反应生成氢气,仅观察产生气泡的快慢无法计算羧基的数目,故D错误;
故选C。3.B
【详解】A.乙醇能使酸性高锰酸钾溶液褪色,A错误;
B.乙醇和钠反应生成氢气,钠的密度比乙醇的大,由于产生气体,所以钠在乙醇内部上
下跳动,产生的氢气点燃火焰为淡蓝色,B正确;
C.乙醇在铜和加热的条件下反应生成乙醛,铜丝加热后变黑,插入乙醇中又变红,C错误;
D.实验室用乙醇和浓硫酸加热到170℃制取乙烯,实验仪器中应该用温度计,D错误;
故选B。
4.D
【详解】A. 与乙醇反应之后变为 ,Cr元素化合价降低,被还原,说明乙醇具有
还原性,A正确;
B.铁离子与氟离子形成的络合离子更稳定,向 稀溶液中加过量含氟牙膏的浸泡
液能形成 ,溶液血红色褪去,B正确;
C.酸性条件下,亚硝酸根离子具有氧化性,能把亚铁离子氧化成铁离子,C正确;
D. 溶液酸化时引入了 ,产生白色沉淀 无法确定 被氧化为 ,D
错误。
故选D。
5.B
【详解】A. 与少量氧气反应生成S单质,S单质与氧气反应生成SO ,HS与SO 反
2 2 2
应生成S单质,故A正确;
B. 发生催化氧化生成乙醛,乙醛发生氧化反应生成乙酸, 与乙酸
不能反应生成乙醛,故B错误;
C. 与少量 反应生成碳酸钠,碳酸钠与 反应生成碳酸氢钠, 与碳酸
氢钠反应生成碳酸钠和水,故C正确;
D. 与少量盐酸反应生成碳酸氢钾,碳酸氢钾与盐酸反应可产生二氧化碳,
与二氧化碳、水反应生成碳酸氢钾,故D正确;
答案第2页,共2页故选B。
6.D
【详解】A.醋酸是弱酸,部分电力,因此1L 0.1 mol∙L−1醋酸中含醋酸分子数小于0.1N ,
A
故A错误;
B.甲烷与氯气反应是一系列的反应,生成四种氯代物,因此1.0mol CH 与1molCl 在光照
4 2
下充分反应生成的CHCl分子数小于N ,故B错误;
3 A
C.78.0g苯物质的量为1mol,苯中不含有碳碳双键,故C错误;
D.根据乙烯与乙醇与氧气完全燃烧的反应关系式CH=CH ~3O, CHCHOH~3O,因此
2 2 2 3 2 2
0.1mol乙烯与乙醇的混合物完全燃烧所消耗的氧分子数为0.3N ,故D正确。
A
综上所述,答案为D。
7.A
【详解】A.在氢氧化钠溶液中,题述4种离子能大量共存,故A正确;
B.硫酸氢钠溶液相当于一元强酸溶液,会发生离子反应:
, ,故B错误;
C.硝酸分别能与 、 反应,故C错误;
D.乙醇能被酸性高锰酸钾溶液氧化,且氢离子与 也能发生反应,故D错误;
故选A。
8.D
【详解】A.乙烯使溴的四氯化碳溶液褪色,则表明乙烯能与溴发生加成反应,且产物溶
于四氯化碳,A正确;
B.钠与乙醇反应比钠与水反应平缓,则表明乙醇电离出H+的能力比水弱,从而得出乙醇
羟基中的氢原子不如水分子中的氢原子活泼,B正确;
C.石蜡油加强热生成的气体能使溴的四氯化碳溶液褪色,则表明石蜡油的分解产物中含
有烯烃,C正确;
D.甲烷与氯气反应产物能使湿润的石蕊试纸变红,则表明有酸性物质生成,CHCl难溶于
3
水,则酸性气体应为HCl,D不正确;
故选D。
9.B
【详解】A.根据图示结构C、H、O原子个数可知,该物质的分子式为C H O,A错误;
13 18 2B.该物质含有羧基,可以与醇在浓硫酸加热的条件下生成酯,B正确;
C.酯化反应也属于取代反应,该物质能发生酯化反应,C错误;
D.该物质结构中含有羧基,可以与钠发生反应生成氢气,D错误;
答案选B。
10.C
【详解】A.氯仿是三氯甲烷,其化学式为CHCl ,故A正确;
3
B.无水乙酸的固态称为冰醋酸,其化学式为CHCOOH,故B正确;
3
C.铁红是氧化铁,化学式为Fe O,故C错误;
2 3
D.金刚砂是碳化硅,化学式为SiC,故D正确。
综上所述,答案为C。
11.D
【详解】A.14C常用于考古断代是因为其有固定的半衰期,而不是采用示踪法,故A错误;
B.上述乙酸和乙醇反应,无论酸脱羟基醇脱氢,还是酸脱氢醇脱羟基,最终D原子均进
入水中,无法确定断键位置,故B错误;
C.平衡体系中生成的乙酸乙酯中均不含D元素,故C错误;
D.CHCOOH和CHCHOD反应生成HDO,生成的乙酸乙酯与HDO发生逆反应时D原
3 3 2
子可以进入乙酸中得到CHCOOD,H原子可以进入乙醇中得到CHCHOH,得到的酸与
3 3 2
醇之间反应时会生成 HO、HDO和DO,故D正确;
2 2
故选:D。
12.A
【详解】A.化合物X中酚羟基、酯基可以和NaOH溶液反应,1molX可以消耗
3molNaOH;Y中酯基和酚羟基可以和NaOH反应,酯基水解后生成酚羟基还可以和NaOH
反应,所以1molY可以消耗3molNaOH,故A错误;
B.根据X的结构简式可知X含碳原子个数为11,O原子个数为5,含有一个苯环和一个
碳氧双键,所以不饱和度为5,所以氢原子个数为11×2+2-5×2=14,所以分子式为
C H O,故B正确;
11 14 5
C.对比X和Y的结构可知,X生成Y的过程中酯基发生水解,羟基发生消去,酯基水解
时会生成甲醇,故C正确;
D.Y含有碳碳双键,可以发生氧化反应和加成反应,故D正确;
故答案为A。
13.D
答案第4页,共2页【详解】A.NaOH溶液与氯气和二氧化硫均反应,故A不合理;
B. 属于挥发性酸的强酸弱碱盐,蒸干时因为水解产生的HCl挥发,生成的氢氧化铝
分解,最后得到氧化铝固体,故B不合理;
C.饱和 溶液和乙酸乙酯互不相溶,可用分液方法,故C不合理;
D.氧化钙溶于水放出大量热使浓氨水分解得到氨气, ,
故D合理;
故选D。
14.C
【分析】钠的密度比水小,比乙醇大,性质活泼,与水剧烈反应生成氢氧化钠和氢气,可
与乙醇反应生成乙醇钠和氢气,与水反应较为剧烈,以此解答该题.
【详解】A.钠和水反应生成氢氧化钠和氢气,则不能置换出水中所有的氢,A错误;
B.钠的密度比水小,比乙醇大,在乙醇的下面,B错误;
C.钠与水、乙醇的反应中钠都可逐渐熔化,都为放热反应,C正确;
D.钠与水反应较为剧烈,D错误。
故答案为:C。
15.C
【详解】乙醇的分子式为C HO,分子中含有6个氢原子,结构简式可能为CHOCH 和
2 6 3 3
C HOH,CHOCH 不能与钠反应,C HOH能与钠反应,1molC HOH与足量的钠反应生
2 5 3 3 2 5 2 5
成0.5 mol H,说明6个氢原子中只有1个氢原子可以被钠置换,这个氢原子与另外的氢
2
原子所处环境应该不同,故选C。
16.(1) 碳碳双键 羧基
(2) 乙烯
(3)乙酸
【详解】(1) 名称为乙烯,其中官能团为碳碳双键; 为乙酸,其中
官能团为(羧基) ,故填碳碳双键;羧基;
(2)能使溴的四氯化碳溶液褪色的物质能与溴单质发生反应,以上三种物质中,乙烯能与溴单质能发生加成反应,使溴的四氯化碳溶液褪色,其反应为
; 、 、 三种物质中,苯
和乙酸均具有气味,苯常做有机溶剂,故填乙烯; ;
;
(3)有机物中,羧酸能与乙醇发生酯化反应,以上三种物质中,乙酸能与乙醇发生酯化反
应,生成乙酸乙酯,其反应为 ,
故填乙酸。
17.(1) CHCHOH CH=CH +H O nCH=CH
3 2 2 2 2 2 2
加聚反应 2CHCHOH + O 2CHCHO + 2H O
3 2 2 3 2
(2) CHCHOH + CH CHOOH CHCHOOCH CH+H O 作吸水剂和催化
3 2 3 3 2 3 2
剂 饱和碳酸钠溶液 防止倒吸
【分析】考查常见简单有机物间的相互转化。反应①是乙烯与水在催化剂条件下发生加成
反应得到乙醇;反应②是乙烯与氧气催化氧化得到乙醛,可通过流程分析出来;反应③是
乙烯发生加聚反应得到聚乙烯;反应④是乙醇发生催化氧化反应得到乙醛;反应⑤是乙醛
催化氧化得到乙酸;反应⑥是乙醇和乙酸发生酯化反应得到乙酸乙酯和水。
【详解】(1)实验室制乙烯是乙醇在浓硫酸作用下发生消去反应得到,方程式是
CHCHOH CH=CH +H O;反应③是乙烯发生加聚反应得到聚乙烯,化学方程式
3 2 2 2 2
是nCH=CH ;反应类型是加聚反应;反应④是乙醇发生催
2 2
答案第6页,共2页化氧化反应得到乙醛,化学方程式是2CHCHOH + O 2CHCHO + 2H O;故答案是
3 2 2 3 2
CHCHOH CH=CH +H O;nCH=CH ;加聚反
3 2 2 2 2 2 2
应;2CHCHOH + O 2CHCHO + 2H O;
3 2 2 3 2
(2)实验室可利用反应⑥制备乙酸乙酯,化学方程式是CHCHOH + CH CHOOH
3 2 3
CHCHOOCH CH+H O;加入浓硫酸的作用是作吸水剂和催化剂;从试管中出
3 2 3 2
来乙酸乙酯、乙醇和乙酸,利用试管G中的溶液除去乙酸和乙醇,并降低乙酸乙酯的溶解
度,故试管G中应加入的溶液是饱和碳酸钠溶液,G中导管不能伸入液面以下的原因是防
止倒吸;
故答案是CHCHOH + CH CHOOH CHCHOOCH CH+H O;作吸水剂和催化剂;
3 2 3 3 2 3 2
饱和碳酸钠溶液;防止倒吸。
18.(1) O-H C-H O-H
(2) O-H O-H
(3) O-H C-O
【详解】(1)乙醇含有-OH,可发生取代反应,与钠反应时,O-H键断裂;在 催化和
加热条件下,乙醇发生催化氧化反应,C-H键、O-H键断裂生成乙醛;
(2)乙酸和钠反应生成CHCOONa和氢气,根据反应原理可知,乙酸和钠反应,O-H键
3
断裂;乙酸和NaOH反应生成CHCOONa和HO,根据反应原理可知,乙酸和NaOH反应,
3 2
O-H键断裂;
(3)乙酸和乙醇发生酯化反应生成乙酸乙酯,根据反应原理可知,乙醇中的O-H键断裂,
乙酸中的C-O键断裂。
19.(1) 第三周期第ⅥA族
(2)
(3)K SO =2K++SO
2 4(4)2H SO (浓)+C CO↑+2SO↑+2H O
2 4 2 2 2
(5) C H CHCHCHCHCH
3 8 3 2 2 2 3
(6)2CH CH+7O 4CO+6H O
3 3 2 2 2
(7)羧基
(8)CH =CH+H O CHCHOH
2 2 2 3 2
(9)氧化反应,酯化反应
【详解】(1)硫元素的质子数16,在周期表的位置是第三周期第ⅥA族。氨气是共价化
合物,电子式为 。
(2)硫化钾是离子化合物,用电子式表示化合物 的形成过程为
。
(3)硫酸钾在水溶液中完全电离,其电离方程式为KSO =2K++SO 。
2 4
(4)在加热条件下木炭与浓硫酸反应的化学方程式为2HSO (浓)+C
2 4
CO↑+2SO↑+2H O。
2 2 2
(5)丁是丙烷,分子式是C H,戊是正戊烷,结构简式为CHCHCHCHCH。
3 8 3 2 2 2 3
(6)乙是乙烷,完全燃烧的化学方程式为2CHCH+7O 4CO+6H O。
3 3 2 2 2
(7)丙烯酸的结构简式为CH=CHCOOH,其中含氧官能团的名称是羧基;
2
(8)乙烯与水在一定条件下反应可制得乙醇,该反应的化学方程式为CH=CH+H O
2 2 2
CHCHOH;
3 2
(9) 中含有羟基,因此能发生氧化反应、取代反应、酯化反应等。
20.(1) 吸收 释放 反应物的总能量与生成物的总能量的相对大
答案第8页,共2页小 放热
(2) CuSO 形成铜锌硫酸原电池加快反应速率
4
(3) 羟基 2C HOH+2Na 2C HONa+H C HOH+3O =2CO +3H O
2 5 2 5 2 2 5 2 2 2
2C HOH+O 2CHCHO+2H O
2 5 2 3 2
【解析】(1)
从能量的角度看,断开化学键要吸收能量,形成化学键要释放能量。化学反应是释放能量
还是吸收能量取决于反应物的总能量与生成物的总能量的相对大小,当反应物的总能量高
于生成物时,表现为能量的释放,该反应为放热反应;
(2)
纯净的锌与稀HSO 反应制氢气,反应速率较小。为了增大反应速率,可以向稀硫酸中加
2 4
入少量硫酸铜,锌与铜离子发生置换生成铜单质,形成铜锌硫酸原电池,加快反应速率;
(3)
乙醇分子中含有羟基,可以与金属钠发生置换反应生成氢气:2C HOH+2Na
2 5
2C HONa+H ;乙醇在空气中完全燃烧生成二氧化碳和水:C HOH+3O =2CO +3H O;
2 5 2 2 5 2 2 2
乙醇在铜作催化剂条件下与氧气发生催化氧化生成乙醛:2C HOH+O
2 5 2
2CHCHO+2H O 。
3 2
21.(1)乙醇、浓硫酸、乙酸
(2)防倒吸
(3) 催化剂 吸水剂
(4) 中和乙酸 吸收乙醇 降低乙酸乙酯在水中的溶解度
(5)小
(6)
【分析】本题主要考查对于实验室制取乙酸乙酯实验的评价。
【详解】(1)在大试管中配制一定比例的乙醇、乙酸和浓硫酸的混合溶液的方法是:在试
管里先加入3mL乙醇,然后一边摇动一边慢慢的加入2mL浓硫酸,再加入2mL乙酸,然后轻轻振荡试管,使之混合均匀。
(2)装置中通蒸气的导管要插在饱和NaCO 溶液的液面上,不能插入溶液中,目的是防
2 3
止倒吸。
(3)浓硫酸的作用是作为该反应的催化剂;同时由于该反应是可逆反应,浓硫酸作为吸水
剂吸收生成的水,从而促进平衡往正向移动,有利于提高乙酸乙酯的产率。
(4)饱和NaCO 溶液的作用是:中和乙酸,溶解乙醇,同时降低乙酸乙酯的溶解度,有
2 3
利于乙酸乙酯的分离。
(5)乙酸乙酯的密度比水小。
(6)根据“酸脱羟基醇脱氢”的反应原理,该反应的化学方程式是:
22.(1) 球形冷凝管 使液体能够顺利流下
(2)离子化合物
(3)
(4)BC
(5)检查是否漏液
(6) 5.0 45.0%
【分析】Ⅰ.KOH、水合肼、亚硝酸异丙酯在乙醇中加热生成叠氮化钾,反应后加无水乙
醇,并用冰盐浴冷却,抽滤得到粗KN ,依次用无水乙醇、乙醚多次洗涤,100℃烘干
3
1~2h得到纯品KN 。Ⅱ.根据c( )——吸光度曲线可以确定样品溶液中的c( ),进而
3
可以计算样品的纯度。
【详解】(1)根据仪器构造可知,仪器B为球形冷凝管,仪器C是恒压滴液漏斗,可以
保证液体顺利滴下。
(2)KN 是由金属阳离子钾离子和阴离子叠氮酸根离子构成,所以属于离子化合物。
3
(3)根据给出的信息,仪器A中发生反应时, 与水合肼( )在碱
性条件下,生成KN 的同时还生成 (异丙醇),根据质量守恒可知,还有水生
3
答案第10页,共2页成,该反应的化学方程式为:
。
(4)A.步骤D是将65gKOH溶于300~400mL无水乙醇中,在甲装置中进行,不需要配
制一定物质的量浓度的容量瓶,需要的乙醇体积不需要准确测量,所以也不需要胶头滴管,
故A不选;
B.制备亚硝酸异丙酯的反应可能放热,用冰盐浴可以防止反应过于剧烈,故B选;
C.步骤F加入无水乙醇的目的是降低KN 的溶解度,促进 KN 的析出,故C选;
3 3
故选BC。
(5)容量瓶上面有一个活塞,所以使用前需要检查是否漏液。
(6)根据已知,曲线的绘制是不同浓度的5.0mL标准溶液,分别加入5.0mL(足量) FeCl
3
溶液得到的,所以步骤②中取用 FeCl 标准液 V=5.0mL;从图像可以看出,吸光度为0.6
3
时,c( )=4.0×10-2mol/L,则0.72g样品中含KN 的质量为4.0×10-2mol/L×0.1L×81g/mol=0.
3
324g,样品的质量分数为 =45.0%。答案第12页,共2页