文档内容
人教版(2019)必修第一册第三章第一节 铁及其化合物
课时训练二
学校:___________姓名:___________班级:___________考号:___________
一、单选题
1.下列有关金属及其化合物的说法错误的是
A.铁丝在氯气中剧烈燃烧,生成FeCl B.配制FeSO 溶液时加入少量的铁粉
2 4
C.Fe(OH) 在空气中易被氧化成红褐色的Fe(OH) D. 可用于制作红色油漆或涂
2 3
料
2.各物质中含有的少量杂质以及除去这些杂质对应的方法如表所示
物质 杂质 除去杂质的方法
① 溶液 加入适量 溶液并过滤
溶
② 加入过量铁粉并过滤
液
先通过盛有 溶液的洗气瓶,再通过盛有浓硫酸的洗
③
气瓶
④ 溶解、过滤、蒸发
其中正确的是A.①②③④ B.④ C.②③④
D.①②③
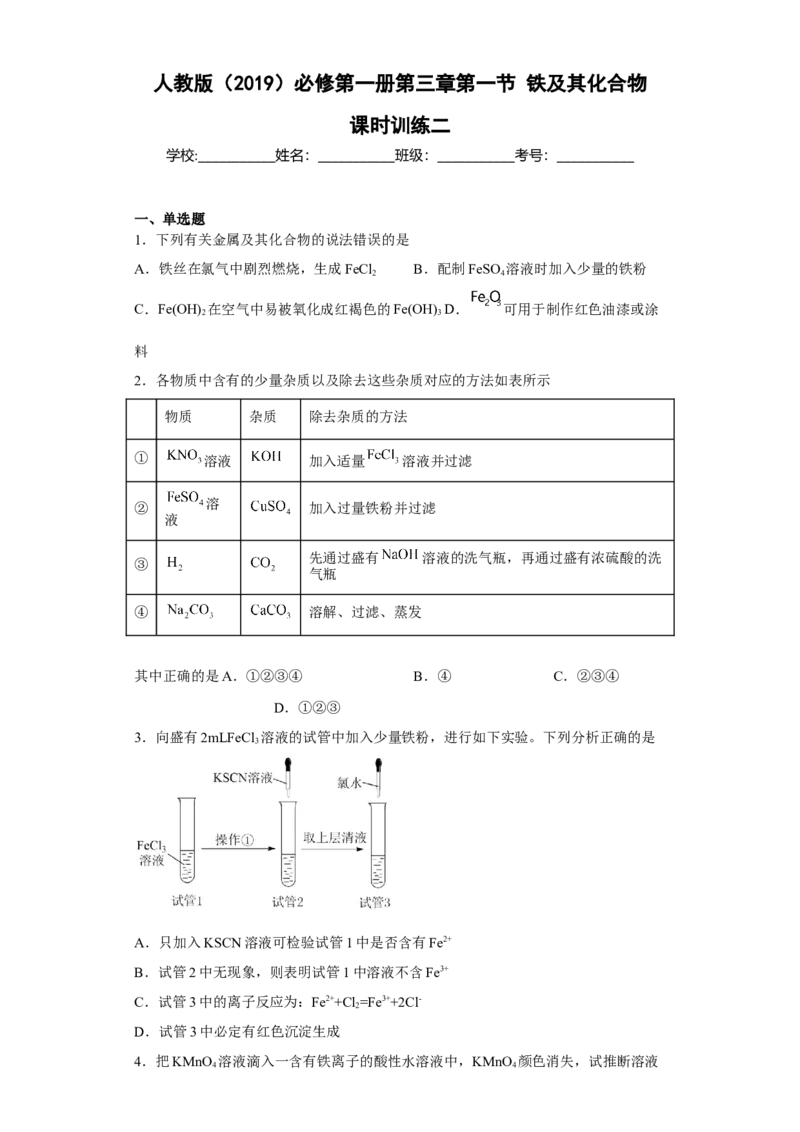
3.向盛有2mLFeCl 溶液的试管中加入少量铁粉,进行如下实验。下列分析正确的是
3
A.只加入KSCN溶液可检验试管1中是否含有Fe2+
B.试管2中无现象,则表明试管1中溶液不含Fe3+
C.试管3中的离子反应为:Fe2++Cl=Fe3++2Cl-
2
D.试管3中必定有红色沉淀生成
4.把KMnO 溶液滴入一含有铁离子的酸性水溶液中,KMnO 颜色消失,试推断溶液
4 4中含有铁离子的种类,最可能的情况是
A.含有Fe2+,但不能确定是否含有Fe3+
B.只含有Fe2+
C.Fe2+和Fe3+都有
D.含有Fe3+,但不能确定是否含有Fe2+
5.下列有关铁和铁的化合物的叙述中,正确的是
A.铁的化学性质比较活泼,它能与许多物质发生化学反应,因此铁在自然界中只能
以化合态存在
B.Fe O 是一种红棕色粉末,俗称铁红,常用作油漆、涂料、油墨和橡胶的红色颜料
3 4
C.Fe(OH) 在空气中容易被氧化,在制取Fe(OH) 时必须隔绝空气
2 2
D.往某溶液中先加入氯水,再加入KSCN溶液,发现溶液变成了红色,证明原溶液
中含有Fe3+
6.检验 溶液中是否混有少量 ,宜选用的试剂是
A.氯气 B.铁粉 C. 溶液 D.铜粉
7.下列微粒中,既有氧化性又有还原性的是( )
A.H+ B.Fe C.Fe2+ D.Fe3+
8.常温下,下列各组离子在指定溶液中能大量共存的是
A.无色透明的溶液中: 、 、 、
B.可以使pH试纸变蓝的溶液中: 、 、 、
C. 的溶液中: 、 、 、
D.能使石蕊试液变红的溶液中: 、 、 、
9.向某溶液中滴加硫氰化钾(KSCN)溶液时无明显现象,再滴入几滴氯水后溶液变成
红色。则原溶液中一定含有
A.CO B.Fe2+ C.Al3+ D.Cl-
10.下列变化过程没有涉及氧化还原反应的是
A.FeO是一种黑色粉末,不稳定,在空气中受热,迅速发生转化
B.Fe(OH) 白色沉淀在空气中放置变成红褐色
2
C.NaO 加入水中后,带火星的木条复燃
2 2
D.用干燥洁净的铂丝蘸取氯化钾溶液放到酒精喷灯火焰上灼烧,透过蓝色钴玻璃观
试卷第2页,共3页察火焰呈紫色
11.甘肃省张掖七彩丹霞景区为国家5A级旅游景区。丹霞地貌的岩层因含有某种物质
而呈红色,这种物质是
A.Fe(OH) B.Fe O C.Fe(OH) D.FeO
3 2 3 2
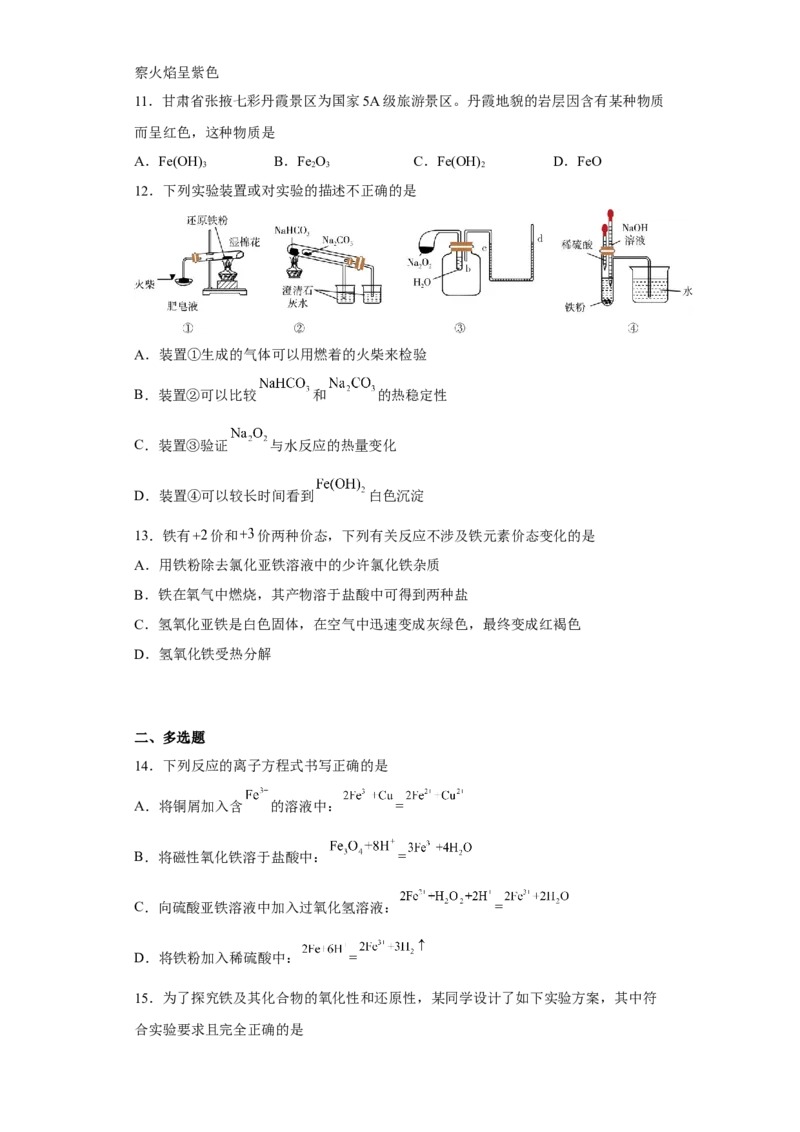
12.下列实验装置或对实验的描述不正确的是
A.装置①生成的气体可以用燃着的火柴来检验
B.装置②可以比较 和 的热稳定性
C.装置③验证 与水反应的热量变化
D.装置④可以较长时间看到 白色沉淀
13.铁有 价和 价两种价态,下列有关反应不涉及铁元素价态变化的是
A.用铁粉除去氯化亚铁溶液中的少许氯化铁杂质
B.铁在氧气中燃烧,其产物溶于盐酸中可得到两种盐
C.氢氧化亚铁是白色固体,在空气中迅速变成灰绿色,最终变成红褐色
D.氢氧化铁受热分解
二、多选题
14.下列反应的离子方程式书写正确的是
A.将铜屑加入含 的溶液中: =
B.将磁性氧化铁溶于盐酸中: =
C.向硫酸亚铁溶液中加入过氧化氢溶液: =
D.将铁粉加入稀硫酸中: =
15.为了探究铁及其化合物的氧化性和还原性,某同学设计了如下实验方案,其中符
合实验要求且完全正确的是选
实验操作 实验现象 离子反应 实验结论
项
向氯化亚铁溶液 浅绿色溶液变成 具有还
A -
中通入氯气 棕黄色溶液 原性
在氯化亚铁溶液 浅绿色溶液变成 具有还
B
中加入锌片 无色溶液 原性
在氯化铁溶液中 棕黄色溶液变成 铁单质具有
C
加入铁粉 浅绿色溶液 还原性
在氯化铁溶液中 蓝色溶液变成棕 具有氧
D
加入铜粉 黄色溶液 化性
A.A B.B C.C D.D
三、填空题
16.铁与空气接触时表面会形成氧化物,如一块低碳钢可以被三种氧化物膜所覆盖与
金属接触的一侧是FeO,与空气接触的一侧是 ,而中间则是 。
(1)中国古代“四大发明”之一最早的指南针“司南”,其具有磁性作用是因为主要含
有上述物质中的___________(填化学式)。
(2) 的一种用途是___________。
(3)FeO可作化妆品中的色素,它还能进行一系列转化:
。
① 时应加入的试剂是___________。
②“速力菲”(主要有效成分是 )是一种常见的补铁药物,欲验证该药物超过保质
期后已变质,可进行的操作是:除去药物表面包装的糖衣后将药物粉碎、加水溶解静
置、取少许溶液于试管中,向其中加入___________,若出现___________现象,则证
明该药物已变质。
③在 中滴加NaOH溶液的实验现象是___________,发生反应的化学方程式是
___________。
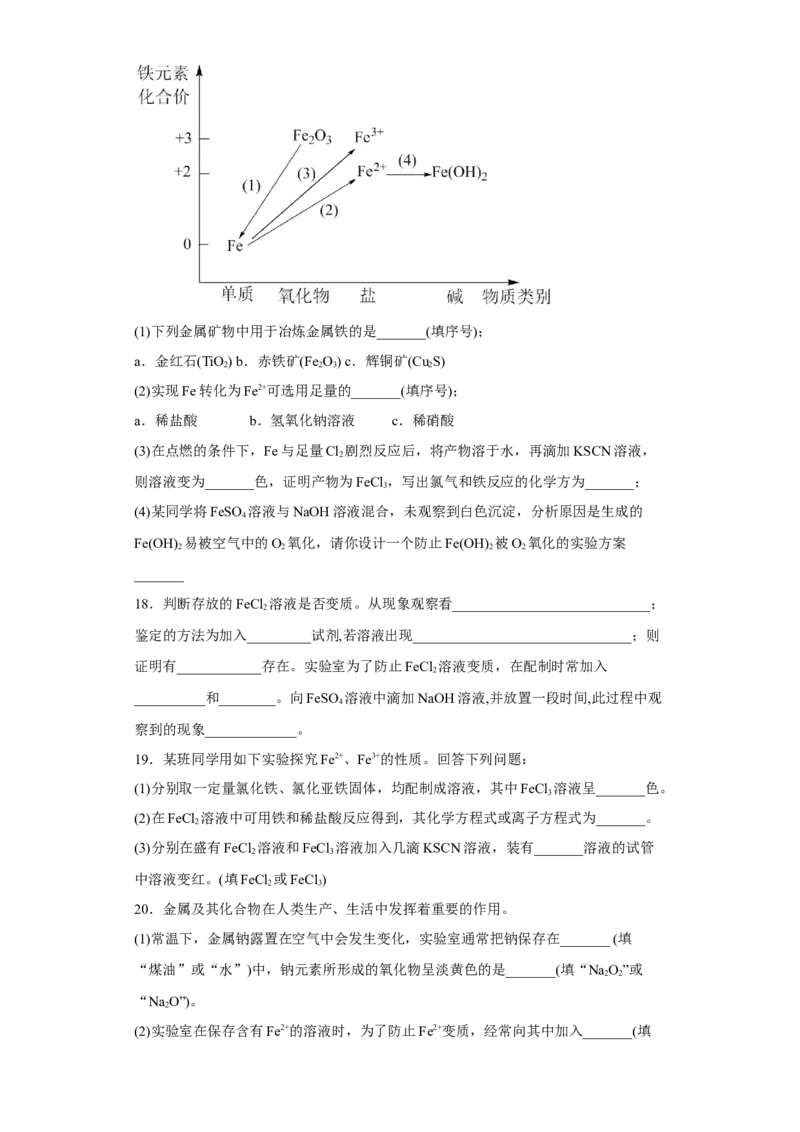
17.铁及其重要化合物之间的部分转化关系如图所示。
试卷第4页,共3页(1)下列金属矿物中用于冶炼金属铁的是_______(填序号);
a.金红石(TiO) b.赤铁矿(Fe O) c.辉铜矿(Cu S)
2 2 3 2
(2)实现Fe转化为Fe2+可选用足量的_______(填序号);
a.稀盐酸 b.氢氧化钠溶液 c.稀硝酸
(3)在点燃的条件下,Fe与足量Cl 剧烈反应后,将产物溶于水,再滴加KSCN溶液,
2
则溶液变为_______色,证明产物为FeCl ,写出氯气和铁反应的化学方为_______;
3
(4)某同学将FeSO 溶液与NaOH溶液混合,未观察到白色沉淀,分析原因是生成的
4
Fe(OH) 易被空气中的O 氧化,请你设计一个防止Fe(OH) 被O 氧化的实验方案
2 2 2 2
_______
18.判断存放的FeCl 溶液是否变质。从现象观察看____________________________;
2
鉴定的方法为加入_________试剂,若溶液出现_______________________________;则
证明有____________存在。实验室为了防止FeCl 溶液变质,在配制时常加入
2
__________和________。向FeSO 溶液中滴加NaOH溶液,并放置一段时间,此过程中观
4
察到的现象_____________。
19.某班同学用如下实验探究Fe2+、Fe3+的性质。回答下列问题:
(1)分别取一定量氯化铁、氯化亚铁固体,均配制成溶液,其中FeCl 溶液呈_______色。
3
(2)在FeCl 溶液中可用铁和稀盐酸反应得到,其化学方程式或离子方程式为_______。
2
(3)分别在盛有FeCl 溶液和FeCl 溶液加入几滴KSCN溶液,装有_______溶液的试管
2 3
中溶液变红。(填FeCl 或FeCl )
2 3
20.金属及其化合物在人类生产、生活中发挥着重要的作用。
(1)常温下,金属钠露置在空气中会发生变化,实验室通常把钠保存在_______ (填
“煤油”或“水”)中,钠元素所形成的氧化物呈淡黄色的是_______(填“NaO”或
2 2
“NaO”)。
2
(2)实验室在保存含有Fe2+的溶液时,为了防止Fe2+变质,经常向其中加入_______(填“铁粉”或“铜粉”)。
四、实验题
21.健康人体内含铁元素大约 2~3g,人体内铁元素以亚铁离子和三价铁离子的形式存
在,Fe2+易被吸收,所以给贫血者补充铁元素时,应补充含 Fe2+的亚铁盐。“速力
菲”(主要成分:琥珀酸亚铁,呈暗黄色)是市场上一种常见的补铁药物。该药品不
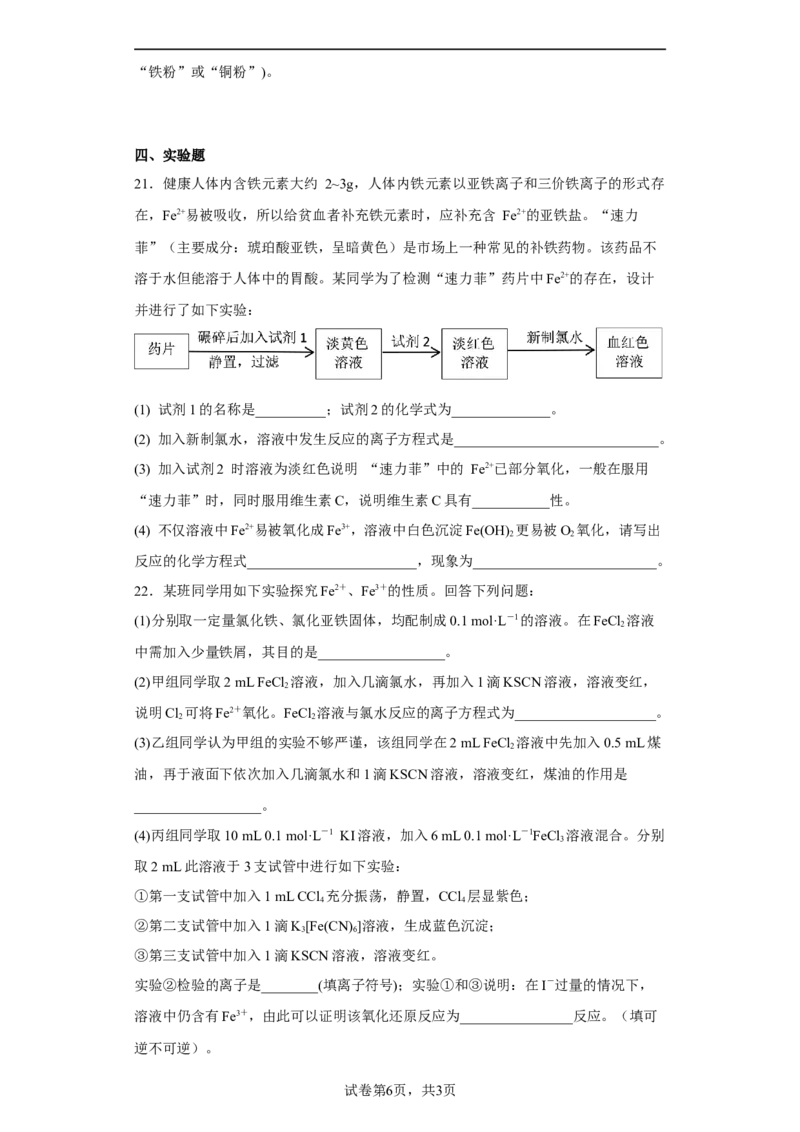
溶于水但能溶于人体中的胃酸。某同学为了检测“速力菲”药片中Fe2+的存在,设计
并进行了如下实验:
(1) 试剂1的名称是__________;试剂2的化学式为______________。
(2) 加入新制氯水,溶液中发生反应的离子方程式是_____________________________。
(3) 加入试剂2 时溶液为淡红色说明 “速力菲”中的 Fe2+已部分氧化,一般在服用
“速力菲”时,同时服用维生素C,说明维生素C具有___________性。
(4) 不仅溶液中Fe2+易被氧化成Fe3+,溶液中白色沉淀Fe(OH) 更易被O 氧化,请写出
2 2
反应的化学方程式________________________,现象为__________________________。
22.某班同学用如下实验探究Fe2+、Fe3+的性质。回答下列问题:
(1)分别取一定量氯化铁、氯化亚铁固体,均配制成0.1 mol·L-1的溶液。在FeCl 溶液
2
中需加入少量铁屑,其目的是__________________。
(2)甲组同学取2 mL FeCl 溶液,加入几滴氯水,再加入1滴KSCN溶液,溶液变红,
2
说明Cl 可将Fe2+氧化。FeCl 溶液与氯水反应的离子方程式为____________________。
2 2
(3)乙组同学认为甲组的实验不够严谨,该组同学在2 mL FeCl 溶液中先加入0.5 mL煤
2
油,再于液面下依次加入几滴氯水和1滴KSCN溶液,溶液变红,煤油的作用是
__________________。
(4)丙组同学取10 mL 0.1 mol·L-1 KI溶液,加入6 mL 0.1 mol·L-1FeCl 溶液混合。分别
3
取2 mL此溶液于3支试管中进行如下实验:
①第一支试管中加入1 mL CCl 充分振荡,静置,CCl 层显紫色;
4 4
②第二支试管中加入1滴K[Fe(CN) ]溶液,生成蓝色沉淀;
3 6
③第三支试管中加入1滴KSCN溶液,溶液变红。
实验②检验的离子是________(填离子符号);实验①和③说明:在I-过量的情况下,
溶液中仍含有Fe3+,由此可以证明该氧化还原反应为________________反应。(填可
逆不可逆)。
试卷第6页,共3页(5)丁组同学向盛有HO 溶液的试管中加入几滴酸化的FeCl 溶液,溶液变成棕黄色,
2 2 2
一段时间后,溶液中有气泡出现,并放热,随后有红褐色沉淀生成。产生气泡的原因
是___。参考答案:
1.A
【详解】A.铁在氯气中燃烧生成氯化铁,A错误;
B.亚铁离子容易被氧化,配制硫酸亚铁溶液时加入少量的铁粉,避免其被氧化,B正确;
C.氢氧化亚铁在空气中容易被氧气氧化生成红褐色氢氧化铁,C正确;
D.氧化铁为红棕色,可以做为红色油漆或涂料,D正确;
故选A。
2.C
【详解】①加入氯化铁与氢氧化钾反应生成的氯化钾新的杂质,故错误;
②加入过量铁粉将铜离子置换除去,同时不引入新的杂质,故正确;
③先通过氢氧化钠溶液可以吸收二氧化碳,再通过浓硫酸除去水蒸气,该过程中既没有消
耗氢气也没有引入新的杂质,故正确;
④碳酸钙不溶于水,碳酸钠可溶于水,所以可以通过溶解、过滤、蒸发得到纯净的碳酸钠,
故正确;
综上所述答案为C。
【点睛】除杂要把握两个原则:一是加入的试剂只能与杂质反应;二是不能引入新的杂质。
3.B
【详解】A.加入KSCN溶液可检验Fe3+,故A错误;
B.加入KSCN溶液可检验Fe3+,试管2中无现象,则表明试管1中溶液不含Fe3+,故B正
确;
C.试管3中的离子反应为:2Fe2++Cl=2Fe3++2Cl-,故C错误;
2
D.试管3中加入氯水将Fe2+氧化为Fe3+,试管2中上层清液含KSCN溶液,与Fe3+结合生
成血红色配合物,不是沉淀,故D错误;
故选:B。
4.A
【分析】紫红色的酸性KMnO 溶液具有强氧化性,能够被强还原性微粒还原成Mn2+。
4
KMnO 颜色消失,说明溶液中含有Fe2+等强还原性微粒。Fe3+具有强氧化性,不能使酸性
4
KMnO 溶液褪色。
4
【详解】A.在酸性的条件下,高锰酸钾氧化亚铁离子后,生成近乎无色的二价锰离子
Mn2+,比高锰酸钾本身的紫色要淡得多,所以表现为“褪色”即KMnO 颜色消失现象。高
4
锰酸钾具有强氧化性,会把二价铁离子氧化为稳定的三价铁离子,但由于高锰酸钾本身就是深紫红色液体,所以与亚铁离子反应后的现象是溶液的紫红色变淡。Fe3+的存在与否不
影响上述现象,故含有Fe2+,但不能确定是否含有Fe3+,故A选项正确;
B.Fe3+的存在与否不影响题干现象,确定含有Fe2+,但不能确定是否含有Fe3+。存在
Fe3+也不影响题干现象,只含Fe2+的描述过于绝对,故B选项错误;
C.根据题干确定含有Fe2+,但不能确定是否含有Fe3+。Fe2+和Fe3+都有的描述错误,故C
选项错误;
D.根据题干确定含有Fe2+,但不能确定是否含有Fe3+,故D选项错误;
故答案选A。
5.C
【详解】A.铁的化学性质比较活泼,铁在自然界中可以像陨铁中的铁那样以单质形态存
在,但主要是以+2价和+3价化合物的形态存在,A错误;
B.Fe O 是一种红棕色粉末,俗称铁红,常用作油漆、涂料、油墨和橡胶的红色颜料,B
2 3
错误;
C.Fe(OH) 在空气中容易被氧化,在制取Fe(OH) 时防止被氧气氧化,故必须隔绝空气,C
2 2
正确;
D.往某溶液中先加入氯水,再加入KSCN溶液,发现溶液变成了红色,不能证明原溶液
中含有Fe3+,如果原溶液中含有Fe2+时现象也一样,D错误;
故选C。
6.C
【详解】 与SCN-化合生成血红色溶液而Fe2+没有此性质,离子方程式为: +3SCN-
=Fe(SCN) ,故检验 溶液中是否混有少量 宜选用的试剂为KSCN溶液,故答案为:
3
C。
7.C
【分析】化合价处于最高价的,只有氧化性;处于最低价的,只有还原性;处于中间价态
的既有氧化性,又有还原性。
【详解】A. H+化合价处于最高价,只有氧化性,故A不选;
B. Fe处于最低价,只有还原性,故B不选;
C. Fe2+处于中间价态的既有氧化性,又有还原性,故C选;
D. Fe3+化合价处于最高价,只有氧化性,故D不选;
答案第2页,共2页故选C。
8.B
【详解】A.无色溶液中不会存在Fe3+,且Fe3+与SCN-在溶液中不会大量共存,A不符合
题意;
B.可以使pH试纸变蓝的溶液显碱性,碱性溶液中四种离子相互之间不反应,也不与氢氧
根反应,可以大量共存,B符合题意;
C.高锰酸根具有强氧化性,不能与具有还原性的Fe2+大量共存,C不符合题意;
D.能使石蕊试液变红的溶液显酸性,碳酸氢根不能大量存在,D不符合题意;
综上所述答案为B。
9.B
【详解】向某溶液中滴加硫氰化钾(KSCN)溶液时无明显现象,说明不含Fe3+,再滴入几滴
氯水后溶液变成红色,说明原溶液中含有Fe2+,被氯水氧化为Fe3+;
故答案为B。
10.D
【详解】A.FeO在空气中受热会被氧化为Fe O,Fe元素被氧化,涉及氧化还原反应,A
3 4
不符合题意;
B.氢氧化亚铁不稳定,易被氧化生成氢氧化铁,发生氧化还原反应,B不符合题意;
C.NaO 与水反应生成氧气,而使带火星的木条复燃,发生氧化还原反应,C不符合题意;
2 2
D.焰色试验属于物理变化,不涉及氧化还原反应,D符合题意;
综上所述答案为D。
11.B
【详解】铁的化合物中呈红褐色的是Fe O,故丹霞地貌的岩层因含有某种物质而呈红色,
2 3
这种物质是Fe O,合理选项是B。
2 3
12.B
【详解】A.铁与水蒸气在高温下生成四氧化三铁和氢气,氢气在肥皂泡中分散分布,点
燃不会发生危险,且氢气点燃火焰呈淡蓝色,因此装置①生成的气体可以用燃着的火柴来
检验,故A正确;
B.比较 和 的热稳定性时,应将 置于内部的小试管中,不能直接
加热,故B错误;
C. 与水反应放热,瓶内气体受热膨胀,图中c处液面低、d处液面高可证明,故C正确;
D.先滴加稀硫酸与铁粉反应生成氢气,排出装置内的空气,再把吸有氢氧化钠溶液的胶
头滴管伸入液面下滴加,氢氧化钠与硫酸亚铁反应生成氢氧化亚铁,该装置能较长时间看
到 白色沉淀,故D正确;
答案选B。
13.D
【详解】A. ,化合价由 价变为 价,故A不符合题意;
B. ,化合价由0价变为 价、 价,故B不符合题意;
C. ,化合价由 价变为 价,故C不符合题意;
D. ,化合价没有变化,故D符合题意;
本题答案D。
14.AC
【详解】A.Fe3+能将铜氧化为铜离子,本身被还原为亚铁离子,满足原子守恒、电荷守恒,
离子方程式书写正确,A正确;
B.磁性氧化铁与盐酸反应生成氯化铁、氯化亚铁和水,正确的离子方程式: F
eO+8H+=2Fe3++ Fe2++4H O,B错误;
3 4 2
C.双氧水的强氧化性将二价铁氧化为三价铁,满足原子守恒、电荷守恒,离子方程式书
写正确,C正确;
D.铁粉与稀硫酸反应生成硫酸亚铁和氢气,正确的离子方程式:Fe+2H+=Fe2++H ↑,D错
2
误;
故答案为AC。
15.AC
【详解】A.向氯化亚铁溶液中通入氯气,其反应为 -,其中Fe2+在
溶液中呈浅绿色,Fe3+在溶液中呈棕黄色,化合价升高,被氧化,具有还原性,溶液由浅
绿色变为棕黄色,故A正确;
答案第4页,共2页B.氯化亚铁与Zn发生置换反应,生成Zn2+和Fe,Zn2+在溶液中呈无色,反应为
,其中Fe元素化合价降低,被还原,具有氧化性,故B错误;
C.氯化铁与铁反应生成氯化亚铁,其反应为 ,其中铁单质被氧化,具有
还原性,溶液由棕黄色变为浅绿色,故C正确;
D.氯化铁与铜反应的离子方程式为 ,其中铁元素化合价降低,被
还原,具有氧化性,溶液由棕黄色变为蓝色,故D错误;
故选AC。
16. 制红色油漆、防锈漆 硫酸 向其中滴加
KSCN溶液,溶液变红, 产生白色沉淀迅速变为灰绿色,最终变为红褐
色
【详解】(1) 古代中国四大发明之一的司南是由天然磁石制成的,磁铁成分主要是四氧化
三铁化学式为Fe O,故答案为:Fe O;
3 4 3 4
(2) 氧化铁是红色固体难溶于水,可以制红色油漆、防锈漆,故答案为:制红色油漆、防
锈漆;
(3) ①FeO→FeSO 时应加入的试剂是稀硫酸,发生FeO+ H SO = FeSO + H O,故答案为:
4 2 4 4 2
稀硫酸;
②速力菲”(主要有效成分是 )是一种常见的补铁药物,欲验证该药物超过保质期后
已变质,可进行的操作是:除去药物表面包装的糖衣后将药物粉碎、加水溶解静置、取少
许溶液于试管中,向其中滴加KSCN溶液,若溶液变红,有铁离子存在,则证明该药物已
变质,反之没有变质,故答案为:其中滴加KSCN溶液,溶液变红;
③在 中滴加NaOH溶液的实验现象是产生白色沉淀迅速变为灰绿色,最终变为红褐
色,发生的化学反应方程式为: ,,故答案为:产生白色沉淀迅速变为灰绿色,最终变为红
褐色, , 。
17. b a 血红色 2Fe+3Cl 2FeCl 先向硫酸亚铁溶液上覆盖
2 3
一层煤油,再将吸有氢氧化钠溶液的胶头滴管插入硫酸亚铁溶液中,轻轻挤入,让两者在
液面下反应即可得氢氧化亚铁
【详解】、
(1) 用于冶炼金属铁,可知化合物含Fe元素,只有赤铁矿符合,故答案为:b;
(2) Fe转化为Fe2+,Fe与弱氧化剂反应,只有稀盐酸符合,与NaOH不反应,硝酸具有强
氧化性,故答案为: a;
(3) 氯气具有强氧化性,与Fe反应生成氯化铁,铁离子遇KSCN溶液为血红色,则点燃的
条件下,Fe与足量Cl 剧烈反应后,将产物溶于水,再滴加KSCN溶液溶液变为血红色,
2
证明产物为FeCl ,该反应的化学方程式2Fe+3Cl 2FeCl ,故答案为:血红色,
3 2 3
2Fe+3Cl 2FeCl ;
2 3
(4) 防止Fe(OH) 被O 氧化的实验方案为在FeSO 溶液表面加入适量的煤油,隔绝空气,在
2 2 4
硫酸亚铁溶液的液面下挤出胶头滴管中的NaOH,故答案为: 先向硫酸亚铁溶液上覆盖一
层煤油,再将吸有氢氧化钠溶液的胶头滴管插入硫酸亚铁溶液中,轻轻挤入,让两者在液
面下反应即可得氢氧化亚铁。
18. 溶液是否变为黄色 KSCN 血红色 Fe3+ 铁
粉 盐酸 白色沉淀生成,且白色沉淀迅速变成灰绿色,最后变成红褐色
【分析】亚铁离子具有强的还原性,能够发生水解,据此性质回答氯化亚铁的相关问题;
铁离子可以用硫氰化钾溶液进行检验。
【详解】在溶液中亚铁离子为浅绿色,铁离子为黄色,从现象观察若溶液颜色变为黄色,则存
放的FeCl 溶液因氧化而变质;加入KSCN溶液试剂,若溶液出现血红色,则证明有Fe3+存在;
2
答案第6页,共2页配制FeCl 溶液要防止其水解,需要加盐酸抑制其水解,为了防止亚铁离子被氧化,需要加
2
铁粉;硫酸亚铁和氢氧化钠发生反应生成氢氧化亚铁白色沉淀,该白色沉淀易被氧化为氢
氧化铁,则向FeSO 溶液中滴加NaOH溶液,并放置一段时间,此过程中观察到的现象:白色沉
4
淀生成,且白色沉淀迅速变成灰绿色,最后变成红褐色,
故答案为:溶液是否变为黄色;血红色;Fe3+;铁粉和盐酸;白色沉淀生成,且白色沉淀迅
速变成灰绿色,最后变成红褐色。
19. 黄 Fe+2H+=Fe2++H ↑ FeCl
2 3
【详解】(1)含Fe3+的溶液呈黄色;
(2)Fe与HCl反应生成FeCl 和H,对应方程式为:Fe+2HCl=FeCl +H ↑或Fe+2H+=Fe2+
2 2 2 2
+H ↑;
2
(3)由反应FeCl +3KSCN=Fe(SCN) (红色)+3KCl,知装有FeCl 的溶液变红。
3 3 3
20.(1) 煤油 NaO
2 2
(2)铁粉
【分析】(1)
钠的化学性质很活泼,容易和空气中的氧气、水蒸气等发生反应,所以保存钠的时候应隔
绝空气,实验室通常把钠保存在煤油中,钠的密度比煤油的大,可以沉入煤油底部。钠的
氧化物主要有氧化钠和过氧化钠,氧化钠是白色的,过氧化钠是淡黄色的。
(2)
Fe2+具有还原性,容易被空气中的氧气氧化,所以实验室在保存含有Fe2+的溶液时,为了防
止Fe2+变质,经常向其中加还原性更强的铁粉。
21. 盐酸 KSCN 2Fe2+ + Cl == 2Fe3+ + 2Cl- 还原性
2
4Fe(OH) + O + 2H O == 4Fe(OH) 白色沉淀迅速变为灰绿色,最终变为红褐色
2 2 2 3
【分析】(1)根据“琥珀酸亚铁不溶于水但能溶于人体中的胃酸”分析,应用盐酸溶解琥
珀酸亚铁;淡黄色溶液加入试剂2变为淡红色,加入新制氯水后溶液变血红色,则加入的
试剂2是KSCN;
(2)加入新制氯水后溶液变为血红色,说明Fe2+被氧化为Fe3+;
(3)Vc可使食物中的Fe3+转化成Fe2+,Fe元素的化合价降低,所以Fe3+是氧化剂,Vc是
还原剂,则Vc具有还原性;
(4)碱性环境中Fe(OH) 被O 氧化为氢氧化铁;现象为白色沉淀迅速变为灰绿色,最终变
2 2为红褐色。
【详解】(1)根据“琥珀酸亚铁不溶于水但能溶于人体中的胃酸”,用盐酸溶解琥珀酸亚
铁,所以试剂1是盐酸;淡黄色溶液加入试剂2变为淡红色,加入新制氯水后溶液变血红
色,则加入的试剂2是KSCN溶液;
故答案为盐酸;KSCN;
(2)加入新制氯水后溶液变为血红色,说明Fe2+被氧化为Fe3+,溶液中发生反应的离子方
程式是2Fe2+ + Cl == 2Fe3+ + 2Cl-;
2
故答案为2Fe2+ + Cl == 2Fe3+ + 2Cl-;
2
(3)Vc可使食物中的Fe3+转化成Fe2+,Fe元素的化合价降低,所以Fe3+是氧化剂,Vc是
还原剂,则Vc具有还原性;
故答案为还原性;
(4)碱性环境中Fe(OH) 被O 氧化为氢氧化铁,反应方程式为4Fe(OH) + O + 2H O ==
2 2 2 2 2
4Fe(OH) ;现象为白色沉淀迅速变为灰绿色,最终变为红褐色;
3
故答案为4Fe(OH) + O + 2H O == 4Fe(OH) ;白色沉淀迅速变为灰绿色,最终变为红褐色。
2 2 2 3
22. 防止氯化亚铁被氧化 2Fe2++Cl=2Fe3++2Cl- 隔绝空气
2
(排除氧气对实验的影响) Fe2+ 可逆 反应生成的Fe3+催化了HO 的分
2 2
解
【分析】(1)铁和氯化铁反应生成氯化亚铁,氯化亚铁溶液中加入铁粉防止氯化亚铁被氧
化;
(2)氯气具有氧化性,能氧化氯化亚铁为氯化铁;
(3)煤油不溶于水,密度比水小,浮在液面上,可以隔绝溶液与空气接触,排除氧气对实
验的影响;
(4)加入1滴K[Fe(CN) ]溶液,生成蓝色沉淀,是亚铁离子检验的特征反应现象,第一
3 6
支试管中加入1mL CCl 充分振荡、静置,CCl 层显紫色说明生成I,碘离子被铁离子氧化
4 4 2
为碘单质,③第三支试管中加入1滴KSCN溶液,溶液变红,说明溶液中含有铁离子,在
I−过量的情况下,溶液中仍含有Fe3+,说明该反应为可逆反应;
(5)向盛有HO 溶液的试管中加入几滴酸化的FeCl 溶液,溶液变成棕黄色,说明过氧化
2 2 2
氢氧化亚铁离子为铁离子,铁离子对过氧化氢分解起到催化剂作用。
【详解】(1)FeCl 易被空气中的氧气氧化,而铁和氯化铁可反应生成氯化亚铁,则在
2
FeCl 溶液中需加入少量铁屑,其目的是防止氯化亚铁被氧化;
2
故答案为防止氯化亚铁被氧化;
答案第8页,共2页(2)氯气具有氧化性,能氧化氯化亚铁为氯化铁,反应的离子方程式为:2Fe2++Cl=
2
2Fe3++2Cl-;
故答案为2Fe2++Cl=2Fe3++2Cl-;
2
(3)FeCl 易被空气中的氧气氧化,煤油不溶于水,密度比水小,浮于液面上,可以隔绝
2
溶液与空气接触,排除氧气对实验的影响;
故答案为隔绝空气(排除氧气对实验的影响);
(4)加入1滴K[Fe(CN) ]溶液,生成蓝色沉淀是亚铁离子检验的特征反应现象,实验②
3 6
检验的离子是Fe2+,①第一支试管中加入1mLCCl 充分振荡、静置,CCl 层显紫色,说明
4 4
生成I,碘离子被铁离子氧化为碘单质,反应的离子方程式为:2Fe3++2I−=I +2Fe2+,③第三
2 2
支试管中加入1滴KSCN溶液,溶液变红,说明溶液中含有铁离子,在I−过量的情况下,
溶液中仍含有Fe3+,说明该反应为可逆反应;
故答案为Fe2+;可逆;
(5)向盛有HO 溶液的试管中加入几滴酸化的FeCl 溶液,溶液变成棕黄色,说明过氧化
2 2 2
氢氧化亚铁离子为铁离子,铁离子对过氧化氢分解起到催化剂作用,产生气泡的原因是反
应生成的Fe3+催化了HO 的分解;
2 2
故答案为反应生成的Fe3+催化了HO 的分解。
2 2答案第10页,共2页