文档内容
第三章 第一节 第2课时 物质的量在化学方程式计算中的应用 测试题
榆次一中 李金虎
一、选择题(每小题只有一个正确选项,每小题4分,共60分)
1. 质量比为2∶3的金属铝分别跟足量稀HSO 和NaOH溶液反应,则产生H 的体积比是( )
2 4 2
A.1∶2 B.1∶3
C.2∶3 D.3∶2
2. 将5.0 g某金属合金放入足量的稀盐酸中,共收集氢气在标准状况下的体积为2.24 L,则该金
属合金可能是( B )
A.MgAl合金 B.FeAl合金
C.FeZn合金 D.CuZn合金
3. 有关Al与NaOH溶液反应的说法中,正确的是( )
A.Al是还原剂,NaOH及HO均是氧化剂
2
B.还原产物是H,且由HO还原所得的H 与由NaOH还原所得的H 物质的量之比为2∶1
2 2 2 2
C.反应中1 mol Al失去4 mol电子
D.此反应中,只有水是氧化剂,NaOH既不是氧化剂也不是还原剂
4. 某金属R的氯化物溶液20 mL,浓度为0.05 mol·L-1。它恰好能与20 mL 0.15 mol·L-1的AgNO
3
溶液完全反应,则该氯化物的化学式为( )
A.RCl B.RCl C.RCl D.RCl
2 3 5
5. 等量的铁分别与足量的盐酸、水蒸气在一定的条件下充分反应,则在相同的条件下,产生氢气
的体积比是( )
A.1∶1 B.3∶4 C.2∶3 D.4∶3
6. 在500 mL NaOH溶液中加入足量铝粉,反应完全后共收集到标准状况下的气体 33.6 L。该
NaOH溶液的物质的量浓度为( )
A.1.0 mol·L-1 B.2.0 mol·L-1
C.1.5 mol·L-1 D.3.0 mol·L-1
7. 铁粉可与高温水蒸气发生反应,若反应后得到的干燥固体质量比反应前铁粉的质量增加了 32
g,则参加反应的铁粉的物质的量是( )
A.0.5 mol B.1 mol
C.1.5 mol D.2 mol
8. 将钠、镁、铝各0.3 mol分别放入100 mL 1 mol/L的盐酸中,同温同压下产生的气体体积比是(
)
A.1∶2∶3 B.6∶3∶2
C.3∶1∶1 D.1∶1∶1
9. 由锌、铁、铝、镁四种金属中的两种组成的混合物10 g,与足量的盐酸反应产生的氢气在标准
状况下为11.2 L,则混合物中一定含有的金属是( )
A.锌 B.铁 C.铝 D.镁
1
学科网(北京)股份有限公司10.若3.6 g某金属与足量盐酸充分反应,放出4.48 L(标准状况)H ,则该金属是( )
2
A.Al B.Mg C.Fe D.Zn
11.甲、乙两烧杯中各盛有100 mL 3 mol·L-1的盐酸和氢氧化钠溶液中,向两烧杯中分别加入等质
量的铝粉,反应结束后测得生成的气体体积比为甲∶乙=1∶2,则加入的铝粉质量为( )
A.5.4 g B.3.6 g C.2.7 g D.1.8 g
12.等质量的两份铝分别与适量的稀HSO 和NaOH溶液完全反应,若消耗两溶液的体积相同,则
2 4
稀HSO 与NaOH溶液的物质的量浓度之比为( )
2 4
A.3∶2 B.2∶3
C.2∶1 D.1∶2
13.将铁加入到100 mL某浓度的盐酸中恰好完全反应,反应后生成的气体为V L(标准状况),将铝
加入到100 mL、2 mol·L-1的NaOH溶液中恰好完全反应,充分反应后生成的气体为3V L。下
列说法正确的是( )
A.原铁和铝的物质的量相等
B.原盐酸的浓度为2 mol·L-1
C.铁加入盐酸中的离子方程式为2Fe+6H+===2Fe3++3H↑
2
D.盐酸与氢氧化钠的物质的量浓度之比为1∶3
14.将a mol钠和a mol铝一同投入m g足量水中,所得溶液密度为d g·mL-1,该溶液中溶质质
量分数为( )
A. % B. % C. % D. %
15.某溶液中可能含有H+、NH、Mg2+、Al3+、Fe3+、CO、SO、NO中的几种。①若加入锌粒,
产生无色无味的气体;②若加入NaOH溶液,产生白色沉淀,且产生的沉淀量与加入NaOH的
物质的量之间的关系如图所示。则下列说法正确的是( )
A.溶液中的阳离子只有H+、Mg2+、Al3+
B.溶液中n(NH)=0.2 mol
C.溶液中一定不含CO,可能含有SO和NO
D.n(H+)∶n(Al3+)∶n(Mg2+)=1∶1∶1
二、填空题(本题包括3个小题,共40分)
16.(12分)向500 mL NaOH溶液中投入10.8 g Al,二者恰好完全反应,计算:
(1)Al的物质的量为 mol。
(2)参加反应的NaOH的物质的量和溶液的物质的量浓度分别为 。
(3)生成的H 在标准状况下的体积为 。
2
17.(12分)将19.5 g锌粒投入250 mL 2 mol·L-1的硫酸溶液中,试计算:
2
学科网(北京)股份有限公司(1)产生的氢气在标准状况下的体积为 L。
(2)忽略溶液体积变化,反应后溶液中氢离子浓度是 。
(3)要配制250 mL 2 mol·L-1的硫酸溶液,需用溶质质量分数为98%,密度为1.84 g·cm-3浓硫
酸的体积为 。(保留三位有效数字)
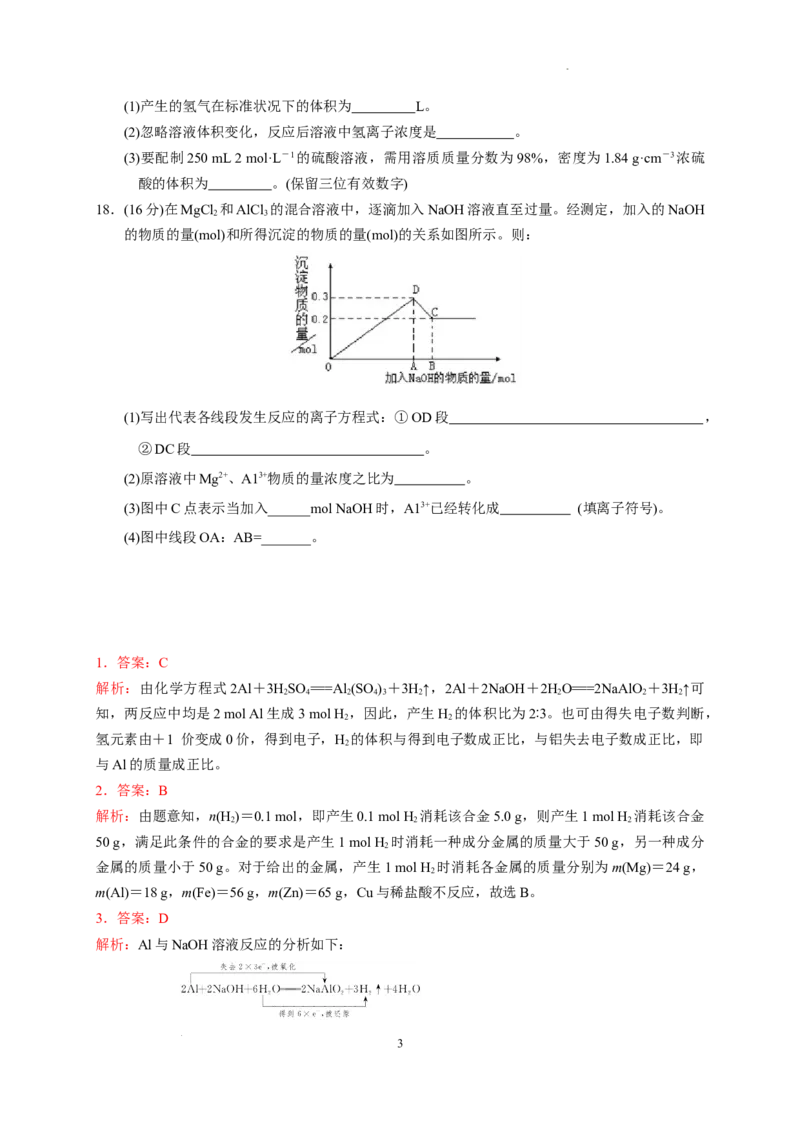
18.(16分)在MgCl 和AlCl 的混合溶液中,逐滴加入NaOH溶液直至过量。经测定,加入的NaOH
2 3
的物质的量(mol)和所得沉淀的物质的量(mol)的关系如图所示。则:
(1)写出代表各线段发生反应的离子方程式:①OD段 ,
②DC段 。
(2)原溶液中Mg2+、A13+物质的量浓度之比为 。
(3)图中C点表示当加入______mol NaOH时,A13+已经转化成 (填离子符号)。
(4)图中线段OA:AB=_______。
1.答案:C
解析:由化学方程式2Al+3HSO ===Al(SO ) +3H↑,2Al+2NaOH+2HO===2NaAlO +3H↑可
2 4 2 4 3 2 2 2 2
知,两反应中均是2 mol Al生成3 mol H ,因此,产生H 的体积比为2∶3。也可由得失电子数判断,
2 2
氢元素由+1 价变成0价,得到电子,H 的体积与得到电子数成正比,与铝失去电子数成正比,即
2
与Al的质量成正比。
2.答案:B
解析:由题意知,n(H )=0.1 mol,即产生0.1 mol H 消耗该合金5.0 g,则产生1 mol H 消耗该合金
2 2 2
50 g,满足此条件的合金的要求是产生1 mol H 时消耗一种成分金属的质量大于50 g,另一种成分
2
金属的质量小于50 g。对于给出的金属,产生1 mol H 时消耗各金属的质量分别为m(Mg)=24 g,
2
m(Al)=18 g,m(Fe)=56 g,m(Zn)=65 g,Cu与稀盐酸不反应,故选B。
3.答案:D
解析:Al与NaOH溶液反应的分析如下:
3
学科网(北京)股份有限公司所以反应中,氧化剂是HO,还原剂是Al,NaOH既不是氧化剂也不是还原剂。
2
4.答案:C
解析:可设该氯化物的化学式为RCl,则:
x
RCl + xAgNO===xAgCl↓+R(NO )
x 3 3 x
1 x
20×10-3×0.05 20×10-3×0.15
列式得:1∶x=(20×10-3×0.05)∶(20×10-3×0.15),解得x=3。
5.答案:B
解析:根据反应的化学方程式知:Fe+2HCl===FeCl +H↑ 3Fe+4HO(g)=====Fe O+4H
2 2 2 3 4 2
1 mol Fe与盐酸反应生成1 mol H ,与水蒸气反应生成 mol H,故相同条件下,产生H 的体积比是
2 2 2
3∶4。
6.答案:B
解析: 2Al+2NaOH+2HO===2NaAlO+3H↑
2 2 2
2 mol 67.2 L
n(NaOH) 33.6 L
n(NaOH)==1 mol, c(NaOH)==2 mol·L-1。
7.答案:C
解析: 3Fe+4HO(g)=====Fe O+4H Δm(固体质量增加)
2 3 4 2
3 16×4
x mol 32 g x=1.5 mol。
8.答案:C
解析:由题意知:钠、镁、铝的物质的量均为0.3 mol,n(HCl)=0.1 L×1 mol·L-1=0.1 mol。经分析
知,钠、镁、铝与盐酸反应时,金属均过量,盐酸量不足。当钠与盐酸反应时,盐酸完全反应后,
钠还可以与水反应生成H ,产生H 的量以钠为准进行计算:2Na~H↑,故0.3 mol钠反应放出H
2 2 2 2
为0.15 mol;当镁、铝分别与盐酸反应时,产生H 的量以盐酸为准进行计算:2HCl~H↑,0.3 mol
2 2
镁、铝与HCl反应分别放出H 0.05 mol,故其体积比为3∶1∶1。
2
9.答案:C
解析:金属与水、酸或碱反应产生H 的量的关系为M~H ,M代表某种金属,n代表金属化合价
2 2
即1 mol金属与水、酸或碱反应产生mol的H。
2
解法一:用极值思想和上述金属与酸反应产生H 的关系式,很容易求解。
2
M~H 由此很快算出,产生标准状况下 11.2 L的H 时,需要各金属的质量分别是 m(Zn)=
2 2
32.5 g,m(Fe)=28 g,m(Mg)=12 g,m(Al)=9 g<10 g。只有当Al与其他任意一种金属混合才可能
⇒
产生标准状况下的H 11.2 L。
2
解法二:也可以用求平均相对原子质量的方法解答。先假定化合价为+2价,求出金属混合物
的平均相对原子质量:10∶=11.2∶22.4,则 =20,而锌、铁、镁的相对原子质量均大于20,铝
r r
作为+2价时,相对原子质量可算作27×=18<20,则必含有铝。
10.答案:A
4
学科网(北京)股份有限公司解析:设该金属的相对原子质量为M(R),与盐酸反应时的化合价为x,则由化学方程式:
r
2R+ 2xHCl === 2RCl + xH↑
x 2
2M(R)g 22.4x L
r
3.6 g 4.48 L 所以=,解得M(R)=9x,
r
讨论:若x=1,则M(R)=9,不符合题意;
r
若x=2,则M(R)=18,不符合题意;
r
若x=3,则M(R)=27,符合题意。
r
11.答案:A
解析:由6HCl+2Al===2AlCl +3H↑,2NaOH+2Al+2HO===2NaAlO +3H↑可知,两份等质量
3 2 2 2 2
的Al都完全反应时,生成的H 等量,消耗的HCl与NaOH不等量。实际上HCl、NaOH同为0.3
2
mol,且已知生成H 的体积比为1∶2,所以发生反应时分别为HCl不足Al过量,NaOH过量Al不
2
足。由生成H 的体积比为1∶2可知,反应的Al的量之比也为1∶2,则与0.3 mol盐酸反应的Al为
2
2.7 g,与NaOH溶液反应的Al为5.4 g。
12.答案:A
解析: 2Al~3HSO 2Al~2NaOH
2 4
2 3 2 2
等量的Al消耗HSO 和NaOH的物质的量之比是3∶2。又因它们体积相同,则物质的量浓度之比
2 4
等于物质的量之比。
13.答案:B
解析:由反应方程式:Fe+2HCl===FeCl +H↑,2Al+2NaOH+2HO===2NaAlO +3H↑,可得生
2 2 2 2 2
成H 的体积之比为1∶3时,消耗的Fe与Al的物质的量之比为1∶2,盐酸与氢氧化钠的物质的量
2
之比为1∶1,从而也就可得盐酸的物质的量浓度为2 mol·L-1。
14.答案:C
解析:由\s\up7(2Na~2NaOH~H2↑)及 \s\up7(2Al~2NaOH~2NaAlO2~3H2↑)
50a+m-(+a)×2=46 a+m 所以,w(NaAlO )=×100%=%。
2
15.答案:B
解析:由①知溶液中一定含有H+,一定没有CO、NO,由②及图像知溶液中一定含有Mg2+、Al3+
和NH,且n(NH)=0.7 mol-0.5 mol=0.2 mol,n(H+)=0.1 mol,n(Al3+)=0.8 mol-0.7 mol=0.1
mol,沉淀Al3+、Mg2+共消耗0.4 mol OH-,其中沉淀Al3+消耗0.3 mol OH-,沉淀Mg2+消耗0.1
mol OH-,根据Mg2+~2OH-,可得n(Mg2+)=0.05 mol,故只有选项B正确。
16.答案: (1) 0.4 (2) 0.4 mol、0.8 mol·L-1 (3) 13.44 L
解析: (1)Al的摩尔质量是27 g·mol-1,n(Al)==0.4 mol。
(2)2Al+2NaOH+2HO===2NaAlO+3H↑
2 2 2
2 2
0.4 mol n(NaOH) 则=,n(NaOH)=0.4 mol
c(NaOH)==0.8 mol·L-1。
5
学科网(北京)股份有限公司(3)2Al+2NaOH+2HO===2NaAlO+3H↑
2 2 2
2 mol 3×22.4 L
0.4 mol V(H )
2
V(H )==13.44 L。
2
17.答案:(1) 6.72 L (2) 1.6 mol·L-1 (3) 27.2 mL
解析:(1)设反应产生氢气的物质的量为x,19.5 g锌粒的物质的量为0.3 mol,250 mL 2 mol·L-1的硫酸
溶质的物质的量为0.25 L×2 mol·L-1=0.5 mol;反应如下:
Zn + HSO ===ZnSO +H↑
2 4 4 2
1 1 1
0.3 mol 0.5 mol x
硫酸过量,按锌进行计算,得x=0.3 mol,体积为0.3 mol×22.4 L·mol-1=6.72 L。
(2)硫酸反应了 0.3 mol,剩余 0.5 mol-0.3 mol=0.2 mol,反应后溶液中氢离子浓度==1.6
mol·L-1。(3)质量分数为98%、密度为1.84 g·cm-3浓硫酸的物质的量浓度为 mol·L-1=18.4 mol·L-1。
设需要浓硫酸的体积为V,浓硫酸在稀释前后溶质的量保持不变,0.25 L×2 mol·L-1=18.4 mol·L-
1×V,V≈0.027 2 L=27.2 mL。
18.答案:(1)Mg2++ 2OH−===Mg(OH) ↓ Al3++3OH−===Al(OH) ↓ Al(OH) +OH−===AlO −+2H O
2 3 3 2 2
(2) 2:1 (3)0.8 AlO − (4)7:1
2
解析:(1)氯化镁和氯化铝均可以和氢氧化钠发生反应,生成沉淀氢氧化镁和氢氧化铝,则 OD段发
生反应的离子方程式为Al3++3OH−===Al(OH) ↓、Mg2++2OH−===Mg(OH) ↓;DC段是氢氧化铝与氢
3 2
氧化钠反应生成偏铝酸钠与水,反应离子方程式为Al(OH) ↓+OH−===AlO −+2H O;(2)由图可知,
3 2 2
沉淀量最大为0.3 mol,沉淀量最小为0.2 mol,可知氢氧化镁为0.2 mol,氢氧化铝为0.3 mol−0.2
mol=0.1 mol,根据原子守恒可知Mg2+、Al3+物质的量浓度之比为0.2 mol:0.1mol=2:1;(3)C点是
氢氧化铝恰好被溶解为偏铝酸钠,此时沉淀为氢氧化镁,Al3+已经转化为AlO−,Mg2+已经转化为
2
Mg(OH) ,氢氧化镁为0.2 mol,氢氧化铝为0.3 mol−0.2 mol=0.1 mol,由Al3++3OH−===Al(OH) ↓、
2 3
Mg2++2OH−===Mg(OH) ↓ 可 知 OA 段 消 耗 NaOH 为 0.1 mol×3+0.2 mol×2=0.7 mol , 由
2
Al(OH) +OH−===AlO −+2H O可知AB段消耗NaOH为0.1 mol,故C点加入NaOH为0.7 mol+0.1
3 2 2
mol=0.8 mol; (4)根据③中计算可知OA段、AB段消耗NaOH物质的量之比0.7 mol:0.1 mol=7:
1。
6
学科网(北京)股份有限公司7
学科网(北京)股份有限公司