文档内容
人教版(2019)高一必修第一册 第三章 铁 金属材料 第二
节 金属材料
学校:___________姓名:___________班级:___________考号:___________
一、单选题
1.下列有关叙述正确的是( )
A.铝和铁在常温下遇硫酸或硝酸发生钝化现象
B.金属钠除保存在煤油中,也可以保存在汽油中
C.湿法治炼就是指金属在溶液中的置换反应,如金属钠置换硫酸铜溶液中的铜
D.涂油层、电镀金属层、制合金等都是保护金属的措施
2.下列说法错误的是
A.不锈钢属于合金 B.14C的中子数为8
C.氯气常用于自来水杀菌消毒 D.铝热反应属于吸热反应
3.下列说法不正确的是
A.二氧化氯可用于自来水消毒
B.硬铝是铝合金的一种,是制造飞机和宇宙飞船的理想材料
C.工业上常利用钠与氯气来制氯化钠
D.铜能与氯化铁溶液反应,该反应可用于印刷电路板的制作
4.下列说法错误的是
A.KAl(SO ) ·12H O溶于水可形成 Al(OH) 胶体
4 2 2 3
B.0.1 mol·L-1 NaOH溶液:Na+、K+、CO 、AlO 能大量共存
C.室温下,Al与4.0 mol﹒L-1NaOH溶液反应生成NaAlO
2
D.因为Al O 具有两性,所以可用于电解冶炼铝
2 3
5.将总物质的量为amol的钠和铝的混合物投入到水中,若两者的物质的量之比
n(Na):n(Al)=2:3,则生成的氢气在标准状况下的体积为
A.11.24a L B.36.6a L C.17.92a L D.44.82a L
6.下列关于金属的说法正确的是
A.铝箔在空气中受热可以熔化且会发生剧烈燃挠
B.Na在空气中燃烧,发出黄色火焰,生成白色固体
C.合金的熔点一定低于成分金属,硬度一定大于成分金属
D.铝制餐具不宜用来蒸煮或者长时间存放酸性或碱性食物
7.常温下,3.0molNa、Fe、Al分别与1.0mol盐酸反应,生成最多氢气的是
A.Na B.Fe C.Al D.Na、Fe一样多
8.从金属利用的历史来看,先是青铜器时代,而后是铁器时代,铝的利用是200来年
的事。下列金属的性质和特点跟这个先后顺序有关的是( )
①地壳中的含量 ②活动性顺序 ③导电性 ④冶炼的难易程度 ⑤延展性
A.①③ B.②⑤ C.③⑤ D.②④
9.由CO、H、CO组成的混合气在同温同压下与氮气的密度相同,则该混合气中
2 2
CO、H、CO的体积比是
2 2
A.26:8:1 B.22:1:14 C.13:8:7 D.26:6:17
二、多选题
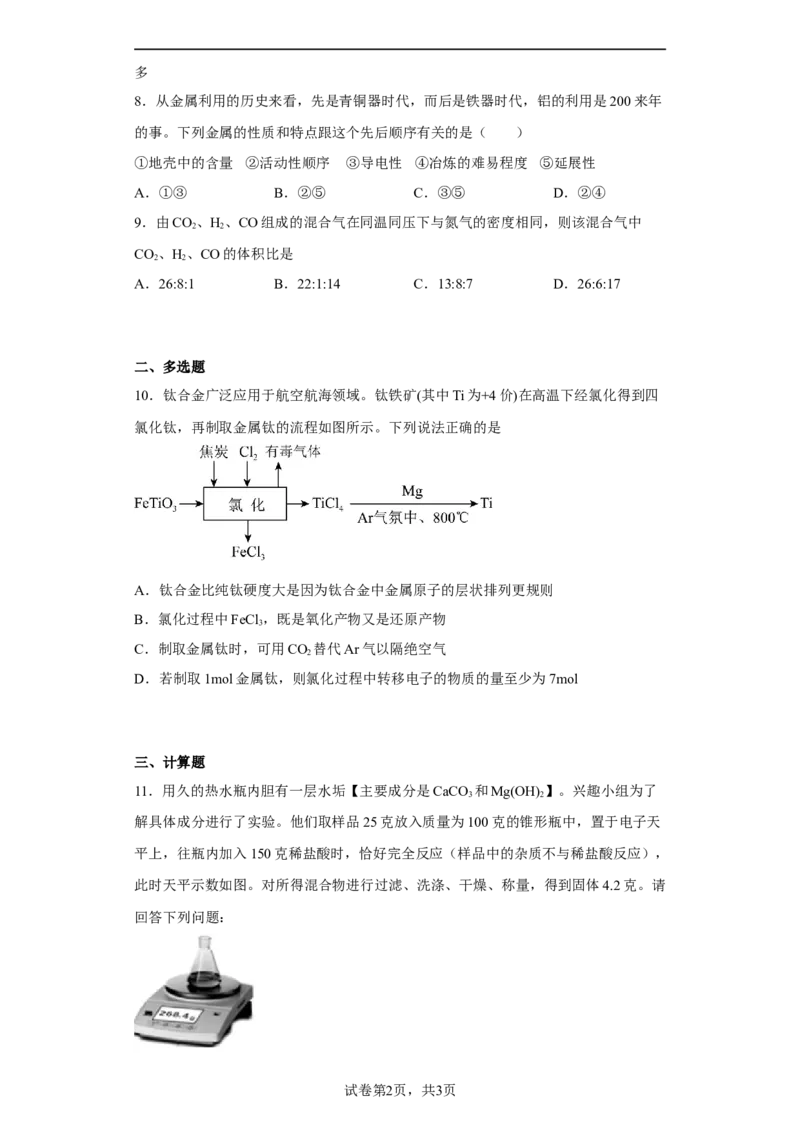
10.钛合金广泛应用于航空航海领域。钛铁矿(其中Ti为+4价)在高温下经氯化得到四
氯化钛,再制取金属钛的流程如图所示。下列说法正确的是
A.钛合金比纯钛硬度大是因为钛合金中金属原子的层状排列更规则
B.氯化过程中FeCl ,既是氧化产物又是还原产物
3
C.制取金属钛时,可用CO 替代Ar气以隔绝空气
2
D.若制取1mol金属钛,则氯化过程中转移电子的物质的量至少为7mol
三、计算题
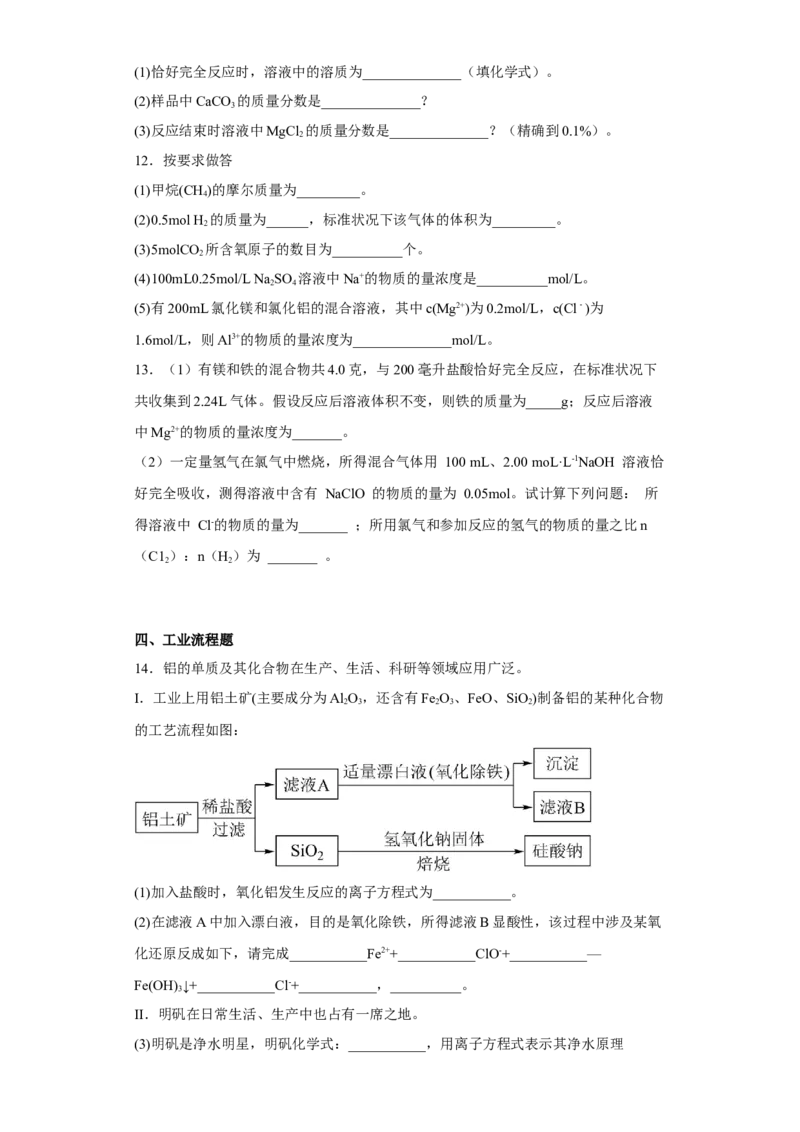
11.用久的热水瓶内胆有一层水垢【主要成分是CaCO 和Mg(OH) 】。兴趣小组为了
3 2
解具体成分进行了实验。他们取样品25克放入质量为100克的锥形瓶中,置于电子天
平上,往瓶内加入150克稀盐酸时,恰好完全反应(样品中的杂质不与稀盐酸反应),
此时天平示数如图。对所得混合物进行过滤、洗涤、干燥、称量,得到固体4.2克。请
回答下列问题:
试卷第2页,共3页(1)恰好完全反应时,溶液中的溶质为______________(填化学式)。
(2)样品中CaCO 的质量分数是______________?
3
(3)反应结束时溶液中MgCl 的质量分数是______________?(精确到0.1%)。
2
12.按要求做答
(1)甲烷(CH)的摩尔质量为_________。
4
(2)0.5mol H 的质量为______,标准状况下该气体的体积为_________。
2
(3)5molCO 所含氧原子的数目为__________个。
2
(4)100mL0.25mol/L Na SO 溶液中Na+的物质的量浓度是__________mol/L。
2 4
(5)有200mL氯化镁和氯化铝的混合溶液,其中c(Mg2+)为0.2mol/L,c(Cl﹣)为
1.6mol/L,则Al3+的物质的量浓度为______________mol/L。
13.(1)有镁和铁的混合物共4.0克,与200毫升盐酸恰好完全反应,在标准状况下
共收集到2.24L气体。假设反应后溶液体积不变,则铁的质量为_____g;反应后溶液
中Mg2+的物质的量浓度为_______。
(2)一定量氢气在氯气中燃烧,所得混合气体用 100 mL、2.00 moL·L-1NaOH 溶液恰
好完全吸收,测得溶液中含有 NaClO 的物质的量为 0.05mol。试计算下列问题: 所
得溶液中 Cl-的物质的量为_______ ;所用氯气和参加反应的氢气的物质的量之比n
(C1 ):n(H)为 _______ 。
2 2
四、工业流程题
14.铝的单质及其化合物在生产、生活、科研等领域应用广泛。
I.工业上用铝土矿(主要成分为Al O,还含有Fe O、FeO、SiO)制备铝的某种化合物
2 3 2 3 2
的工艺流程如图:
(1)加入盐酸时,氧化铝发生反应的离子方程式为___________。
(2)在滤液A中加入漂白液,目的是氧化除铁,所得滤液B显酸性,该过程中涉及某氧
化还原反成如下,请完成___________Fe2++___________ClO-+___________—
Fe(OH) ↓+___________Cl-+___________,__________。
3
II.明矾在日常生活、生产中也占有一席之地。
(3)明矾是净水明星,明矾化学式:___________,用离子方程式表示其净水原理___________。
(4)向0.02 mol的明矾溶液中逐滴加入150 mL0.2 mol/LBa(OH) 溶液生成沉淀的质量为
2
___________克。
15.某铝土矿中主要含有Al O、Al(OH) 还含有Fe O 等杂质。利用拜耳法生产氧化铝
2 3 3 2 3
的流程如图所示:
请回答下列问题:
(1)粉碎后的铝土矿碱浸时应在较高温度下进行,其目的是_______。滤渣1的主要成分
为_______。
(2)AlO 与NaOH溶液反应的离子方程式为_______。
2 3
(3)加Al(OH) 晶核的目的是促进Al(OH) 的析出。上述“稀释、结晶”工艺,也可用通
3 3
入足量的CO 气体的方法来代替,通入足量CO 气体的化学方程式为_______。(已知:
2 2
通入该气体后,其产物之一可用来做发酵粉)。
(4)焙烧过程中发生的化学方程式为_______。
(5)浓缩所得的NaOH溶液由于吸收了空气中的CO 而含有杂质,该杂质可通过苛化(即
2
与少量熟石灰反应)反应除去,写出苛化反应的化学方程式:_______。
(6)该生产流程能实现_______(填化学式)的循环利用。
试卷第4页,共3页参考答案:
1.D
【详解】试题分析:铝和铁在常温下遇浓硫酸或浓硝酸发生钝化现象,A不正确;汽油中
的烃的C原子数比煤油中的少,所以汽油的熔沸点比煤油低,即挥发性比煤油强,易挥发,
所以不用于保存Na,B不正确;钠是活泼的金属,极易和水反应,所以钠一旦投入到水中,
立即和水反应生成氢氧化钠和氢气,然后生成的氢氧化钠再和盐反应,C不正确,答案选
D。
考点:考查钝化、钠的保存、金属的冶炼以及金属的腐蚀与防护
点评:该题是高考中的常见题型和考点,属于基础性试题的考查。该题考查的知识点比较
分散,但很基础,难度不大,主要是对学生基础性知识的巩固训练,学生记住即可。
2.D
【详解】A.不锈钢是Fe、Cr、Ni、Ti、Mn、N、Nb、Mo、Si、Cu等的合金,A正确;
B.14C的质子数为6,质量数为14,中子数为14-6=8,B正确;
C.氯气与水反应产生的HClO有强氧化性,可用于消毒杀菌,因此氯气常用于自来水杀菌
消毒,C正确;
D.铝热反应放出大量的热,属于放热反应,D错误;
答案选D。
3.C
【详解】A.二氧化氯具有强氧化性,可用于自来水消毒,A正确;
B.硬铝的密度小、强度高、具有较强的抗腐蚀能力,是制造飞机和宇宙、飞船的理想材
料,B正确;
C.工业上利用海水晒盐制氯化钠,C不正确;
D.印刷电路板的制作的原理是:Cu+2FeCl =CuCl +2FeCl ,D正确;
3 2 2
故选C。
4.D
【详解】A.KAl(SO )·12H O溶于水电离出的Al3+会发生水解形成Al(OH) 胶体,故A正
4 2 2 3
确;
B.碱性溶液中,Na+、K+、CO 、AlO 之间不会发生反应,且与OH-不会反应,因此能
够大量共存,故B正确;
C.室温下,铝与NaOH溶液反应生成偏铝酸钠和氢气,故C正确;
D.Al O 和酸、碱都反应可以体现 Al O 具有两性,电解冶炼铝,只能说明熔融氧化铝能
2 3 2 3导电,二者没有必然联系,故D 错误;
综上所述,说法错误的是D项,故答案为:D。
5.C
【详解】钠和铝的混合物的总物质的量为amol,且n(Na):n(Al)= 2:3,则n(Na)= mol,
n(Al)= ,根据钠和水的反应列出关系式2Na~2HO~2OH-~H 可知,n(OH-)=n(Na)=
2 2
mol,生气氢气n(H )= n(Na)= mol;根据铝和氢氧化钠的反应列出关系式2Al~
2
2OH-~3H 可知,氢氧根不足,所以n(H )= n(OH-)= mol,共生成氢气 mol+
2 2
mol=0.8amol,准状况下的体积为0.8amol×22.4L/mol=17.92a L,故选C。
6.D
【详解】A.铝和氧气反应生成氧化铝,因氧化铝的熔点高于铝的熔点,而氧化铝在铝的
表面,所以加热铝箔的时候不会剧烈燃烧,故A错误;
B.钠在空气中燃烧,火焰为黄色,生成过氧化钠固体,固体为淡黄色,故B错误;
C.多数合金硬度大于组成它的成分金属;多数合金的熔点低于组成它的成分金属的熔点,
故C错误;
D.铝制餐具表面的氧化铝是两性氧化物,易与强酸、强碱反应,表面腐蚀后金属铝会继
续和酸、强碱反应,所以不宜用来盛装酸性、碱性较强的食物,故D正确;
答案选D。
7.A
【详解】根据2Na + 2HCl = 2NaCl + H ↑,反应后钠剩余,剩余的钠继续与水反应,2Na +
2
2HO=2NaOH + H ↑,则3.0molNa与1.0mol盐酸反应,生成1.5mol氢气;根据Fe + 2HCl =
2 2
FeCl + H ↑,3.0molFe与1.0mol盐酸反应后铁有剩余,放出0.5mol氢气;根据2Al + 6
2 2
HCl 2 AlCl + 3H ↑,反应后,铝剩余,放出0.5mol氢气;因此生成氢气最多的是钠,故
3 2
选A。
【点睛】本题的易错点为A,要注意钠除了与盐酸反应,还能与水反应,两个反应过程中
都能放出氢气。
8.D
【分析】金属的活泼性越强,金属越容易被氧化,越不稳定,在自然界中越容易以化合态
答案第2页,共2页存在,金属的冶炼越难,据此分析解答。
【详解】铜、铁、铝三种金属活动性由强到弱的顺序为:铝>铁>铜,金属的活泼性越强,
金属越容易被氧化、越不稳定,在自然界中越容易以化合态存在,金属的冶炼越难,所以
金属的使用早晚与金属的活动性强弱、金属的冶炼难易程度有关,序号为②④,故合理选
项是D。
【点睛】本题考查了金属活泼性与使用早晚的关系,明确金属活泼性与金属冶炼难易之间
的关系是解题关键。
9.C
【分析】根据CO、H 和CO碳组成的混合气体在同温、同压下与氮气的密度相同,可知
2 2
混合气体的平均相对分子质量等于氮气的相对分子质量,即为28,而CO的相对分子质量
也为28,则二氧化碳与氢气的平均相对分子质量必须为28,据此进行解答。
【详解】CO、H 和CO组成的混合气体在同温、同压下与N 的密度相同,则混合气体的
2 2 2
平均相对分子质量等于氮气的相对分子质量,即为28,由于CO的相对分子质量为28,则
CO 和H 的平均相对分子质量为28即可,CO的体积不受限制,利用十字相乘法得二氧化
2 2
碳和氢气的体积之比: ,则CO 和H 的体积之比为26:16=13:8,CO的体
2 2
积为任意体积,所以只有选项C符合条件,答案选C。
【点睛】本题考查混合气体的计算,难度不大,明确相同条件下气体的密度之比等于相对
分子质量之比计算即可,试题侧重于学生的分析能力和计算能力的考查,注意把握十字交
叉法的运用。
10.BD
【分析】根据得失电子守恒知,氯化过程中发生反应的化学方程式为2FeTiO + 6C+ 7Cl
3 2
2FeCl + 6CO+ 2TiCl ,制取金属钛的化学方程式为:Mg+ TiCl Ti+MgCl ,
3 4 4 2
以此来解析。
【详解】A.合金内加入了其他元素或大或小的原子,改变了金属原子有规则的层状排列,
使原子层之间的相对滑动变得困难,A错误;B.根据得失电子守恒知,氯化过程中发生反应的化学方程式为2FeTiO + 6C+ 7Cl
3 2
2FeCl + 6CO+ 2TiCl ,Fe化合价由+2升高为+3,而Cl的化合价由0价降低为-1价,
3 4
FeCl ,既是氧化产物又是还原产物,B正确;
3
C.制取金属钛时,选用氩气的目的是隔绝空气,防止Ti、Mg与空气中的成分发生,而镁
与二氧化碳反应,不能用CO 替代Ar气以隔绝空气,C错误;
2
D.根据氯化过程中发生反应2FeTiO + 6C+ 7Cl 2FeCl + 6CO+ 2TiCl 和根据化合价
3 2 3 4
升降守恒和原子守恒,可知TiCl ~7mole-~Ti,可知若制取1mol金属钛,氯化过程中转移
4
电子的物质的量至少为7mol,D正确;
故选BD。
11. CaCl 和MgCl 60% 5.8%
2 2
【分析】根据质量守恒定律可知,过程中质量的减少是因为生成了二氧化碳,所以可以求
算二氧化碳的质量,根据二氧化碳的质量和对应的化学方程式求算碳酸钙的质量,进而确
定氢氧化镁的质量,然后结合对应的化学方程式求算氯化镁质量,进而求算其质量分数。
【详解】(1)恰好完全反应时,碳酸钙转化为氯化钙,氢氧化镁转化为氯化镁,所以对应的溶质
的化学式为CaCl 和MgCl ;
2 2
(2)根据质量守恒定律可得,生成的二氧化碳的质量为25g+100g+150g−268.4g=6.6g,设碳
酸钙的质量为x,
列关系式: = ,解得:x=15g,样品中CaCO 的质量分数为 ×100%=60%;
3
(3)样品中氢氧化镁的质量为25g−15g−4.2g=5.8g,设生成的氯化镁的质量为y,
列关系式: = ,解得:y=9.5g,反应结束时溶液中MgCl 的质量分数为
2
答案第4页,共2页×100%=5.8%。
12. 16 g/mol 1 g 11.2 L 10N (或6.02×1024) 0.5 0.4
A
【详解】(1) 摩尔质量以g/mol为单位,数值上等于相对分子质量,所以甲烷(CH)的摩尔
4
质量为16 g/mol。答案:16 g/mol。
(2)根据m=n M=0.5mol 2 g/mol =1g,所以0.5molH 的质量为1g,标准状况下该气体的体
2
积为V=nVm=0.5mol L/mol=11.2 L。答案:1 g 、11.2 L。
(3)根据N=nN =5mol 2 6.02×1023mol-1=6.02×1024,5molCO 所含氧原子的数目为10N 或
A 2 A
6.02×1024。答案:10N 或6.02×1024。
A
(4)根据NaSO 2 Na+,所以0.25mol/L Na SO 溶液中Na+的物质的量浓度是0.5mol/L 。答
2 4 2 4
案:0.5。
(5)设Al3+的物质的量浓度为x mol/L,根据电荷守恒有c(Mg2+) 2+c(Al3+) 3= c(Cl﹣),即为:
0.2 2+3xmol/L=1.6mol/L ,x=0.4 ,所以Al3+的物质的量浓度为0×.4mol/L。答案:
0.4
【点睛】本题考查摩尔质量、物质的量、气体摩尔体积等知识。以物质的量为中心进行的
有关计算。根据公式:m/M=n=V/Vm N/N =n=cV进行相关计算即可。
A
13. 2.8 0.25mol· L-1 0.15 mol 2:1
【详解】试题分析:本题考查混合物的计算,涉及Mg、Fe与酸的反应,Cl 与H、NaOH
2 2
的反应。
(1)根据反应的化学方程式:Mg+2HCl=MgCl +H ↑、Fe+2HCl=FeCl +H ↑可列式:n
2 2 2 2
(Mg)+n(Fe)= ,24g/moln(Mg)+56g/moln(Fe)=4.0g,解得n(Mg)
=0.05mol,n(Fe)=0.05mol;则铁的质量m(Fe)=0.05mol 56g/mol=2.8g;根据Mg守恒,
n(Mg2+)=n(Mg)=0.05mol,c(Mg2+)= =0.25mol/L。
(2)H 在Cl 中燃烧生成HCl,HCl与NaOH溶液的反应为:HCl+NaOH=NaCl+H O;用
2 2 2
NaOH溶液吸收后所得溶液中含NaClO,说明H 在Cl 中燃烧后Cl 过量,过量Cl 与
2 2 2 2
NaOH溶液发生的反应为:Cl+2NaOH=NaCl+NaClO+H O。根据Na和Cl守恒,反应后溶
2 2
液中n(NaCl)+n(NaClO)=n(NaOH)=2mol/L 0.1L=0.2mol,n(NaClO)=0.05mol,
则n(NaCl)=0.2mol-0.05mol=0.15mol,所得溶液中Cl-物质的量为0.15mol。根据Cl守恒,所用Cl 物质的量为(0.15mol+0.05mol) 2=0.1mol;生成0.05molNaClO的同时生成
2
0.05molNaCl,则由HCl与NaOH反应生成的NaCl为0.15mol-0.05mol=0.1mol,HCl物质的
量为0.1mol,根据反应H+Cl 2HCl,参加反应的H 物质的量为0.05mol,所用Cl 与参
2 2 2 2
加反应的H 物质的量之比n(Cl):n(H)=0.1mol:0.05mol=2:1。
2 2 2
14. Al O+6H+=2Al3++3H O 2Fe2++C1O-+5H O=2Fe(OH) ↓+C1-+4H+
2 3 2 2 3
KAl (SO )·12H O A13++3H O Al(OH) (胶体)+3H+ 8.55
4 2 2 2 3
【分析】I.铝土矿(主要成分为Al O,还含有Fe O、FeO、SiO )加入盐酸,过滤得SiO
2 3 2 3 2 2
沉淀, 滤液A为到氯化铝、氯化铁、氯化亚铁混合溶液,向滤液中加入适量的漂白粉氧
化除铁,得沉淀为氢氧化铁,滤液B为氯化铝溶液;SiO 与NaOH混合加热发生反应产生
2
硅酸钠和水;
II.明矾化学式是KAl (SO )·12H O,该物质为强酸弱碱盐,可水解生成具有吸附性的氢氧
4 2 2
化铝胶体,可用于净水;将明矾与Ba(OH) 混合,根据各种离子的物质的量关系计算沉淀
2
的质量。
【详解】I.(1) 铝土矿中含有的金属氧化物能够与酸发生反应,变为可溶性盐进入溶液,
其中Al O 与HCl反应产生AlCl 、HO,反应的离子方程式为:Al O+6H+=2Al3++3H O;
2 3 3 2 2 3 2
(2)向滤液A中加入漂白液,溶液中的Fe2+被氧化为Fe3+,并Fe3+在溶液中形成Fe(OH) 沉淀,
3
ClO-被还原为Cl-,根据电子守恒、电荷守恒、原子守恒,可得该反应的离子方程式为:
2Fe2++C1O-+5H O=2Fe(OH) ↓+C1-+4H+;
2 3
II.(3)明矾化学式是KAl (SO )·12H O,该物质是强酸弱碱盐,Al3+发生水解反应生成具有
4 2 2
吸附性的氢氧化铝胶体,吸附水中悬浮的固体小颗粒,使之形成沉淀,因而明矾可用于净
水,水解反应的离子方程式为:A13++3H O Al(OH) (胶体)+3H+;
2 3
(4)0.02 mol的明矾会电离产生0.02 mol Al3+、0.04 mol ,向其中加入150 mL0.2
mol/LBa(OH) 溶液,n[Ba(OH) ]=0.2 mol/L×0.15 L=0.03 mol,则n(Ba2+)=n[Ba(OH) ]=0.03
2 2 2
mol,n(OH-)=2n[Ba(OH) ]=0.06 mol,n(Al3+):n(OH-)=1:3,二者恰好反应产生Al(OH) 沉
2 3
淀,n[Al(OH) ]=n(Al3+)=0.02 mol,m[Al(OH) ]=0.02 mol×78 g/mol=1.56 g;n(Ba2+)=0.03 mol
3 3
<n( )=0.04 mol,则反应产生0.03 mol BaSO 沉淀,m(BaSO)=0.03 mol×233 g/mol=6.99
4 4
答案第6页,共2页g,故生成沉淀的质量为m(总)=m[Al(OH) ]+m(BaSO)=1.56 g+6.99 g=8.55 g。
3 4
15.(1) 加快反应速率 Fe O
2 3
(2)AlO+2OH-=2 +H O
2 3 2
(3)NaAlO +CO +2H O= NaHCO+Al(OH) ↓
2 2 2 3 3
(4)2Al(OH) Al O+3H O
3 2 3 2
(5)Ca(OH) +Na CO=CaCO ↓+2NaOH
2 2 3 3
(6)NaOH
【分析】利用铝土矿制取Al O,并循环利用NaOH。先将铝土矿溶于NaOH溶液中,
2 3
Fe O 不溶而成为滤渣;往滤液中加入水和Al(OH) 晶核,此时生成Al(OH) 沉淀,焙烧可
2 3 3 3
制得Al O。浓缩滤液并加入少量熟石灰,可生成CaCO 沉淀和NaOH溶液。
2 3 3
(1)
碱浸时,为加快浸取速率,应在较高温度下进行,其目的是:加快反应速率。由分析可知,
滤渣1的主要成分为Fe O。答案为:加快反应速率;Fe O;
2 3 2 3
(2)
Al O 与NaOH溶液反应,生成偏铝酸钠和水,离子方程式为Al O+2OH-=2 +H O。答
2 3 2 3 2
案为:Al O+2OH-=2 +H O;
2 3 2
(3)
偏铝酸钠溶液中通入足量CO 气体,生成氢氧化铝沉淀和碳酸氢钠,化学方程式为
2
NaAlO +CO +2H O= NaHCO+Al(OH) ↓。答案为:NaAlO +CO +2H O=
2 2 2 3 3 2 2 2
NaHCO +Al(OH) ↓;
3 3
(4)
焙烧过程中,氢氧化铝分解生成氧化铝等,化学方程式为2Al(OH) Al O+3H O。答案为:
3 2 3 2
2Al(OH) Al O+3H O;
3 2 3 2(5)
苛化时,碳酸钠与氢氧化钙发生复分解反应,反应的化学方程式:Ca(OH)
2
+Na CO=CaCO ↓+2NaOH。答案为:Ca(OH) +Na CO=CaCO ↓+2NaOH;
2 3 3 2 2 3 3
(6)
由分析可知,该生产流程能实现NaOH的循环利用。答案为:NaOH。
【点睛】偏铝酸钠溶液中通入足量二氧化碳,起初生成的碳酸钠能与二氧化碳在水溶液中
继续反应生成碳酸氢钠。
答案第8页,共2页