文档内容
2024 年高一第二学期期末学业质量检测卷(2)
化 学
时长:75分钟 总分:100分
一、单选题(每题3分,共45分)
1. 下列物质中属于高分子化合物的是( )
①蛋白质 ②植物油 ③纤维素 ④淀粉 ⑤葡萄糖⑥脂肪 ⑦氨基酸
A. ①②⑥ B. ②⑥⑦ C. ①③④ D. ⑤⑥⑦
【答案】C
【解析】
【分析】高分子化合物是指那些由众多原子或原子团主要以共价键结合而成的相对分子量在一万以上的化
合物。由千百个原子彼此以共价键结合形成相对分子质量特别大、具有重复结构单元的化合物。
【详解】淀粉、蛋白质、纤维素都是高分子化合物,植物油、脂肪、氨基酸、葡萄糖均不是高分子化合物,
①③④项正确,C项正确,
故答案选C。
2. 下列属于油脂的用途的是
①人类的营养物质 ②制取肥皂 ③制取甘油 ④制备高级脂肪酸 ⑤制备汽油
A. ①②③⑤ B. ②③④⑤ C. ①③④⑤ D. ①②③④
【答案】D
【解析】
【详解】油脂是人类的基本营养物质,可以通过酸性或碱性水解制取肥皂、甘油和高级脂肪酸;汽油属于
烃类物质,不能由油脂来制取;
答案选D。
3. 下列说法正确的是
A. 食用白糖的主要成分是蔗糖 B. 小苏打的主要成分是碳酸钠
C. 煤气的主要成分是丁烷 D. 植物油的主要成分是高级脂肪酸
【答案】A
【解析】
【详解】A、白糖的主要成分是蔗糖,A正确;
B、小苏打是指碳酸氢钠,B错误;
C、煤气主要成分是CO、H,C错误;
2
D、植物油主要是高级脂肪酸甘油酯,D错误;
第1页/共13页
学科网(北京)股份有限公司答案选A。
4. 下列说法中错误的是
A. 化学反应中的能量变化通常表现为热量的变化
B. 化学键的断裂和形成是化学反应中能量变化的主要原因
C. 需要加热才能发生的反应一定是吸热反应
D. 如果一个反应是放热反应,说明反应物总能量大于生成物总能量
【答案】C
【解析】
【分析】
【详解】A.由于化学反应的本质是旧键断裂新键形成的过程,断键要吸热,形成化学键要放热,这样必
然伴随整个化学反应吸热或放热,所以化学反应中的能量变化通常表现为热量的变化,故A正确;
B.断键要吸热,形成化学键要放热,是反应中能量变化的主要原因,故B正确;
C.一个化学反应是放热还是吸热主要取决于反应物的总能量与生成物总能量的相对大小,与外界条件没
有关系,故C错误;
D.反应物总能量和生成物总能量的相对大小决定了反应是放出能量还是吸收能量,反应物总能量大于生
成物总能量,说明该反应是放热反应,故D正确。
故选C。
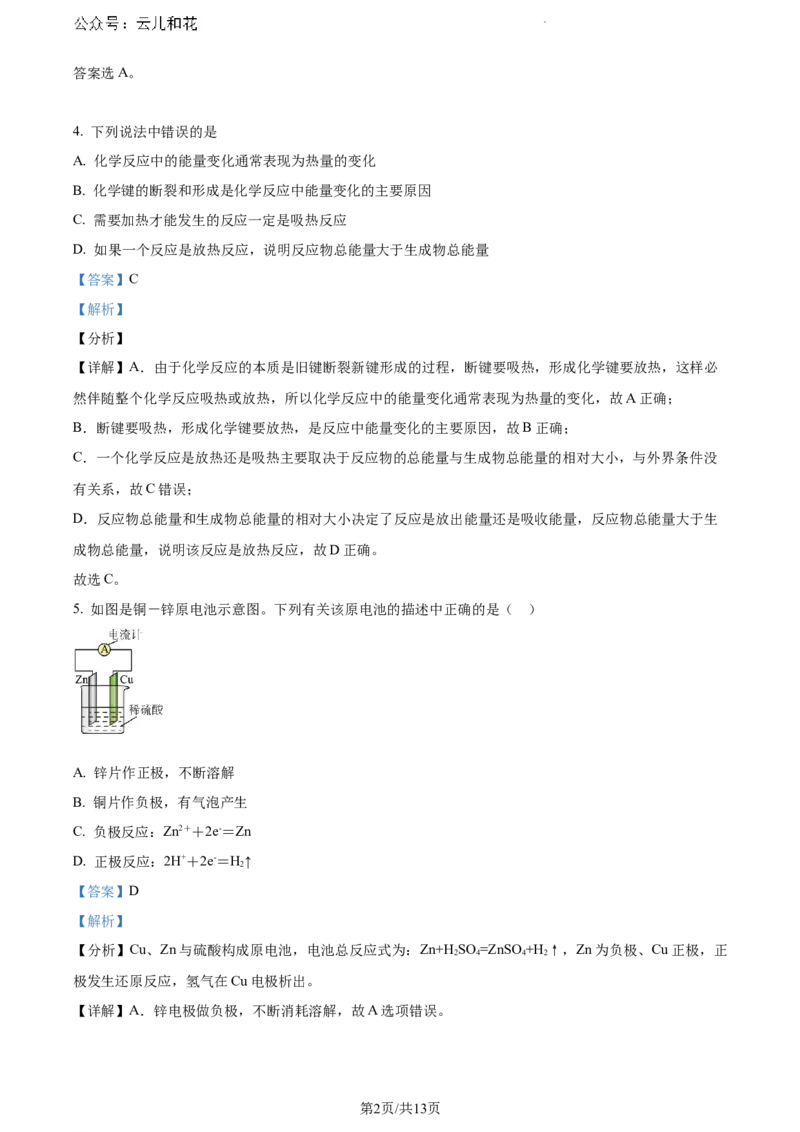
5. 如图是铜-锌原电池示意图。下列有关该原电池的描述中正确的是( )
A. 锌片作正极,不断溶解
B. 铜片作负极,有气泡产生
C. 负极反应:Zn2++2e-=Zn
D. 正极反应:2H++2e-=H↑
2
【答案】D
【解析】
【分析】Cu、Zn与硫酸构成原电池,电池总反应式为:Zn+H SO =ZnSO +H ↑,Zn为负极、Cu正极,正
2 4 4 2
极发生还原反应,氢气在Cu电极析出。
【详解】A.锌电极做负极,不断消耗溶解,故A选项错误。
第2页/共13页
学科网(北京)股份有限公司B.铜电极为正极,发生还原反应,氢气在Cu电极析出,故B选项错误。
C.负极发生的反应是锌做负极失电子发生氧化反应生成锌离子,Zn-2e-=Zn2+,故C选项错误。
D.铜电极为正极,发生还原反应有氢气产生,发生反应2H++2e-=H↑,故D选项正确。
2
故答案选D。
6. 一定条件下,在2 L密闭容器中发生反应:2A(s)+3 B(g)=2 C(g)+4 D(g),测得5 min内,A的物质的量减
小了10 mol, 则0~5 min内该反应的平均速率为
A. v(A)=1.0 mol/(L·min) B. v(B)=1.5 mol/(L·min )
C. v(C)=2.0 mol/( L·min) D. v(D)=0.5 mol/(L·min)
【答案】B
【解析】
【分析】根据反应方程式中各物质反应的量关系,变化量之比等于系数之比,推出速率之比等于各物质的
系数之比。
【详解】A.A是固体不能表示速率,故A不正确;
B.根据A的物质量减少了10mol,B的物质的量减少了则是15mol,根据变化量之比等于系数比,则
=1.5mol/(L·min ),故B正确;
C.根据A的物质量减少了10mol,C的物质的量增加了则是10mol,根据变化量之比等于系数比,
= 1.0 mol/(L·min),故C不正确;
D.根据A的物质量减少了10mol,D的物质的量增加了则是20mol,根据变化量之比等于系数比,
= 2.0 mol/(L·min),故D不正确;
故选答案B。
【点睛】根据速率之比等于化学反应方程式的计量数之比的实质进行分析,注意对于固体和纯液体不能表
示其速率。
7. 下列对物质用途描述不正确的是
A. SO 可用于漂白纸张 B. 浓硫酸可用作干燥剂
2
C. NH NO 可用作氮肥 D. NaO用于呼吸面具供氧
4 3 2
【答案】D
第3页/共13页
学科网(北京)股份有限公司【解析】
【分析】
【详解】A.SO 具有漂白性,能够与某些有色物质结合产生无色物质,因此可用于漂白纸张,A正确;
2
B.浓硫酸具有吸水性,因此可用作干燥剂,B正确;
C.NH NO 是可溶性盐,含有农作物生长需要的氮元素,因此可用作氮肥,C正确;
4 3
D.NaO与CO 或HO都不能反应产生氧气,因此不用于呼吸面具供氧,D错误;
2 2 2
故合理选项是D。
8. 关于氯化铵的叙述中,错误的是
A. 能与碱反应 B. 是离子化合物
C. 固体受热分解可制氨气 D. 固体溶于水吸热
【答案】C
【解析】
【详解】A、氯化铵能跟碱反应生成氨气或一水合氨,故A正确;
B、氯化铵是由铵根离子和氯离子构成的离子化合物,故B正确;
C、氯化铵受热分解生成氨气和氯化氢,氨气和氯化氢又会重新化合生成氯化铵,不能用于制氨气,故C
错误;
D、氯化铵为可溶性盐,易溶于水,溶于水时吸热,故D正确;
综上所述,本题选C。
【点睛】铵盐受热都能分解,但不是都能生成氨气,如果组成铵盐的酸是挥发性的,则固体铵盐受热分解
产生的氨气与酸一起挥发,冷却时又重新结合成铵盐,如氯化铵;硝酸铵比较复杂,加热到190℃时分解
生成一氧化二氮和水,若加热到300℃时分解生成氮气、硝酸和水。
9. 下列说法正确的有
①浓硫酸有强氧化性,所以浓硫酸不可以用于干燥具有还原性的气体SO
2
②氯气能与铁反应,所以液氯不宜存放在钢瓶中
③浓盐酸、浓硫酸两溶液敞口放置一段时间,浓度会下降的原因不同
④浓硫酸具有吸水性,因而能使蔗糖炭化
⑤pH小于7的雨水通常称为酸雨
⑥SO 的漂白原理与Ca(ClO) 溶液、HO 和氯水的漂白原理不同
2 2 2 2
A. ②⑥ B. ③⑥ C. ①④⑥ D. ②④⑤
【答案】B
【解析】
【详解】①浓硫酸有吸水性,且与SO 不反应,故①错误;
2
②铁与干燥的氯气不反应,则液氯可存放在钢瓶中,故②错误;
第4页/共13页
学科网(北京)股份有限公司③浓盐酸、浓硫酸两溶液敞口放置一段时间,浓盐酸会挥发,浓硫酸会吸水,浓度下降的原因不相同,故
③正确;
④浓硫酸具脱水性,因而能使蔗糖炭化,故④错误;
⑤pH小于5.6的雨水是酸雨,故⑤错误;
⑥Ca(ClO) 溶液、HO 和氯水都有强氧化性而能漂白,SO 可与有色物质结合生成无色物质而漂白,漂白
2 2 2 2
原理不同,故⑥正确;
答案选B。
10. 单质能发生如下图转化关系的元素是
A. 氯 B. 硫 C. 铝 D. 铁
【答案】B
【解析】
【详解】A.一般条件下,氯气和氧气不反应,故A错误;
B.硫和氧气反应生成二氧化硫,二氧化硫和水反应生成亚硫酸,亚硫酸可以与碱反应生成盐,故B正确;
C.铝和氧气反应生成氧化铝,氧化铝和水不反应,故C错误;
D.铁和氧气反应生成氧化铁或四氧化三铁,与水都不反应,故D 错误。答案选B。
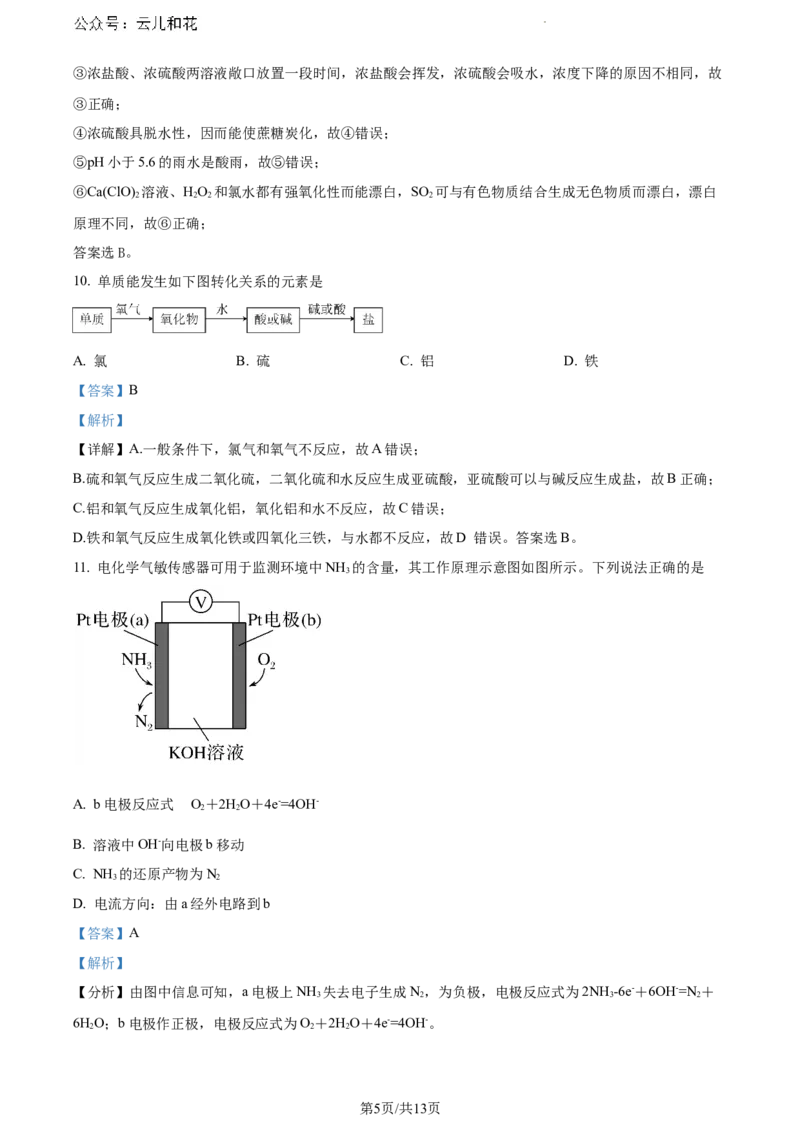
11. 电化学气敏传感器可用于监测环境中NH 的含量,其工作原理示意图如图所示。下列说法正确的是
3
为
A. b电极反应式 O+2HO+4e-=4OH-
2 2
B. 溶液中OH-向电极b移动
C. NH 的还原产物为N
3 2
D. 电流方向:由a经外电路到b
【答案】A
【解析】
【分析】由图中信息可知,a电极上NH 失去电子生成N,为负极,电极反应式为2NH -6e-+6OH-=N +
3 2 3 2
6HO;b电极作正极,电极反应式为O+2HO+4e-=4OH-。
2 2 2
第5页/共13页
学科网(北京)股份有限公司【详解】A.有以上分析可知:b电极反应式为O+2HO+4e-=4OH-,故A正确;
2 2
B.OH-由b极移向a极,故B错误;
C.N 为氧化产物,故C错误;
2
D.电流由b经外电路到a,故D错误;
故选A。
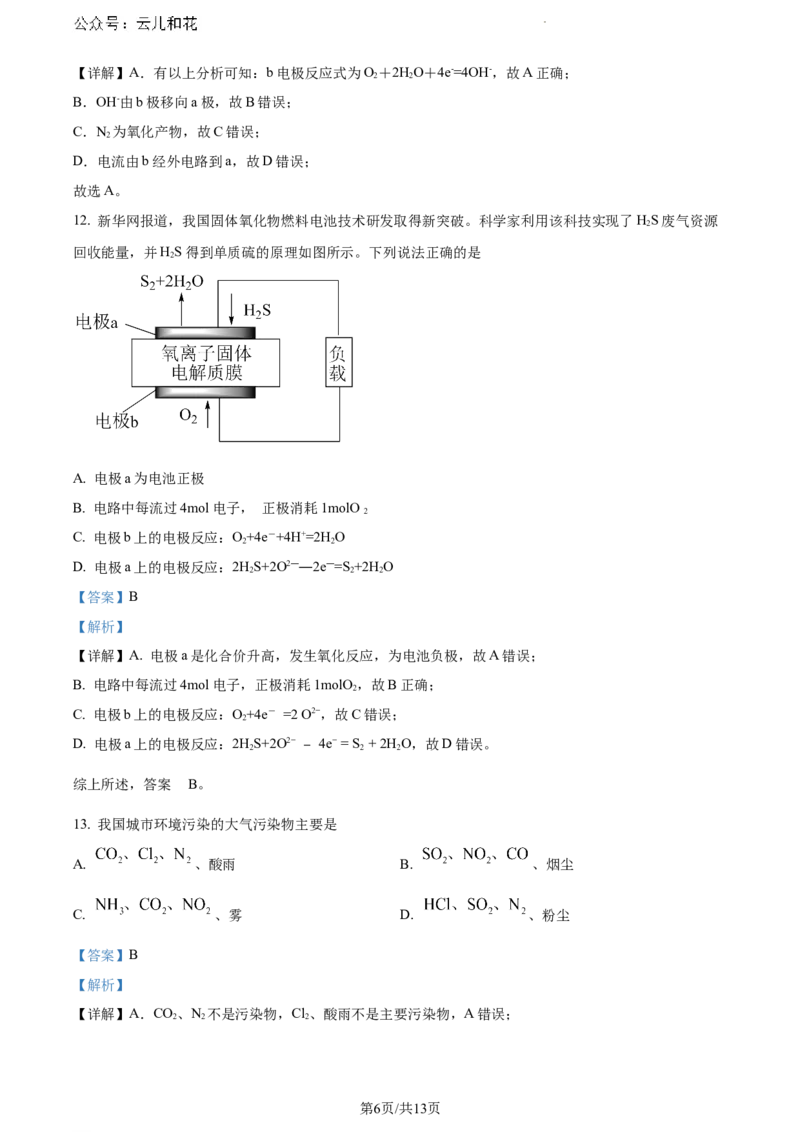
12. 新华网报道,我国固体氧化物燃料电池技术研发取得新突破。科学家利用该科技实现了HS废气资源
2
回收能量,并HS得到单质硫的原理如图所示。下列说法正确的是
2
A. 电极a为电池正极
B. 电路中每流过4mol电子, 正极消耗1molO
2
C. 电极b上的电极反应:O+4e-+4H+=2H O
2 2
D. 电极a上的电极反应:2HS+2O2――2e―=S +2H O
2 2 2
【答案】B
【解析】
【详解】A. 电极a是化合价升高,发生氧化反应,为电池负极,故A错误;
B. 电路中每流过4mol电子,正极消耗1molO ,故B正确;
2
C. 电极b上的电极反应:O+4e- =2 O2−,故C错误;
2
D. 电极a上的电极反应:2HS+2O2− − 4e− = S + 2H O,故D错误。
2 2 2
为
综上所述,答案 B。
13. 我国城市环境污染的大气污染物主要是
A. 、酸雨 B. 、烟尘
C. 、雾 D. 、粉尘
【答案】B
【解析】
【详解】A.CO、N 不是污染物,Cl、酸雨不是主要污染物,A错误;
2 2 2
第6页/共13页
学科网(北京)股份有限公司B.SO 、NO 、CO都是有害气体,烟尘属于可吸入颗粒物为主要污染物,均为大气污染物,B正确;
2 2
C.CO、雾不是污染物,NH 不是主要污染物,C错误;
2 3
D.HCl不是主要污染物,N 不是污染物,SO 、粉尘是主要污染物,D错误;
2 2
故选B。
14. 下列关于硅及其化合的物说法错误的是
A. SiO 能与HF反应,也能与NaOH溶液反应,故SiO 是两性氧化物
2 2
B. 利用焦炭制备粗硅的化学方程式为:SiO+2C Si+2CO↑
2
C. 高温结构陶瓷属于新型陶瓷
D. 硅胶多孔,吸附水分能力强,常用作实验室和袋装食品的干燥剂
【答案】A
【解析】
【详解】A.二氧化硅与氢氟酸反应生成四氟化硅气体和水,没有盐生成,二氧化硅与氢氧化钠反应生成
盐和水,所以二氧化硅属于酸性氧化物,故A错误;
B.碳具有还原性,能够与二氧化硅反应生成粗硅和一氧化碳,方程式书写正确,故B正确;
C.高温结构陶瓷属于新型无机非金属材料,也属于新型陶瓷,故C正确;
D.硅胶多孔,吸收水分能力强,常用作实验室和袋装食品的干燥剂,故D正确;
故选A。
15. 下列溶液中,不能区别SO 和CO 气体的是
2 2
①石灰水②HS溶液③KMnO 溶液④溴水⑤酸化的Ba(NO ) 溶液⑥品红溶液
2 4 3 2
A. ①②③④ B. ②③④⑤ C. 只有① D. ①③
【答案】C
【解析】
【分析】SO 和CO 都是酸性氧化物,都具备酸性氧化物的通性。但SO 中的硫元素的化合价为+4价,处于
2 2 2
中间价态,既能升高,也能降低,因此SO 不仅具有还原性还具有氧化性。同时SO 还具有一定的漂泊性。
2 2
【详解】SO 和CO 都是酸性氧化物,都具备酸性氧化物的通性,都能使澄清石灰水变浑浊。但 SO 还具有
2 2 2
还原性,所以SO 能使酸性高锰酸钾溶液褪色,使溴水褪色,在酸性溶液中能被硝酸钡氧化生成硫酸钡沉
2
淀。另外SO 还具有氧化性,能和硫化氢反应生成单质硫沉淀,所以只有①不能鉴别二者,答案选C。
2
二、多选题(共55分)
16. 大豆含有大量的蛋白质和脂肪,由大豆配制出来的菜肴很多,它是人体营养中最重要的补品之一,我
们几乎每天都要饮食豆制品。请回答下列问题:
(1)我们所吃的豆腐是一种___________(填字母,下同)。
第7页/共13页
学科网(北京)股份有限公司A. 蛋白质凝胶 B. 纯蛋白质 C. 脂肪 D. 淀粉
(2)我们食用的大豆,最终补充给人体的主要成分是___________。
A. 氨基酸 B. 蛋白质 C. 油脂 D. 糖类
(3)蛋白质水解的最终产物是___________,请以甘氨酸(CHNH COOH)为例,写出其与NaOH反应的化
2 2
学方程式:___________。
(4)豆油不能保存较长时间的原因主要是___________,所以必须进行硬化,油脂的硬化是指
___________,人造脂肪指的是___________。
【答案】(1)A (2)A
(3) ①. α− 氨基酸 ②. CHNH COOH+NaOH=CH NH COONa+H O
2 2 2 2 2
(4) ①. 分子中含有碳碳双键,易被空气中的 O 氧化 ②. 对易氧化的不饱和脂肪酸甘油酯进行
2
催化加氢 ③. 经氢化后的饱和高级脂肪酸的甘油酯
【解析】
【小问1详解】
在豆浆中加入少量 的石膏,能使豆浆凝结成豆腐,所以豆腐是一种蛋白质凝胶,它在人体内最终成为补充
给人体的氨基酸,故A正确,故答案为:A;
【小问2详解】
我们食用的大豆,主要含蛋白质,在人体中水解,得到氨基酸,供人体合成蛋白质用,最终补充给人体的
主要成分是氨基酸,故A正确;故答案为:A;
【小问3详解】
蛋白质水解的最终产物是 α− 氨基酸,甘氨酸(CHNH COOH)与NaOH反应生成甘氨酸钠和水,化学方程
2 2
式:CHNH COOH+NaOH=CH NH COONa+H O。故答案为: α− 氨基酸;
2 2 2 2 2
CHNH COOH+NaOH=CH NH COONa+H O;
2 2 2 2 2
【小问4详解】
因豆油中含有碳碳双键,所以易被空气中的 O 氧化而变质,而油脂硬化就是指对易氧化的不饱和脂肪酸
2
甘油酯进行催化氢化,所得的产物即为硬化油,也叫人造脂肪。所以豆油不能保存较长时间的原因主要是
含有碳碳双键,所以易被空气中的 O 氧化而变质,所以必须进行硬化,油脂的硬化是指对易氧化的不饱
2
和脂肪酸甘油酯进行催化氢化,人造脂肪指的是经氢化后的饱和高级脂肪酸的甘油酯。故答案为:分子中
含有碳碳双键,易被空气中的 O 氧化;对易氧化的不饱和脂肪酸甘油酯进行催化加氢;经氢化后的饱和
2
高级脂肪酸的甘油酯。
17. 牛奶放置时间长了会变酸,这是因为牛奶中含有的乳糖在微生物的作用下分解变成了乳酸。乳酸最初
就是从酸牛奶中得到并由此而得名的。乳酸的结构简式为CHCH(OH)COOH。完成下列问题:
3
(1)写出乳酸与足量金属钠反应的化学方程式:__________。
第8页/共13页
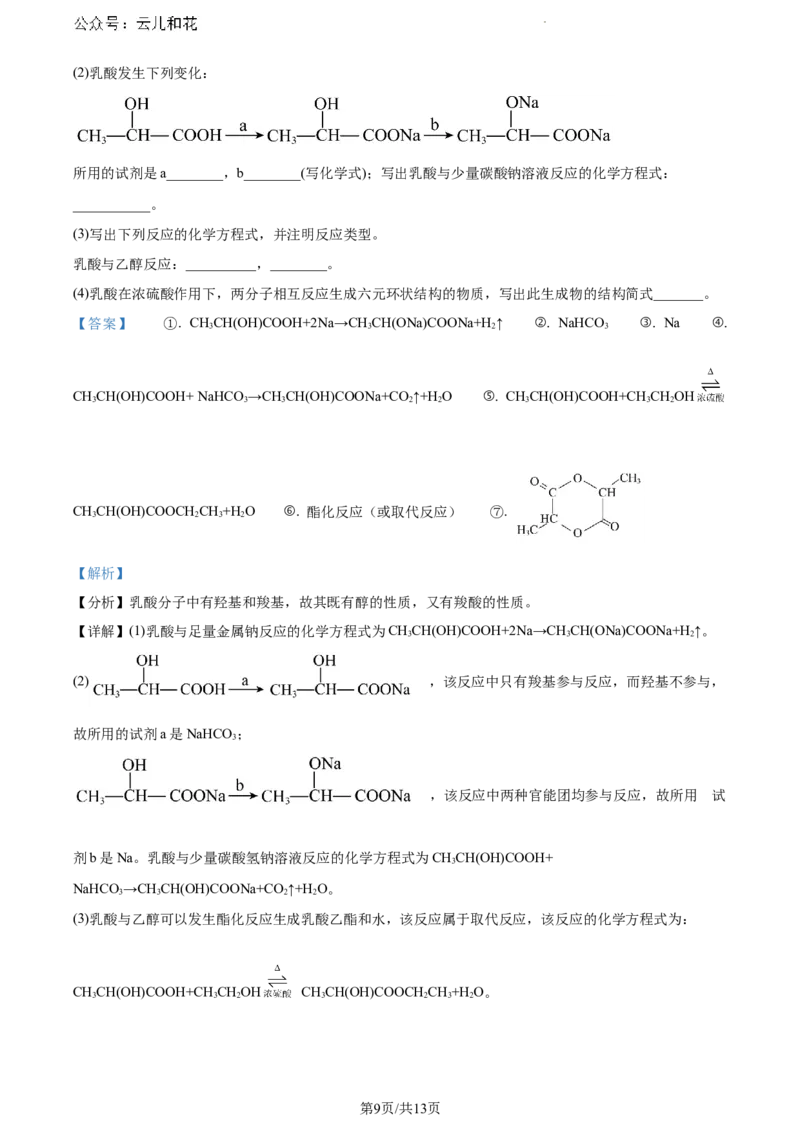
学科网(北京)股份有限公司(2)乳酸发生下列变化:
所用的试剂是a________,b________(写化学式);写出乳酸与少量碳酸钠溶液反应的化学方程式:
___________。
(3)写出下列反应的化学方程式,并注明反应类型。
乳酸与乙醇反应:__________,________。
(4)乳酸在浓硫酸作用下,两分子相互反应生成六元环状结构的物质,写出此生成物的结构简式_______。
【答案】 ①. CHCH(OH)COOH+2Na→CH CH(ONa)COONa+H ↑ ②. NaHCO ③. Na ④.
3 3 2 3
CHCH(OH)COOH+ NaHCO →CHCH(OH)COONa+CO ↑+H O ⑤. CHCH(OH)COOH+CH CHOH
3 3 3 2 2 3 3 2
CHCH(OH)COOCH CH+H O ⑥. 酯化反应(或取代反应) ⑦.
3 2 3 2
【解析】
【分析】乳酸分子中有羟基和羧基,故其既有醇的性质,又有羧酸的性质。
【详解】(1)乳酸与足量金属钠反应的化学方程式为CHCH(OH)COOH+2Na→CH CH(ONa)COONa+H ↑。
3 3 2
(2) ,该反应中只有羧基参与反应,而羟基不参与,
故所用的试剂a是NaHCO ;
3
,该反应中两种官能团均参与反应,故所用 试
的
剂b是Na。乳酸与少量碳酸氢钠溶液反应的化学方程式为CHCH(OH)COOH+
3
NaHCO →CHCH(OH)COONa+CO ↑+H O。
3 3 2 2
(3)乳酸与乙醇可以发生酯化反应生成乳酸乙酯和水,该反应属于取代反应,该反应的化学方程式为:
CHCH(OH)COOH+CH CHOH CHCH(OH)COOCH CH+H O。
3 3 2 3 2 3 2
第9页/共13页
学科网(北京)股份有限公司(4)乳酸在浓硫酸作用下,两分子相互反应生成六元环状结构的交酯,此交酯的结构简式为
。
【点睛】有机化学实际上就是官能团的化学,要求学生要熟悉常见官能团的结构和性质。本题要注意联系
醇和羧酸的化学性质进行分析。特别要注意不同官能团中H原子的活泼性的不同,会比较乙酸、碳酸、苯
酚、碳酸氢根、水、乙醇等分子中羟基H原子的活泼性。
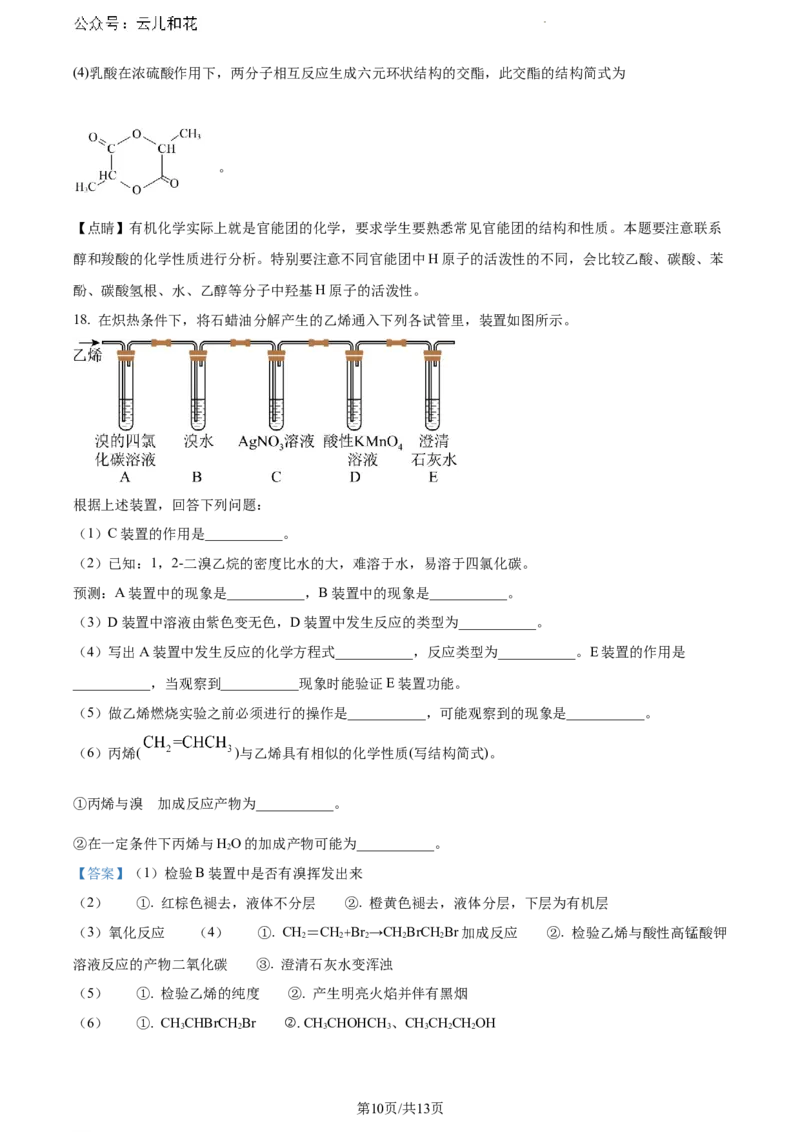
18. 在炽热条件下,将石蜡油分解产生的乙烯通入下列各试管里,装置如图所示。
根据上述装置,回答下列问题:
(1)C装置的作用是___________。
(2)已知:1,2-二溴乙烷的密度比水的大,难溶于水,易溶于四氯化碳。
预测:A装置中的现象是___________,B装置中的现象是___________。
(3)D装置中溶液由紫色变无色,D装置中发生反应的类型为___________。
(4)写出A装置中发生反应的化学方程式___________,反应类型为___________。E装置的作用是
___________,当观察到___________现象时能验证E装置功能。
(5)做乙烯燃烧实验之前必须进行的操作是___________,可能观察到的现象是___________。
(6)丙烯( )与乙烯具有相似的化学性质(写结构简式)。
的
①丙烯与溴 加成反应产物为___________。
②在一定条件下丙烯与HO的加成产物可能为___________。
2
【答案】(1)检验B装置中是否有溴挥发出来
(2) ①. 红棕色褪去,液体不分层 ②. 橙黄色褪去,液体分层,下层为有机层
(3)氧化反应 (4) ①. CH =CH+Br →CHBrCHBr加成反应 ②. 检验乙烯与酸性高锰酸钾
2 2 2 2 2
溶液反应的产物二氧化碳 ③. 澄清石灰水变浑浊
(5) ①. 检验乙烯的纯度 ②. 产生明亮火焰并伴有黑烟
(6) ①. CHCHBrCH Br ②. CH CHOHCH 、CHCHCHOH
3 2 3 3 3 2 2
第10页/共13页
学科网(北京)股份有限公司【解析】
【分析】乙烯通入装置A中生成1,2-二溴乙烷,装置B中乙烯与溴水发生反应,橙黄色褪去,C装置的
作用是检验B装置中是否有溴挥发出来,装置D中乙烯与酸性高锰酸钾溶液发生氧化反应生成的产物为二
氧化碳和水,装置E中用澄清石灰水检验二氧化碳。
【小问1详解】
溴易挥发且溴与AgNO 溶液反应会生成淡黄色AgBr,用AgNO 溶液检验溴是否挥发。C装置的作用是检
3 3
验B装置中是否有溴挥发出来。故答案为:检验B装置中是否有溴挥发出来;
【小问2详解】
1,2-二溴乙烷易溶于四氯化碳,A装置中的现象是红棕色褪去,液体不分层,1,2-二溴乙烷的密度比水
的大,难溶于水,B装置中的现象是橙黄色褪去,液体分层,下层为有机层。故答案为: 红棕色褪去,液
体不分层;橙黄色褪去,液体分层,下层为有机层;
【小问3详解】
乙烯与酸性高锰酸钾溶液发生氧化反应生成的产物为二氧化碳和水,用澄清石灰水检验二氧化碳,D装置
中溶液由紫色变无色,D装置中发生反应的类型为氧化反应。故答案为:氧化反应;
【小问4详解】
A装置中发生反应的化学方程式CH=CH+Br →CHBrCHBr,反应类型为加成反应。E装置的作用是检验
2 2 2 2 2
乙烯与酸性高锰酸钾溶液反应的产物二氧化碳,当观察到澄清石灰水变浑浊现象时能验证E装置功能。故
答案为:CH=CH+Br →CHBrCHBr;加成反应;检验乙烯与酸性高锰酸钾溶液反应的产物二氧化碳;
2 2 2 2 2
澄清石灰水变浑浊;
【小问5详解】
做乙烯燃烧实验之前必须进行的操作是检验乙烯的纯度,可观察到的现象是产生明亮火焰并伴有黑烟。故
答案为: 检验乙烯的纯度;产生明亮火焰并伴有黑烟;
【小问6详解】
丙烯( )与乙烯具有相似的化学性质(写结构简式)。
①丙烯与溴的加成反应产物只有1种:CH3CHBrCH Br。
2
②在一定条件下丙烯与HO的加成产物有2种:CHCHOHCH 、CHCHCHOH。
2 3 3 3 2 2
故答案为:CHCHOHCH 、CHCHCHOH。
3 3 3 2 2
19. (1)下列各组物质中,互为同位素的是__(填序号,下同),互为同系物的是__,互为同分异构体的是
__。
①红磷与白磷
②35Cl与37Cl
第11页/共13页
学科网(北京)股份有限公司③CHCOOCH 与CHCHCOOCH
3 3 3 2 3
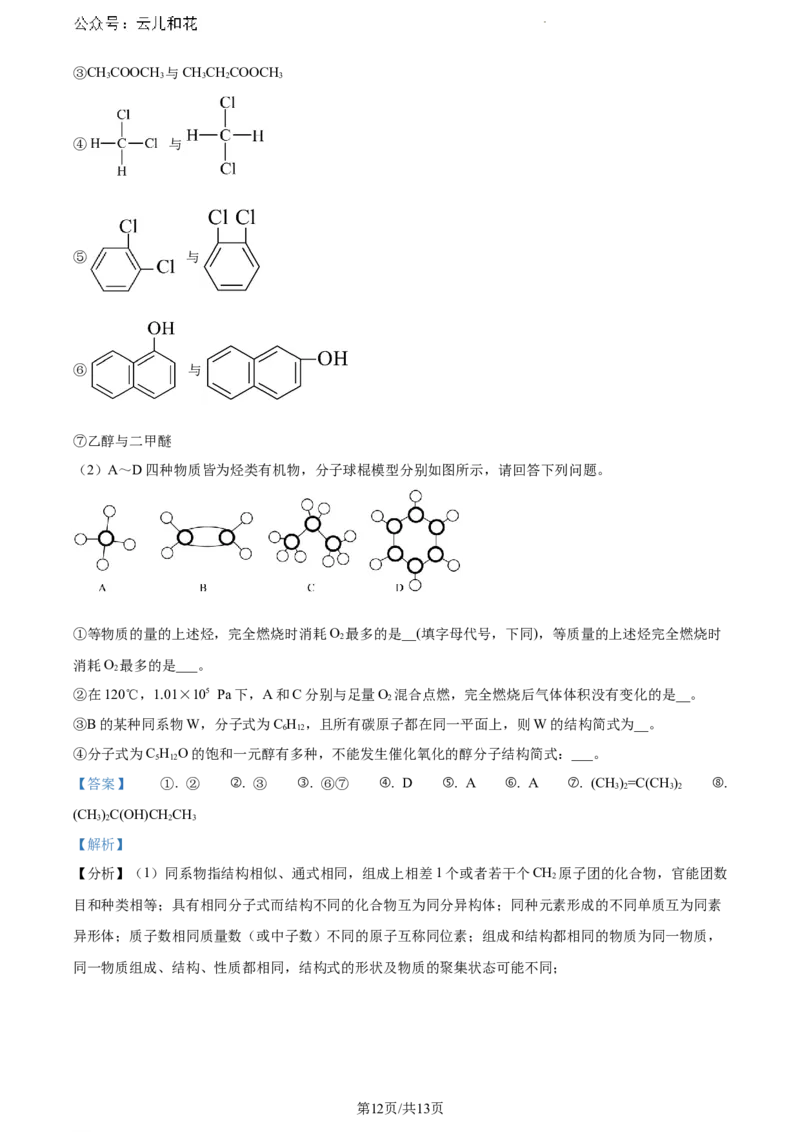
④ 与
⑤ 与
⑥ 与
⑦乙醇与二甲醚
(2)A~D四种物质皆为烃类有机物,分子球棍模型分别如图所示,请回答下列问题。
①等物质的量的上述烃,完全燃烧时消耗O 最多的是__(填字母代号,下同),等质量的上述烃完全燃烧时
2
消耗O 最多的是___。
2
②在120℃,1.01×105 Pa下,A和C分别与足量O 混合点燃,完全燃烧后气体体积没有变化的是__。
2
③B的某种同系物W,分子式为C H ,且所有碳原子都在同一平面上,则W的结构简式为__。
6 12
④分子式为C H O的饱和一元醇有多种,不能发生催化氧化的醇分子结构简式:___。
5 12
【答案】 ①. ② ②. ③ ③. ⑥⑦ ④. D ⑤. A ⑥. A ⑦. (CH)=C(CH ) ⑧.
3 2 3 2
(CH)C(OH)CHCH
3 2 2 3
【解析】
【分析】(1)同系物指结构相似、通式相同,组成上相差1个或者若干个CH 原子团的化合物,官能团数
2
目和种类相等;具有相同分子式而结构不同的化合物互为同分异构体;同种元素形成的不同单质互为同素
异形体;质子数相同质量数(或中子数)不同的原子互称同位素;组成和结构都相同的物质为同一物质,
同一物质组成、结构、性质都相同,结构式的形状及物质的聚集状态可能不同;
第12页/共13页
学科网(北京)股份有限公司(2)①1mol烃C H 的耗氧量为 mol;等质量的上述四种烃,含氢元素的质量越大,耗氧量越大;
x y
②120℃条件下水为气体,燃烧通式C H+ O xCO+ HO(g),完全燃烧前后气体体积没有变
x y 2 2 2
化,则1+ =x+ ,故y=4,以此判断;
③乙烯是平面型结构,根据乙烯的结构确定该物质的结构;
④不能发生催化氧化反应,则羟基相连的碳原子上没有氢原子。
【详解】(1)35Cl和37Cl中子数不同,是氯元素的不同核素,互为同位素,故选②;
CHCOOCH 和CHCHCOOCH 结构相似,相差1个CH 原子团,互为同系物,故选③;
3 3 3 2 3 2
⑥中两种物质分子式相同,结构不同,为官能团位置异构,⑦乙醇与二甲醚,两种物质分子式相同,结构
不同,为官能团异构,故属于同分异构的选⑥⑦;
(2)①1mol烃C H 的耗氧量为 mol,则等物质的量的CH、C H、C H、C H 中消耗O 最多的是
x y 4 2 4 3 8 6 6 2
C H;
6 6
答案选D;
等质量的上述四种烃,含氢元素的质量越大,完全燃烧时消耗O 越多,4种物质中CH 的含氢质量最大,
2 4
等质量时,耗氧量最大;
答案选A;
②120℃条件下水为气体,燃烧通式C H+ O xCO+ HO(g),完全燃烧前后气体体积没有变
x y 2 2 2
化,则1+ =x+ ,故y=4,即A和C中CH 完全燃烧后体积不变;
4
答案选A;
③乙烯是平面型结构,C H 符合单烯烃的通式,且该烃的所有碳原子都在同一平面上,所以可以看作是乙
6 12
烯中的氢原子被甲基取代,所以该物质的结构简式为:(CH)C=C(CH);
3 2 3 2
④不能发生催化氧化反应,则羟基相连的碳原子上没有氢原子,醇分子分子式为C H O,符合条件的饱和
5 12
一元醇的结构简式为:(CH)C(OH)CHCH。
3 2 2 3
第13页/共13页
学科网(北京)股份有限公司