文档内容
甘肃省酒泉市多校联考2025-2026学年高一上学期1月期末化学试题
一、单选题
1.在生产和生活中,金属材料具有广泛的应用,以下关于金属材料的说法不合理的是
A.钠钾合金可用作核反应堆的传热介质
B.硬铝合金因为具有银白色可作为制造飞机的材料
C.常见的一些合金的硬度大于其成分金属
D.Ti-Fe合金具有良好的储氢功能
2.劳动创造美好生活。下列劳动项目对应的化学知识解释错误的是
选项 劳动项目 化学知识
A 食品制作:小苏打可用于烘焙面包 碳酸钠可与酸反应
B 泳池消毒:用漂粉精作游泳池的消毒剂 漂粉精中的 有强氧化性
家庭卫生:用“管道通”(含烧碱和铝粒)清通管
C 使用过程中产生大量气体
道
D 用洁厕灵(主要成分为稀盐酸)除厕所污垢尿碱 洁厕灵呈强酸性
A.A B.B C.C D.D
3.侯氏制碱法不仅解决了索尔维法废料污染问题,还大幅提高了食盐利用率,是中国对世界化学工业的
重大贡献,其主要原理是 ,下列说法正确的是
A.CO 的电子式为
2
B.用电子式表示 NaCl 的形成过程为
C.HO的分子结构模型为
2
D. 中含有的化学键有共价键和离子键
4.高锰酸钾溶液酸化时不能用盐酸,主要发生的反应为
下列关于该反应的说法正确的是A.该反应的氧化剂为
B.该反应中氧化剂和还原剂的物质的量之比为2:16
C.该反应的氧化产物为
D.该反应条件下,Cl 的氧化性比 强
2
5.设N 为阿伏加德罗常数的值,下列说法正确的是
A
A.1mol∙L-1的 NaHCO 溶液中含有 Na+数为N
3 A
B.7.8gNa O 含有阴离子数为0.2N
2 2 A
C.标准状况下,11.2 L CO 中含有的氧原子数为 N
2 A
D.1.8g水中含有的价电子总数为N
A
6.下列各组离子在给定条件下能大量共存的是
A.无色透明溶液中:
B.含 的溶液中:
C.酸性溶液中:
D.NaOH 溶液中:
7.下列离子方程式书写正确的是
A.Cl 与水反应:
2
B.NaO 与水反应:
2 2
C.Cl 通入 NaBr溶液中:
2
D.石灰石与稀盐酸反应:
8.①~⑥均是元素周期表中的短周期主族元素,它们的主要化合价和原子半径如下表所示。下列说法中正
确的是
元素 ① ② ③ ④ ⑤ ⑥
主要化合价原子半径/nm 0.152 0.186 0.160 0.074 0.071 0.099
A.①的原子半径在它同主族的原子中最小
B.②与④形成的化合物中只含有离子键
C.③的单质常温下能与水剧烈反应
D.⑥的最高价氧化物对应的水化物是强酸
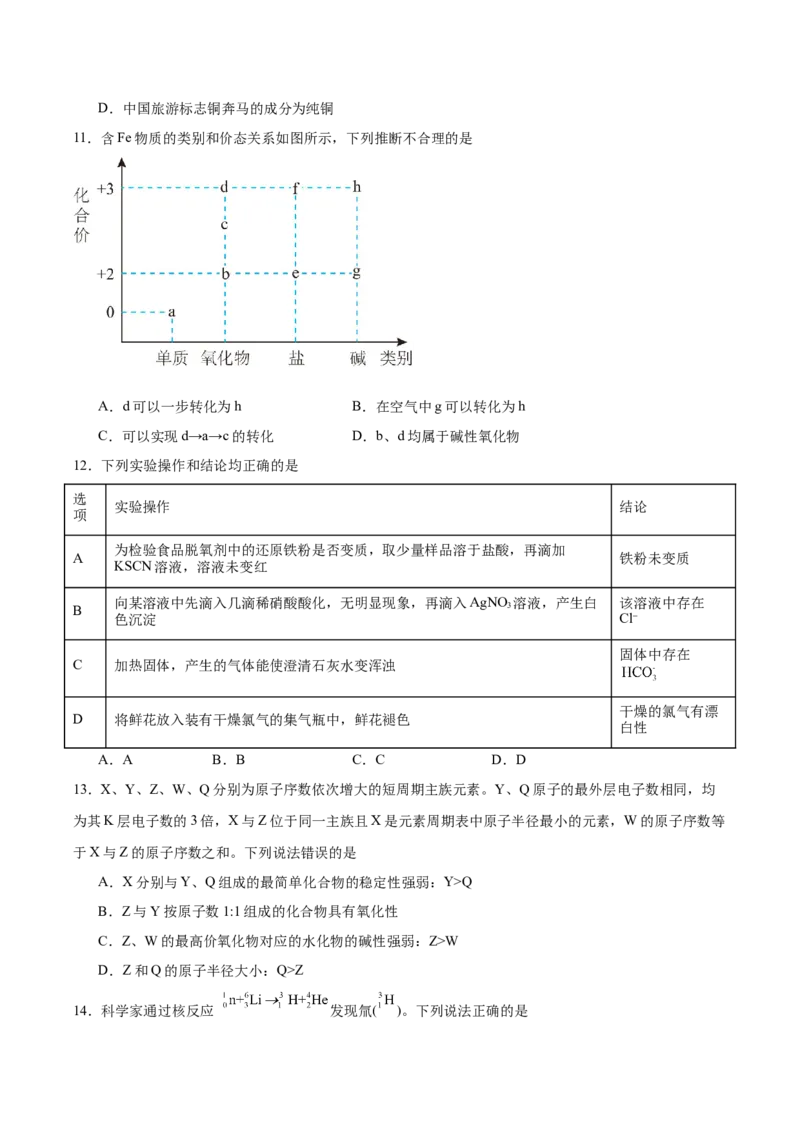
9.用下列实验装置进行实验,能达到相应目的的是
A.除去CO 中的HCl B.观察 NaCl的焰色
2
C.收集Cl D.制备氢氧化铁胶体
2
A.A B.B C.C D.D
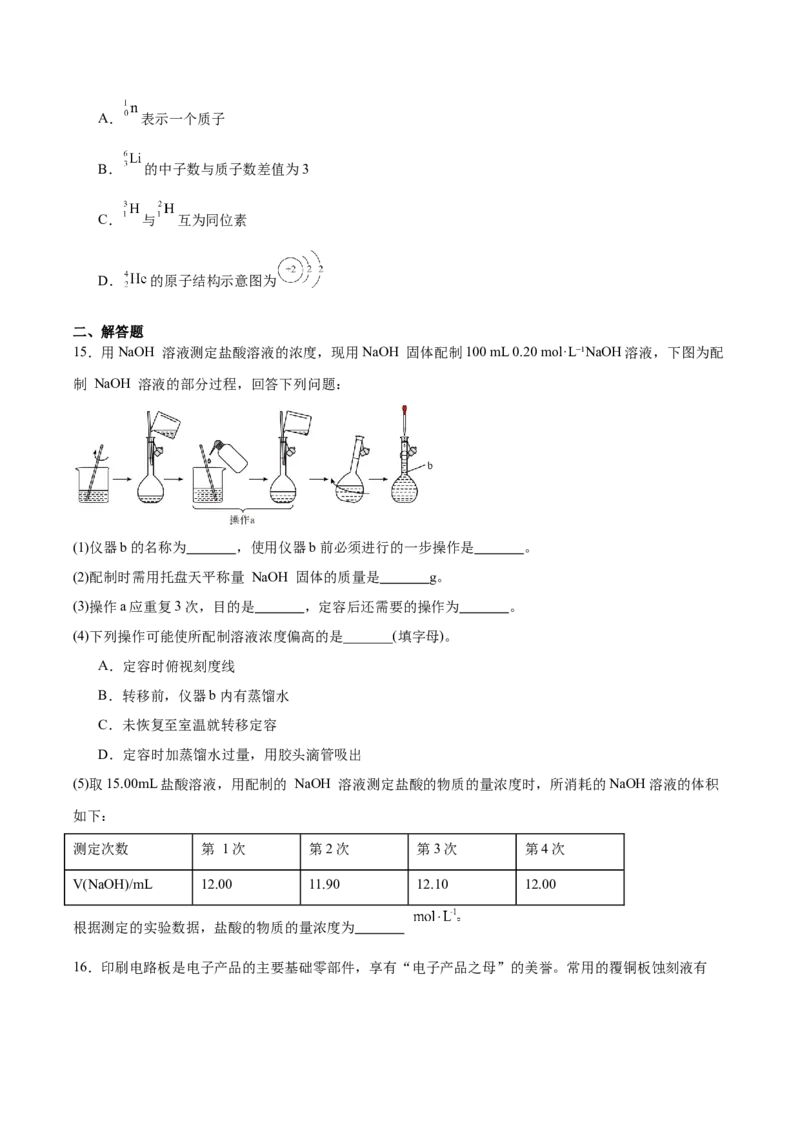
10.某工厂的工业废水中含有大量的 和较多的 为了减少污染并促进废物利用,工厂计划从
该废水中回收 和金属铜。根据以下流程图判断,下列说法正确的是
A.在工业废水中加入铁发生反应的离子方程式为
B.过滤操作中所用的玻璃仪器有漏斗、烧杯、玻璃棒
C.溶液在空气中冷却结晶得到D.中国旅游标志铜奔马的成分为纯铜
11.含Fe物质的类别和价态关系如图所示,下列推断不合理的是
A.d可以一步转化为h B.在空气中g可以转化为h
C.可以实现d→a→c的转化 D.b、d均属于碱性氧化物
12.下列实验操作和结论均正确的是
选
实验操作 结论
项
为检验食品脱氧剂中的还原铁粉是否变质,取少量样品溶于盐酸,再滴加
A 铁粉未变质
KSCN溶液,溶液未变红
向某溶液中先滴入几滴稀硝酸酸化,无明显现象,再滴入AgNO 溶液,产生白 该溶液中存在
B 3
色沉淀 Cl⁻
固体中存在
C 加热固体,产生的气体能使澄清石灰水变浑浊
干燥的氯气有漂
D 将鲜花放入装有干燥氯气的集气瓶中,鲜花褪色
白性
A.A B.B C.C D.D
13.X、Y、Z、W、Q分别为原子序数依次增大的短周期主族元素。Y、Q原子的最外层电子数相同,均
为其K层电子数的3倍,X与Z位于同一主族且X是元素周期表中原子半径最小的元素,W的原子序数等
于X与Z的原子序数之和。下列说法错误的是
A.X分别与Y、Q组成的最简单化合物的稳定性强弱:Y>Q
B.Z与Y按原子数1:1组成的化合物具有氧化性
C.Z、W的最高价氧化物对应的水化物的碱性强弱:Z>W
D.Z和Q的原子半径大小:Q>Z
14.科学家通过核反应 发现氚( )。下列说法正确的是A. 表示一个质子
B. 的中子数与质子数差值为3
C. 与 互为同位素
D. 的原子结构示意图为
二、解答题
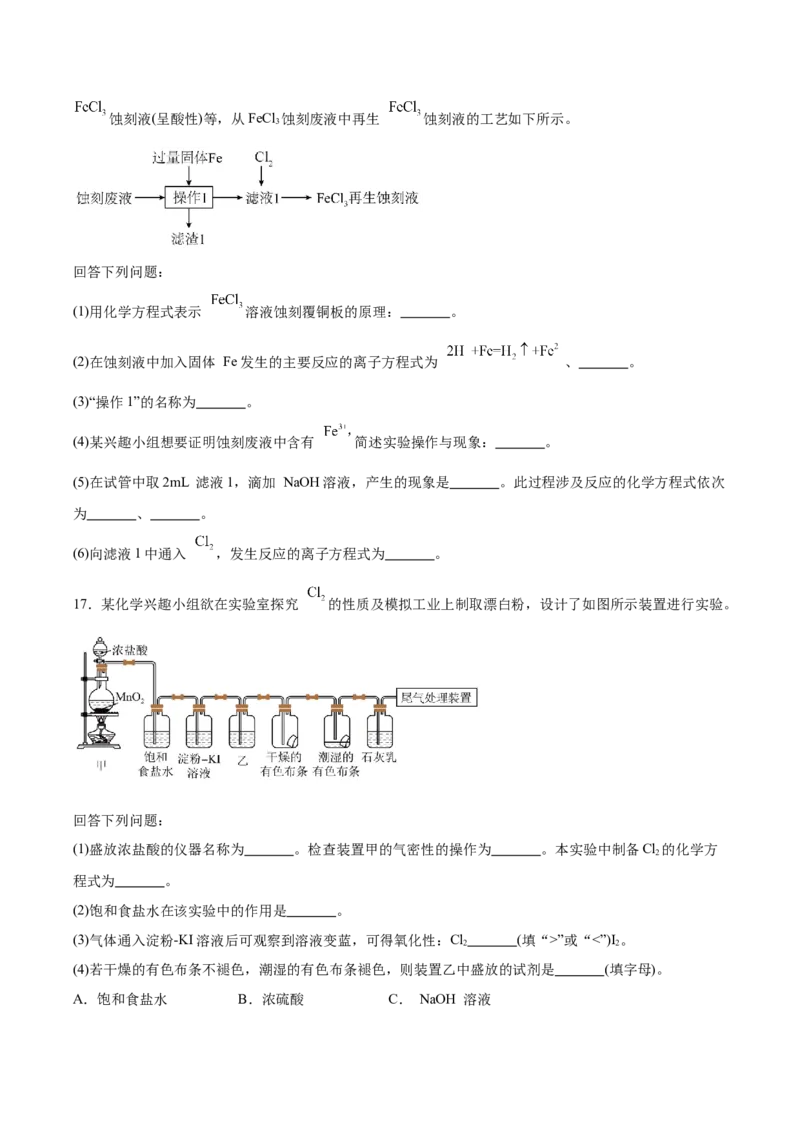
15.用NaOH 溶液测定盐酸溶液的浓度,现用NaOH 固体配制100 mL 0.20 mol·L⁻¹NaOH溶液,下图为配
制 NaOH 溶液的部分过程,回答下列问题:
(1)仪器b的名称为 ,使用仪器b前必须进行的一步操作是 。
(2)配制时需用托盘天平称量 NaOH 固体的质量是 g。
(3)操作a应重复3次,目的是 ,定容后还需要的操作为 。
(4)下列操作可能使所配制溶液浓度偏高的是_______(填字母)。
A.定容时俯视刻度线
B.转移前,仪器b内有蒸馏水
C.未恢复至室温就转移定容
D.定容时加蒸馏水过量,用胶头滴管吸出
(5)取15.00mL盐酸溶液,用配制的 NaOH 溶液测定盐酸的物质的量浓度时,所消耗的NaOH溶液的体积
如下:
测定次数 第 1次 第2次 第3次 第4次
V(NaOH)/mL 12.00 11.90 12.10 12.00
根据测定的实验数据,盐酸的物质的量浓度为
16.印刷电路板是电子产品的主要基础零部件,享有“电子产品之母”的美誉。常用的覆铜板蚀刻液有蚀刻液(呈酸性)等,从FeCl 蚀刻废液中再生 蚀刻液的工艺如下所示。
3
回答下列问题:
(1)用化学方程式表示 溶液蚀刻覆铜板的原理: 。
(2)在蚀刻液中加入固体 Fe发生的主要反应的离子方程式为 、 。
(3)“操作1”的名称为 。
(4)某兴趣小组想要证明蚀刻废液中含有 简述实验操作与现象: 。
(5)在试管中取2mL 滤液1,滴加 NaOH溶液,产生的现象是 。此过程涉及反应的化学方程式依次
为 、 。
(6)向滤液1中通入 ,发生反应的离子方程式为 。
17.某化学兴趣小组欲在实验室探究 的性质及模拟工业上制取漂白粉,设计了如图所示装置进行实验。
回答下列问题:
(1)盛放浓盐酸的仪器名称为 。检查装置甲的气密性的操作为 。本实验中制备Cl 的化学方
2
程式为 。
(2)饱和食盐水在该实验中的作用是 。
(3)气体通入淀粉-KI溶液后可观察到溶液变蓝,可得氧化性:Cl (填“>”或“<”)I 。
2 2
(4)若干燥的有色布条不褪色,潮湿的有色布条褪色,则装置乙中盛放的试剂是 (填字母)。
A.饱和食盐水 B.浓硫酸 C. NaOH 溶液(5)制取漂白粉的化学方程式为 。
三、填空题
18.牙齿的主要成分是难溶的羟基磷酸钙 还含有碳酸盐以及钠、镁、氯、氟等元素,这
些成分共同构成了牙齿的硬组织,使其具有坚硬和耐磨的特性。回答下列问题:
(1)C在元素周期表中的位置是 。
(2)画出 P 的原子结构示意图: 。
(3) 中含有的O——H键属于 (填“离子键”或“共价键”)。
(4)非金属性: Cl强于 Br。
①用原子结构解释原因:Cl和Br位于同一主族, ,得电子能力 Cl强于 Br。
②下列事实能说明非金属性 Cl强于Br 的是 (填字母)。
a.水溶液的酸性:HCl>HBrO
b. Cl 比Br 更容易与 H 反应
2 2 2
(5)金属性:K强于 Na。设计实验证明: 。
(6)高糖饮食、口腔卫生护理不当等原因会造成龋齿,牙膏中加入NaF、SrF 等氟化物能够预防龋齿。Sr与
2
Mg、Ca同主族,位于第五周期。下列说法正确的是 (填字母)。
a. Sr是金属元素
b.原子半径:Mg
(4)B
(5)
18.(1)第二周期第ⅣA族(2)
(3)共价键
(4) 电子层数 ,原子半径 b
(5)分别将少量K和Na投入水中,K反应更剧烈,证明金属性K > Na
(6)ab