文档内容
【冲刺期末】高二化学期末单元复习测试
第二单元 化学反应速率与化学平衡
(时间:90分钟 满分:100分)
一、选择题(本题共15小题,每小题3分,共45分。每小题只有一个选项符合题意)
1.(2021·广东高二期末)下列人们在生活、生产、实验的相关措施中,不是用来调控化学反应速率的是
A.将食物存放在温度较低的地方
B.将氯化铁固体溶于较浓盐酸配制氯化铁溶液
C.将固体试剂溶于水配成溶液后再进行化学实验
D.通常将颗粒状的固体药品研细混匀后进行反应
2.(2022·全国高三专题练习)在密闭容器中进行反应N+O 2NO,下列条件能加快反应速率的是
2 2
A.增大体积使压强减小 B.体积不变,充⇌入N 使压强增大
2
C.体积不变,充入He使压强增大 D.压强不变,充入气体Ne
3.(2022·吉林长春)工业制硫酸的接触室中发生反应: 。该反应在
500℃和催化剂存在下进行,下列有关说法正确的是
A.如果使氧气过量,并给足够时间让反应充分进行,SO 可以全部转化为SO
2 3
B.该反应的平衡常数(K)随体系压强的增加而增大
C.该反应选择在500℃和催化剂存在下进行,因此该反应是吸热反应
D.反应达到化学平衡后,只改变温度,化学平衡一定会被破坏
4.已知反应CO(g)+HO(g) CO(g)+H(g) ΔH<0。在一定温度和压强下于密闭容器中,反应达到平衡。
2 2 2
下列叙述正确的是( )
⇌
A.升高温度,K减小 B.减小压强,n(CO)增加
2
C.更换高效催化剂,α(CO)增大 D.充入一定量的氮气,n(H )变大
2
5.下列由实验得出的结论正确的是( )
选项 实验 实验结论或解释
向2 mL 0.1 mol·L-1 FeCl 溶液中滴加0.1
3
mol·L-1 KI溶液5~6滴,充分反应后,再滴
A Fe3+与I-之间的反应属于可逆反应
加几滴0.01 mol·L-1 KSCN溶液,出现血红
色溶液。
探究温度对硫代硫酸钠与硫酸反应速率的影
B 响时,若先将两种溶液混合并计时,再用水 则测得的反应速率偏高
浴加热至设定温度
C 分别向装有2 mL 0.1 mol·L-1 H C O 溶液和 探究浓度对反应速率的影响
2 2 42 mL 0.2 mol·L-1 H C O 溶液的两支试管中
2 2 4
加入4 mL 0.01 mol·L-1酸性KMnO 溶液,
4
振荡,后者溶液先褪色。
将石灰石与盐酸反应产生的气体直接通入水
D 非金属性:C>Si
玻璃中,生成白色沉淀
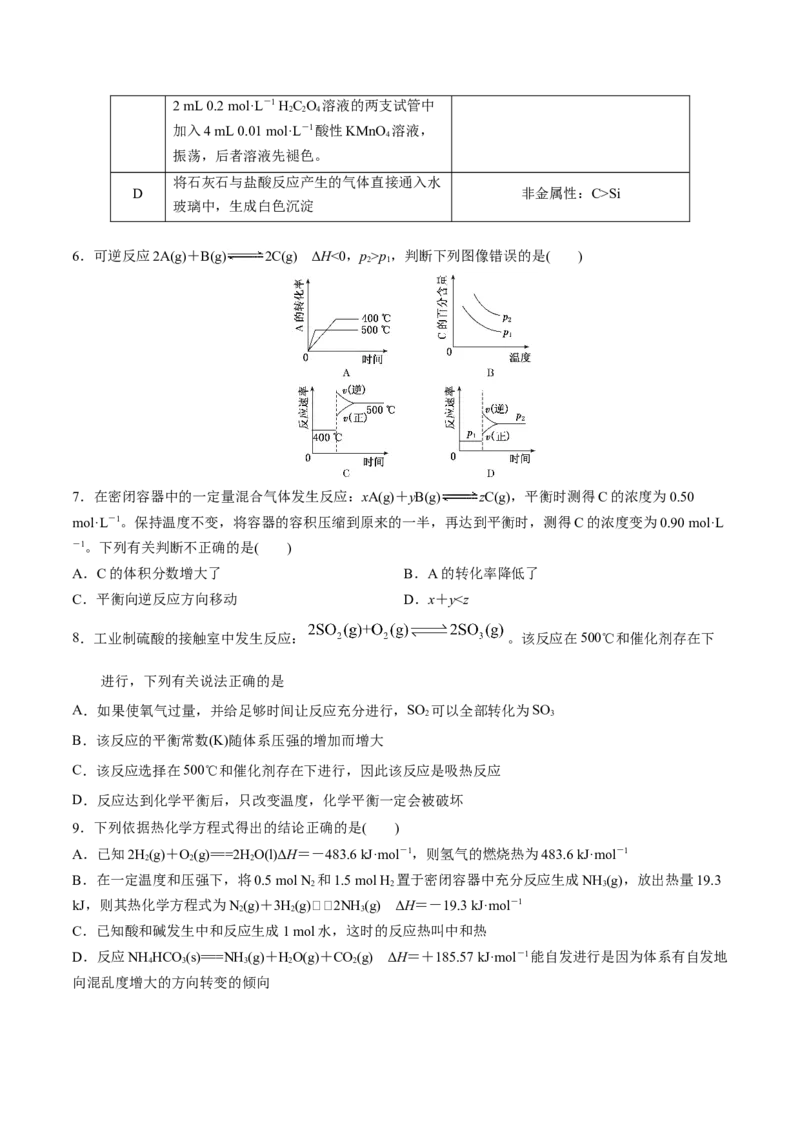
6.可逆反应2A(g)+B(g) 2C(g) ΔH<0,p>p,判断下列图像错误的是( )
2 1
7.在密闭容器中的一定量混合气体发生反应:xA(g)+yB(g) zC(g),平衡时测得C的浓度为0.50
mol·L-1。保持温度不变,将容器的容积压缩到原来的一半,再达到平衡时,测得C的浓度变为0.90 mol·L
-1。下列有关判断不正确的是( )
A.C的体积分数增大了 B.A的转化率降低了
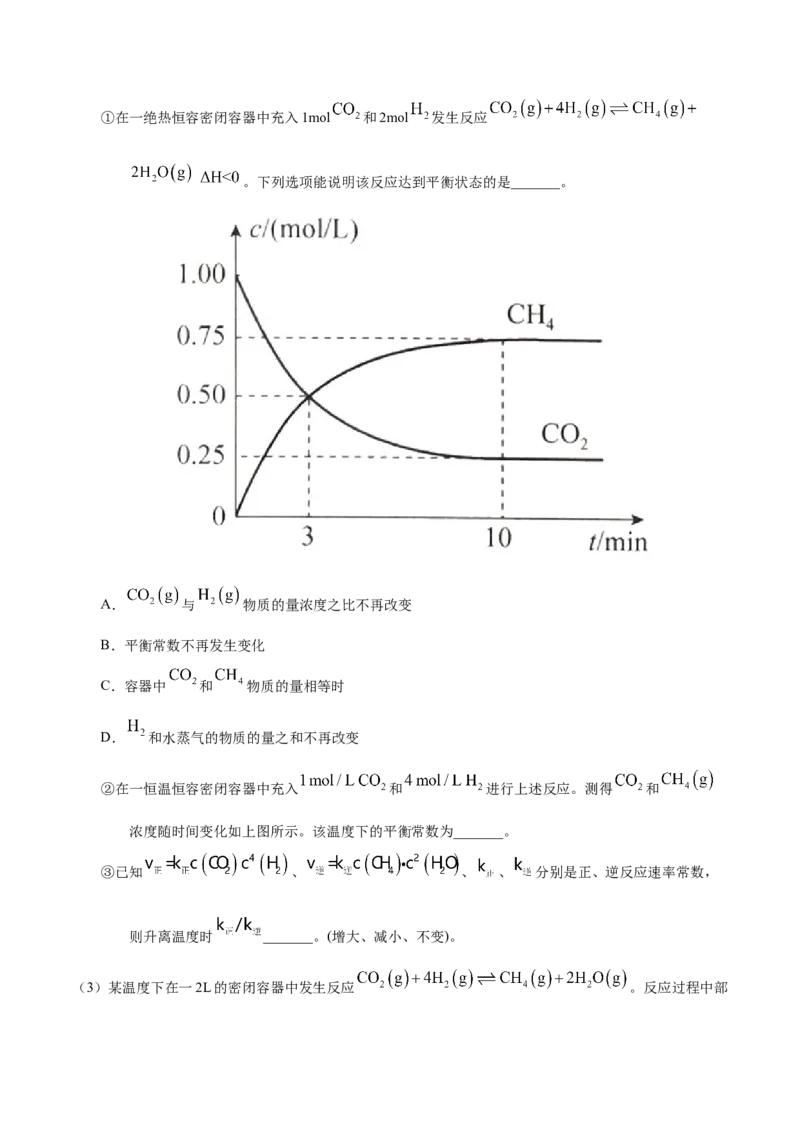
C.平衡向逆反应方向移动 D.x+y”、“<”或“=”)
②对反应I,前10min内的平均反应速率 _______,若30min时间容器中再充入
和 ,则平衡_______移动(填“正向”、“逆向”或“不”)。
17.(14分)科学家研究出一种以天然气为燃料的“燃烧前捕获系统”,其简单流程如图所示(条件及物质未
标出)。
(1)已知:CH、CO、H 的燃烧热分别为890.3 kJ·mol-1、283.0 kJ·mol-1、285.8 kJ·mol-1,则上述流
4 2
程中第一步反应2CH(g)+O(g)===2CO(g)+4H(g)的ΔH=______________。
4 2 2
(2)工业上可用H 和CO 制备甲醇,其反应方程式为CO(g)+3H(g)CH OH(g)+HO(g),某温度下,
2 2 2 2 3 2
将1 mol CO 和3 mol H 充入容积不变的2 L密闭容器中,发生上述反应,测得不同时刻反应前后的压强关
2 2
系如下表:
时间/h 1 2 3 4 5 6
0.90 0.85 0.83 0.81 0.80 0.80①用H 表示前2 h 的平均反应速率v(H )=______________________________
2 2
__________________________________________;
②该温度下,CO 的平衡转化率为________。
2
(3)在300 ℃、8 MPa下,将CO 和H 按物质的量之比为1∶3 通入一密闭容器中发生(2)中反应,达到平
2 2
衡时,测得CO 的平衡转化率为50%,则该反应条件下的平衡常数为K =________(用平衡分压代替平衡
2 p
浓度计算,分压=总压×物质的量分数)。
(4)CO 经催化加氢可合成低碳烯烃:2CO(g)+6H(g)C H(g)+4HO(g) ΔH。在0.1 MPa时,按
2 2 2 2 4 2
n(CO)∶n(H )=1∶3投料,如图所示为不同温度(T)下,平衡时四种气态物质的物质的量(n)关系。
2 2
①该反应的ΔH________0(填“>”或“<”)。
②曲线c表示的物质为________。
③为提高H 的平衡转化率,除改变温度外,还可采取的措施是
2
________________________________________________________________________。
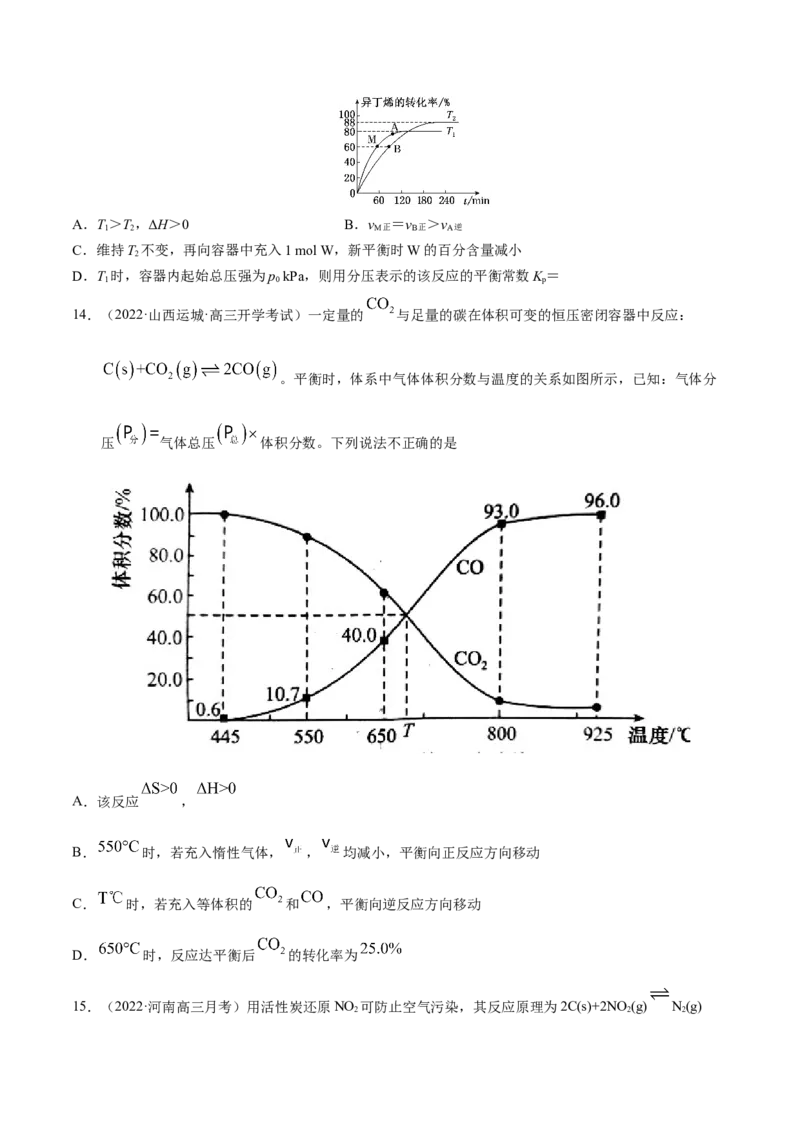
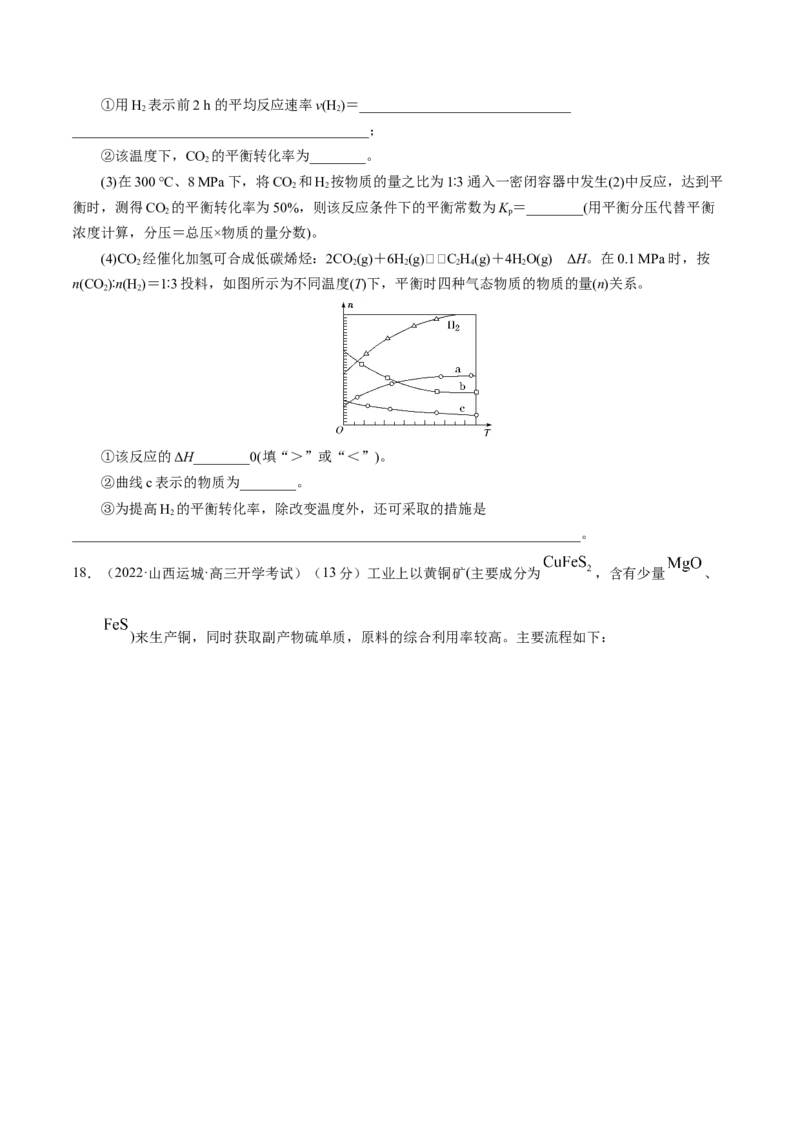
18.(2022·山西运城·高三开学考试)(13分)工业上以黄铜矿(主要成分为 ,含有少量 、
)来生产铜,同时获取副产物硫单质,原料的综合利用率较高。主要流程如下:(1)为加快溶浸速率,可采取的措施有___________(只写一条即可)。
(2) 溶液与 反应的化学方程式为___________;该反应中消耗 时被 氧化
生成的物质的量为___________。
(3)该流程中可以循环利用的物质有___________。
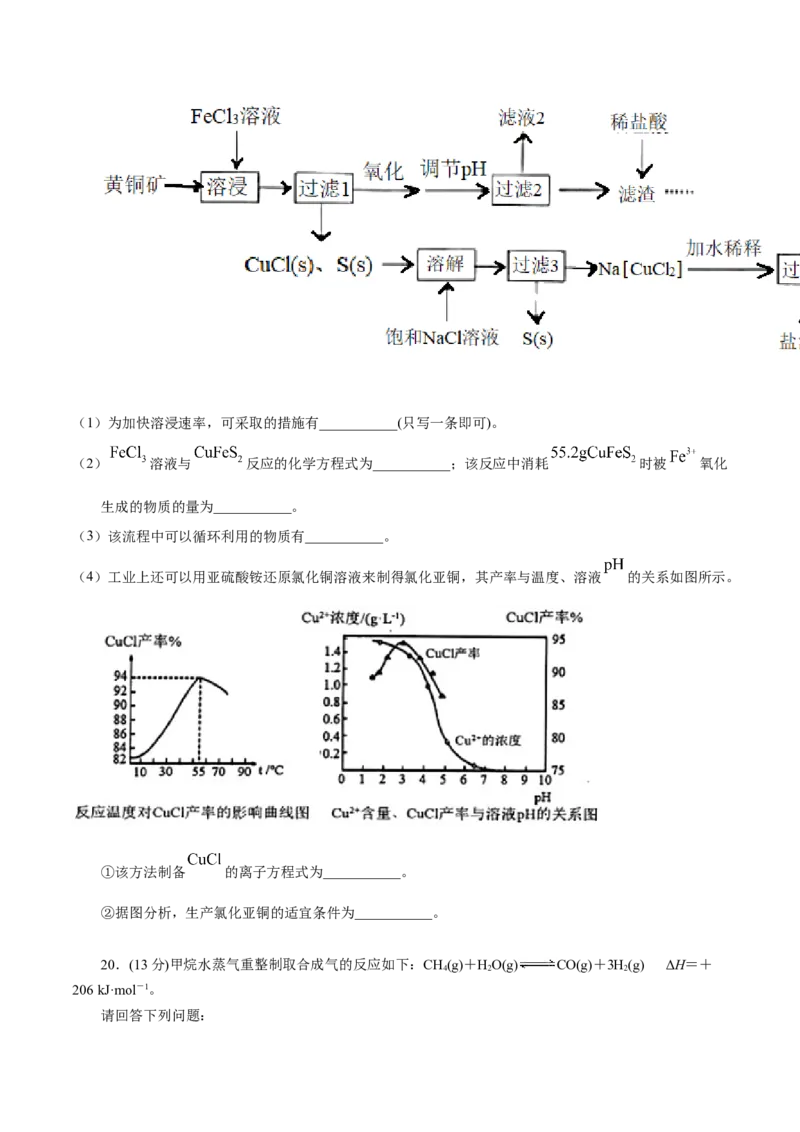
(4)工业上还可以用亚硫酸铵还原氯化铜溶液来制得氯化亚铜,其产率与温度、溶液 的关系如图所示。
①该方法制备 的离子方程式为___________。
②据图分析,生产氯化亚铜的适宜条件为___________。
20.(13分)甲烷水蒸气重整制取合成气的反应如下:CH(g)+HO(g) CO(g)+3H(g) ΔH=+
4 2 2
206 kJ·mol-1。
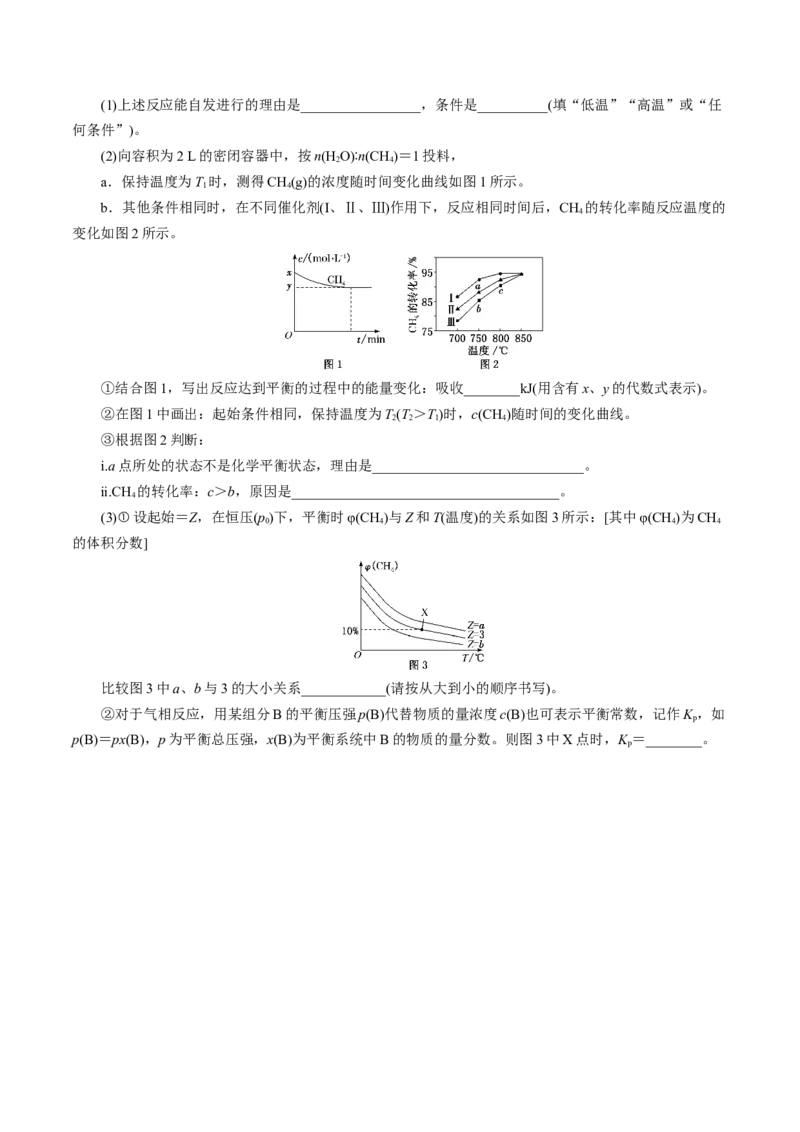
请回答下列问题:(1)上述反应能自发进行的理由是_________________,条件是__________(填“低温”“高温”或“任
何条件”)。
(2)向容积为2 L的密闭容器中,按n(H O)∶n(CH)=1投料,
2 4
a.保持温度为T 时,测得CH(g)的浓度随时间变化曲线如图1所示。
1 4
b.其他条件相同时,在不同催化剂(Ⅰ、Ⅱ、Ⅲ)作用下,反应相同时间后,CH 的转化率随反应温度的
4
变化如图2所示。
①结合图1,写出反应达到平衡的过程中的能量变化:吸收________kJ(用含有x、y的代数式表示)。
②在图1中画出:起始条件相同,保持温度为T(T>T)时,c(CH)随时间的变化曲线。
2 2 1 4
③根据图2判断:
ⅰ.a点所处的状态不是化学平衡状态,理由是______________________________。
ⅱ.CH 的转化率:c>b,原因是______________________________________。
4
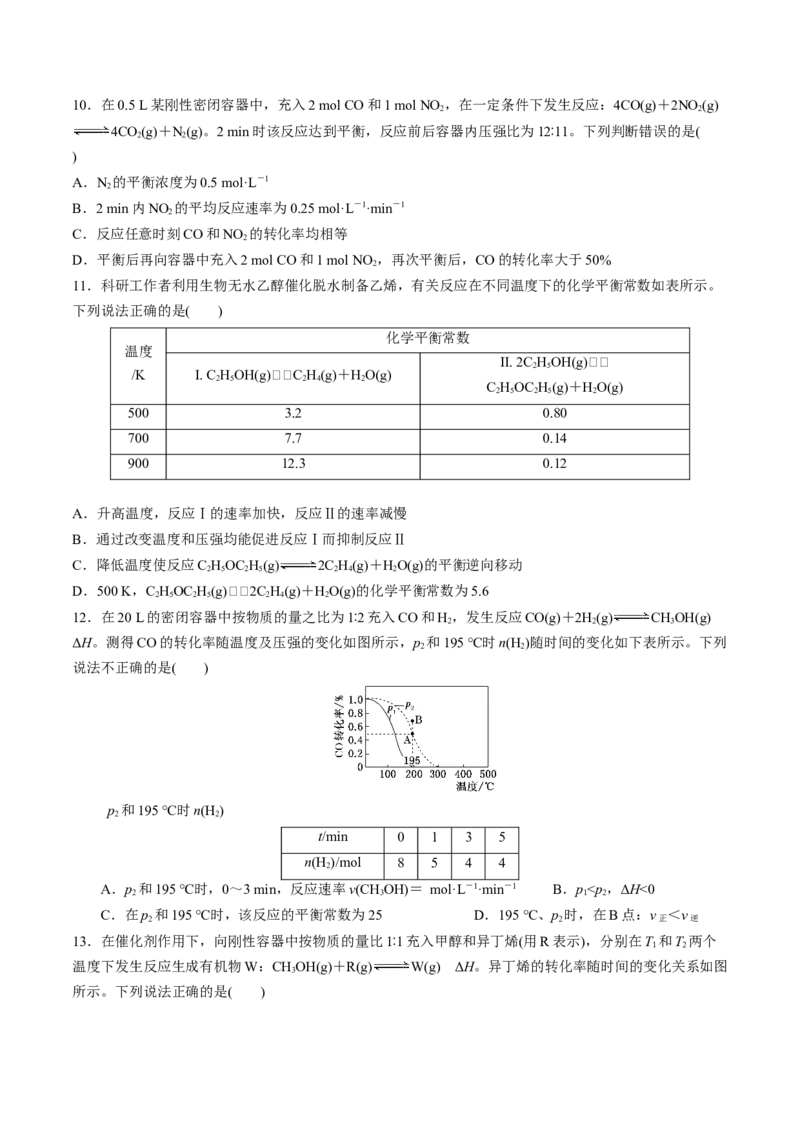
(3)①设起始=Z,在恒压(p)下,平衡时φ(CH)与Z和T(温度)的关系如图3所示:[其中φ(CH)为CH
0 4 4 4
的体积分数]
比较图3中a、b与3的大小关系____________(请按从大到小的顺序书写)。
②对于气相反应,用某组分B的平衡压强p(B)代替物质的量浓度c(B)也可表示平衡常数,记作K ,如
p
p(B)=px(B),p为平衡总压强,x(B)为平衡系统中B的物质的量分数。则图3中X点时,K =________。
p