文档内容
人教版(2019)高一必修第一册 第二章 海水中的重要元素
第三节 物质的量
学校:___________姓名:___________班级:___________考号:___________
一、单选题
1.下列各组数据中,前者刚好是后者两倍的是
A.20%氢氧化钠溶液中氢氧化钠物质的量浓度和10%氢氧化钠溶液中氢氧化钠物质的
量浓度
B.100mL2mol/L氯化钠溶液中c(Cl-)和200mL1mol/L氯化镁溶液中c(Cl-)
C.44g二氧化碳中氧原子数和标准状况下22.4L一氧化碳中氧原子数
D.2mol水的摩尔质量和 1mol水的摩尔质量
2.N 为阿伏伽德罗常数的值。下列叙述正确的是
A
A.lmolNaHSO 固体中所含阴阳离子数目总数为3N
4 A
B.14g分子式为C H 的链烃中含有的C-H键的数目为2N
n 2n A
C.27g铝与lmol/L的盐酸充分反应,转移电子数目为3N
A
D.标准状况下,44.8升NO与22.4升O 完全反应所得分子数目为2N
2 A
3.设N 代表阿伏加德罗常数,下列说法不正确的是
A
A.1.5 mol NO 与足量的HO反应,转移的电子数为N
2 2 A
B.常温常压下,18g D O含有的原子数为3N
2 A
C.氧气和臭氧的混合物32 g中含有2N 个氧原子
A
D.在标准状况下,0.5N 个氯气分子所占体积约是11.2 L
A
4.两个容积相同的密闭容器,一个盛有氯化氢,另一个盛有H 和Cl 的混合气体,在
2 2
同温同压下,两个容器内的气体一定具有相同的:①质量②密度③分子总数④原子总
数
A.①② B.②④ C.③④ D.①③
5.下列叙述正确的是
①摩尔是国际单位制中七个基本物理量之一
②二氧化硫的摩尔质量是64 g
③质量相等,密度不等的CO和C H 的分子数相等
2 4
④一个钠原子的质量约等于 g
⑤标准状况下,11.2 L HO含有的分子数约为3.01×1023个
2
⑥常温常压下,11.2 L CH 中含有的原子数约为1.505×1024个
4⑦1 mol H 和N 的混合气体在标准状况下的体积约为22.4 L
2 2
⑧常温常压下,22 g CO 中含有的原子的物质的量为1.5 mol
2
A.①④⑥⑧ B.③④⑥⑦ C.①②⑤⑦ D.③④⑦⑧
6.下列叙述正确的是
A.1mol任何气体的体积一定是22.4L
B.同温同压下两种气体,只要它们的分子数相同,所占体积也一定相同
C.在标准状况下,体积为22.4L的物质都是1mol
D.在非标准状况下,1mol任何气体的体积不可能是22.4L
7.下列溶液中,负离子浓度最大的是
A.0.5 mol·L-1 HSO 溶液50 mL B.0.5 mol·L-1 CaCl 溶液35 mL
2 4 2
C.0.5 mol·L-1 NaCl溶液70 mL D.0.5 mol·L-1 Al (NO) 溶液60 mL
3 3
8.下列溶液中Cl- 浓度与50mL 1mol·L﹣1 MgCl 溶液中Cl-浓度相等的是
2
A.100mL 1 mol·L﹣1 NaCl溶液 B.100 mL 1 mol·L﹣1 CaCl 溶液
2
C.50 mL 2 mol·L﹣1 BaCl 溶液 D.50 mL 2 mol·L﹣1 AlCl 溶液
2 3
9.4℃时,在100mL水中溶解22.4L(标准状况下)HCl气体形成溶液。下列说法正确的
是
A.该溶液的物质的量浓度为10mol·L-1
B.由于溶液的密度未知,故该溶液的物质的量浓度无法求得
C.所得溶液的体积为22.5L
D.由于溶液的密度未知,故该溶液中溶质的质量分数无法求得
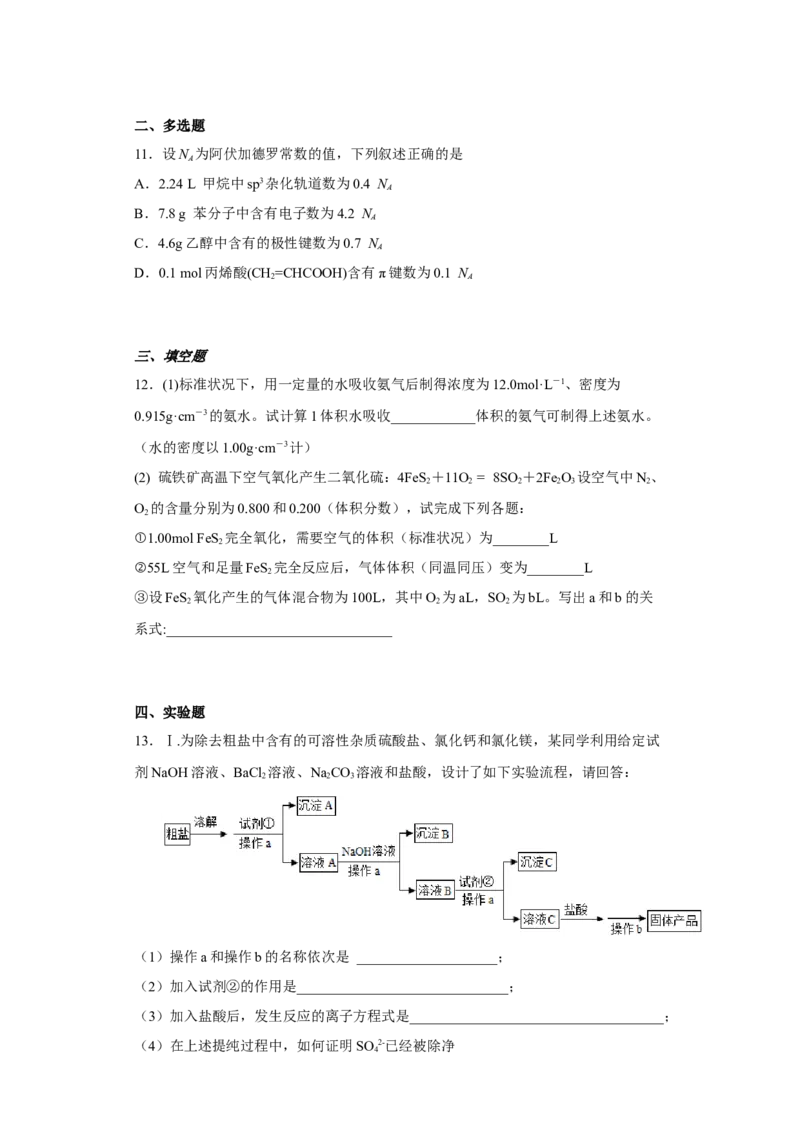
10.配制一定物质的量浓度的 溶液的操作过程示意图如下:
下列说法中错误的是
A.“操作1”需将溶解的 溶液及烧杯洗涤液全部转移到容量瓶中
B.“操作2”中玻璃棒起引流作用
C.“操作4”定容时俯视刻度线会造成所配溶液浓度偏低
D.所配制的 溶液中 为
试卷第2页,共3页二、多选题
11.设N 为阿伏加德罗常数的值,下列叙述正确的是
A
A.2.24 L 甲烷中sp3杂化轨道数为0.4 N
A
B.7.8 g 苯分子中含有电子数为4.2 N
A
C.4.6g乙醇中含有的极性键数为0.7 N
A
D.0.1 mol丙烯酸(CH=CHCOOH)含有π键数为0.1 N
2 A
三、填空题
12.(1)标准状况下,用一定量的水吸收氨气后制得浓度为12.0mol·L-1、密度为
0.915g·cm-3的氨水。试计算1体积水吸收____________体积的氨气可制得上述氨水。
(水的密度以1.00g·cm-3计)
(2) 硫铁矿高温下空气氧化产生二氧化硫:4FeS+11O = 8SO +2Fe O 设空气中N、
2 2 2 2 3 2
O 的含量分别为0.800和0.200(体积分数),试完成下列各题:
2
①1.00mol FeS 完全氧化,需要空气的体积(标准状况)为________L
2
②55L空气和足量FeS 完全反应后,气体体积(同温同压)变为________L
2
③设FeS 氧化产生的气体混合物为100L,其中O 为aL,SO 为bL。写出a和b的关
2 2 2
系式:________________________________
四、实验题
13.Ⅰ.为除去粗盐中含有的可溶性杂质硫酸盐、氯化钙和氯化镁,某同学利用给定试
剂NaOH溶液、BaCl 溶液、NaCO 溶液和盐酸,设计了如下实验流程,请回答:
2 2 3
(1)操作a和操作b的名称依次是 ____________________;
(2)加入试剂②的作用是______________________________;
(3)加入盐酸后,发生反应的离子方程式是____________________________________;
(4)在上述提纯过程中,如何证明SO 2-已经被除净
4_______________________________。
Ⅱ.实验需要0.1mol/LNaOH溶液450ml,根据溶液配制中情况回答下列问题:
(1)根据计算得知,所需NaOH的质量为__________g。
(2)配制一定物质的量浓度溶液的实验中,如果出现以下操作:A.称量用了生锈的
砝码; B.将NaOH放在纸张上称量; C.定容时仰视刻度线; D.往容量瓶转移时,
有少量液体溅出; E.未洗涤溶解NaOH的烧杯;F.容量瓶未干燥即用来配制溶液;
G.定容后塞上瓶塞反复摇匀,静置后液面不到刻度线,未加水至刻度线;H.未冷却
至室温就进行定容; I.定容时有少量水洒在容量瓶外。对配制的溶液物质的量浓度大
小可能造成的影响是(填写字母)偏大的有______________________;偏小的有
____________________________。
14.右图为实验室某浓盐酸试剂瓶上的标签,回答下列问题
(1)该浓盐酸中HCl的物质的量浓度为__________mol/L。
(2)配制240mL 0.3mol/L的盐酸溶液
A.用________mL量筒量取所需的浓盐酸的体积__________mL,沿玻璃棒倒入烧杯
中,再加入蒸馏水,用玻璃棒慢慢搅动,使其混合均匀。
B.将已冷却的盐酸沿玻璃棒注入___________mL容量瓶中。
C.用蒸馏水洗涤___________________________2—3次,洗涤液均注入容量瓶,振荡。
D.继续往容量瓶内加水直到液面接近刻度线1-2cm处,改用_________加水,使溶液
凹面恰好与刻度相切。
E.将容量瓶盖紧,振荡,摇匀。
(3)若实验中出现下列现象对所配溶液浓度有什么影响?(填偏高、偏低、无影响)
①将烧杯中溶液转移到容量瓶之前,容量瓶中有少量蒸馏水 ______________ ;
②向容量瓶中转移溶液时不慎有液滴掉在容量瓶外面,则浓度______________;
③定容时俯视容量瓶刻度线 __________________。
④洗涤量取浓盐酸后的量筒,并将洗涤液转移到容量瓶中 __________________。
(4)某同学用NaCO 配制50 mL 1.0 mol/L的NaCO 溶液的过程如图所示:
2 3 2 3
试卷第4页,共3页你认为该同学的错误步骤有______________。(填序号)
15.某兴趣小组模拟工业制漂白粉,设计了如图所示的实验装置。
已知:①氯气和碱反应放出热量②6Cl+6Ca(OH) 5CaCl +Ca(ClO)+6H O。
2 2 2 3 2 2
(1)甲装置中仪器a的名称是____。
(2)圆底烧瓶内发生反应的化学反应方程式为_____。
(3)装置乙所装溶液为____。
(4)装置丁中发生反应的化学反应方程式为____。
(5)漂白粉的有效成分为____;漂白粉的漂白原理为____(用化学方程式表示)。
(6)该小组制得的漂白粉中n(CaCl )远大于n[Ca(ClO) ],其主要原因是____。
2 2
(7)该小组使用17.4gMnO 与过量浓盐酸反应,产生的氯气在标准状况下的体积为
2
____L。参考答案:
1.C
【详解】A.因为两种溶液的密度不同,所以20%氢氧化钠溶液中氢氧化钠物质的量浓度不
是10%氢氧化钠溶液中氢氧化钠物质的量浓度的2倍, 故A不选;
B . 100mL2mol/L氯化钠溶液中c(Cl-)为:2mol/L×1=2mol/L,200mL1mol/L氯化镁溶液中
c(Cl-)为:1mol/L×2=2mol/L,氯离子浓度相同,故B不选;
C . 44g二氧化碳的物质的量为: =1mol,氧原子数为2N ,标准状况下22.4L一氧
A
化碳的物质的量为1mol,氧原子数为N ,前者刚好是后者两倍,故C选;
A
D .水的摩尔质量是相同的,都是18g/mol,故D不选;
故选C。
2.B
【详解】A、 lmolNaHSO 固体中,只有Na+ 和HSO ―两种离子,所含阴阳离子数目总数
4 4
为2N ,故A错误;B、14g分子式为C H 的链烃中含有的C-H键的数目为2N ,故B正
A n 2n A
确;C、 27g铝与lmol/L的盐酸充分反应,盐酸没给出体积,转移电子数目无法确定为
3N ,故C错误;D、NO 与NO 的转化是可逆反应,故D错误;故选B。
A 2 2 4
3.B
【详解】A.NO 与水反应方程式为3NO +H O=2HNO +NO,NO为唯一还原产物,N的化
2 2 2 3
合价由+4价变为+2价,所以3molNO 反应时转移2mol电子,故1.5molNO 参与反应转移
2 2
1mol电子即N 个,故A正确;
A
B.18g D O的物质的量为 =0.9mol,所以含有的原子数为2.7N 个,故B错误;
2 A
C.氧气和臭氧均为氧原子构成的单质,所以32g氧气和臭氧的混合物即32g氧原子,物质
的量为 =2mol,即2N ,故C正确;
A
D.0.5N 个氯气分子的物质的量为0.5mol,标况下体积为0.5mol×22.4L/mol=11.2L,故D
A
正确;
故答案为B。
4.C
【详解】同温同压下,两个容器容积相同,则气体的物质的量相同,所含的分子数相同,
又因HCl、H、Cl 都是双原子分子,故原子总数也相同;而H 和Cl 的混合气体中二者的
2 2 2 2相对含量未知,则两个容器内气体的质量、密度不一定相同,所以③④正确;
故选C。
5.D
【详解】①摩尔是物质的量的单位,①错误;
②二氧化硫的摩尔质量是64 g/mol,②错误;
③CO和C H 的相对分子质量相等,所以质量相等,密度不等的CO和C H 的物质的量相
2 4 2 4
等,则二者所含的分子数也相等,③正确;
④Na相对原子质量是23,1 molNa原子质量是23 g,含有约6.02×1023个个Na原子,则一
个钠原子的质量约等于 g,④正确;
⑤标准状况下,HO不是气态,因此不能使用气体摩尔体积进行有关计算,⑤错误;
2
⑥常温常压下气体摩尔体积大于22.4 L/mol,则11.2 LCH 的物质的量小于0.5 mol,故其中
4
含有的原子数小于为1.505×1024个,⑥错误
⑦标准状况下气体摩尔体积为22.4 L/mol,则根据阿伏伽德罗定律可知1 mol H 和N 的混
2 2
合气体在标准状况下的体积约为22.4 L,⑦正确;
⑧常温常压下,22 g CO 的物质的量是0.5 mol,则其中含有的原子的物质的量为3×0.5
2
mol=1.5 mol,⑧正确;
综上所述可知:说法正确的是③④⑦⑧,故合理选项是D。
6.B
【详解】A.气体的体积取决于温度和压强的大小,在标准状况下,V =22.4L/mol,在其
m
它条件下,1mol气体的体积不一定为22.4L,A错误;
B.根据n= = ,同温同压下两种气体,气体的分子个数与体积呈正比,B正确;
C.在标准状况下,只有体积为22.4L的气体物质才是1mol,其它状态的物质的
V ≠22.4L/mol,C错误;
m
D.根据PV=nRT可知,并不是只有在标准状况下V =22.4L/mol,V 取决于温度和压强的
m m
大小,D错误;
答案选B。
【点晴】本题考查阿伏加德罗定律及其推论,本题注意阿伏加德罗定律只适用于气体,另
外在标准状况下,V =22.4L/mol,其它条件下也有可能为22.4L/moL。解答时注意灵活应
m
答案第2页,共2页用。
7.D
【详解】A.0.5mol/L H SO 溶液50mL,阴离子的总浓度为0.5mol•L-1;
2 4
B.0.5 mol·L-1 CaCl 溶液35mL,阴离子浓度为1.0mol•L-1;
2
C.0.5mol/L NaCl溶液70mL,阴离子浓度为0.5mol•L-1;
D.0.5 mol·L-1 Al (NO) 溶液60mL,阴离子总浓度为1.5mol/L;
3 3
则阴离子浓度最大的为D,故选D。
8.B
【分析】50.0mLlmol•L-1MgCl 溶液中的Cl-浓度为1mol/L×2=2mol/L,结合物质的浓度和组
2
成分析解答。
【详解】A、100mL1.0mol•L-1NaCl溶液中氯离子的浓度为1mol/L,与题意不符,A错误;
B、100mL1.0mol•L-1CaCl 溶液中氯离子的浓度为1mol/L×2=2mol/L,与题意相符,B正确;
2
C、50mL2.0mol·L-1BaCl 溶液中氯离子的浓度为2mol/L×2=4mol/L,与题意不符,C错误;
2
D、50mL2mol•L-1A1C1 溶液中氯离子的浓度为2mol/L×3=6mol/L,与题意不符,D错误;
3
答案选B。
【点睛】本题考查了溶液中离子浓度的计算,明确溶液中离子的浓度=溶质的物质的量浓度
×化学式中离子个数是解本题的关键,与溶液体积无关。
9.B
【详解】A.22.4L HCl气体的物质的量为 ,若形成溶液的体积为
100mL,则浓度为10mol/L,但溶液的体积不等于溶剂的体积100mL,故A错误;
B.由于没有提供溶液的密度,无法计算出溶液的体积,因此该溶液的物质的量浓度无法
计算,故B正确;
C.液体积不等于溶剂的体积与溶质的体积之和,溶液的体积远远小于HCl体积,故C错
误;
D.22.4L(标准状况下)HCl的物质的量 ,溶质的质量为
m=nM=1mol×36.5 g/mol=36.5g,溶液质量为36.5g+100 mL×1 g/mL=136.5 g,溶质的质量分数为 ,所以不知溶液的密度可求溶质的质量分数,故D错误;
故选:B。
10.C
【详解】A.溶解得到的溶液及洗涤烧杯2~3次的洗涤液均需转移到容量瓶中,保证溶质
完全转移,A项正确;
B.向容量瓶中转移溶液时用玻璃棒引流,B项正确;
C.定容时若俯视刻度线,水的量不足,溶液体积减小,造成所配溶液浓度偏大,C项错误;
D.碳酸钠的质量为10.6g, ,容量瓶规格为100mL, 溶液的物
质的量浓度为 , ,D项正确;
答案选C。
11.BC
【详解】A.没有指明温度和压强,无法计算2.24 L 甲烷中sp3杂化轨道数,故A错误;
B.7.8 g 苯的物质的量为0.1mol,1个苯分子中含有42个电子,则0.1mol苯中含有的电子
数为4.2 N ,故B正确;
A
C.4.6g乙醇为0.1mol,1个乙醇分子中含有6个C-H键,1个O-H键,1个C-C键,C-H
和O-H是极性键,即1个乙醇分子中含有7个极性键,所以0.1mol乙醇中含有的极性键数
为0.7 N ,故C正确;
A
D.丙烯酸中有碳碳双键和碳氧双键,所以1个丙烯酸分子中含有2个π键,则0.1 mol丙
烯酸(CH=CHCOOH)含有π键数为0.2 N ,故D错误;
2 A
故选BC。
12. 378 308 52 13b=200-10a
【分析】(1)假设溶液体积为1.00L,根据n(NH )=c(NH )×V,求出1L溶液中所含
3 3
氨气的物质的量,求出标准状况下氨气的体积;根据水的质量=氨水的质量-氨气的质量,
求出水的质量,进而求出水的体积;由V(NH/V(H O)求出1体积水所吸收氨气的体积。
3 2
(2)①根据方程式计算需要氧气的物质的量,再根据V=nV 氧气的体积,根据空气中氧
m
气的体积分数计算需要空气的体积;
②计算空气中氧气的体积,利用差量法计算反应后气体体积变化,据此解答;
③根据二氧化硫的体积计算参加反应氧气体积,表示出氮气的体积,利用氮气体积不变列
答案第4页,共2页关系式解答;
【详解】(1)假设溶液体积为1.00L,1.00L该氨水含氨的物质的量为1.00L×12.0mol/
L=12.0mol,V(NH )=12.0mol×22.4L/mol=268.8L;1.00L该氨水中含水的质量m(HO)=1
3 2
12 =711g,V(H O)= L=0.711L;标准状况下,1体积水吸收氨气的体
2
积为V(H )=(268L/0.711L) 1L=378L,本题答案为:378
2
(2)①根据方程式4FeS+11O =8SO+2Fe O 可以知道,1.00molFeS 完全氧化需要氧气物
2 2 2 2 3 2
质的量=11/4mol,故需要空气的体积= =308L,因此,本题答案为:308;
②55L空气中氧气的体积=55L×0.2=11L,则:4FeS+11O =8SO+2Fe O
2 2 2 2 3
11 8 V = 11-8=3
故反应后气体的体积为55L-3L=52L,因此△,本题正确答案是:52;
③4FeS +11O =8SO+2Fe O
2 2 2 2 3
11 8
( 11/8 )b b
反应前后氮气的体积不变,则:(aL+ bL) 4=100L-aL-bL,整理可得:13b=200-10a,
因此,本题答案是:13b=200-10a。
13. 过滤、蒸发 除去钙离子和钡离子 CO2-+2 H+= CO+
3 2
HO OH -+ H+= HO 取少量A溶液于试管中,滴加BaCl 溶液若出现浑浊或白色沉淀,
2 2 2
说明溶液中含有硫酸根,否则不含硫酸根 2.0 g AH BCDE
【分析】Ⅰ.根据实验流程可知,操作a过滤,操作b是蒸发;根据加入氢氧化钠可将氯化
镁转化成氢氧化镁沉淀,除去硫酸钠需要在除去氯化钙之前,加入的碳酸钠可以将过量的
氯化钡除去,所以试剂①是BaCl 溶液,目的是除去SO 2-离子,试剂②是NaCO 溶液,目
2 4 2 3
的是除尽溶液的离子Ba2+、Ca2+,根据加入的除杂试剂氢氧化钠和碳酸钠都是过量的,所
以在蒸发之前需要加入盐酸将碳酸钠和氢氧化钠除去。
Ⅱ.根据n=cv计算氢氧化钠的物质的量,再根据m=nM计算所需氢氧化钠的质量;根据
C=n/V
,通过判断不当操作对溶质的物质的量n和溶液体积V的影响来分析误差。
【详解】Ⅰ.(1)通过分析实验流程可知,操作a是溶解,操作b是过滤,操作c是蒸发,故答案为过滤;蒸发;
(2)试剂②是NaCO 溶液,目的是除尽溶液的离子Ba2+、Ca2+,故答案为除去钙离子和钡
2 3
离子;
(3)加入盐酸的目的是将碳酸钠和氢氧化钠除去,反应的离子方程式为OH -+ H+=H O,
2
CO2-+2H+=CO +H O,故答案为OH-+H+=H O;CO2-+2H+= CO+H O;
3 2 2 2 3 2 2
(4)证明SO 2-已经被除净,即证明溶液中不存在SO 2-离子,具体操作为:取少量A溶液
4 4
于试管中,滴加BaCl 溶液若出现浑浊或白色沉淀,说明溶液中含有硫酸根,否则不含硫
2
酸根,故答案为取少量A溶液于试管中,滴加BaCl 溶液若出现浑浊或白色沉淀,说明溶
2
液中含有硫酸根,否则不含硫酸根;
Ⅱ.(1)由于无450ml的容量瓶,故选用500ml的容量瓶,故配制的是500ml0.1mol/LNaOH
溶液,根据n=CV可知需要的NaOH的物质的量n=0.5L×0.1mol/L=0.05mol,NaOH质量
m=nM=0.05mol×40g/mol=2.0g,故答案为2.0g;
(2)A、生锈的砝码质量偏大,而m =m +m ,故称量出的药品的质量偏重,则配制出
物 砝 游
的溶液的浓度偏大;
B、将NaOH放在纸张上称量会潮解,导致真正的NaOH的质量偏小,则配制出的溶液的
浓度偏小;
C、定容时俯视刻度线观察液面,所加水量偏少,结果偏高;
D、往容量瓶转移时,有少量液体溅出,会导致溶质的损失,则溶液浓度偏小;
E、未洗涤溶解NaOH的烧杯,会导致溶质的损失,则溶液浓度偏小;
F、只要最后定容时凹液面与刻度线相切即可,至于水是事先就有的还是后来加入的,对浓
度无影响;
G、定容后塞上瓶塞反复摇匀,静置后,液面不到刻度线是正常的,未加水对浓度无影响;
H、热溶液注入容量瓶会导致容量瓶热膨胀,体积变大,最终导致溶液浓度偏小;
I、滴管加水时,有少量水滴到容量瓶外,溶液的体积不变,浓度不变。
故答案为AH;BCDE。
14. 12 10 6.3 250 烧杯、玻璃棒 胶头滴管 无影
响 偏低 偏高 偏高 ①②⑤
【详解】(1) = =12mol/L;(2)配制240mL 0.3mol/L的盐酸溶液,
需要250ml容量瓶,则250mL ×0.3mol/L==12mol/L×V,V=6.25mL,所以需要10mL的同筒
量取浓度为12mol/L的盐酸6.3mol,按物质的量浓度配制的操作要求进行正确操作;(3)
答案第6页,共2页①将烧杯中溶液转移到容量瓶之前,容量瓶中有少量蒸馏水,对配制溶液的浓度没有影响;
②向容量瓶中转移溶液时不慎有液滴掉在容量瓶外面,溶质减少,则浓度偏低;③定容时
俯视容量瓶刻度线,加水的体积减少,溶液体积减小,浓度偏高;④洗涤量取浓盐酸后的
量筒,并将洗涤液转移到容量瓶中,溶质增大,浓度偏高。(4)配制50 mL 1.0 mol/L的
NaCO 溶液,①中碳酸钠直接放在托盘上称量,②中量取了100mL水溶液碳酸钠,①②错
2 3
误;定容时眼睛视线要平视而不是仰视,⑤错误。
15.(1)分液漏斗
(2)
(3)饱和食盐水
(4)Cl +2NaOH=NaCl+NaClO+H O
2 2
(5) Ca(ClO) ##次氯酸钙 Ca(ClO) +CO +H O=CaCO +2HClO
2 2 2 2 3
(6)氯气和碱反应会放出热量,导致温度升高,发生了副反应
(7)4.48
【分析】模拟工业制漂白粉:装置A制取 ,a为分液漏斗,可以控制加入的浓盐酸,圆
底烧瓶中盛放二氧化锰,反应的方程式为: ,
HCl易挥发,制得的氯气中含有氯化氢,可以用食盐水来除杂,乙装置除去氯气中的氯化
氢,丙装置 与 的反应制漂白粉, 有毒,需进行尾气处理,装置丁吸收多余
的氯气。
(1)
)甲装置中仪器a具有球形特征,有玻璃活塞,在该实验中,可以控制加入的浓盐酸,为分
液漏斗,故答案为:分液漏斗;
(2)
浓盐酸和二氧化锰反应过程中会发出氯化氢气体,反应的方程式为;
(3)
生成氯气中含有挥发出的氯化氢气体,氯化氢在饱和食盐水中易溶,而氯气难溶,通过饱
和食盐水的作用是除去 中混有的HCl气体;故装置乙所装溶液为饱和食盐水;
(4)
装置丁中氢氧化钠可以吸收氯气生成氯化钠、次氯酸钠,防止污染空气,发生反应
Cl+2NaOH=NaCl+NaClO+H O;
2 2
(5)
漂白粉有效成分为次氯酸钙,次氯酸钙与空气中的水、 作用生成具有漂白性的HClO
和碳酸钙,所以反应的化学方程式为Ca(ClO) +CO +H O=CaCO +2HClO;
2 2 2 3
(6)
已知:①氯气和碱反应放出热量②6Cl+6Ca(OH) 5CaCl +Ca(ClO)+6H O。氯气和碱反
2 2 2 3 2 2
应会放出热量,温度升高,当温度高时,发生了副反应,导致制得的漂白粉中 远
大于 ;
(7)
17.4gMnO 的物质的量为17.4g÷87g/mol=0.2mol,由化学方程式体现的量的关系可知,
2
=0.2mol,则产生的氯气在标准状况下的体积为
。
答案第8页,共2页