文档内容
第三单元 金属材料
第2课 金属材料(一)
一、基础巩固
1.下列关于铝及其化合物说法,不正确的是( )
A.不能用铝制容器腌咸菜,因为铝单质会和较浓的Cl﹣发生络合反应
B.铝热反应过程会放出大量的热,这说明构成氧化铝的微粒间存在着强烈的作用力
C.氢氧化铝不溶于过量氨水,但氢氧化铜、氢氧化银沉淀都溶于过量氨水
D.刚玉是一种高硬度、高熔点的化合物,刚玉坩埚不能用来熔融纯碱
2.既能与酸(H+)反应,又能与碱(OH﹣)反应的化合物是( )
①MgO②Al(OH) ③NaHSO ④NaHCO ⑤CH COONH ⑥Al
3 4 3 3 4
A.②④ B.②③④ C.②④⑤ D.②④⑤⑥
3.用高铁酸钠(Na FeO )处理河流湖泊的水用于饮用,是一项较新的技术,与此有关的以下叙述中,正
2 4
确的是( )
①高铁酸钠溶液有强酸性②高铁酸钠有强氧化性③高铁酸钠可使水软化④该过程中水被消毒和净化
A.①③ B.②④ C.①② D.③④
4.28g CO气体在1mol的氧气中燃烧后,所得的气体通过足量Na O 固体中充分反应后,下列说法不正确
2 2
的是( )
A.CO与氧气反应,只消耗了0.5mol氧气
B.充分反应后Na O 固体质量增加了28 g
2 2
C.通过以上两步反应后余下氧气物质的量为0.5mol
D.若2gH 替代 28g的CO发生上述反应,则Na O 固体质量增加了2g
2 2 2
5.生铁的熔点是1100~1200℃,则纯铁的熔点可能是( )
A.1085℃ B.1160℃ C.1200℃ D.1535℃
6.下列说法错误的是( )
A.越王勾践剑的铸造材料主要是铜锡合金
B.青花瓷的制作原料的主要成分是硅酸盐C.以毛竹为原料制作的竹纤维属于高分子材料
D.石墨烯是一种能导电的有机高分子材料
7. 钠、铝和铁是三种重要的金属,回答问题:
(1)三种金属中,既能与盐酸反应又能与NaOH溶液反应 (填化学式),写出它与NaOH溶
液反应的离子方程式
(2)三种金属在一定条件下均能与水发生反应。写出铁与水蒸气反应的化学方程式 。取一小
块金属钠放入滴有酚酞的水中,可观察到的实验现象是 。(填字母序号)。
①钠浮在水面迅速反应②钠沉在水底迅速反应 ③钠熔成小球并迅速游动④反应中可以听到嘶嘶的响声
⑤反应后的溶液变为红色
A.①④⑤B.②③④⑤C.①③④⑤
二、拓展提升
8.(1)标准状况下,用一定量的水吸收氨气后制得浓度为 12.0mol/L、密度为0.915g/cm3的氨水。试计
算1体积水吸收 体积的氨气可制得上述氨水。(水的密度以1.00g/cm3计)
(2)硫铁矿高温下空气氧化产生二氧化硫:4FeS +11O 8SO +2Fe O 设空气中N 、O 的含量
2 2 2 2 3 2 2
分别为0.800和0.200(体积分数),试完成下列各题:
①1.00mol FeS 完全氧化,需要空气的体积(标准状况)为 L。
2
②55L空气和足量FeS 完全反应后,气体体积(同温同压)变为 L。
2
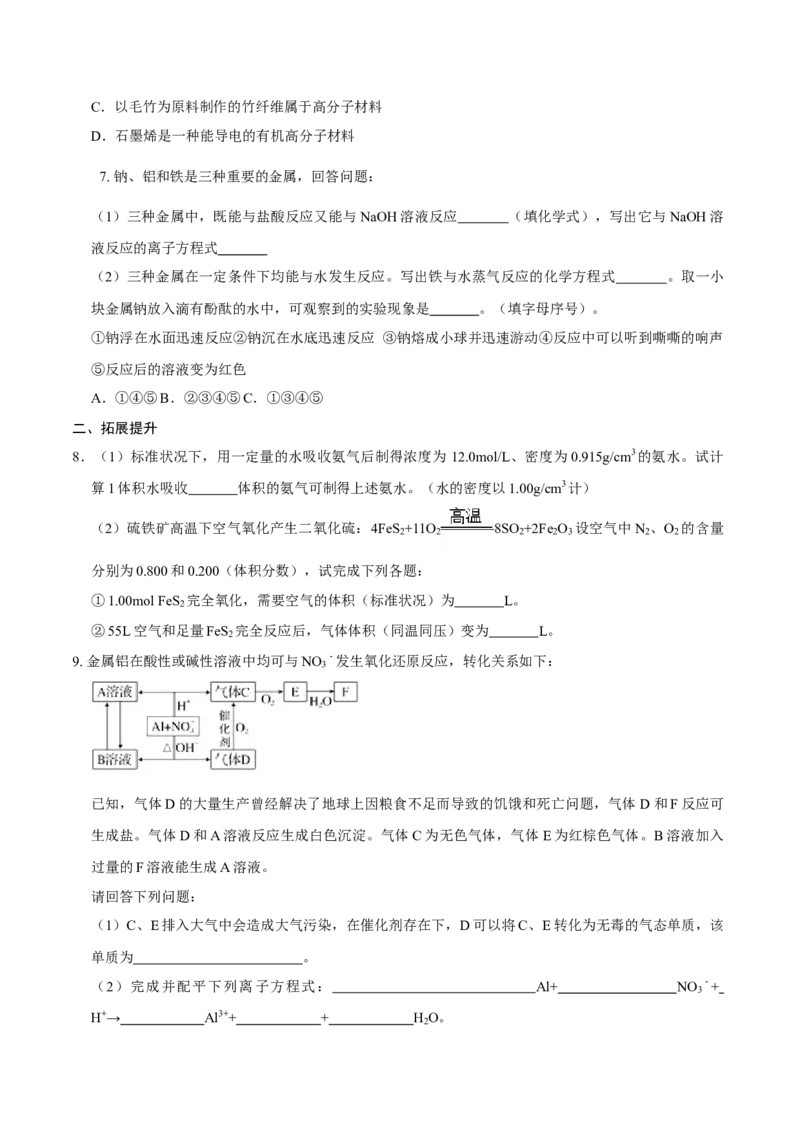
9. 金属铝在酸性或碱性溶液中均可与NO ﹣发生氧化还原反应,转化关系如下:
3
已知,气体D的大量生产曾经解决了地球上因粮食不足而导致的饥饿和死亡问题,气体D和F反应可
生成盐。气体D和A溶液反应生成白色沉淀。气体C为无色气体,气体E为红棕色气体。B溶液加入
过量的F溶液能生成A溶液。
请回答下列问题:
(1)C、E排入大气中会造成大气污染,在催化剂存在下,D可以将C、E转化为无毒的气态单质,该
单质为 。
(2)完成并配平下列离子方程式: Al+ NO ﹣+
3
H+→ Al3++ + H O。
2(3)D→C反应的化学方程式是 。
(4)除去气体C中的杂质气体E的化学方法: (用化学方程式表示)。
10. 动手实践:某同学探究同周期元素性质递变规律实验时,自己设计了一套实验方案,并记录了有关实
验现象(见下表,表中的“实验步骤”与“实验现象”前后不一定是对应关系)。
实验步骤 实验现象
①将镁条用砂纸打磨后,放入试管中,加 A.浮在水面上,熔成小球,四处游
入少量水后,加热至水沸腾;再向溶液中 动,发出“嘶嘶”声,随之消失,溶液
滴加酚酞溶液 变成红色
②向新制的Na S溶液中滴加新制的氯水 B.有气体产生,溶液变成浅红色
2
③将一小块金属钠放入滴有酚酞溶液的冷 C.剧烈反应,迅速产生大量无色气体
水中
④将镁条投入稀盐酸中 D.反应不十分剧烈;产生无色气体
⑤将铝条投入稀盐酸中 E.生成白色胶状沉淀,继而沉淀消失
⑥向AlCl 溶液中滴加NaOH溶液至过量 F.生成淡黄色沉淀
3
请你帮助该同学整理并完成实验报告。
(1)实验目的:研究 元素性质递变规律。
(2)实验用品:
试剂:金属钠,镁条,铝条,稀盐酸,新制氯水,新制Na S溶液,AlCl 溶液,NaOH溶液,酚酞溶液
2 3
等。
仪器:① ,② ,③ ,
试管夹,胶头滴管,镊子,小刀,玻璃片,砂纸,火柴等。
(3)实验内容:(填写与实验步骤对应的实验现象的编号和①②的化学方程式)
实验内容 ① ② ③ ④ ⑤ ⑥
实验现象(填A~F)
①的化学方程式 ,
②的化学方程式 。
(4)实验结论:
失电子能力: ,得电子能力: 。