文档内容
巴蜀中学 2024 届高考适应性月考卷(六)
化学参考答案
一、选择题:本题共14小题,每小题3分。
题号 1 2 3 4 5 6 7
答案 A C A B C C D
题号 8 9 10 11 12 13 14
答案 D D B A D C B
【解析】
1.A项,富勒烯是碳单质。
2.A项,CO不会导致温室效应。B项,SO 不能用来漂白。D项,ClO 不是酸性氧化物。
3 2
3.B项,铁片钝化生成致密氧化膜。C项,H S不拆。D项,发生氧化还原,不发生复分解。
2
4.B项,HF标况下是液态。
5.A项,试管口应该朝下。B项,长管进短管出。D项,不能得到纯净的氯仿。
6.Z是Li,从而X、Y一定是H和He,W就是S。C项,Li是同周期原子半径最大的。
7.A 项,含有的官能团是酯基和羟基。B 项,酚酞没有手性碳原子。C 项,不能发生消除
反应。
8.A 项,可能有乙醇挥发出来也能使酸性高锰酸钾褪色。B 项,银镜反应之前需要加碱。C
项,Cl 没有漂白性,有漂白性的是HClO。
2
9.配合物是中性分子,而镍离子是二价阳离子,所以两个丁二酮肟各解离出一个氢离子形成
负一价阴离子。A 项,由于失去了一个氢离子,所以分子式为 C H N O 。B 项,四个 N
4 8 2 2
位于Ni的同一平面,所以不可能是sp3杂化。C项,丁二酮肟只有在与水形成氢键时才会
增大溶解度,分子间形成氢键会减低溶解度。
10.B项,当Ca2+放在顶点时,O2−在面心,Ti4+在体心。
11.A项,Pb是氢前金属,能与酸反应生成铅离子和氢气。
12.电池工作时,左侧紫色变绿色是氧化反应,左侧是负极,右侧是正极。A项,右侧还原反
应,黄色变蓝色。B 项,充电过程左侧正电荷变少,右侧正电荷变多,H+从右向左移动
从而平衡电荷。C 项,电解产生 1mol Cl 时,转移 2mol 电子,左侧增加 2mol 正电荷,
2
所以2mol H+从左向右移动,左室质量减少2g。
13.由图可知,K = 10−4.2,K = 10−5.6,说明HA-的电离大于水解。C项,当溶液中HA-和
a1 a2
A2−浓度相等时,溶液显酸性,若使溶液显中性,则需要再加入 NaOH,从而 A2−比 HA-
浓度大。
化学参考答案·第1页(共4页)
{#{QQABSYgAogigAhBAAQgCAwUKCEOQkBAACAoGhAAMMAAByAFABAA=}#}14.A项,如图所示x是0.5和1.5时,x是1.5时H 的平衡转化率要大。B项,列三段法计
2
7 13
算,需要开方,然后解一个一元二次方程,最后结果为 ,约等于 56.7%,C 项,
6
0.7320.2 4.2680.2
列三段法计算,最后转化为比较两个数字的大小, 与 比大小,
10.7320.6 14.2680.6
第一种方法是暴力算,能算出来后者大,第二种方法是如果不考虑分母中的1,则二者都
1
是 ,分母加 1 对前者的影响更大,所以前者小,第三种方法是抽象成一个函数
3
0.2x
f(x) ,易证这个函数在(0, +∞)单调递增,则后者大于前者。D项,由于反
10.6x
应物和生成物气体系数和相等,所以HI的平衡转化率一直不变。
二、非选择题:本题共4小题,共58分。
15.(除特殊标注外,每空2分,共14分)
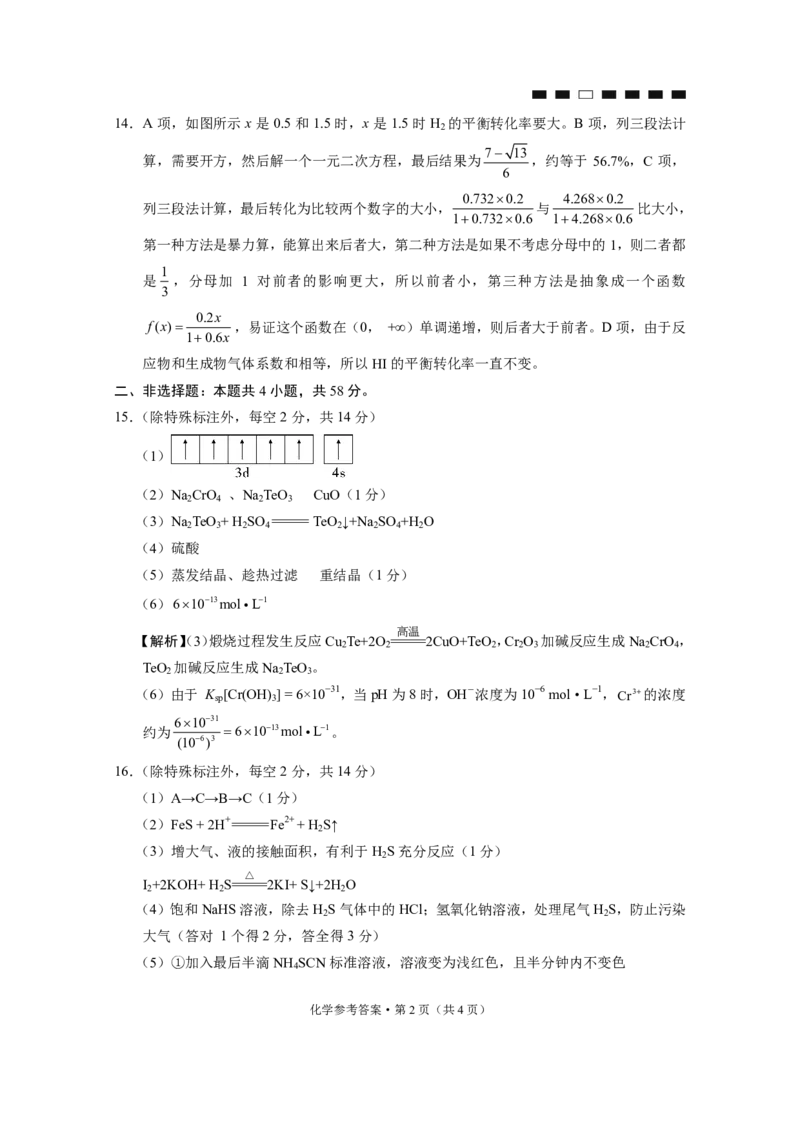
(1)
(2)Na CrO 、Na TeO CuO(1分)
2 4 2 3
(3)Na TeO + H SO = TeO ↓+Na SO +H O
2 3 2 4 2 2 4 2
(4)硫酸
(5)蒸发结晶、趁热过滤 重结晶(1分)
(6)61013molL1
高温
【解析】(3)煅烧过程发生反应Cu Te+2O =====2CuO+TeO ,Cr O 加碱反应生成Na CrO ,
2 2 2 2 3 2 4
TeO 加碱反应生成Na TeO 。
2 2 3
(6)由于 K [Cr(OH) ] = 6×10−31,当pH为8时,OH-浓度为10−6 mol·L−1,Cr3的浓度
sp 3
61031
约为 61013molL1。
(106)3
16.(除特殊标注外,每空2分,共14分)
(1)A→C→B→C(1分)
(2)FeS + 2H+=Fe2+ + H S↑
2
(3)增大气、液的接触面积,有利于H S充分反应(1分)
2
△
I +2KOH+ H S=====2KI+ S↓+2H O
2 2 2
(4)饱和NaHS溶液,除去H S气体中的HCl;氢氧化钠溶液,处理尾气H S,防止污染
2 2
大气(答对 1个得2分,答全得3分)
(5)①加入最后半滴NH SCN标准溶液,溶液变为浅红色,且半分钟内不变色
4
化学参考答案·第2页(共4页)
{#{QQABSYgAogigAhBAAQgCAwUKCEOQkBAACAoGhAAMMAAByAFABAA=}#}② 72.6%
③偏低(1分)
【解析】(4)A 装置制备 H S,通过 C 装置除去 H S 中的 HCl,再进入 B 装置制取 KI,
2 2
最后用C装置处理尾气。所以第一次用C装置盛装饱和NaHS溶液除去H S中的HCl,
2
第二次用C装置盛装氢氧化钠溶液处理尾气H S。
2
(5)①滴定终点时 Ag+反应完,加入的 NH SCN 与 Fe3+反应,溶液呈浅红色,所以滴定
4
终点现象为加入最后半滴NH SCN标准溶液,溶液变为浅红色,且半分钟内不变色;
4
②消耗NH SCN溶液体积平均为12.50mL,根据Ag++SCN-=AgSCN↓可知与I-反应
4
后剩余的 n(Ag+)=0.01250L×0.1000mol/L=0.00125mol,则和 I-反应的银离子的物质的量
=0.0300L×0.1000mol/L−0.00125mol=0.00175mol,则20.00mL待测液中n(I-)=0.00175mol,
0.001755(39127)
所以样品中KI的含量为 100%72.6%。
2
③若滴定前酸式滴定管未用标准液润洗,则标准液浓度减小,滴定所耗 NH SCN 标准溶
4
液体积增大,计算出的I-的物质的量减小,从而导致结果偏低。
17.(除特殊标注外,每空2分,共15分)
(1)液氨可以用作制冷剂(1分)
(2)①温度(1分) 在该温度条件下催化剂的活性高
②NH 浓度较大时,占据催化剂表面更多活性位点,阻碍N 的吸附 液化分离(1分)
3 2
(3)①p (1分) 75%
1
② 4.63
(4)①sp3(1分)
【解析】(3)①该反应前后为气体总物质的量减小的反应,当温度不变时,增大压强,平
衡正向移动,氨气的体积分数增大,故压强p、p、p 中,最大的是p 。n(N )∶n(H )=1∶3,
1 2 3 1 2 2
设n(N )=1mol,n(H )=3mol,用三段式可计算得 A点N 的平衡转化率为75%。
2 2 2
②设n (N ) = 1mol,n (H ) = 3mol,已知N 平衡转化率α=30%,列三段式
初 2 初 2 2
N (g) + 3H (g) = 2NH (g)
2 2 3
n /mol 1 3 0
初
Δn/mol 0.3 0.9 0.6
n /mol 0.7 2.1 0.6
平
7 21 6
p 平 p p p
34 总 34 总 34 总
化学参考答案·第3页(共4页)
{#{QQABSYgAogigAhBAAQgCAwUKCEOQkBAACAoGhAAMMAAByAFABAA=}#} 6 2
p
34 总
K 0.03MPa2,解得 p =4.63MPa。
p 7 21 3 总
p p
34 总 34 总
18.(除特殊标注外,每空2分,共15分)
(1)C H NO (1分)
11 11 2
(2)羧基(1分) 还原反应(1分)
(3)
(4)与HCl反应,有利于平衡正向移动
(5)酯基中碳氧元素间电负性差值大,极性强,容易断裂,形成酰胺比较容易;羧基中
氧氢元素间电负性差值最大,比碳氧键更容易断裂,易形成铵盐
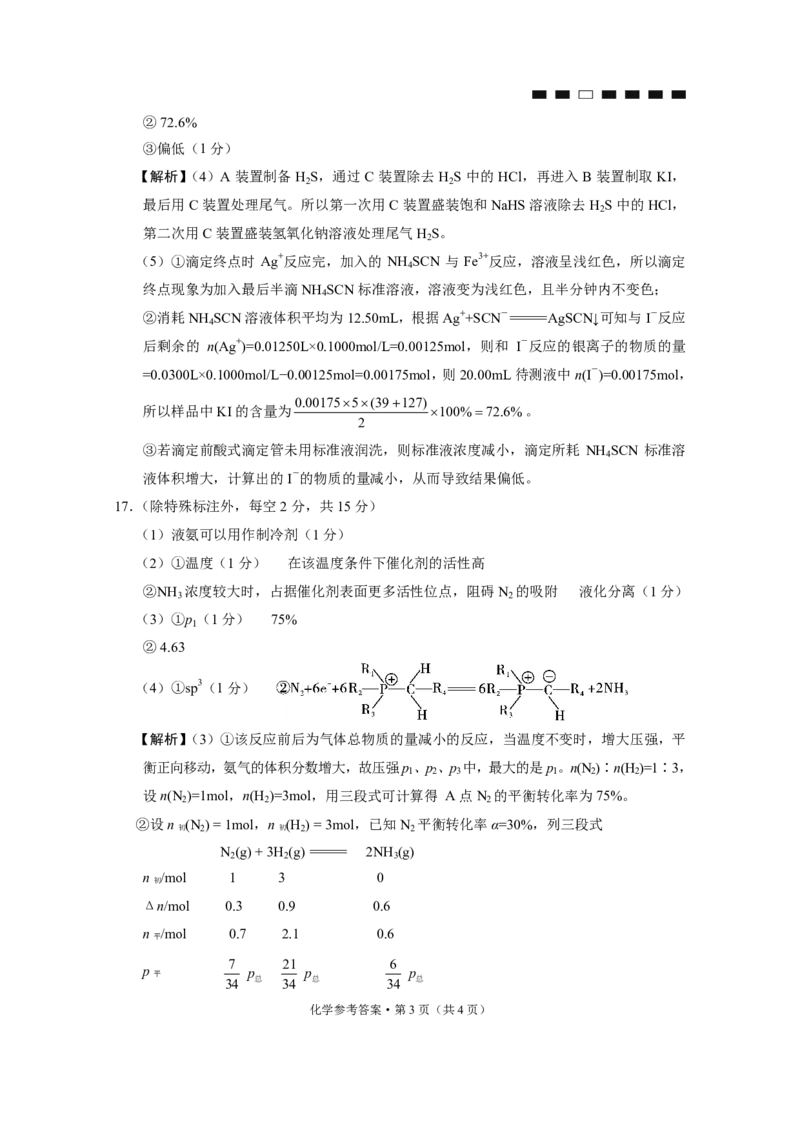
(6)① ②形成了更大范围的共轭体系,能量更低
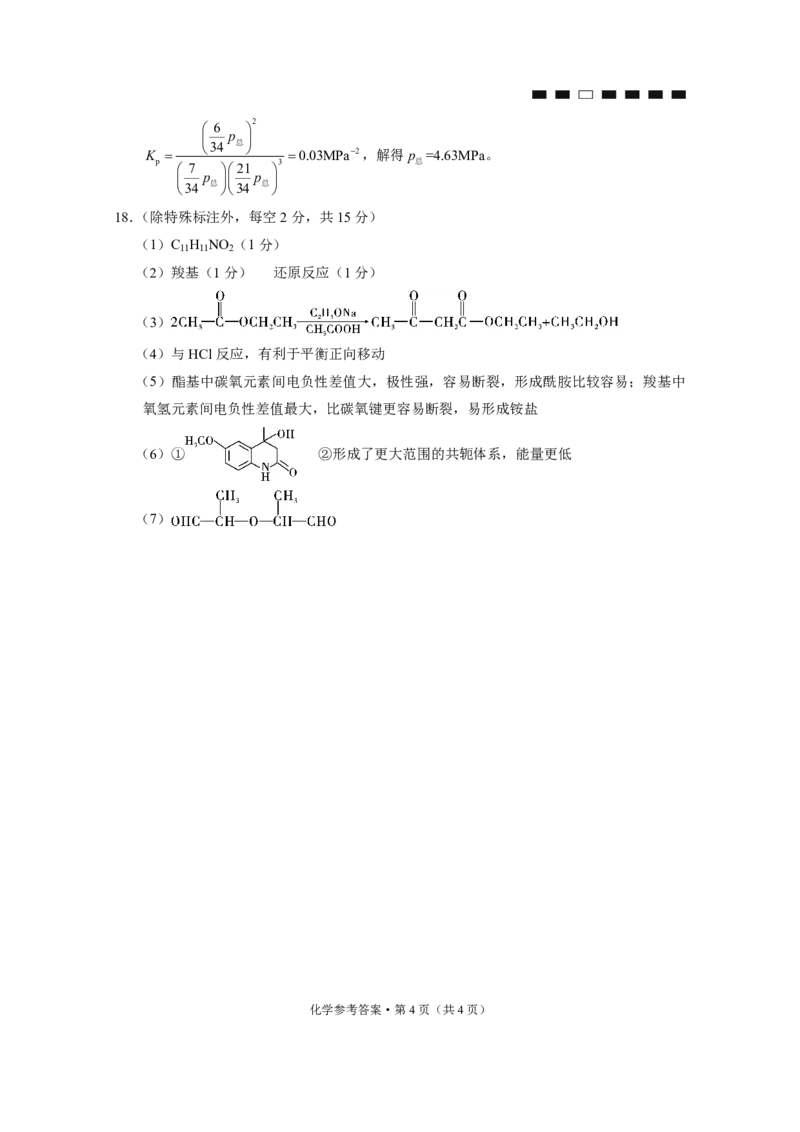
(7)
化学参考答案·第4页(共4页)
{#{QQABSYgAogigAhBAAQgCAwUKCEOQkBAACAoGhAAMMAAByAFABAA=}#}