文档内容
2022--2023学年必修第二册人教版第5章第二节 氮及其化
合物 课时1氮气和氮的氧化物
学校:___________姓名:___________班级:___________考号:___________
一、单选题
1.下列气体中,对人体无毒的气体是( )
A.SO B.N C.NO D.CO
2 2
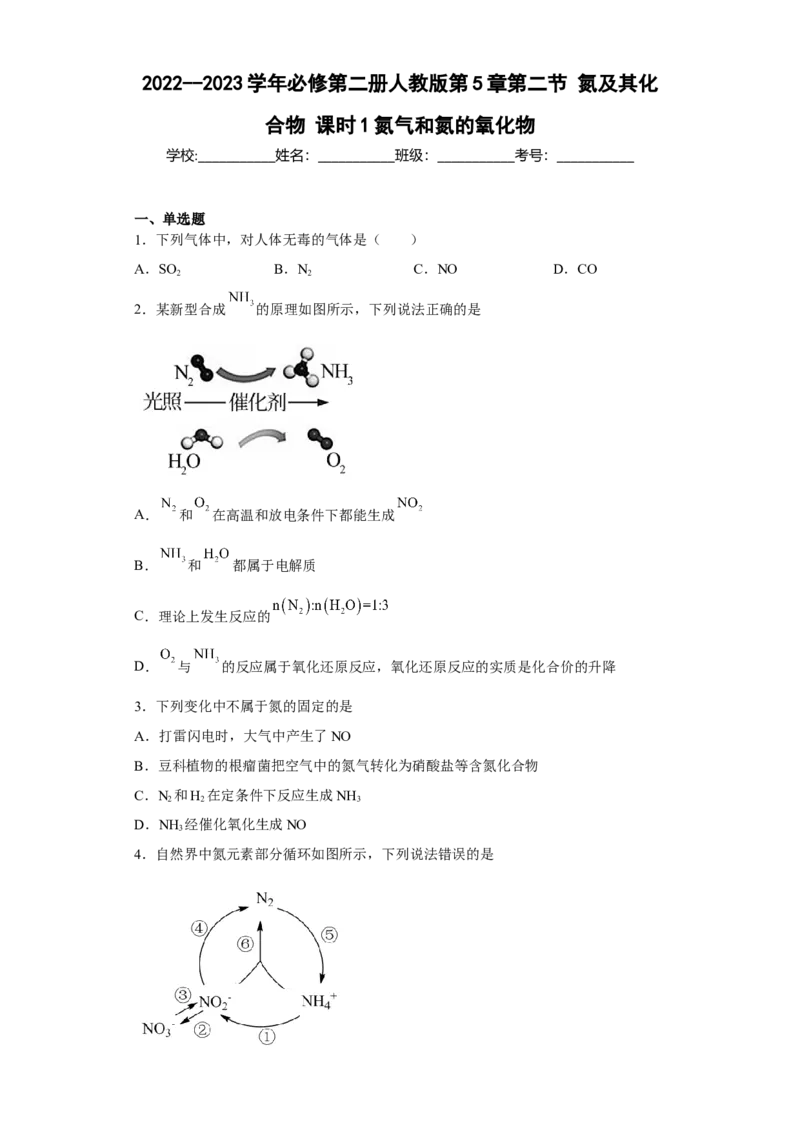
2.某新型合成 的原理如图所示,下列说法正确的是
A. 和 在高温和放电条件下都能生成
B. 和 都属于电解质
C.理论上发生反应的
D. 与 的反应属于氧化还原反应,氧化还原反应的实质是化合价的升降
3.下列变化中不属于氮的固定的是
A.打雷闪电时,大气中产生了NO
B.豆科植物的根瘤菌把空气中的氮气转化为硝酸盐等含氮化合物
C.N 和H 在定条件下反应生成NH
2 2 3
D.NH 经催化氧化生成NO
3
4.自然界中氮元素部分循环如图所示,下列说法错误的是A.反应①~⑥均属于氧化还原反应
B.反应①②⑤均属于氮的固定
C.反应⑥的离子方程式为NH +NO =N ↑+2H O
2 2
D.向水体中大量排放NH 及NO 能引起水质恶化
5.下列关于N 的叙述错误的是
2
A.N 既可作氧化剂又可作还原剂
2
B.雷雨天,空气中的N 和O 可反应生成NO
2 2
C.氮的固定是将N 转化成含氮化合物的过程
2
D.氮气的化学性质比较活泼,通常情况下可以与很多物质发生反应
6.为使天更蓝,空气质量更好,火力发电厂采用了脱硫和脱硝(氮)。脱硝是除去煤
燃烧过程中产生的
A.NH NO B.N C.NO D.NH
4 3 2 x 3
7.下列说法错误的是
A.安装燃煤“固硫”装置,可以降低酸雨发生率
B.氮的固定只有在高温、高压、催化剂的条件下才能实现
C.研发易降解塑料,防止白色污染
D.日用铝制品表面覆盖着氧化膜,对内部金属起保护作用
8.N、O、Si、S是重要的非金属元素。下列说法正确的是
A.N、O、S、Si的原子半径逐渐增大,非金属性逐渐减弱
B.氮的氧化物和硫的氧化物既是形成光化学烟雾的主要物质,又是形成酸雨的主要物
质
C.汽车尾气中排放的氮氧化物主要是由游离态氮转化来的
D.N、Si、S的单质均能和氧气反应,生成的产物分别是NO 、SiO 和SO
2 2 2
9.研究氮及其化合物的性质,可以有效改善人类的生存环境。氮元素化合价---物质类
别关系图如下,图中a、b、c和d分别代表一种含氮化合物。
试卷第2页,共3页下列说法中正确的是
A.a催化氧化可以生成b
B.从化合价角度分析,a与b能发生氧化还原反应。
C.从物质类别角度分析,d可以和a、b、c发生反应
D. 转化过程中物质类别和化合价均发生变化
10.按下图进行实验,试管内装有12mL NO,然后间歇而缓慢地通入8 mLO,下面有
2
关实验最终状态的描述正确的是
A.试管内气体呈红棕色 B.试管内气体为无色是NO
C.试管内气体为无色是O D.试管内液面上升至充满整个试管
2
11.下列说法正确的是
A.pH=6的降雨是酸雨
B.氯气泄漏后应顺风向低处跑
C.把饱和FeCl 溶液滴加到NaOH溶液中,用来制备Fe(OH) 胶体
3 3
D.我国城市环境中的大气污染物主要有SO 、NO 、CO、可吸入颗粒物等
2 2
12.海水中的各种元素氯、钠、钙、镁、硫、溴主要存在形式是
A.离子 B.分子 C.单质 D.原子
13.下列叙述正确的是
A.HO的摩尔质量为18g
2
B.16克CH 含有的分子数为6.02×1023
4
C.常温、常压下1molNH 的体积约为22.4L
3
D.1L1mol·L—1NaSO 溶液中含Na+为1mol
2 4
14.1.28g铜投入一定量的浓硝酸中,铜完全溶解,生成气体颜色越来越浅,共收集到
VmL气体(标准状况),将盛有此气体的容器倒扣在水中,通入氧气恰好使气体完全
溶解在水中,则需要标准状况下的氧气体积为( )
A.504mL B.336mL C.224mL D.168mL
15.32g铜与150mL一定浓度的硝酸恰好完全反应,产生的NO 和NO混合气体在标
2
准状况下的体积为11.2L。则该硝酸的物质的量浓度为
A.5mol/L B.15mol/L C.10mol/L D.8mol/L
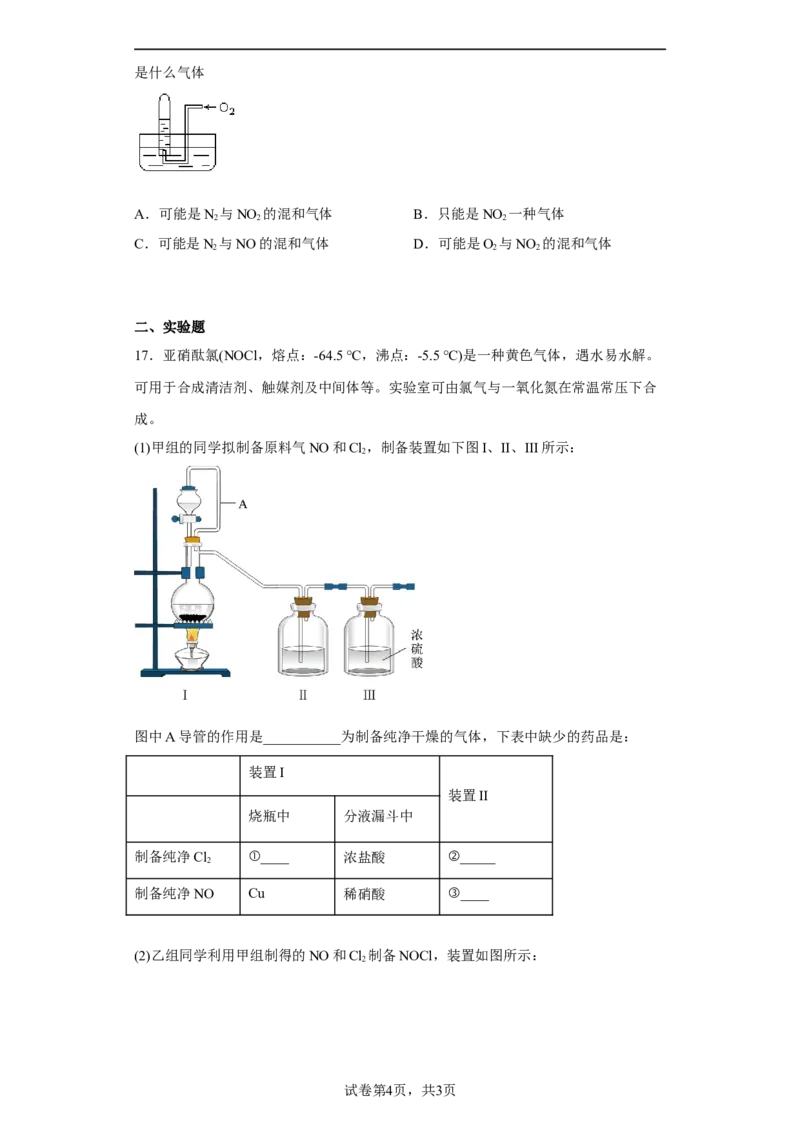
16.如图所示,试管中盛装的是红棕色气体(可能是混合物),当倒扣在盛有水的水
槽中时,试管内水面上升,但不能充满试管,当向试管内鼓入氧气后,可以观察到试
管中水柱继续上升,经过多次重复后,试管内完全被水充满,原来试管中盛装的可能是什么气体
A.可能是N 与NO 的混和气体 B.只能是NO 一种气体
2 2 2
C.可能是N 与NO的混和气体 D.可能是O 与NO 的混和气体
2 2 2
二、实验题
17.亚硝酞氯(NOCl,熔点:-64.5 ℃,沸点:-5.5 ℃)是一种黄色气体,遇水易水解。
可用于合成清洁剂、触媒剂及中间体等。实验室可由氯气与一氧化氮在常温常压下合
成。
(1)甲组的同学拟制备原料气NO和Cl,制备装置如下图I、II、III所示:
2
图中A导管的作用是___________为制备纯净干燥的气体,下表中缺少的药品是:
装置I
装置II
烧瓶中 分液漏斗中
制备纯净Cl ①____ 浓盐酸 ②_____
2
制备纯净NO Cu 稀硝酸 ③____
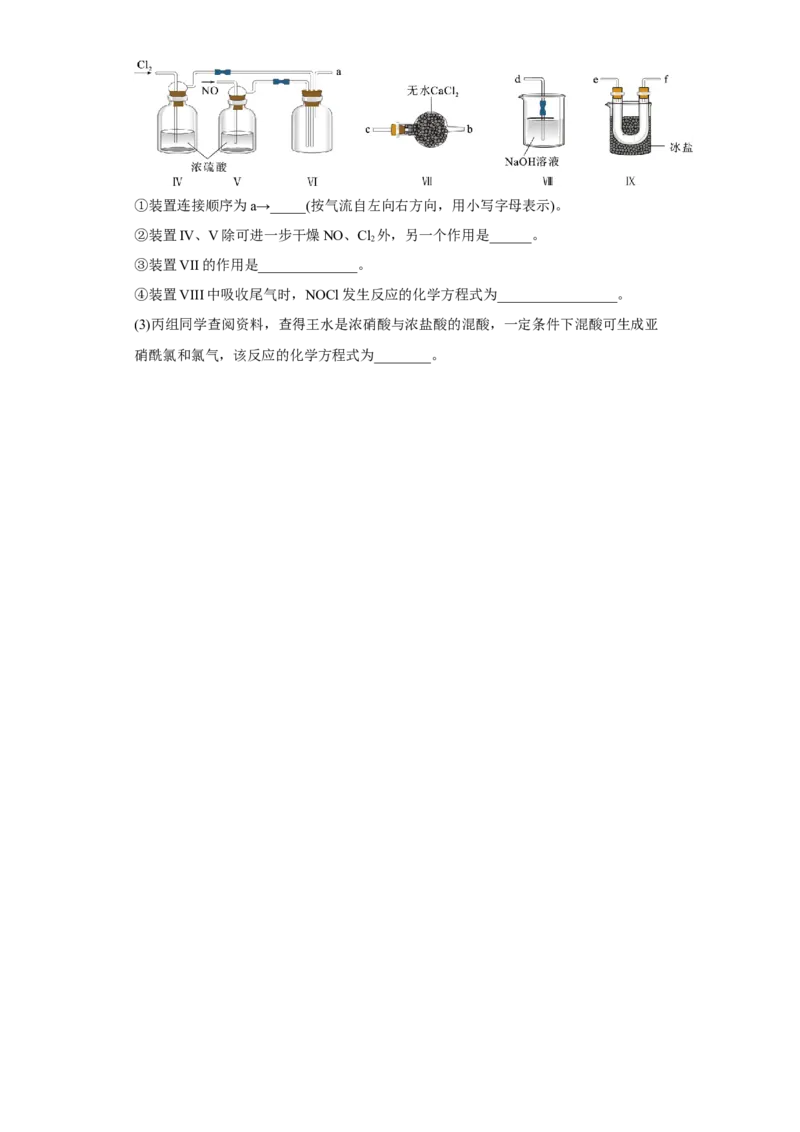
(2)乙组同学利用甲组制得的NO和Cl 制备NOCl,装置如图所示:
2
试卷第4页,共3页①装置连接顺序为a→_____(按气流自左向右方向,用小写字母表示)。
②装置IV、V除可进一步干燥NO、Cl 外,另一个作用是______。
2
③装置VII的作用是______________。
④装置VIII中吸收尾气时,NOCl发生反应的化学方程式为_________________。
(3)丙组同学查阅资料,查得王水是浓硝酸与浓盐酸的混酸,一定条件下混酸可生成亚
硝酰氯和氯气,该反应的化学方程式为________。参考答案:
1.B
【详解】A.二氧化硫是有毒有刺激性的气体,对人体健康有害,故A错误;
B.氮气是空气的主要成分,氮气无毒,故B正确;
C.NO是有毒气体,对人体健康有害,故C错误;
D.CO是无色无味的有毒气体,对人体健康有害,故D错误;
故选:B。
2.C
【详解】A.N 性质稳定,N 和O 在高温和放电条件下都能反应,但只能产生NO,故A
2 2 2
错误;
B.氨气自身不能发生电离,属于非电解质,水是电解质,故B错误;
C.该反应的化学方程式为2N+6HO=4NH +3O,所以发生反应的 n(N ):n(H O)=
2 2 3 2 2 2
1:3,故C正确;
D.O 分别与 N、NH 的反应中,O、N元素的化合价发生变化,属于氧化还原反应,氧
2 2 3
化还原反应的实质是电子的得失,故D错误;
故选:C。
3.D
【详解】A. 空气中N 是游离态,NO是化合态,属于固氮,是自然固氮中的高能固氮,故
2
A不选;B. 空气中N 是游离态,硝酸盐中的氮是化合态,属于固氮,是自然固氮中的生
2
物固氮,故B不选;C. 氮气中的氮是游离态,NH 中的氮是化合态,属于固氮,是人工固
3
氮,故C不选;D. NH 经催化氧化生成NO,由化合态变成化合态,不属于氮的固定,故
3
D选;答案选D。
点睛:解答本题时,需要熟练掌握氮的固定及化合态、游离态的含义。游离态指的是元素
以单质形态存在,化合态指的是元素以化合物形态存在,氮的固定指的是由游离态的氮转
化为化合态的氮的过程,氮的固定可以分为人工固氮和自然固氮。
4.B
【详解】A.反应①~⑥中N的化合价均发生变化,均属于氧化还原反应,故A正确;
B.氮的固定是指氮由游离态转化为化合态,只有反应⑤属于氮的固定,故B错误;
C.反应⑥为NH 和NO 发生归中反应得到N,反应的离子方程式为NH +NO
2
=N ↑+2H O,故C正确;
2 2D.NH 及NO 属于氮肥,向水体中大量排放NH 及NO 造成富营养化,能引起水质恶
化,故D正确;
故选B。
5.D
【详解】A、N 中N的化合价可以降低生成NH ,也可以升高生成NO等,故N 既可作氧
2 3 2
化剂又可作还原剂,A正确;
B、雷雨天时,空气中N 和O 可反应生成NO,B正确;
2 2
C、氮的固定是将大气中游离态的氮(N )转化为含氮化合物的过程,C正确;
2
D、氮气的化学性质很稳定,通常情况下难以与其他物质发生化学反应,D错误;
答案选D。
6.C
【详解】煤燃烧产生的烟气中含有氮氧化物(NO ),容易形成酸雨污染环境,可以通过多种
x
化学方法进行脱硝处理,除去煤燃烧过程种产生的有氮氧化物(NO ),C选项正确;
x
答案选C。
7.B
【详解】试题分析:A、安装燃煤“固硫”装置,可减少二氧化硫的排放,降低酸雨发生
率,正确;B、生物固氮在通常条件下就能实现,错误;C、可降解塑料可在自然条件下转
化为小分子,能防止白色污染,正确;D、常温下,铝与空气中的氧气反应,铝表面形成
致密的氧化膜,阻止内部金属继续反应,对内部金属起保护作用,正确。
考点:考查化学与环境保护,氮的固定,铝的性质。
8.C
【详解】A.O、N、S、Si的原子半径逐渐增大,非金属性逐渐减弱,故A错误;
B.硫的氧化物不形成光化学烟雾,光化学烟雾主要是氮氧化合物造成的,故B错误;
C.描述正确,汽车尾气中的NOx主要由空气中的氮气和氧气在气缸内化合生成,故C正
确;
D.氮气和氧气反应生成NO,得不到NO ,故D错误;
2
故选C。
9.B
【分析】由图可知,abcd分别为NH 、NO 、HNO、NH ∙H O;
3 2 3 3 2
【详解】A.由图可知,ab分别为NH 、NO ,氨气催化氧化生成一氧化氮不是二氧化氮,
3 2
答案第2页,共2页A错误;
B.ab中氮元素化合价分别为-3、+4,氮元素存在中间价态,能发生氧化还原反应,B正确;
C.c为硝酸,硝酸和二氧化氮不能反应,C错误;
D.d为碱是一水合氨,一水合氨生成氨气过程中各元素化合价没有发生改变,D错误;
故选B。
10.B
【详解】试管内装有12mL NO,然后间歇而缓慢地通入8mL 氧气,依据反应定量关系分
析,当一氧化氮和氧气恰好反应生成硝酸发生的反应为:4NO+3O +2H O=4HNO ,结合一
2 2 3
氧化氮和氧气按照4:3全部溶于水,试管内装有12mL NO,然后间歇而缓慢地通入8mL
O,反应后剩余一氧化氮12ml-8×4/3ml=4/3ml,答案选B。
2
11.D
【详解】A. 正常降雨因为雨水中溶解了二氧化碳而显酸性,所以当pH≤5.6时的降雨是酸
雨,故A错误;
B. 氯气的密度大于空气,所以泄漏后应逆风向高处跑,故B错误;
C. 把饱和FeCl 溶液滴加到NaOH溶液中,得到的是氢氧化铁沉淀,故C错误;
3
D. 根据空气质量报告分析,我国城市环境中的大气污染物主要有SO 、NO 、CO、可吸入
2 2
颗粒物等,故D正确;
故选D。
12.A
【详解】海水中的各种元素氯、钠、钙、镁、硫、溴主要以离子形式存在于盐中;
故选A。
13.B
【详解】试题分析:A.单位错误,HO的摩尔质量应为18g/mol。
2
B.16克CH 为1mol,含有的分子数为6.02×1023,正确
4
C.状态错误,常温、常压下1molNH 的体积不一定为22.4L。
3
D.1L1mol·L—1NaSO 溶液中含NaSO 为1mol,则Na+为2mol。
2 4 2 4
考点:物质的量的相关计算
点评:此题不难,考查学生对基本公式的熟练程度,掌握物质的量的相关计算公式就能解
决。
14.C【详解】1.28g铜的物质的量为 =0.02mol,Cu与硝酸反应生成硝酸铜与氮的氧化
物,而氮的氧化物倒扣在水中,通入氧气,恰好使气体完全溶于水中,又生成硝酸,纵观
整个反应过程可知,铜提供的电子等于通入的氧气获得的电子,故通入氧气的物质的量为
=0.01mol,通入氧气的体积=0.01mol×22.4L/mol=0.224L=224mL;
故选C。
15.C
【详解】试题分析:32g铜的物质的量为0.5mol,反应后溶液的溶质为Cu(NO ), Cu2+的
3 2
物质的量为0.5mol,那么NO -的物质的量为1mol,NO 和NO混合气体在标准状况下的体
3 2
积为11.2L,总物质的量为0.5mol,N元素的总物质的量为1mol+0.5mol=1.5mol,N元素都
来自硝酸,则硝酸的物质的量为1.5mol,则浓度为:1.5mol÷0.15L=10mol/L。
考点:质量守恒的运用、物质的量的计算。
16.D
【详解】A.N 和水不反应且不溶于水,在有O 的条件下N 也不与水反应,则通入O 后
2 2 2 2
试管内不能完全被水充满,故A错误;
B.O 与NO 可在溶液中发生反应4NO +O +2H O=4HNO ,试管内只有NO 气体,通入O
2 2 2 2 2 3 2 2
后能完全被水充满,但还有其它可能,如NO和NO 的混合气体或只有NO,故B错误;
2
C.N 和水不反应且不溶于水,在有O 的条件下氮气也不与水反应,则通入O 后试管内不
2 2 2
能完全被水充满,故C错误;
D.O 与NO 的混和气体可在水中发生反应4NO +O +2H O=4HNO ,则通入适量O 后试管
2 2 2 2 2 3 2
内能完全被水充满,故D正确;
故答案为D。
17. 平衡气压,便于浓盐酸顺利流下 MnO 饱和食盐水
2
水 e→f→c→h→b→d 通过观察气泡调节气体的流速 防止水蒸气进入
反应器 NOCl+2NaOH=NaCl+NaNO +H O HNO+HCl= NOCl↑+Cl ↑+H O
3 2 3 2 2
【分析】由实验装置图可知,装置Ⅳ中盛有的浓硫酸用于干燥氯气,装置Ⅴ中盛有的浓硫
酸用于干燥一氧化氮,除干燥氯气和一氧化氮外,装置IV、V还能起到通过观察气泡调节
气体的流速达到氯气和一氧化氮完全反应的目的,装置Ⅵ中氯气与一氧化氮反应生成亚硝
酞氯,装置Ⅸ用于冷凝收集亚硝酞氯,装置Ⅶ中盛有的氯化钙用于吸收水蒸气,防止水蒸
答案第4页,共2页气进入反应器导致亚硝酞氯发生水解,装置Ⅷ中盛有的氢氧化钠溶液用于吸收未反应的有
毒的氯气和挥发出的亚硝酞氯,防止污染空气,则乙组同学设计实验所用装置连接顺序为
a→e→f→c→h→b→d。
【详解】(1) 由实验装置图可知,装置图中A导管能起到平衡气压,便于浓盐酸顺利流下
的作用;若Ⅰ中分液漏斗中盛有浓盐酸,由二氧化锰与浓盐酸共热反应制备氯气可知,圆
底烧瓶中盛有二氧化锰固体,因浓盐酸具有挥发性,制得的氯气中混有氯化氢气体,则装
置Ⅱ中盛有的饱和食盐水用于除去氯化氢气体;若分液漏斗中盛有稀硝酸,圆底烧瓶中盛
有铜,由铜与稀硝酸反应生成硝酸铜、一氧化氮和水可知,一氧化氮易被空气中氧气氧化
生成二氧化氮,则装置Ⅱ中盛有的水用于将一氧化氮中混有的二氧化氮转化为一氧化氮,
达到除杂的目的,故答案为:平衡气压,便于浓盐酸顺利流下;MnO ;饱和食盐水;水;
2
(2) ①由分析可知,乙组同学设计实验所用装置连接顺序为a→e→f→c→h→b→d,故答案
为:e→f→c→h→b→d;
②由分析可知,装置IV、V除可进一步干燥一氧化氮和氯气的作用外,还能起到通过观察
气泡调节气体的流速达到氯气和一氧化氮完全反应的目的,故答案为:通过观察气泡调节
气体的流速;
③由分析可知,装置VII中盛有的氯化钙用于吸收水蒸气,防止水蒸气进入反应器导致亚
硝酞氯发生水解,故答案为:防止水蒸气进入反应器;
④由分析可知,装置VIII中盛有的氢氧化钠溶液用于吸收未反应的有毒的氯气和挥发出的
亚硝酞氯,防止污染空气,亚硝酞氯与氢氧化钠溶液发生的反应为亚硝酞氯与氢氧化钠溶
液反应生成氯化钠、硝酸钠和水,反应的化学方程式为
NOCl+2NaOH=NaCl+NaNO +H O,故答案为:NOCl+2NaOH=NaCl+NaNO +H O;
3 2 3 2
(3)由题意可知,王水中浓硝酸与浓盐酸发生的反应为浓硝酸与浓盐酸发生氧化还原反应生
成亚硝酞氯、氯气和水,反应的化学方程式为HNO+HCl= NOCl↑+Cl ↑+H O,故答案为:
3 2 2
HNO+HCl= NOCl↑+Cl ↑+H O。
3 2 2答案第6页,共2页