文档内容
课时作业
A篇·知识对点训练
知识点1 氨的性质
1.下列过程没有起到氮的固定作用的是( )
A.N 与O 反应生成NO
2 2
B.N 与H 在一定条件下合成氨
2 2
C.NH 经催化氧化生成NO
3
D.豆科植物的根瘤菌将空气中的氮气转化为含氮化合物
答案 C
解析 氮的固定指游离态的氮反应生成化合态的氮,即由N 到含氮化合物。
2
2.下列有关氨的说法正确的是( )
A.氨属于电解质
B.液氨是纯净物,氨水是混合物
C.氨气遇浓盐酸、浓硫酸、浓硝酸都能产生白烟
D.氨气易液化,所以可用来做喷泉实验
答案 B
解析 氨是非电解质,A错误;浓H SO 难挥发,C错误;喷泉实验是利用
2 4
了NH 极易溶于水的性质,D错误。
3
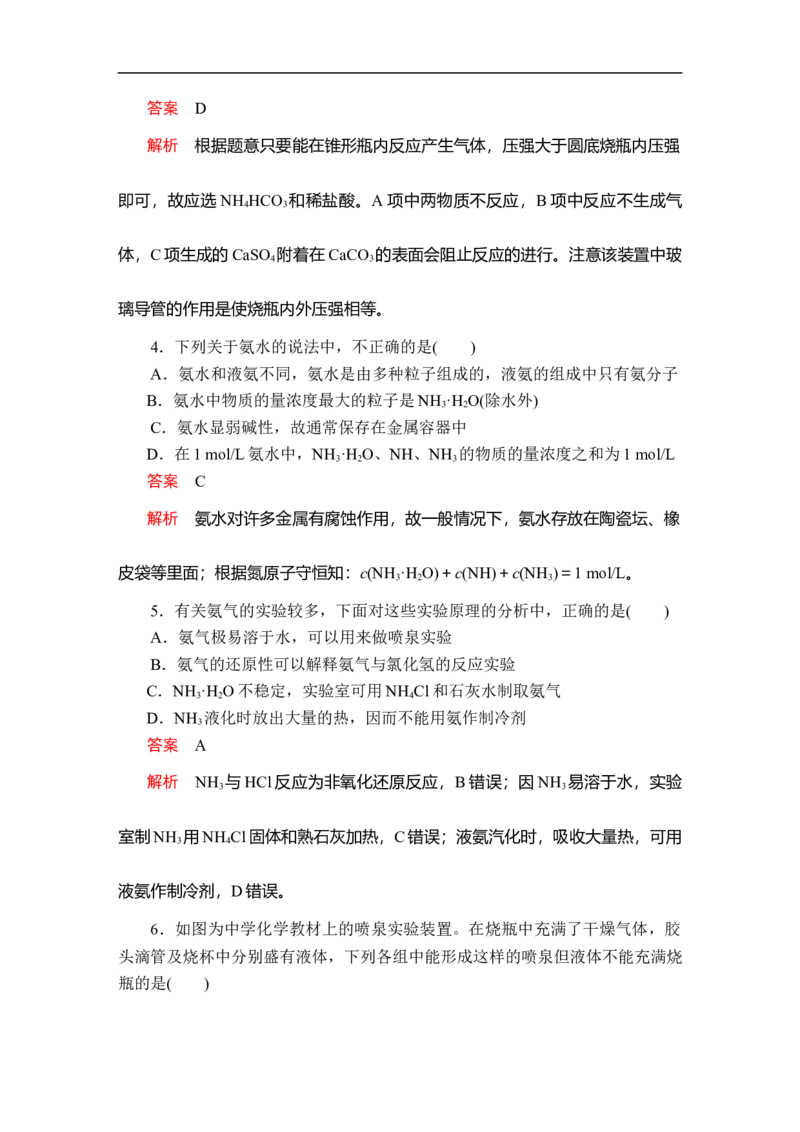
3.利用如图所示装置,在锥形瓶中,分别加入足量的下列物质,反应后可
能产生喷泉的是( )
A.Cu与稀盐酸
B.NaHCO 与NaOH溶液
3
C.CaCO 与稀硫酸
3
D.NH HCO 与稀盐酸
4 3答案 D
解析 根据题意只要能在锥形瓶内反应产生气体,压强大于圆底烧瓶内压强
即可,故应选NH HCO 和稀盐酸。A项中两物质不反应,B项中反应不生成气
4 3
体,C项生成的CaSO 附着在CaCO 的表面会阻止反应的进行。注意该装置中玻
4 3
璃导管的作用是使烧瓶内外压强相等。
4.下列关于氨水的说法中,不正确的是( )
A.氨水和液氨不同,氨水是由多种粒子组成的,液氨的组成中只有氨分子
B.氨水中物质的量浓度最大的粒子是NH ·H O(除水外)
3 2
C.氨水显弱碱性,故通常保存在金属容器中
D.在1 mol/L氨水中,NH ·H O、NH、NH 的物质的量浓度之和为1 mol/L
3 2 3
答案 C
解析 氨水对许多金属有腐蚀作用,故一般情况下,氨水存放在陶瓷坛、橡
皮袋等里面;根据氮原子守恒知:c(NH ·H O)+c(NH)+c(NH )=1 mol/L。
3 2 3
5.有关氨气的实验较多,下面对这些实验原理的分析中,正确的是( )
A.氨气极易溶于水,可以用来做喷泉实验
B.氨气的还原性可以解释氨气与氯化氢的反应实验
C.NH ·H O不稳定,实验室可用NH Cl和石灰水制取氨气
3 2 4
D.NH 液化时放出大量的热,因而不能用氨作制冷剂
3
答案 A
解析 NH 与HCl反应为非氧化还原反应,B错误;因NH 易溶于水,实验
3 3
室制NH 用NH Cl固体和熟石灰加热,C错误;液氨汽化时,吸收大量热,可用
3 4
液氨作制冷剂,D错误。
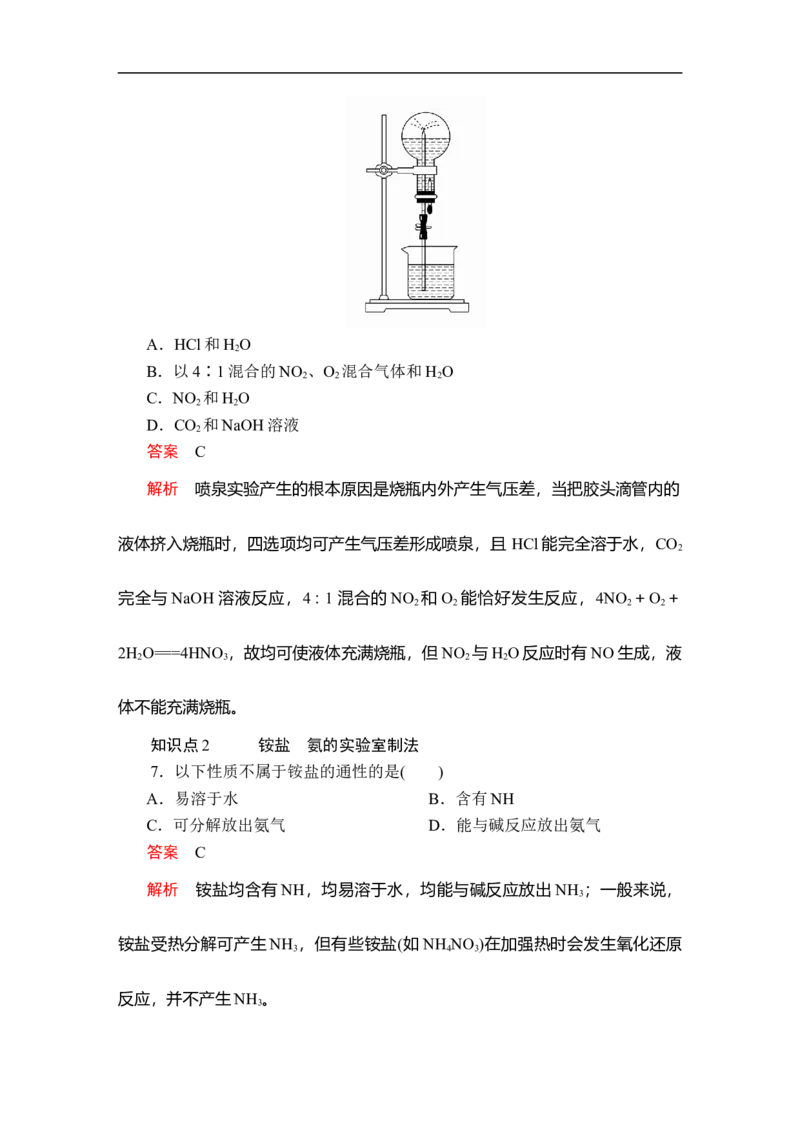
6.如图为中学化学教材上的喷泉实验装置。在烧瓶中充满了干燥气体,胶
头滴管及烧杯中分别盛有液体,下列各组中能形成这样的喷泉但液体不能充满烧
瓶的是( )A.HCl和H O
2
B.以4∶1混合的NO 、O 混合气体和H O
2 2 2
C.NO 和H O
2 2
D.CO 和NaOH溶液
2
答案 C
解析 喷泉实验产生的根本原因是烧瓶内外产生气压差,当把胶头滴管内的
液体挤入烧瓶时,四选项均可产生气压差形成喷泉,且 HCl能完全溶于水,CO
2
完全与 NaOH溶液反应,4∶1混合的 NO 和O 能恰好发生反应,4NO +O +
2 2 2 2
2H O===4HNO ,故均可使液体充满烧瓶,但 NO 与H O反应时有NO生成,液
2 3 2 2
体不能充满烧瓶。
知识点2 铵盐 氨的实验室制法
7.以下性质不属于铵盐的通性的是( )
A.易溶于水 B.含有NH
C.可分解放出氨气 D.能与碱反应放出氨气
答案 C
解析 铵盐均含有NH,均易溶于水,均能与碱反应放出 NH ;一般来说,
3
铵盐受热分解可产生NH ,但有些铵盐(如NH NO )在加强热时会发生氧化还原
3 4 3
反应,并不产生NH 。
38.为了检验某固体物质中是否含有NH,你认为下列试纸和试剂可用到的是
( )
①蒸馏水 ②NaOH溶液 ③红色石蕊试纸 ④蓝色石蕊试纸 ⑤稀硫酸
A.①②④ B.①②③ C.②③ D.①③⑤
答案 B
解析 固体溶于 NaOH 溶液后,加热,若含有 NH,则发生 NH+OH-
=====NH ↑+H O,NH 能使湿润(用到蒸馏水)的红色石蕊试纸变蓝,故选B。
3 2 3
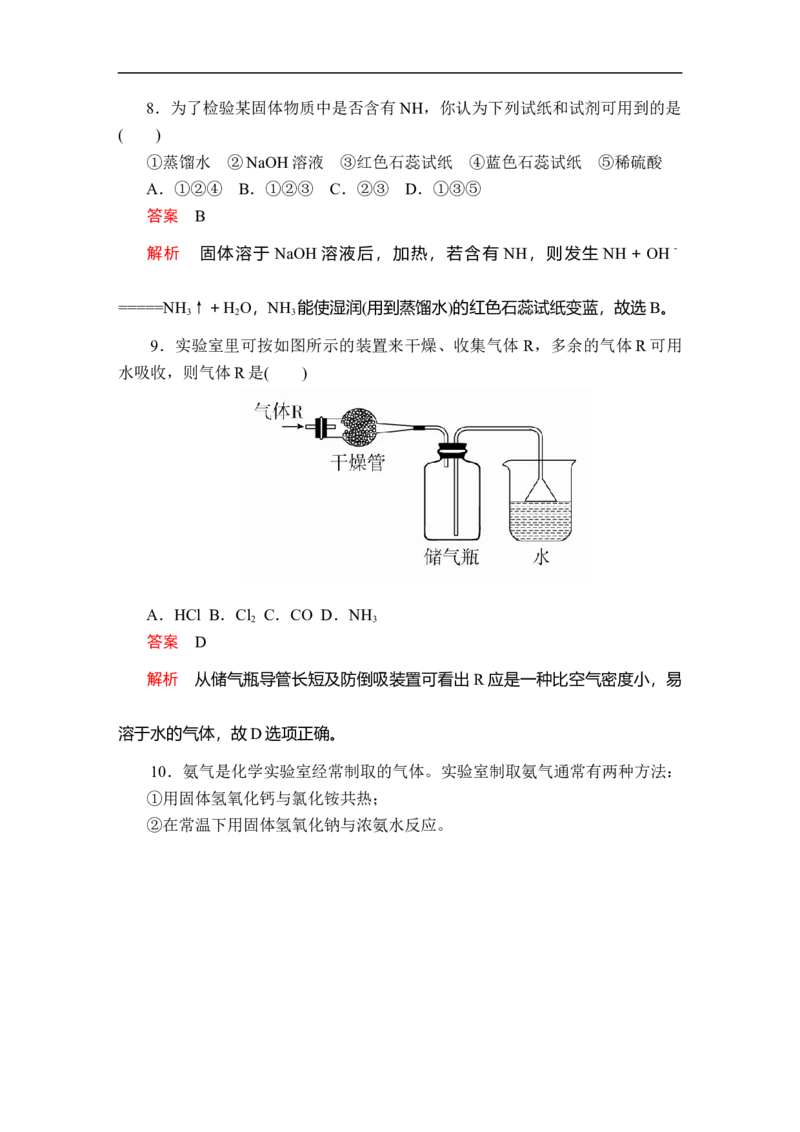
9.实验室里可按如图所示的装置来干燥、收集气体 R,多余的气体R可用
水吸收,则气体R是( )
A.HCl B.Cl C.CO D.NH
2 3
答案 D
解析 从储气瓶导管长短及防倒吸装置可看出R应是一种比空气密度小,易
溶于水的气体,故D选项正确。
10.氨气是化学实验室经常制取的气体。实验室制取氨气通常有两种方法:
①用固体氢氧化钙与氯化铵共热;
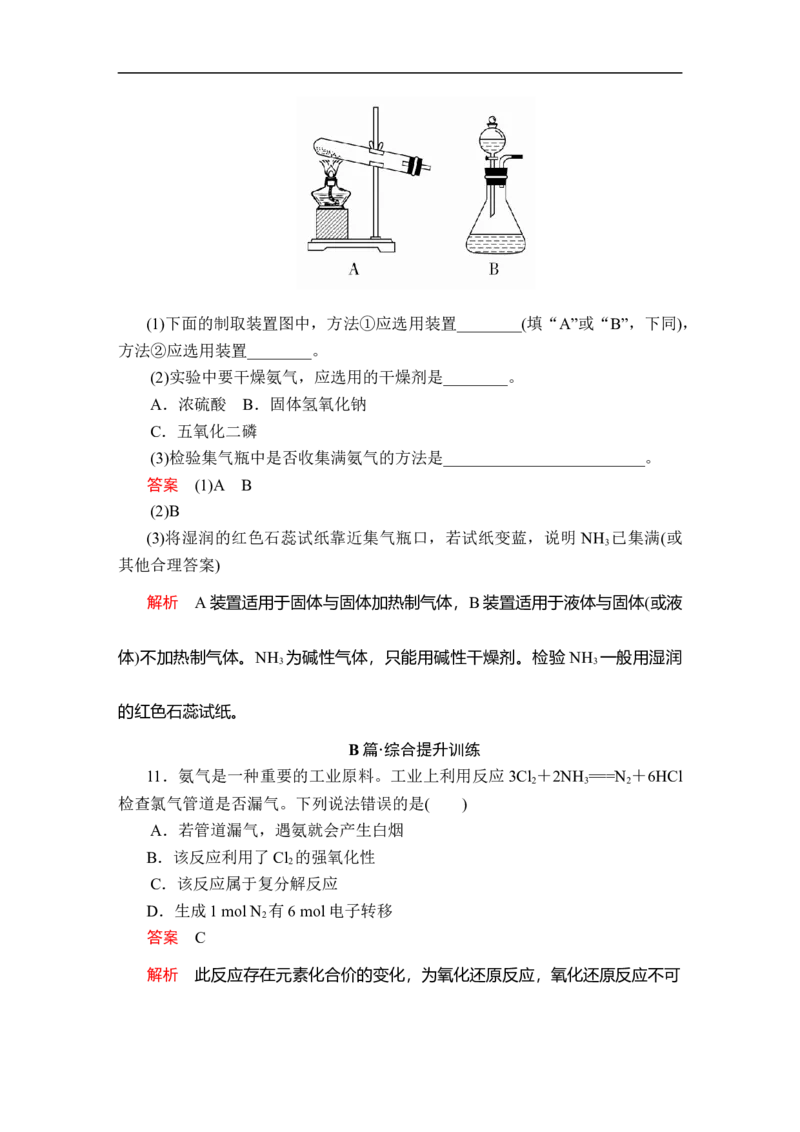
②在常温下用固体氢氧化钠与浓氨水反应。(1)下面的制取装置图中,方法①应选用装置________(填“A”或“B”,下同),
方法②应选用装置________。
(2)实验中要干燥氨气,应选用的干燥剂是________。
A.浓硫酸 B.固体氢氧化钠
C.五氧化二磷
(3)检验集气瓶中是否收集满氨气的方法是_________________________。
答案 (1)A B
(2)B
(3)将湿润的红色石蕊试纸靠近集气瓶口,若试纸变蓝,说明 NH 已集满(或
3
其他合理答案)
解析 A装置适用于固体与固体加热制气体,B装置适用于液体与固体(或液
体)不加热制气体。NH 为碱性气体,只能用碱性干燥剂。检验 NH 一般用湿润
3 3
的红色石蕊试纸。
B篇·综合提升训练
11.氨气是一种重要的工业原料。工业上利用反应3Cl +2NH ===N +6HCl
2 3 2
检查氯气管道是否漏气。下列说法错误的是( )
A.若管道漏气,遇氨就会产生白烟
B.该反应利用了Cl 的强氧化性
2
C.该反应属于复分解反应
D.生成1 mol N 有6 mol电子转移
2
答案 C
解析 此反应存在元素化合价的变化,为氧化还原反应,氧化还原反应不可能为复分解反应,C错误;Cl 在此反应中作氧化剂,体现强氧化性,B正确;
2
反 应 生 成 的 HCl 遇 到 挥 发 出 来 的 NH 生 成 白 烟 (NH Cl) , A 正 确 ;
3 4
2NH ――→N ,所以生成1 mol N 将有6 mol电子转移,D正确。
3 2 2
12.下列关于氨与铵盐的叙述中正确的是( )
A.铵盐加热时都能产生NH ,并可以用湿润的红色石蕊试纸检验
3
B.干燥NH 时,不可以用酸性干燥剂,用中性干燥剂CaCl 即可
3 2
C.铵盐作氮肥时,与生石灰混用的效果更好
D.铵盐的物理共性是铵盐都是晶体,都能溶于水
答案 D
解析 选项A,如NH NO 加热时不产生NH ;选项B,NH 能与CaCl 反应,
4 3 3 3 2
所以不能用 CaCl 干燥 NH ;选项 C,生石灰与环境中的 H O 反应生成
2 3 2
Ca(OH) ,Ca(OH) 与铵盐反应生成极易挥发的NH ,从而大大地降低了肥效。
2 2 3
13.氨溶于水得到氨水,氯气溶于水得到氯水,下列关于新制的氨水、氯水
的描述中正确的是( )
A.“两水”都是混合物,溶液中含有的粒子种类、数目相同
B.“两水”都有刺激性气味,都能漂白有机色素
C.“两水”中都存在可逆反应
D.“两水”放置时间较久后都会因为相同的原理而变质
答案 C
解析 新制的氯水中存在的微粒(三分子四离子):Cl 、H O、HClO和Cl-、
2 2
ClO-、H+、OH-;氨水中存在的微粒(三分子三离子):NH 、H O、NH ·H O和
3 2 3 2
NH、H+、OH-,A错误;氨水无漂白性,B错误;氨溶于水发生反应:NH +
3
H ONH ·H O;氯气溶于水发生反应:Cl +H OHClO+HCl,C正确;新
2 3 2 2 2
制的氯水长时间放置,因HClO发生分解最终形成稀盐酸(化学变化),新制的氨水长时间放置,因NH 易挥发而变稀,但不会变质,D错误。
3
14.某混合气体中可能含有Cl 、O 、HCl、NH 、NO、NO 中的两种或多种
2 2 3 2
气体。现将此无色透明的混合气体通过浓 H SO 后,体积缩小,把剩余气体排入
2 4
空气中,很快变成红棕色。对于原混合气体成分的判断正确的是( )
A.肯定有O
2
B.肯定没有Cl 、NH 、NO
2 3 2
C.肯定有NH 、NO、HCl
3
D.肯定含有NH 和NO
3
答案 D
解析 无色确定无Cl 、NO ;体积缩小,有NH 无HCl;变红棕色有NO而
2 2 3
无O 。
2
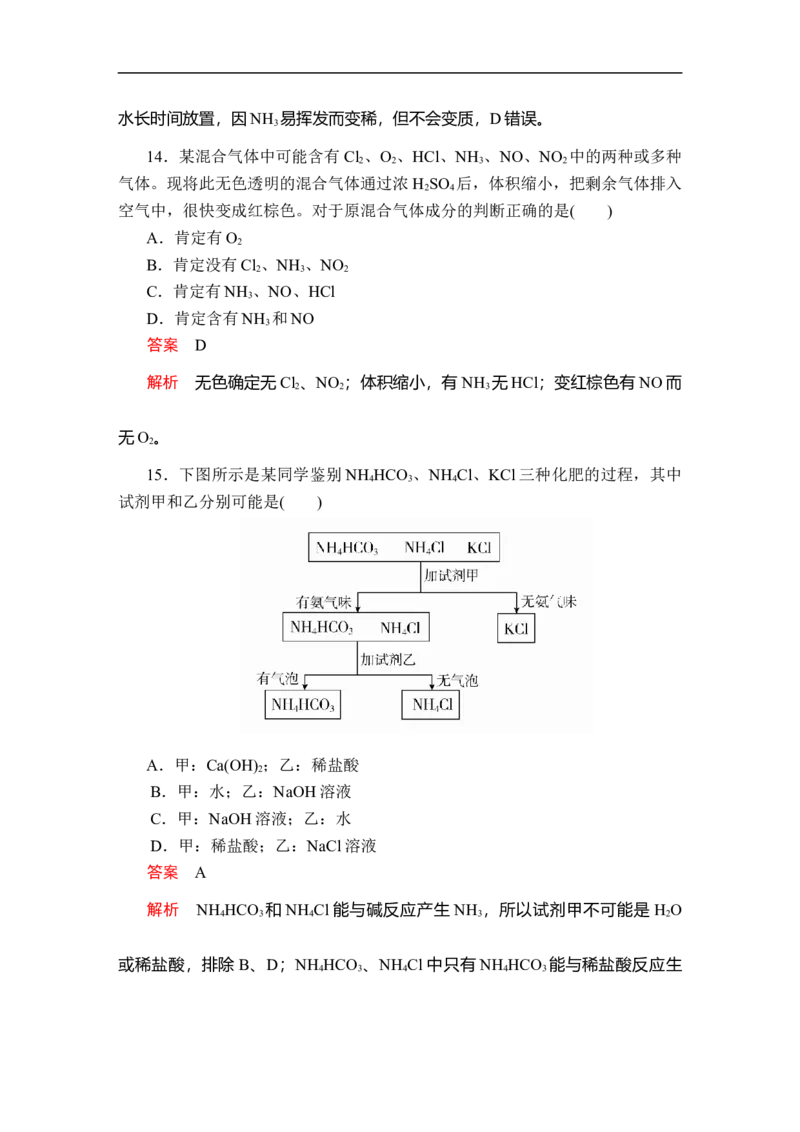
15.下图所示是某同学鉴别NH HCO 、NH Cl、KCl三种化肥的过程,其中
4 3 4
试剂甲和乙分别可能是( )
A.甲:Ca(OH) ;乙:稀盐酸
2
B.甲:水;乙:NaOH溶液
C.甲:NaOH溶液;乙:水
D.甲:稀盐酸;乙:NaCl溶液
答案 A
解析 NH HCO 和NH Cl能与碱反应产生 NH ,所以试剂甲不可能是 H O
4 3 4 3 2
或稀盐酸,排除 B、D;NH HCO 、NH Cl中只有NH HCO 能与稀盐酸反应生
4 3 4 4 3成气泡(CO ),故A符合。
2
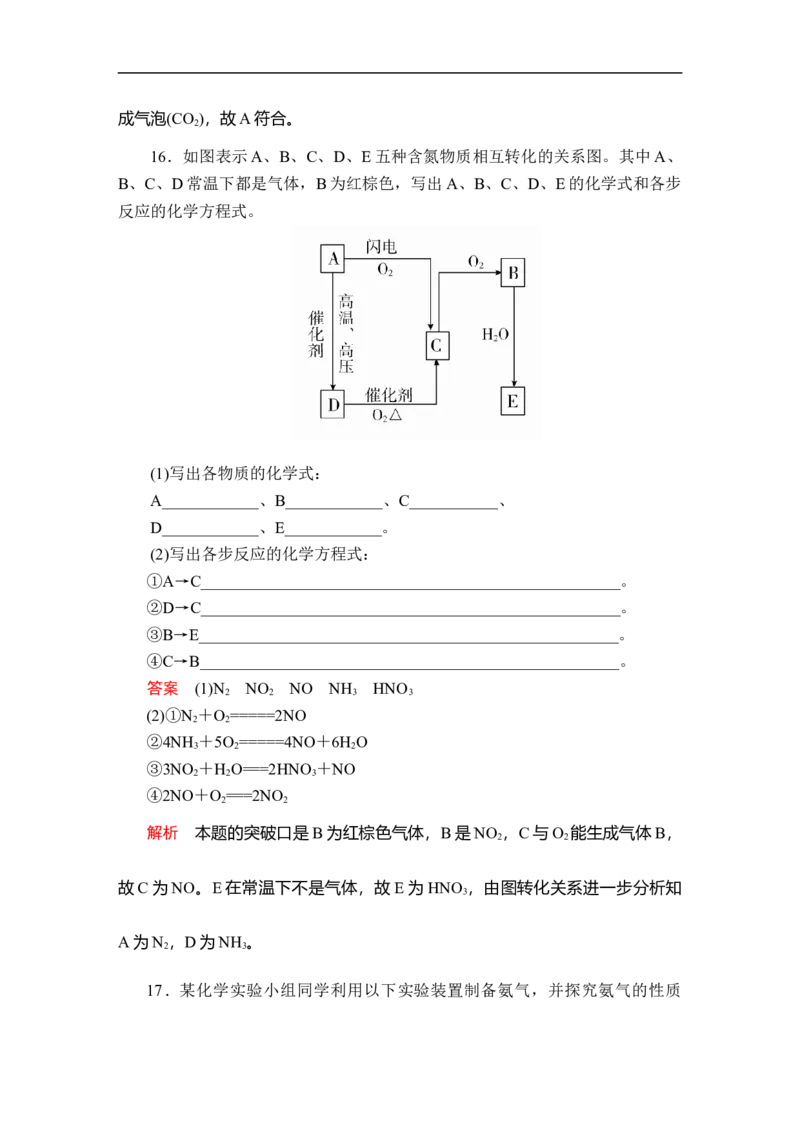
16.如图表示A、B、C、D、E五种含氮物质相互转化的关系图。其中A、
B、C、D常温下都是气体,B为红棕色,写出A、B、C、D、E的化学式和各步
反应的化学方程式。
(1)写出各物质的化学式:
A____________、B____________、C___________、
D____________、E____________。
(2)写出各步反应的化学方程式:
①A→C____________________________________________________。
②D→C____________________________________________________。
③B→E____________________________________________________。
④C→B____________________________________________________。
答案 (1)N NO NO NH HNO
2 2 3 3
(2)①N +O =====2NO
2 2
②4NH +5O =====4NO+6H O
3 2 2
③3NO +H O===2HNO +NO
2 2 3
④2NO+O ===2NO
2 2
解析 本题的突破口是B为红棕色气体,B是NO ,C与O 能生成气体B,
2 2
故C为NO。E在常温下不是气体,故E为HNO ,由图转化关系进一步分析知
3
A为N ,D为NH 。
2 3
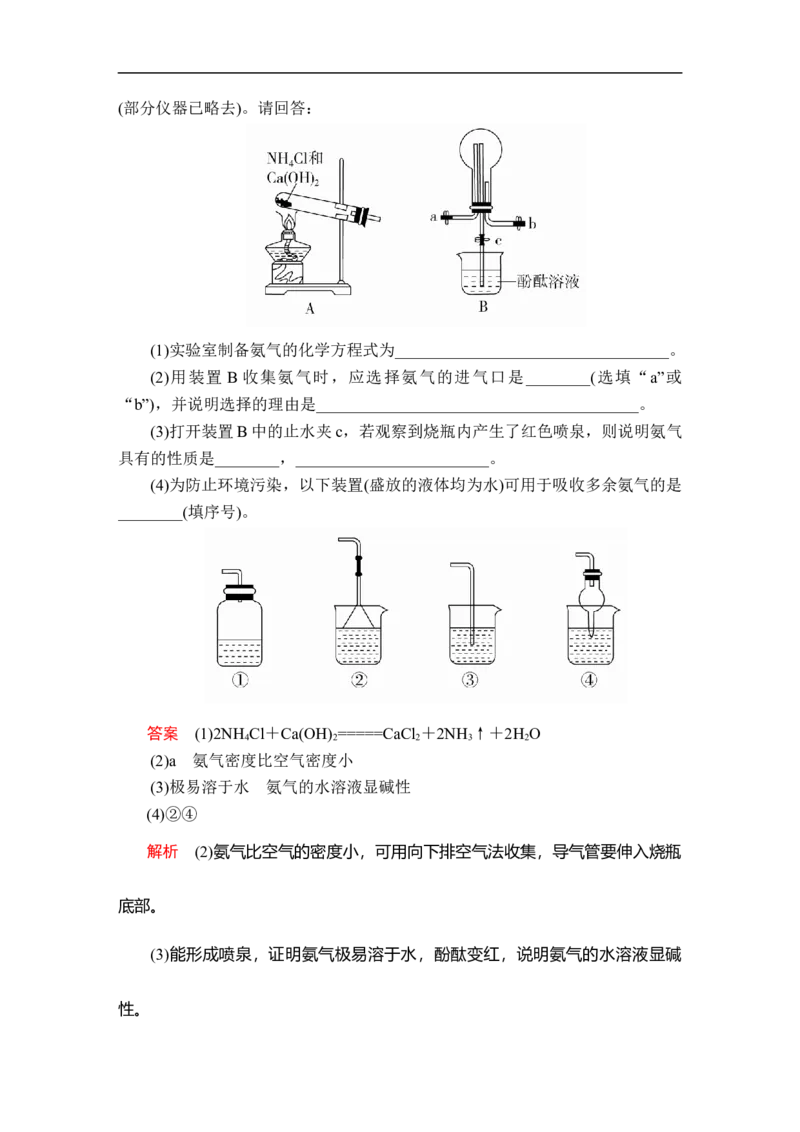
17.某化学实验小组同学利用以下实验装置制备氨气,并探究氨气的性质(部分仪器已略去)。请回答:
(1)实验室制备氨气的化学方程式为__________________________________。
(2)用装置 B 收集氨气时,应选择氨气的进气口是________(选填“a”或
“b”),并说明选择的理由是________________________________________。
(3)打开装置B中的止水夹c,若观察到烧瓶内产生了红色喷泉,则说明氨气
具有的性质是________,________________________。
(4)为防止环境污染,以下装置(盛放的液体均为水)可用于吸收多余氨气的是
________(填序号)。
答案 (1)2NH Cl+Ca(OH) =====CaCl +2NH ↑+2H O
4 2 2 3 2
(2)a 氨气密度比空气密度小
(3)极易溶于水 氨气的水溶液显碱性
(4)②④
解析 (2)氨气比空气的密度小,可用向下排空气法收集,导气管要伸入烧瓶
底部。
(3)能形成喷泉,证明氨气极易溶于水,酚酞变红,说明氨气的水溶液显碱
性。(4)①不能使NH 进入瓶中,②、④能防止倒吸,③会发生倒吸。
3