文档内容
西南大学附中高 2027 届高一上定时检测(一)
化 学 试 题
(满分:100分;考试时间:75分钟)
2024年10月
注意事项:
1.答卷前考生务必把自己的姓名,准考证号填写在答题卡上。
2.回答选择题时用2B铅笔将答题卡上对应题目的答案标号涂黑;回答非选择题时,用0.5
毫米黑色签字笔将答案写在答题卡上,写在本试卷上无效。
3.考试结束后,将答题卡交回(试题卷自己保管好,以备评讲)。
可能用到的相对原子质量:H 1 O 16 C 12 Na 23 Cl 35.5
一、 选择题:每个小题只有一个正确的选项,本大题共14小题,每题3分,共42分。
1. 下列物质属于有机化合物的是
A. C B.CO C.CH D.CaCO
2 4 3
2. 分类是一种重要的学习方法。下列物质分类完全正确的是
选项 单质 化合物 混合物
A 铁 苛性钠 冰水混合物
B 水银 苏打 空气
C 煤炭 生石灰 天然气
D 液氧 盐酸 生理盐水
3. 下列说法正确的是
A.金属氧化物一定是碱性氧化物,酸性氧化物一定是非金属氧化物
B.同素异形体是由同一种元素构成的单质,所以同素异形体的性质相同
C.纯碱和烧碱在工业上合称为“两碱”,它们均属于碱
D.CH COOH是一种一元酸,它与足量NaOH溶液反应生成CH COONa
3 3
4. 当光束通过下列物质时,一定不会出现丁达尔效应的是
①医用酒精 ②有色玻璃 ③云、雾 ④蔗糖水
A.①② B.③④ C.②③ D.①④
5. 下列物质在水溶液中的电离方程式正确的是
A.NaHCO Na+ + H+ + CO2- B.H CO ⥫⥬ 2H+ + CO2-
3 3 2 3 3
C.FeCl
3
Fe3+ + 3Cl— D.NH
3
·H
2
O NH+
4
+ OH—
高一化学 第 1 页(共 6 页)
{#{QQABSQSUggCoABAAAAhCEQGACAAQkgACCSgGhFAMoAAAiANABAA=}#}6. 下列叙述正确的是
A.氯化钠在熔融状态下能导电,由此可知电解质在熔融状态下都能导电
B.碳酸钠晶体不导电,由此可知碳酸钠晶体中不存在阴阳离子
C.在通电条件下,电解质在溶液中电离产生阴阳离子,故电解质溶液可以导电
D.相同温度下,浓盐酸的导电性一定比稀盐酸的导电性强
7. 下列离子方程式书写不正确的是
A.将二氧化碳通入石灰浆:Ca2++ 2OH— + CO CaCO ↓+ H O
2 3 2
B.单质铁与稀盐酸反应:Fe + 2H+ Fe2+ + H ↑
2
C.氧化铜与稀硫酸反应:CuO + 2H+ Cu2+ + H O
2
D.碳酸钡与稀盐酸反应:BaCO + 2H+ Ba2+ + H O + CO ↑
3 2 2
8. 锌、稀硫酸、Ba(OH) 溶液、CuCl 溶液四种物质之间的反应关系如图所示,其中交叉部分
2 2
对应的离子方程式不正确的是
A.Zn + 2H+ Zn2+ + H ↑
2
B.SO2-+ H+ + OH— + Ba2+ BaSO ↓+ H O
4 4 2
C.Cu2+ + 2OH— Cu(OH) ↓
2
D.Zn + Cu2+ Zn2+ + Cu
9. 下列各组离子在溶液中一定能大量共存的是
A.Mg2+、Cu2+、Cl—、NO- B.K+、NH+、Cl—、OH—
3 4
C.Na+、Ba2+、OH—、CO2- D.Ca2+、Na+、SO2-、Cl—
3 4
10. 下列关于物质之间的转化,不能实现的一组是
A.CuO2CuOH2 SO 4CuSO
Δ Δ 4
B.CaCO 高温CaOH2 OCaOH
3 2
C.
高一化学 第 2 页(共 6 页)
K M n O
4
Δ O
2
F点 e燃 F e
2
O
3
H O2 F e O H
3
D. B a C O
3
盐 酸 B a C l
2
稀 硫 酸 H C l
11. 根据下列实验操作及现象,所得结论不正确的是
选项 实验操作及现象 结论
A 取少量试样,加入CaCl 溶液,有白色沉淀产生 原溶液中含有CO2-
2 3
取少量试样,加入稀硝酸酸化的AgNO 溶液,有白色沉
B 3 原溶液中含有Cl—
淀产生
取少量试样,先加入过量稀盐酸,无明显现象;再加入
C 原溶液中含有SO2-
BaCl 溶液,有白色沉淀产生 4
2
D 取少量试样,常温下,用pH试纸测得溶液pH=2 原溶液中含有H+
{#{QQABSQSUggCoABAAAAhCEQGACAAQkgACCSgGhFAMoAAAiANABAA=}#}12. 在量子点的发现和合成领域有重大贡献的三位科学家在 2023 年获得了诺贝尔化学奖。实
验室制备的硫化镉(CdS)量子点的尺寸在1~50 nm之间,它们具有高比表面积、容易吸
附阴离子而带负电荷等性质。下列关于CdS量子点的说法不正确的是
A.CdS量子点在水中形成的分散系属于胶体
B.CdS量子点分散在水中可产生丁达尔效应
C.向CdS量子点在水中形成的分散系中加入KNO 会发生聚沉
3
D.可以用滤纸分离CdS量子点与NaCl溶液
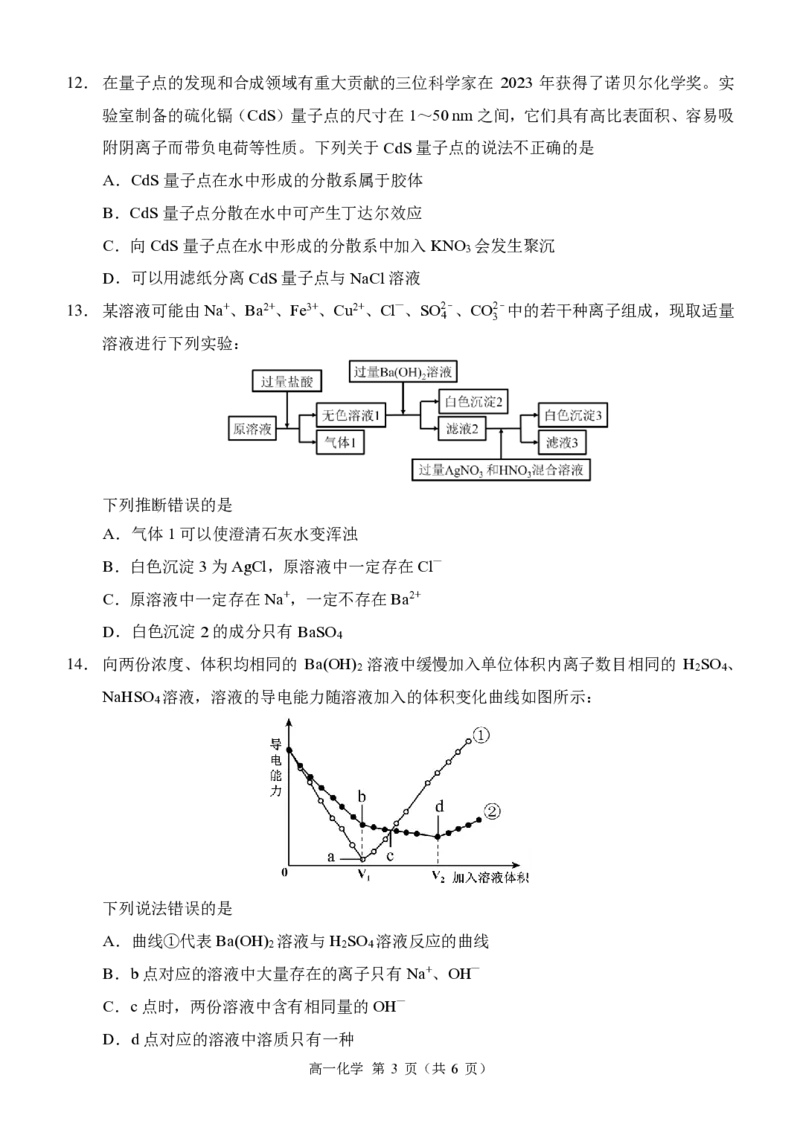
13. 某溶液可能由Na+、Ba2+、Fe3+、Cu2+、Cl—、SO2-、CO2-中的若干种离子组成,现取适量
4 3
溶液进行下列实验:
下列推断错误的是
A.气体1可以使澄清石灰水变浑浊
B.白色沉淀3为AgCl,原溶液中一定存在Cl—
C.原溶液中一定存在Na+,一定不存在Ba2+
D.白色沉淀2的成分只有BaSO
4
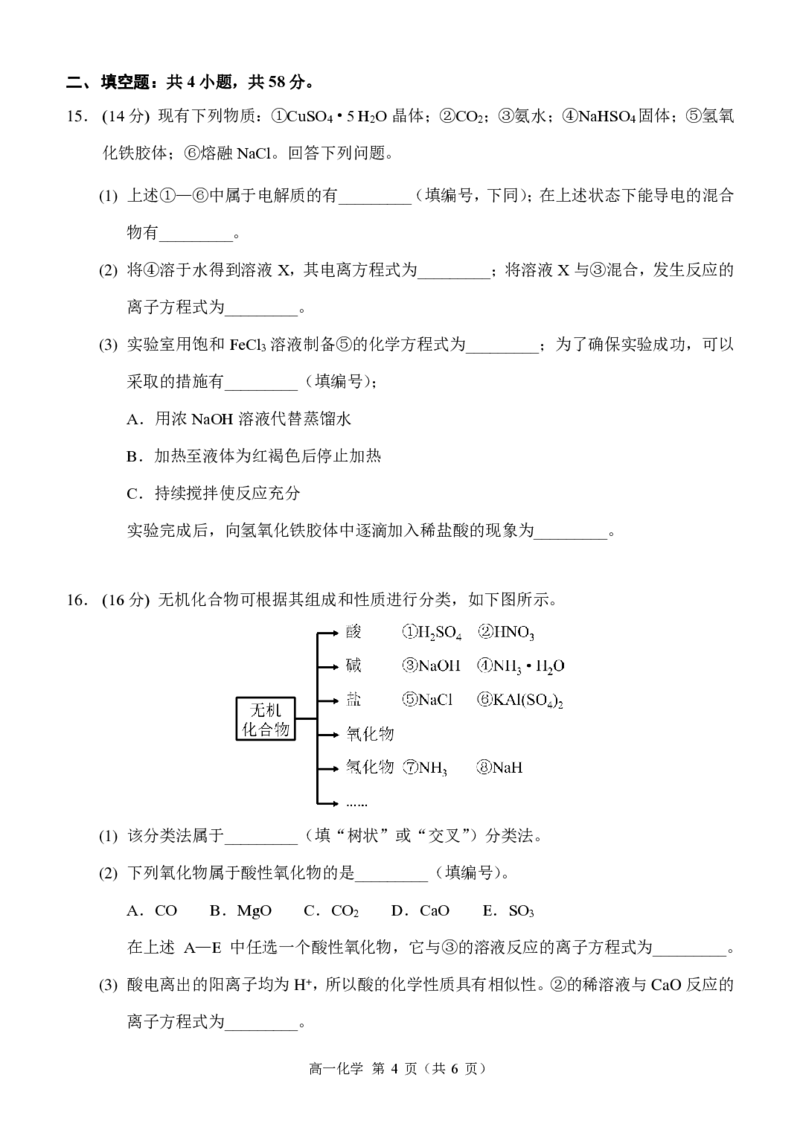
14. 向两份浓度、体积均相同的 Ba(OH) 溶液中缓慢加入单位体积内离子数目相同的 H SO 、
2 2 4
NaHSO 溶液,溶液的导电能力随溶液加入的体积变化曲线如图所示:
4
下列说法错误的是
A.曲线①代表Ba(OH) 溶液与H SO 溶液反应的曲线
2 2 4
B.b点对应的溶液中大量存在的离子只有Na+、OH—
C.c点时,两份溶液中含有相同量的OH—
D.d点对应的溶液中溶质只有一种
高一化学 第 3 页(共 6 页)
{#{QQABSQSUggCoABAAAAhCEQGACAAQkgACCSgGhFAMoAAAiANABAA=}#}二、 填空题:共4小题,共58分。
15. (14分) 现有下列物质:①CuSO ·5 H O晶体;②CO ;③氨水;④NaHSO 固体;⑤氢氧
4 2 2 4
化铁胶体;⑥熔融NaCl。回答下列问题。
(1) 上述①—⑥中属于电解质的有_________(填编号,下同);在上述状态下能导电的混合
物有_________。
(2) 将④溶于水得到溶液X,其电离方程式为_________;将溶液X与③混合,发生反应的
离子方程式为_________。
(3) 实验室用饱和 FeCl 溶液制备⑤的化学方程式为_________;为了确保实验成功,可以
3
采取的措施有_________(填编号);
A.用浓NaOH溶液代替蒸馏水
B.加热至液体为红褐色后停止加热
C.持续搅拌使反应充分
实验完成后,向氢氧化铁胶体中逐滴加入稀盐酸的现象为_________。
16. (16分) 无机化合物可根据其组成和性质进行分类,如下图所示。
(1) 该分类法属于_________(填“树状”或“交叉”)分类法。
(2) 下列氧化物属于酸性氧化物的是_________(填编号)。
A.CO B.MgO C.CO D.CaO E.SO
2 3
在上述 A—E 中任选一个酸性氧化物,它与③的溶液反应的离子方程式为_________。
(3) 酸电离出的阳离子均为H+,所以酸的化学性质具有相似性。②的稀溶液与CaO反应的
离子方程式为_________。
高一化学 第 4 页(共 6 页)
{#{QQABSQSUggCoABAAAAhCEQGACAAQkgACCSgGhFAMoAAAiANABAA=}#}(4) 碱在一定条件下可以转化为盐。③转化为⑤的化学方程式为_________(任写一个)。
(5) ⑥属于复盐,其电离方程式为_________。
(6) 只由两种元素组成且其中一种元素是氢元素的化合物称为氢化物。⑧中 H 的化合价为
_________价。已知⑧可以与水反应,生成一种常见的可燃性气体和一种碱,该反应的
化学方程式为_________。
17. (16 分) 某白色粉末中可能含有 BaCl 、K SO 、CaCO 、NaOH、CuSO 中的一种或几种,
2 2 4 3 4
为了探究它的成分,进行以下实验:
①向白色粉末中加入适量的水,充分振荡后过滤,得到白色滤渣A和无色滤液B;
②向白色滤渣A中加入足量稀盐酸,滤渣全部溶解,得到无色气体C;
③将无色气体C通入①中所得无色滤液B中,生成白色沉淀D。
(1) 步骤①中得到的白色滤渣 A 为_________(填名称),步骤②中得到的无色气体 C 为
_________(填化学式)。
(2) 根据上述实验现象可知,该白色粉末中一定含有_________(填化学式)。
(3) 步骤①中过滤所需的玻璃仪器有烧杯、漏斗和_________,它的作用是_________。
(4) 步骤②中发生反应的离子方程式为_________。
(5) 步骤③中生成的白色沉淀 D 为_________(填化学式),发生反应的离子方程式为
_________。
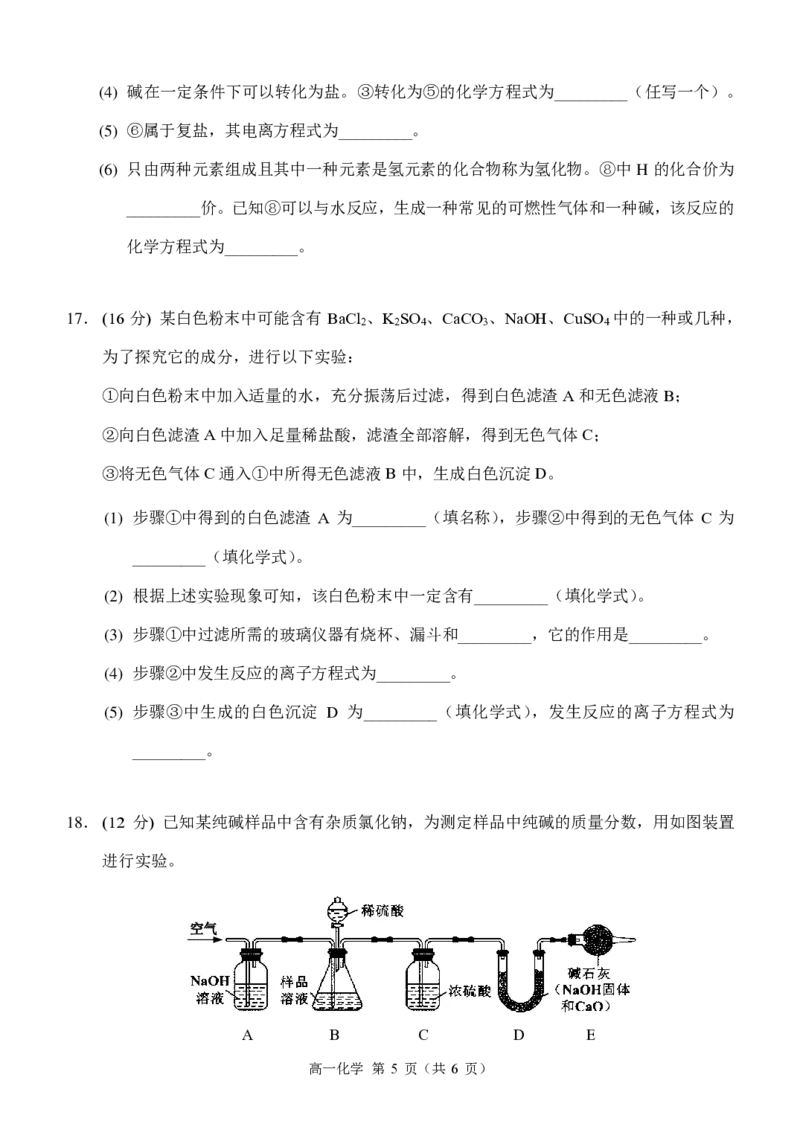
18. (12 分) 已知某纯碱样品中含有杂质氯化钠,为测定样品中纯碱的质量分数,用如图装置
进行实验。
空气
A B C D E
高一化学 第 5 页(共 6 页)
{#{QQABSQSUggCoABAAAAhCEQGACAAQkgACCSgGhFAMoAAAiANABAA=}#}主要步骤如下:
①按图组装仪器,并检查装置的气密性。
②将a g样品放入装置B的锥形瓶中,加适量蒸馏水溶解,得到样品溶液。
③通过装置A通入一段时间空气后,称量装置D的质量为b g。
④通过分液漏斗向装置B的样品溶液,加入稀硫酸,直到不再产生气体。
⑤通过装置A缓缓鼓入一定量空气。
⑥再次称量装置D的质量为c g。
回答下列问题:
(1) 步骤③中称量使用的主要仪器是_________。
(2) 装置B中发生反应的离子方程式为_________。
(3) 装置E的作用是_________。
(4) 如果撤掉装置A,测试的结果将_________(填“偏高”“偏低”或“不变”)。
(5) 步骤⑤的目的是_________。
(6) 该样品中纯碱的质量分数的计算式为 w=_________(用含 a、b、c 的式子表示,要
求化简)。
(命题、审题人:高一化学备课组)
高一化学 第 6 页(共 6 页)
{#{QQABSQSUggCoABAAAAhCEQGACAAQkgACCSgGhFAMoAAAiANABAA=}#}