文档内容
2025—2026 学年度第一学期期末模拟测试
高一化学
注意事项:
1.本卷满分 100 分,考试时间 75 分钟。
2.考生务必将答案涂写答题卡上规定的位置,答在试卷上的无效。
可能用到的相对原子质量:H-1 C-12 N-14 O-16 Mg-24 Al-27 S-32 Cl-35.5 Fe-56
Cu6-4 Zn-65
一、选择题:本题共 14 小题,每小题 3 分,共 42 分。每小题列出的四个选项中,只有一项
符合题目要求。
1. 化学在生产生活中应用广泛,下列叙述错误的是
A. 过氧化钠可作供氧剂 B. Cl 与石灰乳反应制漂白粉
2
C. 铁红常用作红色油漆和涂料 D. 小苏打可用于治疗胃酸过多,成分是 NaCO
2 3
2. 下列化学用语表达正确的是
A. 质量数为 37 的氯原子为 B. 的电子式为:
C. 、 、 互为同位素 D. HClO 的结构式为
3. 下列物质分类的正确组合是
选项 混合物 纯净物 单质 电解质
A 盐酸 NaOH 石墨 KSO 溶液
2 4
B 空气 Fe(OH) 胶体 铁 NaCO
3 2 3
C CuSO ·5HO CaCl 水银 铜
4 2 2
D 氨水 明矾 Cu NaCl
A. A B. B C. C D. D
4. 下列各组离子在指定溶液中能大量共存的是
A. 无色透明的溶液: 、 、 、
B. 强酸性溶液: 、 、 、
第 1页/共 11页C. 强碱性溶液: 、 、 、
D. 含 Fe3+的溶液: 、 、 、
5. 下列各组物质的转化中,不是通过一步反应实现的是
A. B.
C. D.
6. 下列性质的比较,不能用元素周期律解释的是
A. 酸性:HClO>H SO >H PO B. 稳定性:HF>HCl>HBr
4 2 4 3 4
C. 溶解度:NaCO>NaHCO D. 金属性:Na>Mg>Al
2 3 3
7. 下列关于钠、铁、氯及其化合物的说法正确的是
A. 钠投入硫酸铜溶液中,先与水反应生成 NaOH,再与 CuSO 反应生成 Cu(OH) 沉淀
4 2
B. 铁丝在氯气中燃烧,生成 FeCl
2
C 向饱和氯化钠溶液中通入足量 CO,可析出 NaHCO 晶体
2 3
D. 氯水久置后,溶液酸性减弱,漂白性增强
8. 工业上常用“滴定法”测定漂白粉中有效氯含量,涉及反应 。下列说
法不正确的是
A. 该反应中 是还原剂 B. 每生成 1 mol Cl ,转移 1 mol 电子
2
C. 还原性比 强 D. 反应中 H+ 既不是氧化剂也不是还原剂,不参与电
子转移
9. 下列实验方案设计、现象和结论均正确的是
选项 实验方案 现象 结论
向久置在空气中的 NaO 固体滴
2 2
NaO 没有变质成
2 2
A 加足量的稀硫酸,将产生的气体通 溶液未产生白色沉淀
NaCO
2 3
入 CaCl 溶液中
2
将铁的氧化物溶于浓盐酸中,再向 铁的氧化物中含有
Fe2 B 紫色褪去
溶液中滴加酸性 KMnO 4 溶液 + 的铁
第 2页/共 11页C 向 NaS 溶液中通入少量 Cl 产生少量黄色固体 非金属性:Cl>S
2 2
用玻璃棒蘸取 NaClO 溶液点在 pH
D 试纸先变蓝,再变白 溶液只有漂白性
试纸上
A. A B. B C. C D. D
10. N 表示阿伏加德罗常数的值,下列说法中正确的是
A
A. 100mL0.1mol/L 氯水中含氯气分子数为 0.01N
A
B. 常温常压下,22gCO 所含有的分子数为 0.5N
2 A
C. 标准状况下,11.2LI 所含有的碘原子数为 N
2 A
D. 1mol/L 的 CaCl 溶液中含有 Cl-的数目为 2N
2 A
11. 下列离子方程式书写正确的是
A 铝与氢氧化钠溶液反应:
B 铁与稀硫酸反应:
C. 氢氧化钡溶液与稀硫酸反应:
D. 碳酸钙与稀盐酸反应:
12. X、Y、Z、W 为原子序数依次增大的短周期主族元素,X 的最外层电子数是其电子层数的 2 倍,Y 是地
壳中含量最高的金属元素,Z 的最高正价与最低负价代数和为 4,W 的原子半径在同周期最小。下列说法正
确的是
A. 原子序数:Y>Z>W>X B. 简单离子半径:Z>W>Y
C. 最高价氧化物对应水化物酸性:X>W D. 化合物 ZW 中含有离子键
2
13. 如图装置(部分夹持装置省略)所示的实验方案正确的是
A.制备氢氧化亚铁 B.制备 NaHCO
3
第 3页/共 11页C.验证碳酸钠和碳酸氢钠的稳定性 D.证明 Cl 能否溶于 NaOH 溶液
2
A. A B. B C. C D. D
14. “价类二维图”是学习元素化合物知识的高效模型。下图为铁元素的“价类二维图”,图中字母代表含铁元
素的物质。下列判断正确的是
A. X 在高温下与水蒸气反应可生成 Z
B. 在常温下 N 能与氧气、水发生化合反应生成 M
C. Y 是一种红棕色粉末,常用作红色油漆和涂料
D. Q 可以是一种新型净水剂碱式硫酸铁
二、非选择题:本大题共 4 小题,共 58 分。
15. 元素周期表反映元素之间的内在联系,是化学学习、研究和应用的一种重要工具。下图是元素周期表的
一部分。回答下列问题:
(1)元素 b 在元素周期表中的位置是_______。
(2)g、h、i 三种元素对应的简单气态氢化物,其中最稳定的是_______(填化学式)。
(3)下列有关性质的比较,正确的是_______(填字母)
第 4页/共 11页A. 单质的熔点:ah
C. 金属性:d>e D. d 单质可在 CuSO 溶液中置换出 Cu
4
(4)c、d 元素可形成一种淡黄色的离子化合物,该离子化合物中阴离子与阳离子个数之比是_______;该
离子化合物可在呼吸面具中作供氧剂,其原理是_______(用化学方程式表示)。
(5)d 的最高价氧化物对应的水化物与 f 单质可制成一种固体管道疏通剂,加水即可起作用,用离子方程
式解释其疏通原理_______。
(6)用电子式表示 d 和 h 的单质形成化合物的过程_______。
16. 工业上以侯氏制碱法为基础生产焦亚硫酸钠(化学式:NaSO 能溶于水),并获得副产品 CuSO ·5H O
2 2 5 4
的工艺流程如图所示。
已知:反应Ⅰ的原理为
(1)“反应Ⅰ”先向饱和 NaCl 溶液中通入较多的 NH (溶液显碱性),再通入足量的 ,其主要原因是
3
_______(填序号)。
①氨气极易溶于水,且溶液呈碱性,能吸收更多的 CO
2
②NH 比 CO 更易制取
3 2
③CO 的密度比 NH 大
2 3
(2)“反应Ⅰ”生成 NaHCO 晶体,可用_______方法将其从溶液中分离出来。
3
(3)循环使用的物质除 HO 外,还有_______,主要目的是_______。
2
(4)“灼烧”时发生反应的化学方程式为_______。
(5)“反应Ⅲ”_______(填“属于”或“不属于”)氧化还原反应。
(6)流程中“操作”步骤包括: 蒸发浓缩、_______、过滤、洗涤、干燥。
17. 2020 年初,突如其来的新型冠状肺炎在全世界肆虐,社会生产、人民生活都受到了一定程度的影响。某
中学课外实验研究小组的几位同学就查阅了大量资料,并进行相关实验探究,来认识可以有效灭活新型冠
状病毒的含氯消毒剂次氯酸钠 NaClO。
I.次氯酸钠的制备和性质
第 5页/共 11页(1)家中常用的 84 消毒液的有效成分即是次氯酸钠,NaClO 中氯元素的化合价为_______,若将 Cl 通入
2
冷的稀 NaOH 溶液中则可制得消毒液,该反应的离子方程式为_______。
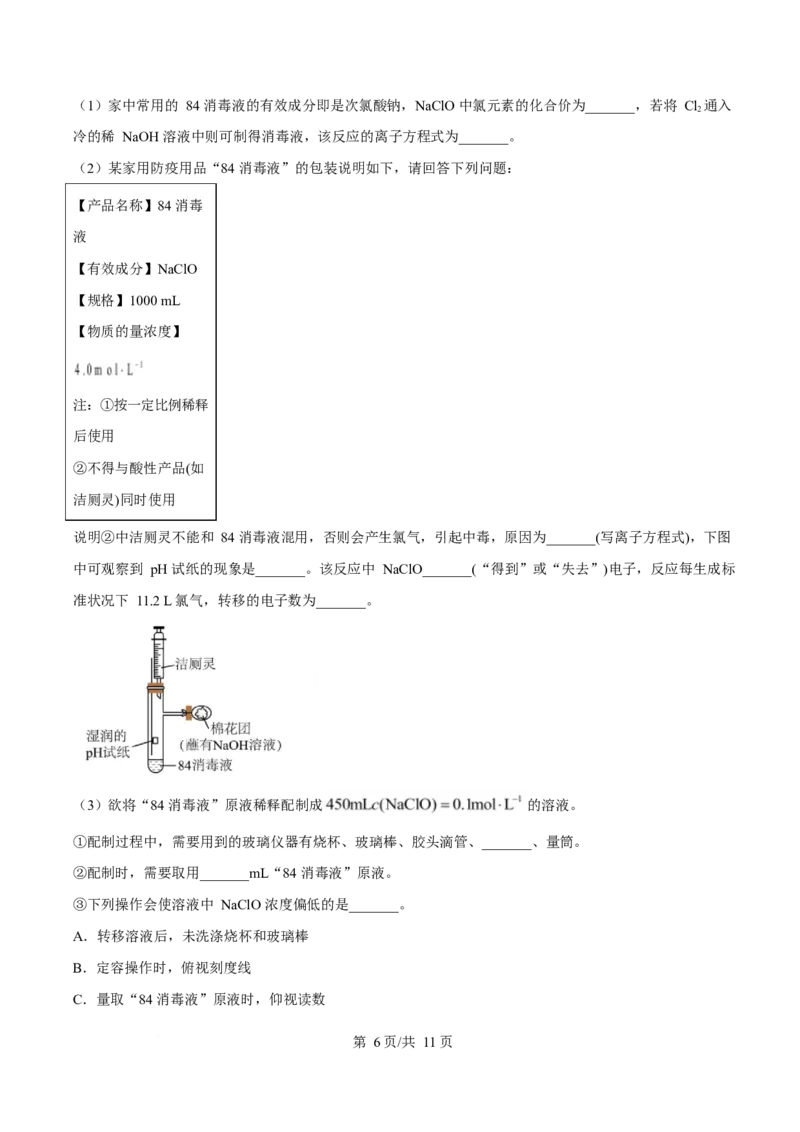
(2)某家用防疫用品“84 消毒液”的包装说明如下,请回答下列问题:
【产品名称】84 消毒
液
【有效成分】NaClO
【规格】1000 mL
【物质的量浓度】
注:①按一定比例稀释
后使用
②不得与酸性产品(如
洁厕灵)同时使用
说明②中洁厕灵不能和 84 消毒液混用,否则会产生氯气,引起中毒,原因为_______(写离子方程式),下图
中可观察到 pH 试纸的现象是_______。该反应中 NaClO_______(“得到”或“失去”)电子,反应每生成标
准状况下 11.2 L 氯气,转移的电子数为_______。
(3)欲将“84 消毒液”原液稀释配制成 的溶液。
①配制过程中,需要用到的玻璃仪器有烧杯、玻璃棒、胶头滴管、_______、量筒。
②配制时,需要取用_______mL“84 消毒液”原液。
③下列操作会使溶液中 NaClO 浓度偏低的是_______。
A.转移溶液后,未洗涤烧杯和玻璃棒
B.定容操作时,俯视刻度线
C.量取“84 消毒液”原液时,仰视读数
第 6页/共 11页D.定容摇匀后,液面低于刻度线,再加水至刻度线
Ⅱ.同学们探究 84 消毒液在不同 pH 下使红纸褪色的情况,做了如下实验。
步骤 1:将 5 mL 市售 84 消毒液稀释 100 倍,测得稀释后溶液的 pH=12;
步骤 2:将稀释后的溶液各 20 mL 分别加入 a、b、c 三个洁净的烧杯中;
步骤 3:用 HSO 溶液将 a、b、c 三个烧杯内溶液的 pH 分别调至 10、7 和 4(溶液体积变化忽略不计);
2 4
步骤 4:在 3 个烧杯中分别放入大小相同的红纸,观察现象,记录如表。
烧杯 溶液的 pH 现象
10min 后,红纸基本不
a 10
褪色;4h 后红纸褪色
10min 后,红纸颜色变
b 7
浅;4h 后红纸褪色
10min 后,红纸颜色比
c 4 b 烧杯中 10min 后 浅
;4h 后红纸褪色
已知溶液中 Cl、HCIO 和 的物质的量分数(α)随溶液 pH 变化的关系如图所示:
2
(4)由实验现象可获得结论:溶液的 pH 在 4-10 范围内,pH 越大,红纸褪色_______(填“越快”或“越慢”)
。
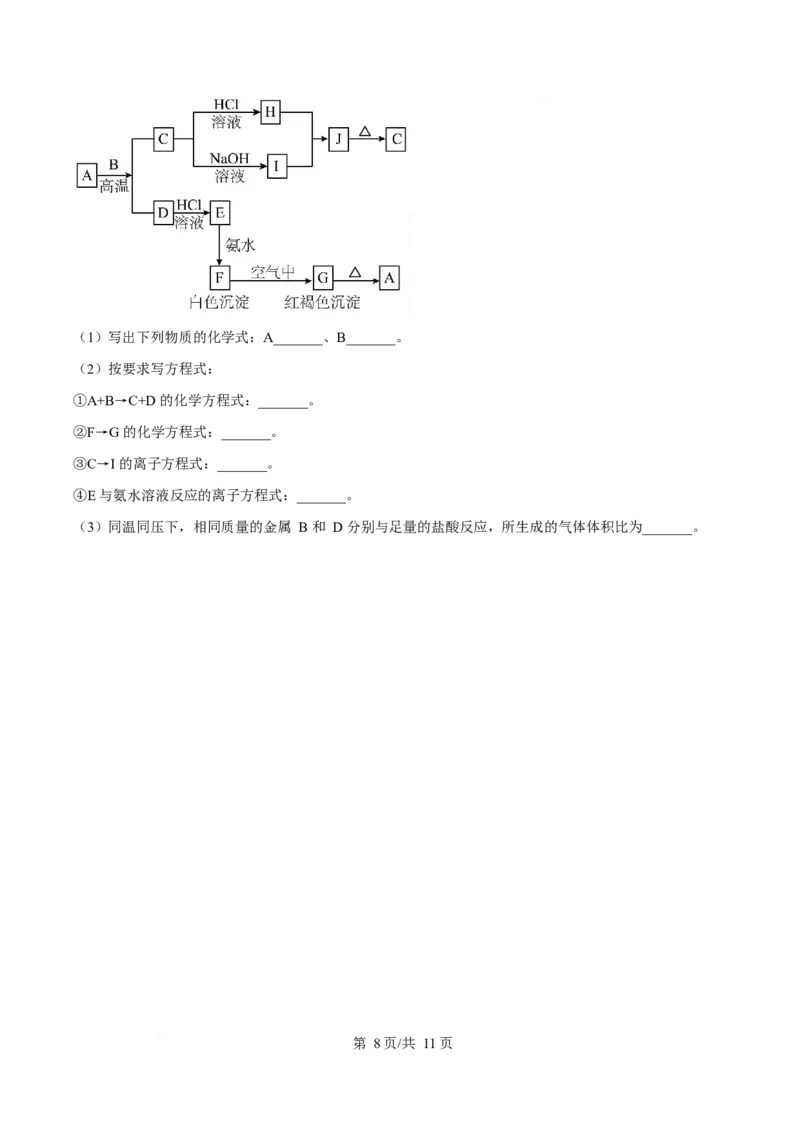
18. 已知 A 是一种红棕色金属氧化物,B、D 是金属单质,C 是两性金属氧化物,J 是一种难溶于水的白色
化合物,受热后容易发生分解。
第 7页/共 11页(1)写出下列物质的化学式:A_______、B_______。
(2)按要求写方程式:
①A+B→C+D 的化学方程式:_______。
②F→G 的化学方程式:_______。
③C→I 的离子方程式:_______。
④E 与氨水溶液反应的离子方程式:_______。
(3)同温同压下,相同质量的金属 B 和 D 分别与足量的盐酸反应,所生成的气体体积比为_______。
第 8页/共 11页2025—2026 学年度第一学期期末模拟测试
高一化学
注意事项:
1.本卷满分 100 分,考试时间 75 分钟。
2.考生务必将答案涂写答题卡上规定的位置,答在试卷上的无效。
可能用到的相对原子质量:H-1 C-12 N-14 O-16 Mg-24 Al-27 S-32 Cl-35.5 Fe-56
Cu6-4 Zn-65
一、选择题:本题共 14 小题,每小题 3 分,共 42 分。每小题列出的四个选项中,只有一项
符合题目要求。
【1 题答案】
【答案】D
【2 题答案】
【答案】A
【3 题答案】
【答案】D
【4 题答案】
【答案】C
【5 题答案】
【答案】A
【6 题答案】
【答案】C
【7 题答案】
【答案】A
【8 题答案】
【答案】A
【9 题答案】
【答案】C
【10 题答案】
【答案】B
第 9页/共 11页【11 题答案】
【答案】B
【12 题答案】
【答案】B
【13 题答案】
【答案】D
【14 题答案】
【答案】B
二、非选择题:本大题共 4 小题,共 58 分。
【15 题答案】
【答案】(1)第二周期第ⅣA 族
(2)HCl (3)BC
(4) ①. ②. 或者
(5)
(6)
【16 题答案】
【答案】(1)① (2)过滤
(3) ①. CO ②. 提高原料利用率
2
(4)
(5)不属于 (6)冷却结晶
【17 题答案】
【答案】(1) ①. +1 价 ②.
(2) ①. ②. 先变红后褪色 ③. 得到 ④. 或
(3) ①. 500 mL 容量瓶 ②. 12.5 ③. AD
(4)越慢
【18 题答案】
第 10页/共 11页【答案】(1) ①. Fe O ②. Al
2 3
( 2) ① . ② . ③ .
④.
(3)
第 11页/共 11页