文档内容
200 2 年上海高考化学真题及答案
本试卷分为第Ⅰ卷(第1~4页)和第Ⅱ卷(第5~10页)两部分。全卷共10页。满
分150分。考试时间120分钟。
第I卷(共66分)
考生注意:
1.答第Ⅰ卷前。考生务必在答题卡上用钢笔或圆珠笔清楚填写姓名、准考证号、校验
码,并用铅笔正确涂写准考证号和校验码。
2.第Ⅰ卷(1~22题),由机器阅卷,答案必须全部涂写在答题纸上。考生应将代表
正确答案的小方格用铅笔涂黑。注意试题题号和答题纸编号—一对应,不能错位。答案需
要更改时,必须将原选项用橡皮擦去,重新选择。答案不能写在试卷上,写在试卷上一律
不给分。
可能用到的相对原子质量:
H-1 C-12 N-14 O-16 S-32 Cl-35.5 K-39 Ca-40 Cu-64
一、选择题(本题共10分),每小题2分,只有一个正确选项,答案涂写在答题纸上。
1.为维持人体内电解质平衡,人在大量出汗后应及时补充的离子是 C
A. Mg2+ B. Ca2+ C. Na+ D. Fe3+
2.C 与现代足球 有很相似的结构,它与石墨互为 B
60
A 同位素 B 同素异形体 C 同分异构体 D 同系物
3.下列表达方式错误的是 C
A 甲烷的电子式
B. 氟化钠的电子式
C. 硫离子的核外电子排布式 1s22s22p63s23p4
D. 碳-12原子
4.将饱和FeCl 溶液分别滴入下述液体中,能形成胶体的是 B
3
A. 冷水 B. 沸水 C. NaOH浓溶液 D. NaCl浓溶液
5.两次获得诺贝尔奖,在化学界享有盛名的科学家是 C
A. 爱因斯坦 B. 达尔文 C. 居里夫人 D. 欧拉
二、选择题(本题共36分),每小题3分,只有一个正确选项,答案涂写在答题纸上。
6.有人认为在元素周期表中,位于ⅠA族的氢元素,也可以放在ⅦA族,下列物质能
支持这种观点的是 C
第1页 | 共11页
A. HF B. HO+ C. NaH D. HO
3 2 2
解析:NaH与NaCl都是离子化合物,H 与Cl 相似。
7.在下列有关晶体的叙述中错误的是 C
A. 离子晶体中,一定存在离子键 B. 原子晶体中,只存在共价键
C. 金属晶体的熔沸点均很高 D. 稀有气体的原子能形成分子晶体
解析:金属晶体的熔沸点可能比较高,如金属钨的熔点可达3410℃;而金属汞的熔点
非常低,常温下呈液态,故C项的说法是错误的。对于稀有气体是单原子分子,它们可按
范德华力结合成分子晶体,因此D项是正确的。
8.N为阿佛加德罗常数,下述正确的是 A
A
A. 80 g硝酸铵含有氮原子数为2N
A
B. 1 L 1 mol / L的盐酸溶液中,所含氯化氢分子数为N
A
C. 标准状况下,11.2 L四氯化碳所含分子数为0.5 N
A
D. 在铜与硫的反应中,1 mol铜失去的电子数为2 N
A
9.在pH=1的无色溶液中能大量共存的离子组是 A
A. 、Mg2+、 、Cl- B. Ba2+、K+、OH-、
C. Al3+、Cu2+、 、Cl- D. Na+、Ca2+、Cl-、
10.水的状态除了气、液和固态外,还有玻璃态。它是由液态水急速冷却到165K时形
成的,玻璃态的水无固定形状,不存在晶体结构,且密度与普通液态水的密度相同,有关
玻璃态水的叙述正确的是 C
A. 水由液态变为玻璃态,体积缩小 B. 水由液态变为玻璃态,体积膨胀
C. 玻璃态是水的一种特殊状态 D. 玻璃态水是分子晶体
解析:玻璃态水的的密度与普通液态水的密度相同,因此体积不会减小,也不会膨胀。
玻璃态的水无固定形状,不存在晶体结构,也不会是晶体。故只有C的叙述是正确的。
11.已知自然界氧的同位素有16O、17O、18O,氢的同位素有 H、D,从水分子的原子组
成来看,自然界的水一共有 C
A. 3种 B. 6种 C. 9种 D. 12种
12.维通橡胶是一种耐腐蚀、耐油、耐高温、耐寒性能
都特别好的氟橡胶。它的结构简式见右图:
合成它的单体为 B
A. 氟乙烯和全氟异丙烯 B. 1,1-二氟乙烯和全氟丙烯
C. 1-三氟甲基-1,3-丁二烯 D. 全氟异戊二烯
13.以下实验能获得成功的是 D
A. 用含结晶水的醋酸钠和碱石灰共热制甲烷气体
B. 将铁屑、溴水、苯混合制溴苯
C. 在苯酚溶液中滴入少量稀溴水出现白色沉淀
第2页 | 共11页D. 将铜丝在酒精灯上加热后,立即伸入无水乙醇中,铜丝恢复成原来的红色
14.拟除虫菊酯是一类高效、低毒、对昆
虫具有强烈触杀作用的杀虫剂,其中对光稳定
的溴氰菊酯的结构简式如右图:
下列对该化合物叙述正确的是
D
A. 属于芳香烃 B. 属于卤代烃
C. 在酸性条件下不水解 D. 在一定条件下可以发生加成反应
解析:只含有C、H且带有苯环的有机物是芳香烃,卤代烃分子里只含有C、H和卤素
原子,而所给的物质还含有N和O原子,所以它既不是芳香烃,也不是卤代烃。该分子里
含有酯基,可以在碱性或酸性条件下水解,分子里含有碳碳双键,是可以发生加成反应的
故正确的是D。
15.将足量CO 通人KOH和CaOH 的混合稀溶液中,生成沉淀的物质的量(n)和通入
2 2
CO 体积(y)的关系正确的是 D
2
A B C D
16.某学生想制作一种家用环保型消毒液发生器,用石墨作电极电
解饱和氯化钠溶液,通电时,为使Cl 被完全吸收,制得有较强杀菌能
2
力的消毒液,设计了如图的装置,则对电源电极名称和消毒液的主要成
分判断正确的是 B
A. a为正极,b为负极;NaClO和NaCl
B. a为负极,b为正极;NaClO和NaCl
C. a为阳极,b为阴极;HClO和NaCl
D. a为阴极,b为阳极;HClO和NaCl
解析:用石墨做电极电解饱和食盐水发生的反应是:2NaCl+2HO 2NaOH+
2
H↑+Cl↑。伴随电解过程所发生的副反应是Cl +2NaOH=NaCl+NaClO+HO,则可推知
2 2 2 2
使Cl 被完全吸收制得有较强杀菌能力的消毒液主要成分是NaClO和NaCl,起消毒作用的
2
是NaClO。电解过程阴极产生氢气,结合图示,,消毒液发生器的液体上部空间充满的是
氢气,从中推知电源a极是负极,b极为正极。
17.1998年诺贝尔化学奖授予科恩(美)和波普尔(英),以表彰他们在理论化学领
域作出的重大贡献。他们的工作使实验和理论能够共同协力探讨分子体系的性质,引起整
个化学领域正在经历一场革命性的变化。下列说法正确的是
A
A. 化学不再是纯实验科学 B. 化学不再需要实验
C. 化学不做实验,就什么都不知道 D. 未来化学的方向还是经验化
三、选择题(本题共20分),每小题4分,每小题有一个或两个正确选项。只有一个
正确选项的,多选不给分;有两个正确选项的,选对一个给 2分,选错一个该小题不给分,
答案涂写在答题纸上。
18.在相同温度时100 mL 0.01 mol / L的醋酸溶液与10 mL 0.01 mol / L的醋酸溶
第3页 | 共11页液 相 比 较 , 下 列 数 值 前 者 大 于 后 者 的 是
BC
A. 中和时所需NaOH的量 B. 电离度
C. 对的物质的量 D. CHCOOH的物质的量
3
19.下列离子方程式书写正确的是 B
A. FeCl 溶液中通入Cl:Fe2++Cl→Fe3++2Cl-
2 2 2
B. 澄清石灰水与少量小苏打溶液混合:Ca2+十OH-+ →CaCO↓+HO
3 2
C. FeS固体放入稀硝酸溶液中:FeS+2H+→Fe2++HS↑
2
D. AlCl 溶液中加入过量氨水:Al3++4OH-→ +2HO
3 2
解析:A违背了离子电荷守恒,B;C违背了客观性原理,稀硝酸将氧化FeS,不可能
生成氢气。D 既违背了书写规则,又违背了客观性原理,氨水应写 NH·HO,生成的
3 2
AlOH 不会溶解于氨水中:Al3++3NH·HO=AlOH+3
3 3 2 3
20.在常温下10 mL pH=10的KOH溶液中,加人pH=4的一元酸HA溶液至pH刚好等
于7(假设反应前后体积不变),则对反应后溶液的叙述正确的是 AD
A. cA-=cK+ B. cH+=cOH-<cK+<cA-
C. V ≥20 mL D. V ≤20 mL
总 总
21.混合下列各组物质使之充分反应,加热蒸干产物并在300℃灼烧至质量不变,最
终残留固体为纯净物的是
BD
A. 向CuSO 溶液中加入适量铁粉
4
B. 等物质的量浓度、等体积的NHSO 与BaCl 溶液
4 2 4 2
C. 等物质的量的NaHCO 与NaO 固体
3 2 2
D. 在NaBr溶液中通入过量氯气
22.0.03 mol铜完全溶于硝酸,产生氮的氧化物NO、NO、NO 混合气体共0.05 mol。
2 2 4
该混合气体的平均相对分子质量可能是 BC
A. 30 B. 46 C. 50 D. 66
第Ⅱ卷(共84分)
考生注意:
1.答第Ⅱ卷前,考生务必将姓名、准考证号、校验码等填写清楚。
2.第Ⅱ卷从第23题到第31题,考生应用钢笔或圆珠笔将答案直接写在试卷上。
四、(本题共24分)
23.在氯氧化法处理含CN-的废水过程中,液氯在碱性条件下可以将氰化物氧化成氰
酸盐(其毒性仅为氰化物的千分之一),氰酸盐进一步被氧化为无毒物质。
(1)某厂废水中含KCN,其浓度为650 mg / L。现用氯氧化法处理,发生如下反应
(其中N均为-3价):
KCN+2KOH+Cl → KOCN+2KCl+HO
2 2
被氧化的元素是 _________ _ 。
(2)投入过量液氯,可将氰酸盐进一步氧化为氮气。请配平下列化学方程式,并标出
第4页 | 共11页电子转移方向和数目:
KOCN+ KOH+ Cl → CO + N + KCl + HO
2 2 2 2
(3)若处理上述废水20 L,使KCN完全转化为无毒物质,至少需液氯 g。
23.(1)碳或(C)
(3) 35.5
24.在一定体积的密闭容器中,进行如下化学反应:COg+Hg COg+HO
2 2 2
(g),
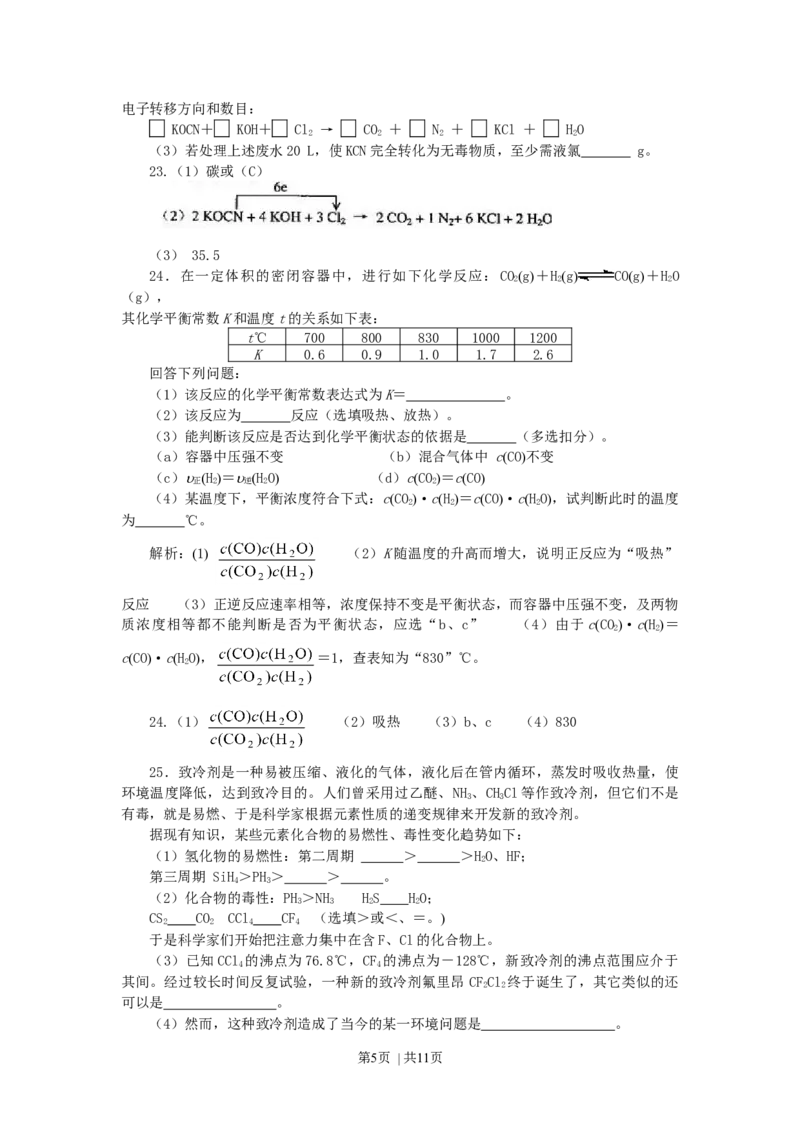
其化学平衡常数K和温度t的关系如下表:
t℃ 700 800 830 1000 1200
K 0.6 0.9 1.0 1.7 2.6
回答下列问题:
(1)该反应的化学平衡常数表达式为K= 。
(2)该反应为 反应(选填吸热、放热)。
(3)能判断该反应是否达到化学平衡状态的依据是 (多选扣分)。
(a)容器中压强不变 (b)混合气体中 cCO不变
(c) H= HO (d)cCO=cCO
正 2 逆 2 2
(4)某温度下,平衡浓度符合下式:cCO·cH=cCO·cHO,试判断此时的温度
2 2 2
为 ℃。
解析:1 (2)K随温度的升高而增大,说明正反应为“吸热”
反应 (3)正逆反应速率相等,浓度保持不变是平衡状态,而容器中压强不变,及两物
质浓度相等都不能判断是否为平衡状态,应选“b、c” (4)由于cCO·cH=
2 2
cCO·cHO, =1,查表知为“830”℃。
2
24.(1) (2)吸热 (3)b、c (4)830
25.致冷剂是一种易被压缩、液化的气体,液化后在管内循环,蒸发时吸收热量,使
环境温度降低,达到致冷目的。人们曾采用过乙醚、NH 、CHCl等作致冷剂,但它们不是
3 3
有毒,就是易燃、于是科学家根据元素性质的递变规律来开发新的致冷剂。
据现有知识,某些元素化合物的易燃性、毒性变化趋势如下:
(1)氢化物的易燃性:第二周期 > >HO、HF;
2
第三周期 SiH>PH> > 。
4 3
(2)化合物的毒性:PH>NH HS HO;
3 3 2 2
CS CO CCl CF (选填>或<、=。
2 2 4 4
于是科学家们开始把注意力集中在含F、Cl的化合物上。
(3)已知CCl 的沸点为76.8℃,CF 的沸点为-128℃,新致冷剂的沸点范围应介于
4 4
其间。经过较长时间反复试验,一种新的致冷剂氟里昂 CFCl 终于诞生了,其它类似的还
2 2
可以是 。
(4)然而,这种致冷剂造成了当今的某一环境问题是 。
第5页 | 共11页但求助于周期表中元素及其化合物的 变化趋势来开发致冷剂的科学思维方法是
值得借鉴的。(填写字母,多选扣分)
① 毒性 ② 沸点 ③ 易燃性 ④ 水溶性 ⑤ 颜色
(a)①②③ (b)②④⑤ (c)②③④
25.(1)CH>NH,HS>HCl (2) > ,>
4 3 2
(3) CFCl 或CFCl) (4)使大气臭氧层出现空洞
3( 3
五、(本题共24分)
26.为探究乙炔与溴的加成反应,甲同学设计并进行了如下实验:先取一定量工业用
电石与水反应,将生成的气体通入溴水中,发现溶液褪色,即证明乙炔与溴水发生了加成
反应。
乙同学发现在甲同学的实验中,褪色后的溶液里有少许淡黄色浑浊,推测在制得的乙
炔中还可能含有少量还原性的杂质气体,由此他提出必须先除去之,再与溴水反应。
请你回答下列问题:
(1)写出甲同学实验中两个主要的化学方程式 。
(2)甲同学设计的实验 (填能或不能)验证乙炔与澳发生加成反应,其理由
是 (多选扣分)。
(a)使溴水褪色的反应,未必是加成反应
(b)使溴水褪色的反应,就是加成反应
(c)使溴水褪色的物质,未必是乙炔
(d)使溴水褪色的物质,就是乙炔
(3)乙同学推测此乙炔中必定含有的一种杂质气体是 ,它与溴水反应的化
学方程式是 ;在验证过程中必须全部除去。
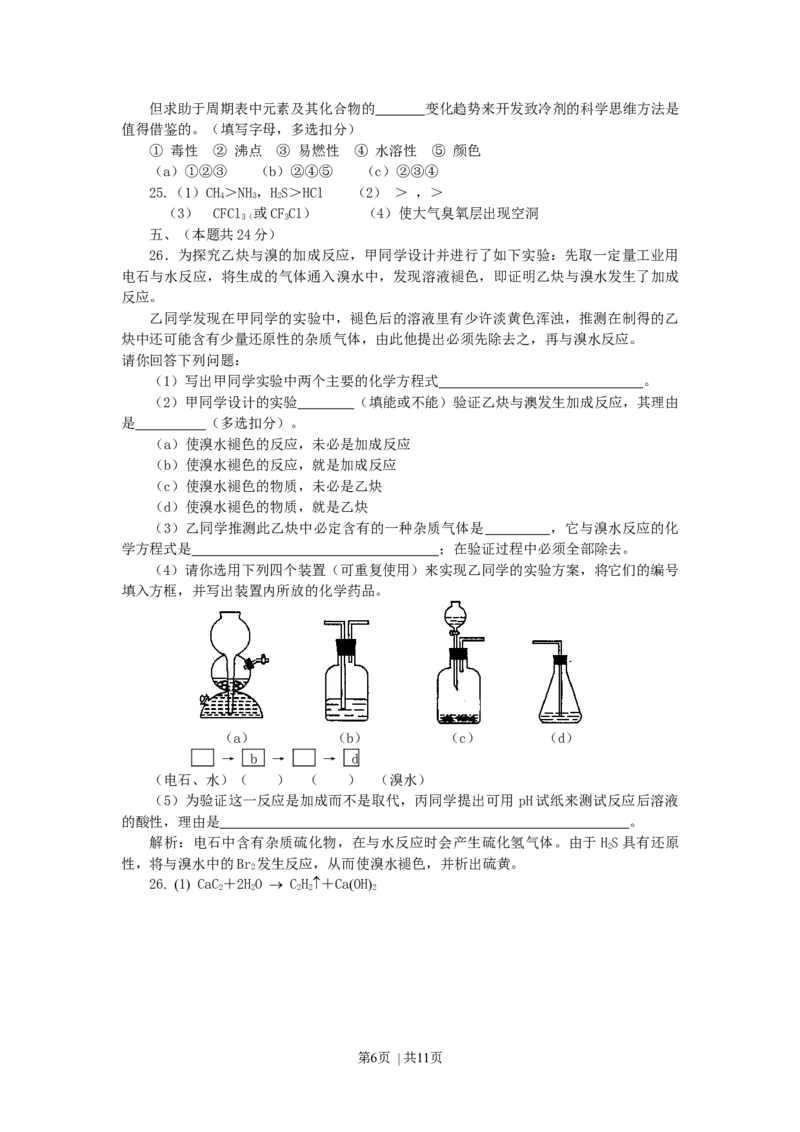
(4)请你选用下列四个装置(可重复使用)来实现乙同学的实验方案,将它们的编号
填入方框,并写出装置内所放的化学药品。
(a) (b) (c) (d)
→ b → → d
(电石、水)( ) ( ) (溴水)
(5)为验证这一反应是加成而不是取代,丙同学提出可用 pH试纸来测试反应后溶液
的酸性,理由是 。
解析:电石中含有杂质硫化物,在与水反应时会产生硫化氢气体。由于HS具有还原
2
性,将与溴水中的Br 发生反应,从而使溴水褪色,并析出硫黄。
2
26 1 CaC+2HO CH+CaOH
2 2 2 2 2
第6页 | 共11页+
(2)不能 a、c
(3)HS Br+HS→S↓+2HBr
2 2 2
(4) c b
(CuSO 溶液)(CuSO 溶液)
4 4
(5)如若发生取代反应,必定生成HBr,溶液酸性将会明显增强,故可用pH试纸验
证。
27.Ag/α-AlO 是石油化学工业的一种重要催化剂,其中Ag起催化作用,α-AlO
2 3 2 3
是载体且不溶于硝酸,该催化剂的回收实验如下图所示。其中的转化反应为:
6AgCl+FeO→3AgO+2FeCl
2 3 2 3
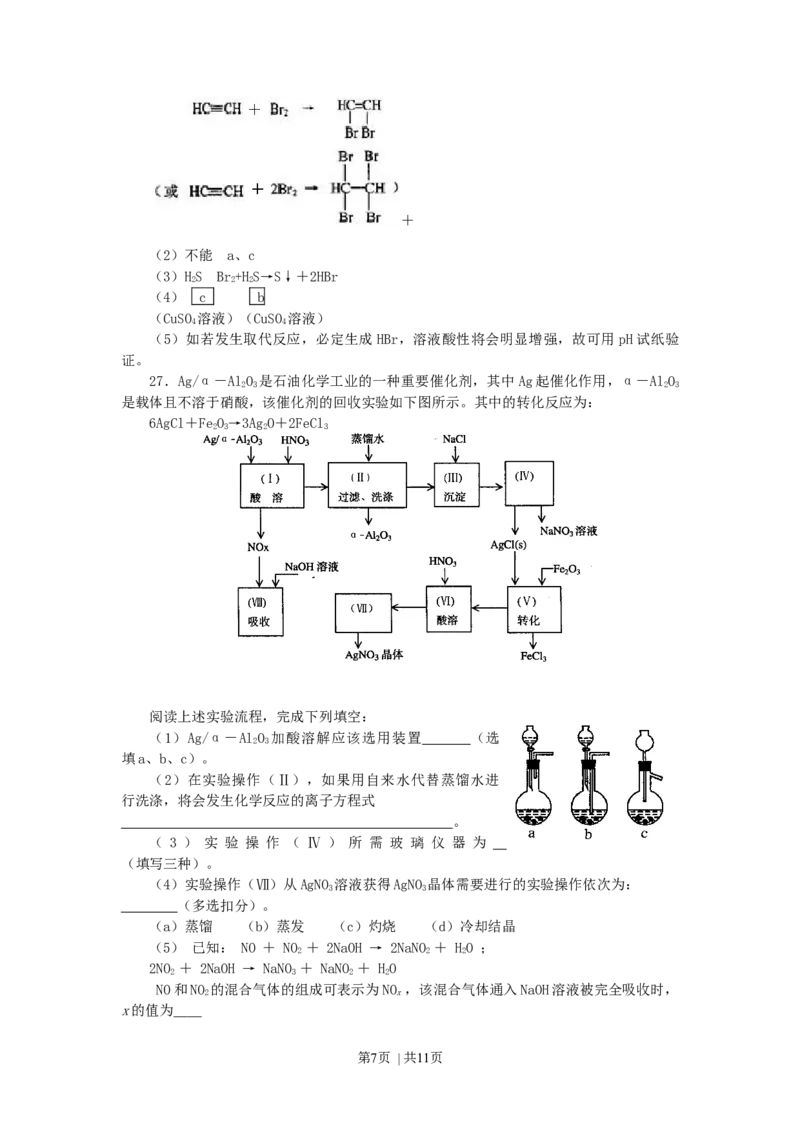
阅读上述实验流程,完成下列填空:
(1)Ag/α-AlO 加酸溶解应该选用装置 (选
2 3
填a、b、c)。
(2)在实验操作(Ⅱ),如果用自来水代替蒸馏水进
行洗涤,将会发生化学反应的离子方程式
。
( 3 ) 实 验 操 作 ( Ⅳ ) 所 需 玻 璃 仪 器 为
(填写三种)。
(4)实验操作(Ⅶ)从AgNO 溶液获得AgNO 晶体需要进行的实验操作依次为:
3 3
(多选扣分)。
(a)蒸馏 (b)蒸发 (c)灼烧 (d)冷却结晶
(5) 已知: NO + NO + 2NaOH → 2NaNO + HO ;
2 2 2
2NO + 2NaOH → NaNO + NaNO + HO
2 3 2 2
NO和NO 的混合气体的组成可表示为NO ,该混合气体通入NaOH溶液被完全吸收时,
2 x
x的值为__
第7页 | 共11页(a)x≤1.5 (b)x=1.2 (c)x≥1.5
已知Ag/α—AlO 中Ag的质量分数,若计算Ag的回收率,还必须知道的实验数据为
2 3
和 。
27.(1)a
(2)Ag++Cl-→AgCl↓
(3)漏斗、烧杯、玻棒
(4)b、c、d
(5)c
(6)催化剂的质量,AgNO 的质量
3
六、(本题共20分)
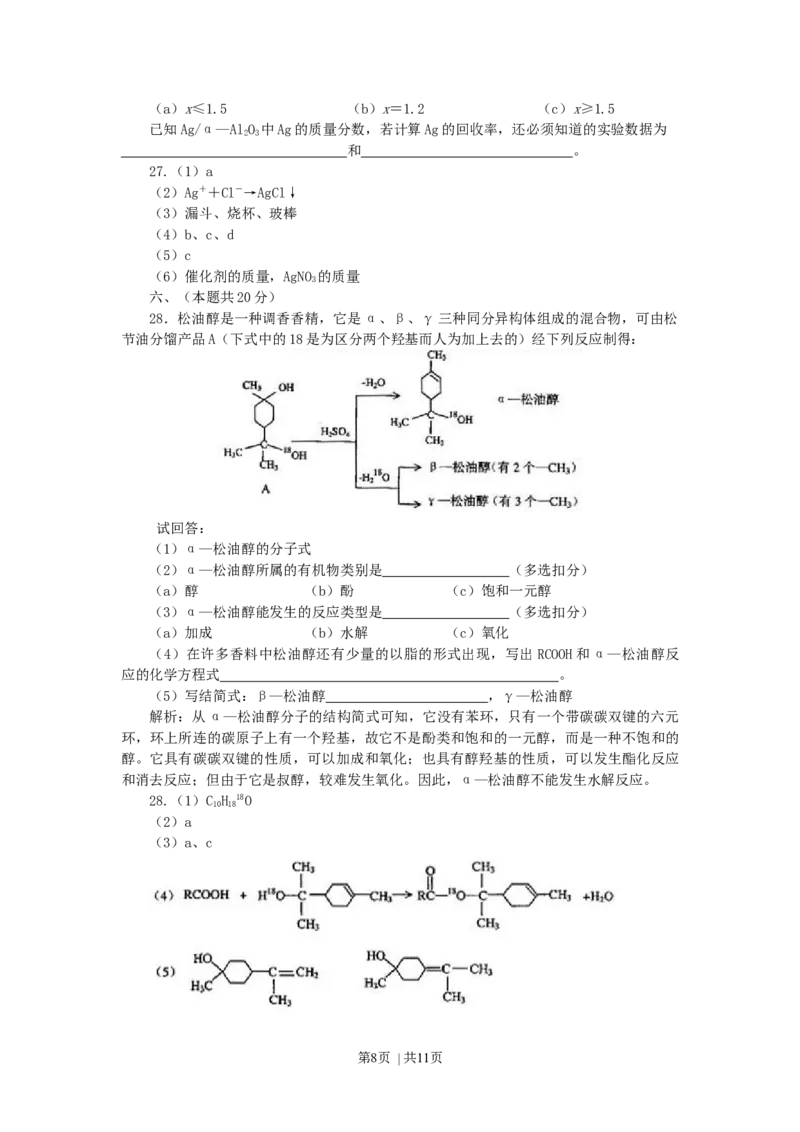
28.松油醇是一种调香香精,它是α、β、γ三种同分异构体组成的混合物,可由松
节油分馏产品A(下式中的18是为区分两个羟基而人为加上去的)经下列反应制得:
试回答:
(1)α—松油醇的分子式
(2)α—松油醇所属的有机物类别是 (多选扣分)
(a)醇 (b)酚 (c)饱和一元醇
(3)α—松油醇能发生的反应类型是 (多选扣分)
(a)加成 (b)水解 (c)氧化
(4)在许多香料中松油醇还有少量的以脂的形式出现,写出RCOOH和α—松油醇反
应的化学方程式 。
(5)写结简式:β—松油醇 ,γ—松油醇
解析:从α—松油醇分子的结构简式可知,它没有苯环,只有一个带碳碳双键的六元
环,环上所连的碳原子上有一个羟基,故它不是酚类和饱和的一元醇,而是一种不饱和的
醇。它具有碳碳双键的性质,可以加成和氧化;也具有醇羟基的性质,可以发生酯化反应
和消去反应;但由于它是叔醇,较难发生氧化。因此,α—松油醇不能发生水解反应。
28.(1)C H 18O
10 18
(2)a
(3)a、c
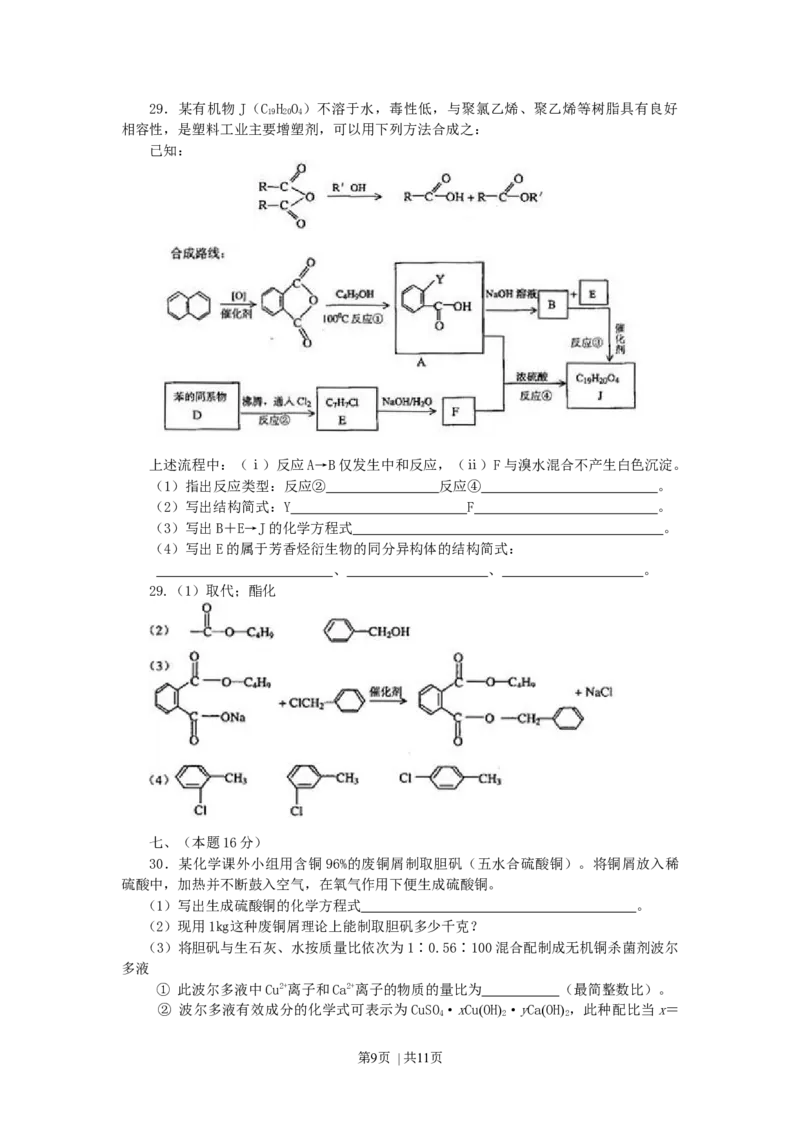
第8页 | 共11页29.某有机物J(C H O )不溶于水,毒性低,与聚氯乙烯、聚乙烯等树脂具有良好
19 20 4
相容性,是塑料工业主要增塑剂,可以用下列方法合成之:
已知:
上述流程中:(ⅰ)反应A→B仅发生中和反应,(ⅱ)F与溴水混合不产生白色沉淀。
(1)指出反应类型:反应② 反应④ 。
(2)写出结构简式:Y F 。
(3)写出B+E→J的化学方程式 。
(4)写出E的属于芳香烃衍生物的同分异构体的结构简式:
、 、 。
29.(1)取代;酯化
七、(本题16分)
30.某化学课外小组用含铜96%的废铜屑制取胆矾(五水合硫酸铜)。将铜屑放入稀
硫酸中,加热并不断鼓入空气,在氧气作用下便生成硫酸铜。
(1)写出生成硫酸铜的化学方程式 。
(2)现用1㎏这种废铜屑理论上能制取胆矾多少千克?
(3)将胆矾与生石灰、水按质量比依次为1∶0.56∶100混合配制成无机铜杀菌剂波尔
多液
① 此波尔多液中Cu2+离子和Ca2+离子的物质的量比为 (最简整数比)。
② 波尔多液有效成分的化学式可表示为CuSO·xCuOH·yCaOH ,此种配比当x=
4 2 2
第9页 | 共11页1时,试确定у的数值。
30.(1)2Cu+O+2HSO→2CuSO+2HO
2 2 4 4 2
(2)
(3) ① 2∶5
② CuSO+CaOH CuOH+CaSO
4 2 2 4
反应前 2 5 0 0
反应后 1 4 1 1
因此,CuSO·CuOH·yCaOH 中,y=4
4 2 2
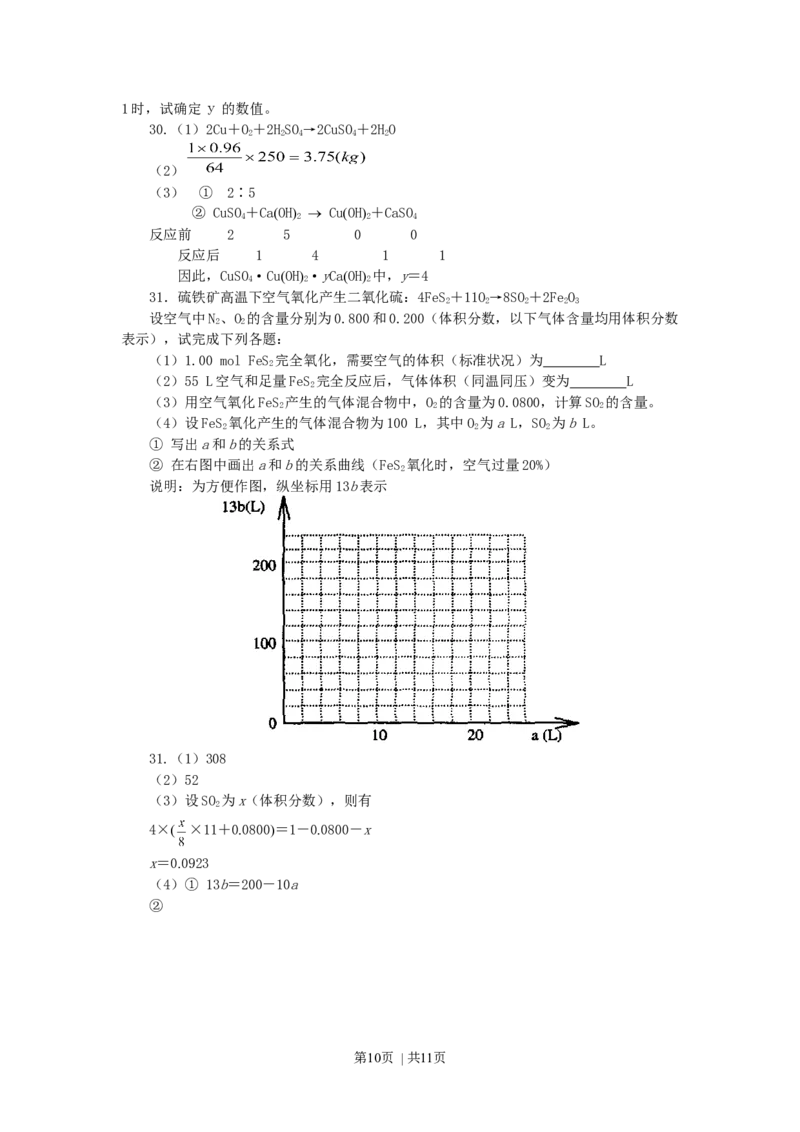
31.硫铁矿高温下空气氧化产生二氧化硫:4FeS+11O→8SO+2FeO
2 2 2 2 3
设空气中N、O 的含量分别为0.800和0.200(体积分数,以下气体含量均用体积分数
2 2
表示),试完成下列各题:
(1)1.00 mol FeS 完全氧化,需要空气的体积(标准状况)为 L
2
(2)55 L空气和足量FeS 完全反应后,气体体积(同温同压)变为 L
2
(3)用空气氧化FeS 产生的气体混合物中,O 的含量为0.0800,计算SO 的含量。
2 2 2
(4)设FeS 氧化产生的气体混合物为100 L,其中O 为a L,SO 为b L。
2 2 2
① 写出a和b的关系式
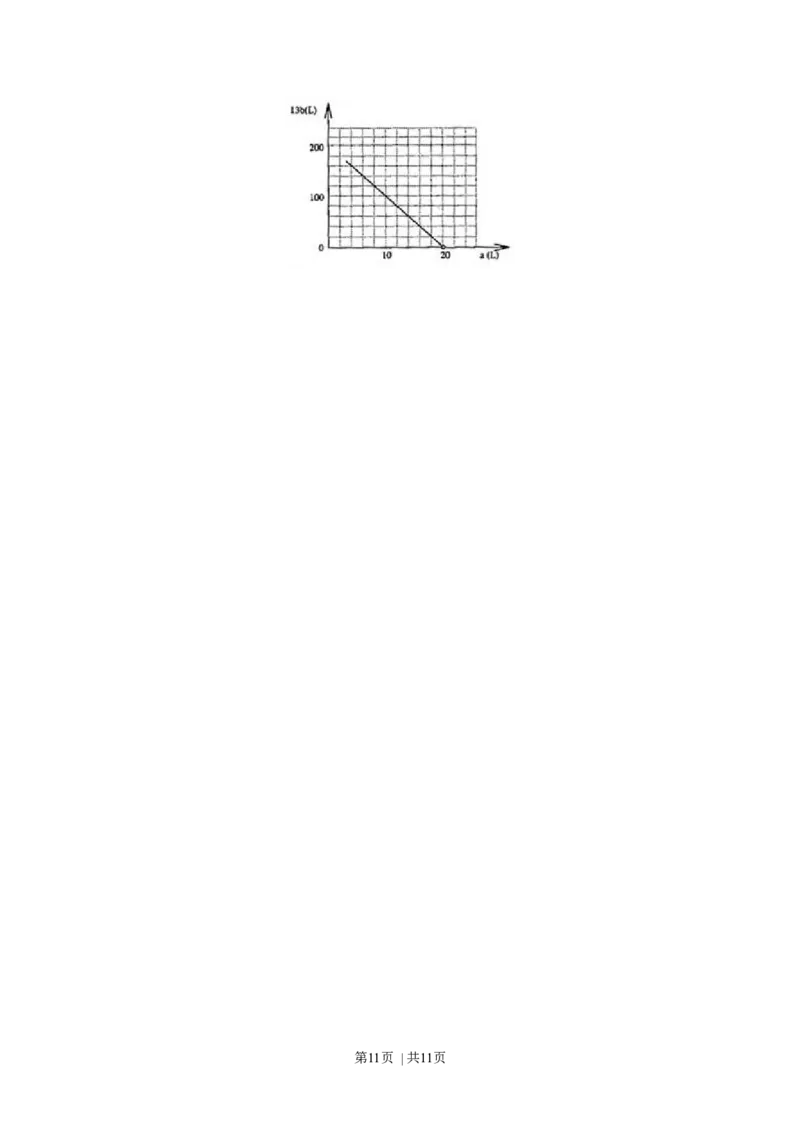
② 在右图中画出a和b的关系曲线(FeS 氧化时,空气过量20%)
2
说明:为方便作图,纵坐标用13b表示
31.(1)308
(2)52
(3)设SO 为x(体积分数),则有
2
4× ×11+00800=1-00800-x
x=00923
(4)① 13b=200-10a
②
第10页 | 共11页第11页 | 共11页