文档内容
【试卷总评】
本试卷整体特点是:题型与往年类似、总体难度不大、亮点比较多。其中第9题要注意反
应是在“常温下”;第10题的B项水的离子积不变,但n(H+)与n(OH-)的乘积随溶液的体积
而发生变化;第11题D项转移电子数与离子的减少数不等;第12题以图表、数据形式,给出
一氧化二氮分解的实验数据,学生要提取有效信息,利用图表中的横纵坐标,进行分析,其中,
试题中半衰期是一个提示,学生要能从中分析出半衰期的变化规律,分析得出4个选项中相一
致的正确项;第25题以“焦亚硫酸钠的制取、性质、含量的测定”为素材,考查学生的化学
实验综合探究能力,对学生的分析解决问题的能力要求很高。这些对高考考试方向均很好的导
向作用,在教与学中不能把有些知识讲得太绝对,要具体问题进行具体分析,切忌思维定势。
第 I 卷
6.下列有关物质应用的说法正确的是
A.生石灰用作食品抗氧剂 B.盐类都可作调味品
C.铝罐可久盛食醋 D.小苏打是面包发酵粉的主要成分
7.下列关于乙醇的说法不正确的是
A.可用纤维素的水解产物制取 B.可由乙烯通过加成反应制取
C.与乙醛互为同分异构体 D.通过取代反应可制取乙酸乙酯
8.下列实验能达到目的的是
A.只滴加氨水鉴别NaCl、AlCl 、MgCl 、Na SO 四种溶液
3 2 2 4
B.将NH Cl溶液蒸干制备NH Cl固体
4 4
C.用萃取分液的方法除去酒精中的水
D.用可见光束照射以区别溶液和胶体
9.常温下,下列各组物质中,Y既能与X反应又能与Z反应的是
X Y Z
[来源:学科网ZXXK]
① NaOH溶液 Al(OH) 稀硫酸
3
② KOH溶液 SiO 稀盐酸
2
③ O N H
2 2 2
第1页 | 共6页④ FeCl 溶液 Cu 浓硝酸
3
A.①③ B.①④ C.②④ D.②③
10.下列关于0.10 mol·L-1 NaHCO 溶液的说法正确的是
3
A.溶质的电离方程式为NaHCO =Na++ H++ CO2 -
3 3
B.25 ℃时,加水稀释后,n(H+)与n(OH-)的乘积变大
C.离子浓度关系:c(Na+)+c(H+)=c(OH-)+c(HCO - )+c(CO2 -)
3 3
D.温度升高,c(HCO - )增大
3
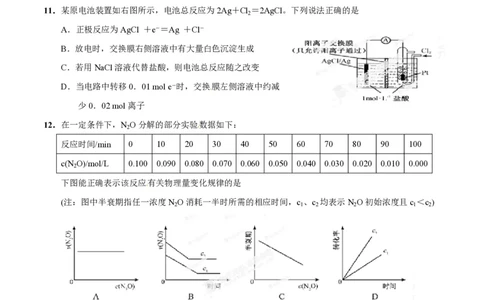
11.某原电池装置如右图所示,电池总反应为2Ag+Cl =2AgCl。下列说法正确的是
2
A.正极反应为AgCl +e-=Ag +Cl-
B.放电时,交换膜右侧溶液中有大量白色沉淀生成
C.若用NaCl溶液代替盐酸,则电池总反应随之改变
D.当电路中转移0.01 mol e-时,交换膜左侧溶液中约减
少0.02 mol离子
12.在一定条件下,N O分解的部分实验数据如下:
2
反应时间/min 0 10 20 30 40 50 60 70 80 90 100
c(N O)/mol/L 0.100 0.090 0.080 0.070 0.060 0.050 0.040 0.030 0.020 0.010 0.000
2
下图能正确表示该反应有关物理量变化规律的是
(注:图中半衰期指任一浓度N O消耗一半时所需的相应时间,c 、c 均表示N O初始浓度且c <c )
2 1 2 2 1 2
第 II 卷
23.(15分)元素周期表中第VIIA族元素的单质及其化合物的用途广泛。
[来源:学科网]
(1)与氯元素同族的短周期元素的原子结构示意图为 。
(2)能作为氯、溴、碘元素非金属性(原子得电子能力)递变规律的判断依据是 (填序号)。
a.Cl 、Br 、I 的熔点 b. Cl 、Br 、I 的氧化性
2 2 2 2 2 2
c.HCl、HBr、HI的热稳定性 d. HCl、HBr、HI的酸性
第2页 | 共6页(3)工业上,通过如下转化可制得KClO 晶体:
3
NaCl溶液 NaClO 溶液 KClO 晶体
3 3
①完成I中反应的总化学方程式:□NaCl+□H O=□NaClO +□ 。
2 3
②II中转化的基本反应类型是 ,该反应过程能析出KClO 晶体而无其它
3
晶体析出的原因是 。
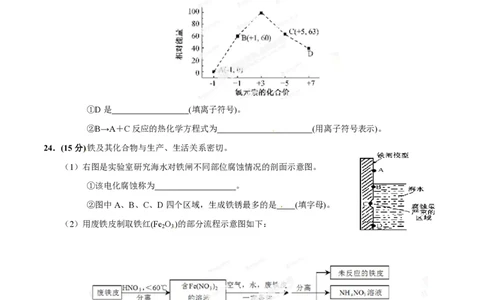
(4)一定条件,在水溶液中1 mol Cl-、ClO-(x=1,2,3,4)的能量(KJ)相对大小如右图所示。
①D是 (填离子符号)。
②B→A+C反应的热化学方程式为 (用离子符号表示)。
24.(15分)铁及其化合物与生产、生活关系密切。
(1)右图是实验室研究海水对铁闸不同部位腐蚀情况的剖面示意图。
①该电化腐蚀称为 。
②图中A、B、C、D四个区域,生成铁锈最多的是 (填字母)。
(2)用废铁皮制取铁红(Fe O )的部分流程示意图如下:
2 3
①步骤I若温度过高,将导致硝酸分解。硝酸分解的化学方程式为 。
②步骤II中发生反应:4Fe(NO ) +O +(2n+4)H O=2Fe O ·nH O+8HNO ,反应产生的HNO
3 2 2 2 2 3 2 3 3
又将废铁皮中的铁转化为Fe(NO ) ,该反应的化学方程式为 。
3 2
③上述生产流程中,能体现“绿色化学”思想的是 (任写一项)。
(3)已知t℃时,反应FeO(s)+CO(g) Fe(s)+CO (g)的平衡常数K=0.25。
2
第3页 | 共6页①t℃时,反应达到平衡时n(CO):n(CO )= 。
2
②若在1 L密闭容器中加入0.02 mol FeO(s),并通入xmolCO,t℃时反应达到平衡。此时FeO(s)
转化率为50%,则x= 。
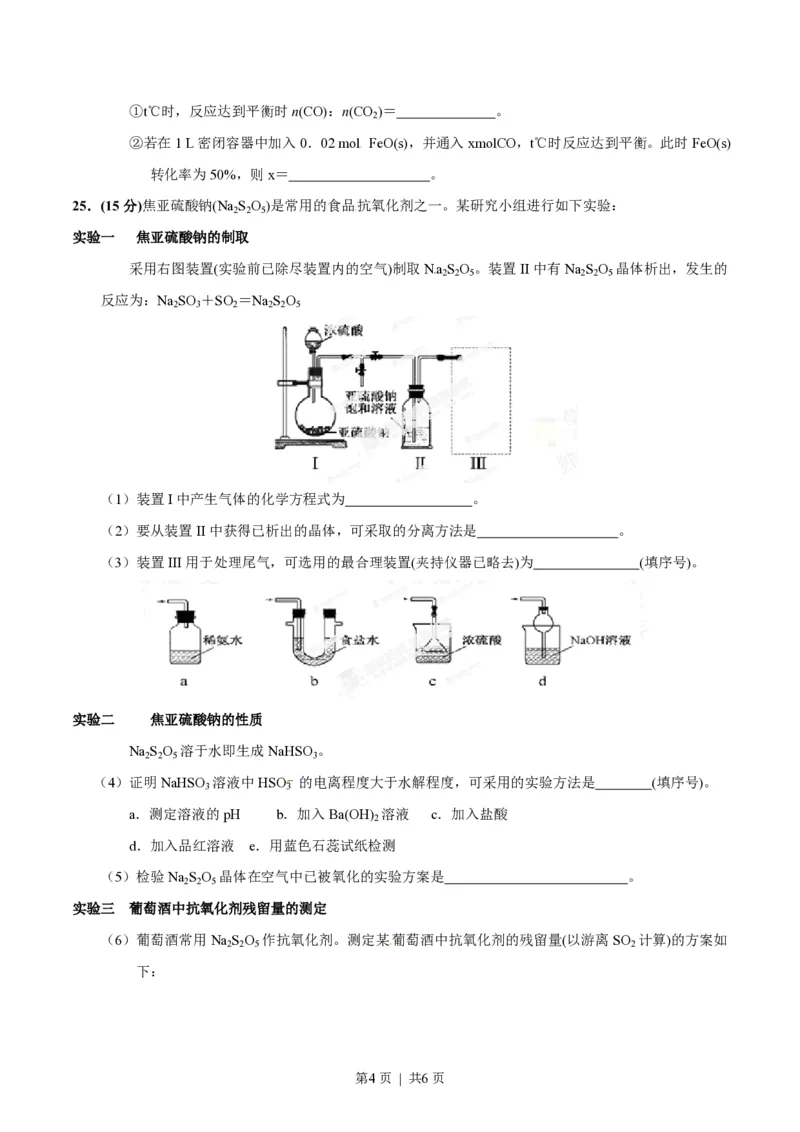
25.(15分)焦亚硫酸钠(Na S O )是常用的食品抗氧化剂之一。某研究小组进行如下实验:
2 2 5 [来源:学#科#网]
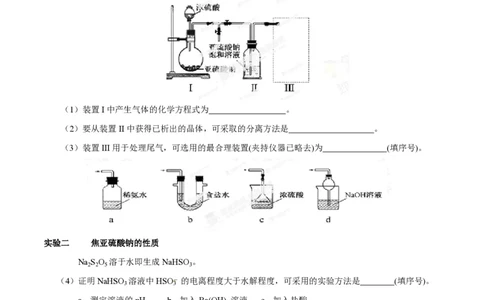
实验一 焦亚硫酸钠的制取
采用右图装置(实验前已除尽装置内的空气)制取Na S O 。装置II中有Na S O 晶体析出,发生的
2 2 5 2 2 5
反应为:Na SO +SO =Na S O
2 3 2 2 2 5
(1)装置I中产生气体的化学方程式为 。
(2)要从装置II中获得已析出的晶体,可采取的分离方法是 。
(3)装置III用于处理尾气,可选用的最合理装置(夹持仪器已略去)为 (填序号)。
[来源:学§科§网Z§X§X§K]
实验二 焦亚硫酸钠的性质
Na S O 溶于水即生成NaHSO 。
2 2 5 3
(4)证明NaHSO 溶液中HSO - 的电离程度大于水解程度,可采用的实验方法是 (填序号)。
3 3
a.测定溶液的pH b.加入Ba(OH) 溶液 c.加入盐酸
2 [来源:学_科_网Z_X_X_K]
d.加入品红溶液 e.用蓝色石蕊试纸检测
(5)检验Na S O 晶体在空气中已被氧化的实验方案是 。
2 2 5
实验三 葡萄酒中抗氧化剂残留量的测定
(6)葡萄酒常用Na S O 作抗氧化剂。测定某葡萄酒中抗氧化剂的残留量(以游离SO 计算)的方案如
2 2 5 2
下:
第4页 | 共6页(已知:滴定时反应的化学方程式为SO +I +2H O=H SO +2HI)
2 2 2 2 4
①按上述方案实验,消耗标准I 溶液25.00 mL,该次实验测得样品中抗氧化剂的残留量(以游离
2
SO 计算)为 g·L-1。
2
②在上述实验过程中,若有部分HI被空气氧化,则测得结果 (填“偏高”“偏低”或“不变”)。
31.化学-物质结构与性质(13分)
氮化硼(BN)晶体有多种相结构。六方相氮化硼是通常存在的稳定相,与石墨相似,具有层状结构,
可作高温润滑剂。立方相氮化硼是超硬材料,有优异的耐磨性。它们的晶体结构如右图所示。
(1)基态硼原子的电子排布式为 。
(2)关于这两种晶体的说法,正确的是 (填序号)。
a.立方相氮化硼含有σ键和π键,所以硬度大 b.六方相氮化硼层间作用力小,所以质地软
c.两种晶体中的B-N键均为共价键 d.两种晶体均为分子晶体
(3)六方相氮化硼晶体层内一个硼原子与相邻氮原子构成的空间构型为 ,其结构与石墨相
似却不导电,原因是 。
(4)立方相氮化硼晶体中,硼原子的杂化轨道类型为 。该晶体的天然矿物在青
藏高原在下约300Km的古地壳中被发现。根据这一矿物形成事实,推断实验室由六方相氮化硼
合成立方相氮化硼需要的条件应是 。
[来源:学科网]
(5)NH BF (氟硼酸铵)是合成氮化硼纳米管的原料之一。1mo NH BF 含有 mol配位
4 4 4 4
键。
32.化学-有机化学基础(13分)
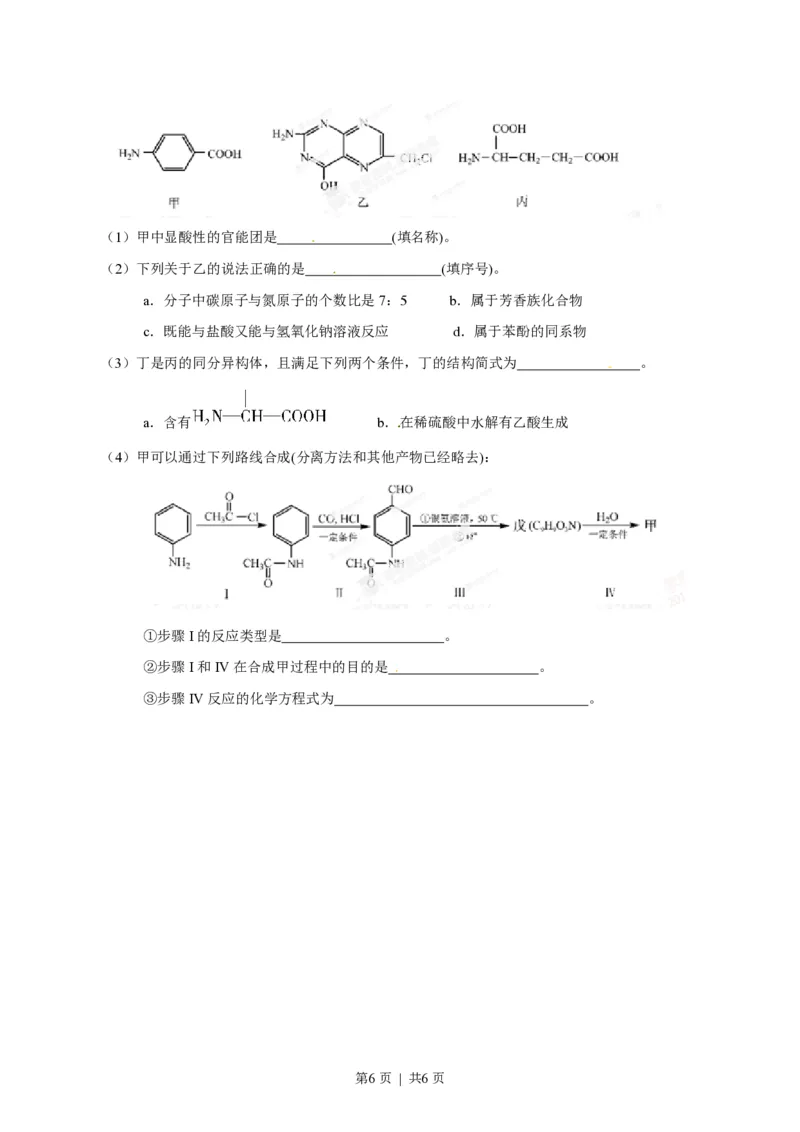
叶酸是维生素B族之一,可以由下列甲、乙、丙三种物质合成。
第5页 | 共6页[来源:学科网ZXXK]
(1)甲中显酸性的官能团是 (填名称)。
(2)下列关于乙的说法正确的是 (填序号)。
a.分子中碳原子与氮原子的个数比是7:5 b.属于芳香族化合物
c.既能与盐酸又能与氢氧化钠溶液反应 d.属于苯酚的同系物
(3)丁是丙的同分异构体,且满足下列两个条件,丁的结构简式为 。
[来源:学科网ZXXK]
a.含有 b.在稀硫酸中水解有乙酸生成
(4)甲可以通过下列路线合成(分离方法和其他产物已经略去):
①步骤I的反应类型是 。
②步骤I和IV在合成甲过程中的目的是 。
③步骤IV反应的化学方程式为 。
第6页 | 共6页