文档内容
兰州一中 2024-2025-1 学期 10 月月考试题
高二化学
说明:本试卷分为第Ⅰ卷(选择题)和第Ⅱ卷(非选择题)两部分,满分100分。考试时间75分钟。答案
写在答题卡上,交卷时只交答题卡
答题可能用到的原子量:H:1 C:12 O:16 Na:23 Ca:40
第Ⅰ卷(共42分)
一、单选题(每小题只有一个选项符合题意,每题3分,共42分)
1.生活处处都与化学反应有关,下列生活中发生的反应属于吸热反应的是( )
A.钢铁生锈 B.蒸馒头时小苏打受热分解
C.食物的腐败 D.生石灰制熟石灰
2.下列说法正确的是( )
A.1mol可燃物完全燃烧生成氧化物所释放的热量为燃烧热
B.1molC完全燃烧放热 ,其热化学方程式为
C.在稀溶液中,强酸与强碱发生中和反应生成 时的反应热叫做中和热
D.表示中和热的热化学方程式为
3.在相同条件下,下列两个反应放出的热量分别用 和 表示: ;
。则( )
A. B. C. D.无法确定
4.在反应 中,有关反应条件改变使反应速率增大的原因分析中,不正确的是( )
A.加入适宜的催化剂,可降低反应的活化能
B.增大 ,单位体积内活化分子数增大
C.升高温度,单位时间内有效碰撞次数增加
D.增大压强,活化分子的百分数增大5.一定条件下,一定容积的密闭容器中,反应 达到平衡状态的标志是
( )
A.压强不随时间变化
B.气体平均相对分子质量不随时间变化
C.气体密度不随时间变化
D.单位时间内生成 ,同时生成2n molAB
6.在保温杯式量热计中,将 溶液与 溶液混合,
温度从25.0℃升高到27.7℃。下列说法错误的是( )
A.若量热计的保温瓶绝热效果不好,则所测 偏大
B.搅拌器一般选用导热性差的玻璃搅拌器
C.若选用同浓度同体积的盐酸,则溶液温度将升高至不超过27.7℃
D.分多次把NaOH溶液倒入 溶液混合,所测 偏大
7.已知 。蒸发 需要吸收的能量
为44kJ,其他相关数据如下表所示:
物质
1mol分子中的化学键断裂时需要吸收的能量/kJ a b z d
则表中 (用x、a、b、d表示)的大小为( )
B.
A.
C. D.
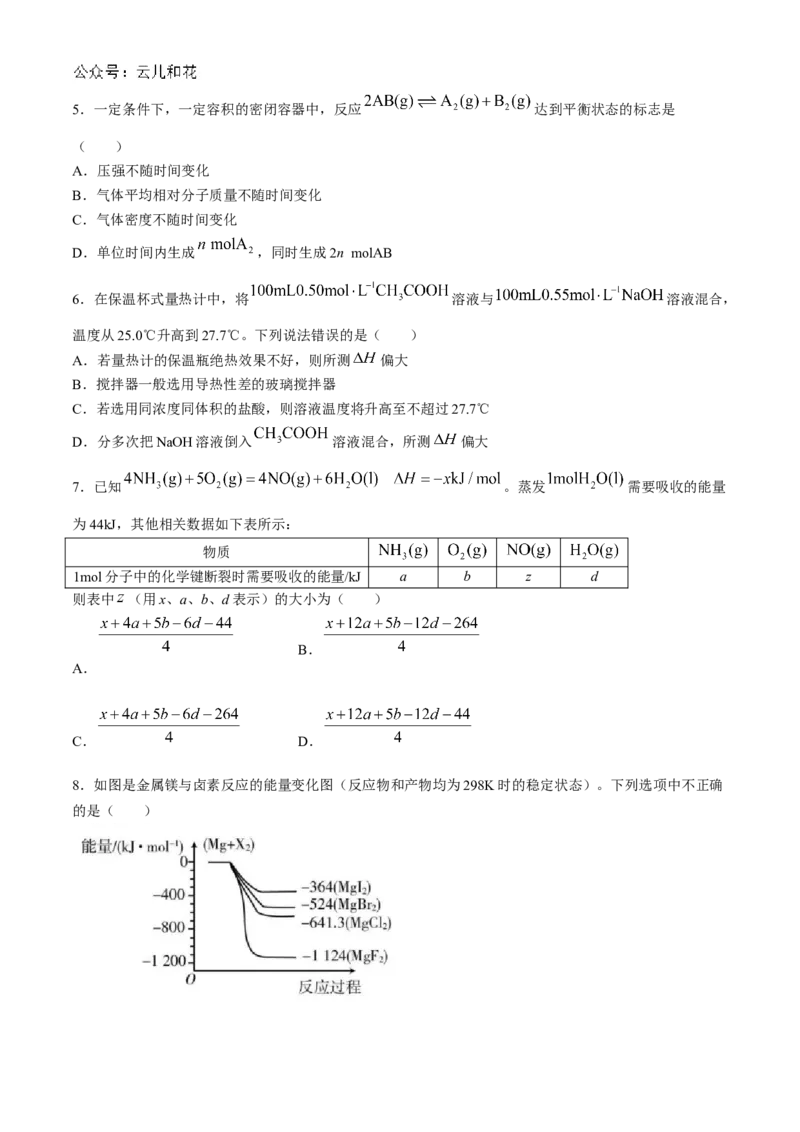
8.如图是金属镁与卤素反应的能量变化图(反应物和产物均为298K时的稳定状态)。下列选项中不正确
的是( )A.在所有卤素单质中,Mg和 反应最容易
B.
C. 与 反应的
D.化合物的热稳定性顺序:
9.下列关于化学反应速率的说法正确的有多少个( )
①恒温时,增大体系压强,化学反应速率一定加快
②其他条件不变,温度越高化学反应速率越快
③使用催化剂可改变反应速率,从而改变该反应过程中吸收或放出的热量
④ 的反应速率一定比 的反应速率大
⑤有气体参加的化学反应,若增大压强(即缩小反应容器的体积),可增加单位体积内活化分子数,从而
使反应速率增大
⑥增大反应物浓度,可增大活化分子的百分数,从而使单位时间有效碰撞次数增多
A.1个 B.2个 C.3个 D.4个
10.室温下将 溶于水会使溶液温度降低,热效应为 ,将 溶于
水会使溶液温度升高,热效应为 ; 受热分解的化学方程式为
,热效应为 。则下列判断中正确的是( )
B. C. D.
A.
.在一定条件下, 和CO燃烧的热化学方程式如下:
11
如果有 和CO的混合气体充分燃烧,放出的热量为262.9kJ,生成的 用过量的饱和石灰水完全吸
收,可得到50g白色沉淀。则混合气体中 和CO的体积比为( )
A.1:2 B.1:3 C.2:3 D.3:2
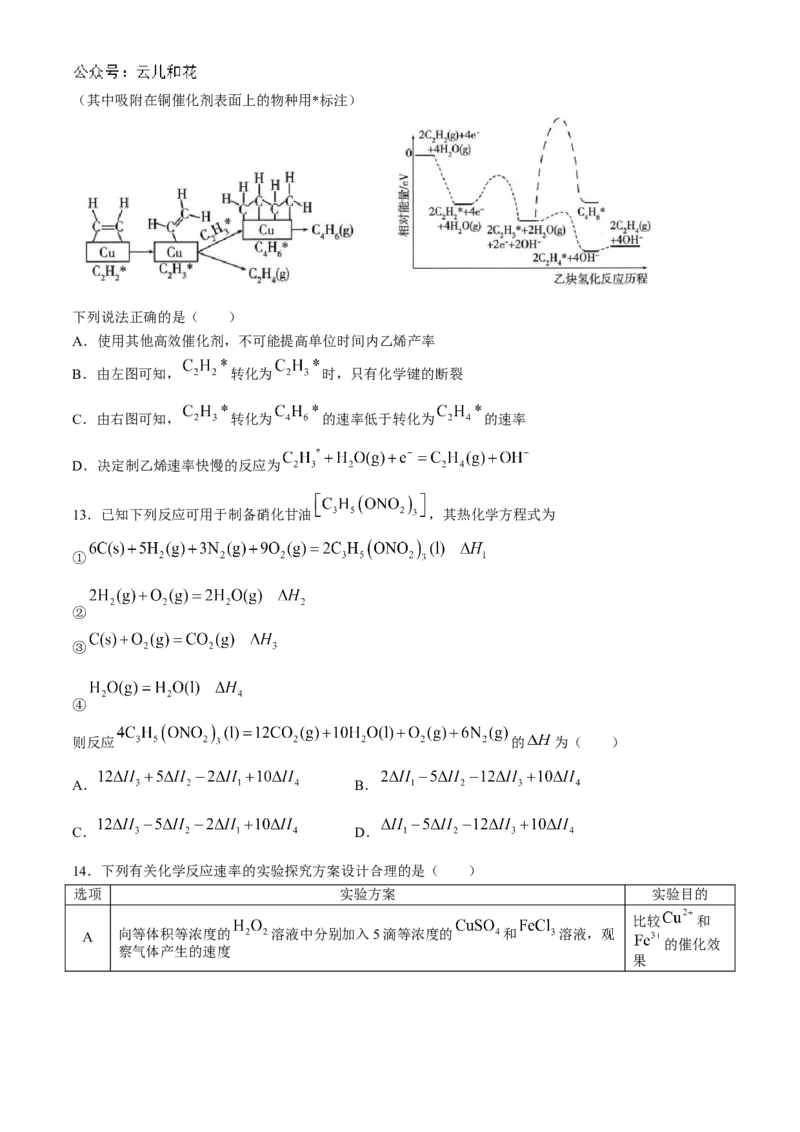
12.科学研究者实现了常温常压下利用铜催化乙炔选择性制备乙烯,副产物 。其反应机理如图所示(其中吸附在铜催化剂表面上的物种用*标注)
下列说法正确的是( )
A.使用其他高效催化剂,不可能提高单位时间内乙烯产率
B.由左图可知, 转化为 时,只有化学键的断裂
C.由右图可知, 转化为 的速率低于转化为 的速率
D.决定制乙烯速率快慢的反应为
13.已知下列反应可用于制备硝化甘油 ,其热化学方程式为
①
②
③
④
则反应 的 为( )
A. B.
C. D.
14.下列有关化学反应速率的实验探究方案设计合理的是( )
选项 实验方案 实验目的
比较 和
A 向等体积等浓度的 溶液中分别加入5滴等浓度的 和 溶液,观
的催化效
察气体产生的速度
果探究温度对反
B
应速率的影响
两支试管,都加入 的酸性 溶液,再同时向两支试管分别
加入 的 溶液和 的 溶液,观 探究草酸浓度
C
对应速率影响
察高锰酸钾溶液褪色所需时间
探究硫酸浓度
D 对反应速率影
响
在锥形瓶内各盛有2g锌粒(颗粒大小基本相同),然后通过分液漏斗分别加入
和 的硫酸。比较两者收集10mL氢气所用的时
间
A.A B.B C.C D.D
第Ⅱ卷(共58分)
二、填空题
15.(14分)在日常生活和工农业生产中经常涉及到吸热反应和放热反应,回答下面问题:
(1)下列反应一定属于吸热反应的是______。
A.酸碱中和反应 B.燃烧反应
C.铝热反应 D. 生成
(2)在101kPa时, 在 中完全燃烧,生成2.0mol液态水,放出571.6kJ的热量,表示氢气燃
烧热的热化学方程式为______,氢气的燃烧热为______ 。
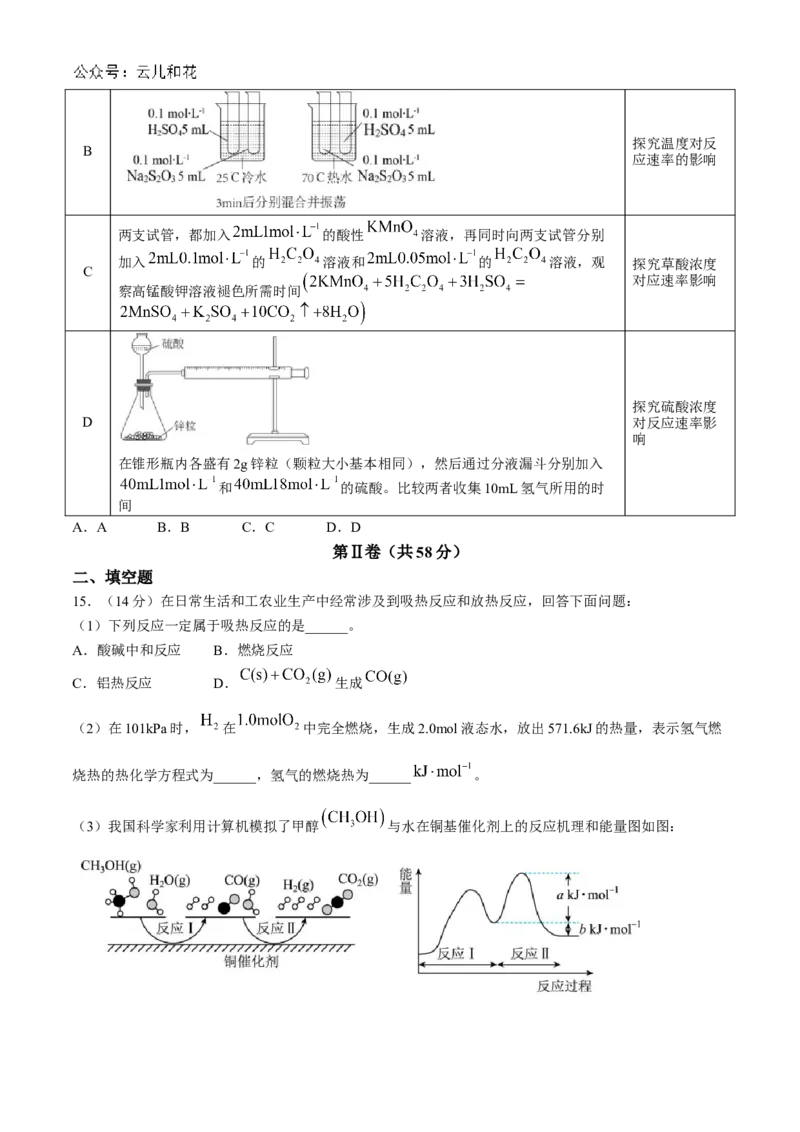
(3)我国科学家利用计算机模拟了甲醇 与水在铜基催化剂上的反应机理和能量图如图:①反应Ⅰ的 ______0(填“<”“>”或“=”),反应Ⅱ的活化能是______ 。
②在相同条件下反应Ⅰ的反应速率______(填“<”“>”或“=”)反应Ⅱ的反应速率。
③写出反应Ⅱ的热化学方程式______。
16.(15分)某实验小组用 溶液与 硫酸溶液进行中和热的
测定,装置如图所示。回答下列问题:
(1)若实验共需要400mLNaOH溶液,实验室在配制该溶液时则需要称量NaOH固体______g。在配制该
溶液时必需用到的玻璃仪器有玻璃棒,烧杯和______。
(2)图中碎泡沫塑料的作用是______。
(3)用同一温度计测量完硫酸溶液,再去测量氢氧化钠溶液的温度之前,所需的操作是______。
(4)请填写表中的平均温度差:
起始温度
实验序号
NaOH 平均值
1 26.2 26.0 26.1 30.1
______
2 27.0 27.4 27.2 31.2
3 25.9 25.9 25.9 29.8
4 26.4 26.2 26.3 30.4
(5)近似认为 溶液与 硫酸溶液的密度都是 ,中和后生成溶液的
比热容 ,则上述实验测得的中和热 ______(结果保留至小数点后一位)。
(6)上述实验测得中和热的数值小于 ,产生偏差的原因可能是______
A.量取NaOH溶液时俯视读数 B.配制NaOH溶液定容时俯视
C.实验装置保温隔热效果差 D.向酸溶液中一次性加入碱溶液
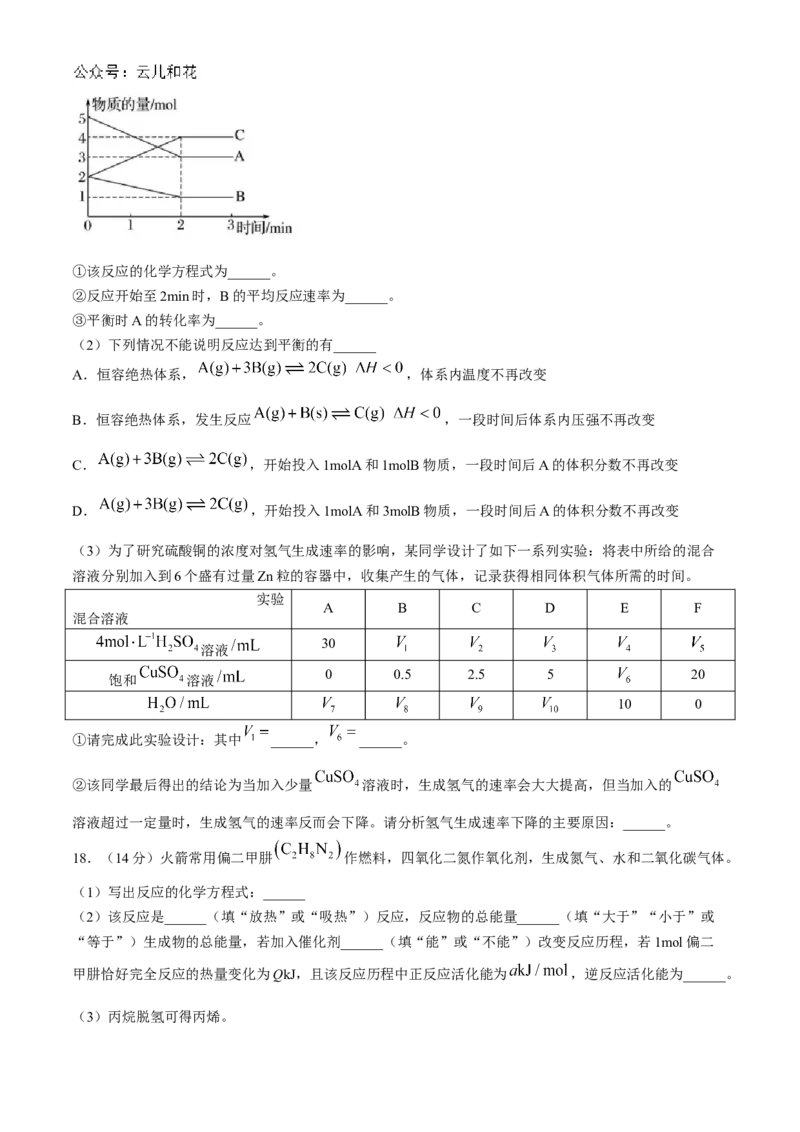
17.(15分)(1)某反应在体积为5L的恒容密闭的容器中进行,各物质的量随时间的变化情况如图所示
(已知A、B、C均为气体)。①该反应的化学方程式为______。
②反应开始至2min时,B的平均反应速率为______。
③平衡时A的转化率为______。
(2)下列情况不能说明反应达到平衡的有______
A.恒容绝热体系, ,体系内温度不再改变
B.恒容绝热体系,发生反应 ,一段时间后体系内压强不再改变
C. ,开始投入1molA和1molB物质,一段时间后A的体积分数不再改变
D. ,开始投入1molA和3molB物质,一段时间后A的体积分数不再改变
(3)为了研究硫酸铜的浓度对氢气生成速率的影响,某同学设计了如下一系列实验:将表中所给的混合
溶液分别加入到6个盛有过量Zn粒的容器中,收集产生的气体,记录获得相同体积气体所需的时间。
实验
A B C D E F
混合溶液
30
溶液
0 0.5 2.5 5 20
饱和 溶液
10 0
①请完成此实验设计:其中 ______, ______。
②该同学最后得出的结论为当加入少量 溶液时,生成氢气的速率会大大提高,但当加入的
溶液超过一定量时,生成氢气的速率反而会下降。请分析氢气生成速率下降的主要原因:______。
18.(14分)火箭常用偏二甲肼 作燃料,四氧化二氮作氧化剂,生成氮气、水和二氧化碳气体。
(1)写出反应的化学方程式:______
(2)该反应是______(填“放热”或“吸热”)反应,反应物的总能量______(填“大于”“小于”或
“等于”)生成物的总能量,若加入催化剂______(填“能”或“不能”)改变反应历程,若1mol偏二
甲肼恰好完全反应的热量变化为QkJ,且该反应历程中正反应活化能为 ,逆反应活化能为______。
(3)丙烷脱氢可得丙烯。已知:
则相同条件下,丙烷脱氢得丙烯的热化学方程式为______。
______。兰州一中 2024-2025-1 学期 10 月月考化学答案
一、单选题
1-5 BDBDD 6-10 CCDBC 11-14 CCAB
15.(1)D (2) ;285.8
(3)①>;a ②< ③
16.(1)10.0 (2)胶头滴管;500mL容量瓶 (3)隔热;防止热量散失
(4)用水清洗温度计,并用滤纸擦干 (4)4.0 (5)-53.8kJ/mol【3分】
(6)AC
17.(1)① ② ③ (2)C【3分】
(3)①30;10
②当加入一定量的硫酸铜后,生成的Cu覆盖(沉积)在Zn的表面,减小了Zn与硫酸接触面积。
18.(1)
(2)放热;大于;能;
(3)
(4)