文档内容
东北育才高中 2025-2026 学年度上学期
高二年级化学科期中考试试卷
可能用到的相对原子质量:H 1 O 16 S 32 Cu 64
I卷 选择题(每小题只有一个正确答案,每题3分,共45分)
1.下列化学与文化结合的场景中描述错误的是
A.“炉火照天地,红星乱紫烟”描绘了古代炼铜的场景,炼铜时C还原CuO反应为
放热反应,但仍需不断补充能量
B.“煮豆燃豆萁,豆在釜中泣”描述了豆萁燃烧产生热量煮豆的过程,其中豆萁燃
烧放出的热量大于釜传递的热量
C.“尚吐石窦油,颇疑岩腹烧”描绘了石油从石缝中涌出的奇特景象,石油经过提
炼后得到的汽油有固定的燃烧热
D.“路遥知马力,日久见人心”描述了马在长途跋涉过程中的惊人毅力,马长期拉
货物过程中体内脂肪提供能量的过程是放热反应
2.25℃时,在等体积的① 的 溶液、② 的NaOH溶液、③ 的
溶液中,由水电离的的物质的量之比是
A. B. C. D.
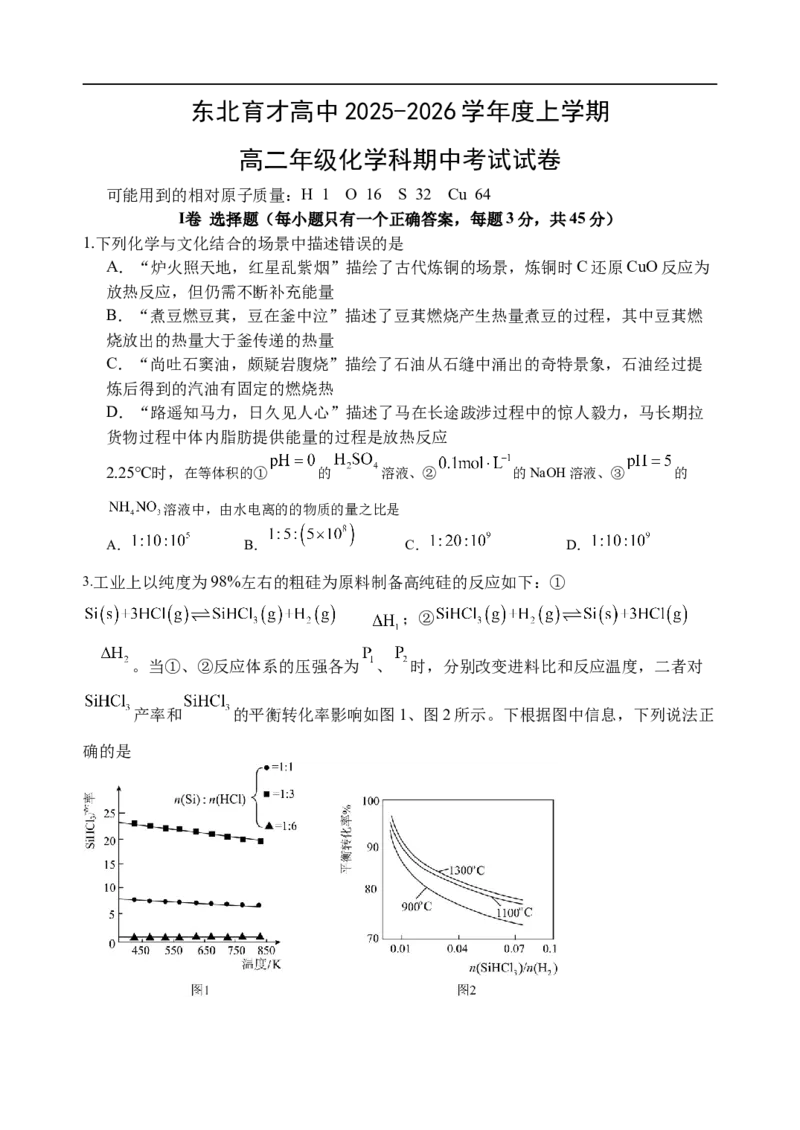
3.工业上以纯度为98%左右的粗硅为原料制备高纯硅的反应如下:①
;②
。当①、②反应体系的压强各为 、 时,分别改变进料比和反应温度,二者对
产率和 的平衡转化率影响如图1、图2所示。下根据图中信息,下列说法正
确的是A.
B.反应①,增加HCl浓度,反应速率加快, 产率增大
C.反应①更适合在较低温度下进行
D.反应②,工业上选择反应温度1300℃更合适
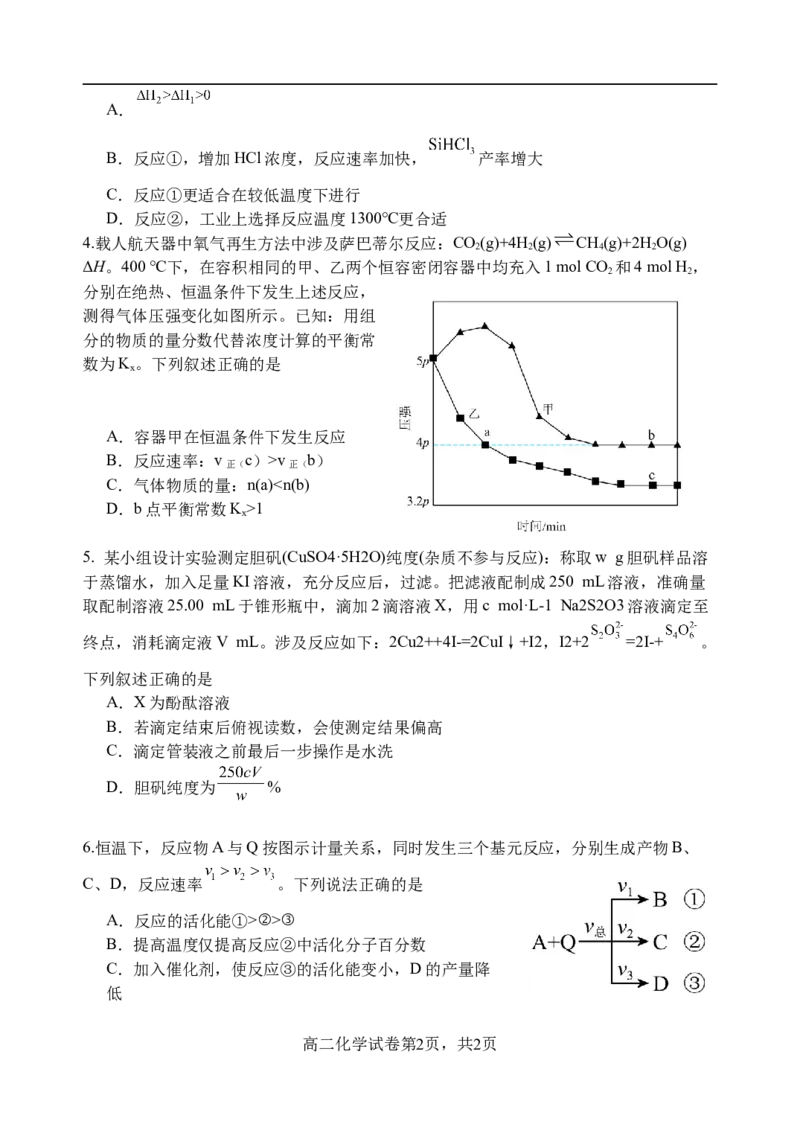
4.载人航天器中氧气再生方法中涉及萨巴蒂尔反应:CO(g)+4H(g) CH(g)+2HO(g)
2 2 4 2
ΔH。400 ℃下,在容积相同的甲、乙两个恒容密闭容器中均充入1 mol CO 和4 mol H ,
2 2
分别在绝热、恒温条件下发生上述反应,
测得气体压强变化如图所示。已知:用组
分的物质的量分数代替浓度计算的平衡常
数为K。下列叙述正确的是
x
A.容器甲在恒温条件下发生反应
B.反应速率:v c)>v b)
正( 正(
C.气体物质的量:n(a)1
x
5. 某小组设计实验测定胆矾(CuSO4·5H2O)纯度(杂质不参与反应):称取w g胆矾样品溶
于蒸馏水,加入足量KI溶液,充分反应后,过滤。把滤液配制成250 mL溶液,准确量
取配制溶液25.00 mL于锥形瓶中,滴加2滴溶液X,用c mol·L-1 Na2S2O3溶液滴定至
终点,消耗滴定液V mL。涉及反应如下:2Cu2++4I-=2CuI↓+I2,I2+2 =2I-+ 。
下列叙述正确的是
A.X为酚酞溶液
B.若滴定结束后俯视读数,会使测定结果偏高
C.滴定管装液之前最后一步操作是水洗
D.胆矾纯度为 %
6.恒温下,反应物A与Q按图示计量关系,同时发生三个基元反应,分别生成产物B、
C、D,反应速率 。下列说法正确的是
A.反应的活化能①>②>③
B.提高温度仅提高反应②中活化分子百分数
C.加入催化剂,使反应③的活化能变小,D的产量降
低
高二化学试卷第2页,共2页D.总反应速率
7.下列实验操作与现象及实验结论均正确的是
选
实验操作与现象 实验结论
项
将两个活泼性不同的电极插入一只鲜橙并与电流计
A. 构成闭合回路,接通电源,电流计指针发生明显偏 橙子汁是电解质
转
室温下,用pH试纸测得0.1mol·L-1 溶液
B. 醋酸的酸性强于碳酸氢根
的pH为9,等浓度 溶液的pH为12
向2mL1mol/L的 溶液中滴入2滴0.1mol/
C.
LNaOH溶液,再滴加2滴 溶液。先产
生蓝色沉淀,再产生黑色沉淀
Cu与浓硫酸共热反应有白色固体生成,为验证其成
D. 分,向反应后溶液中加入适量的水,固体溶解,溶 白色固体是
液变蓝
A.A B.B C.C D.D
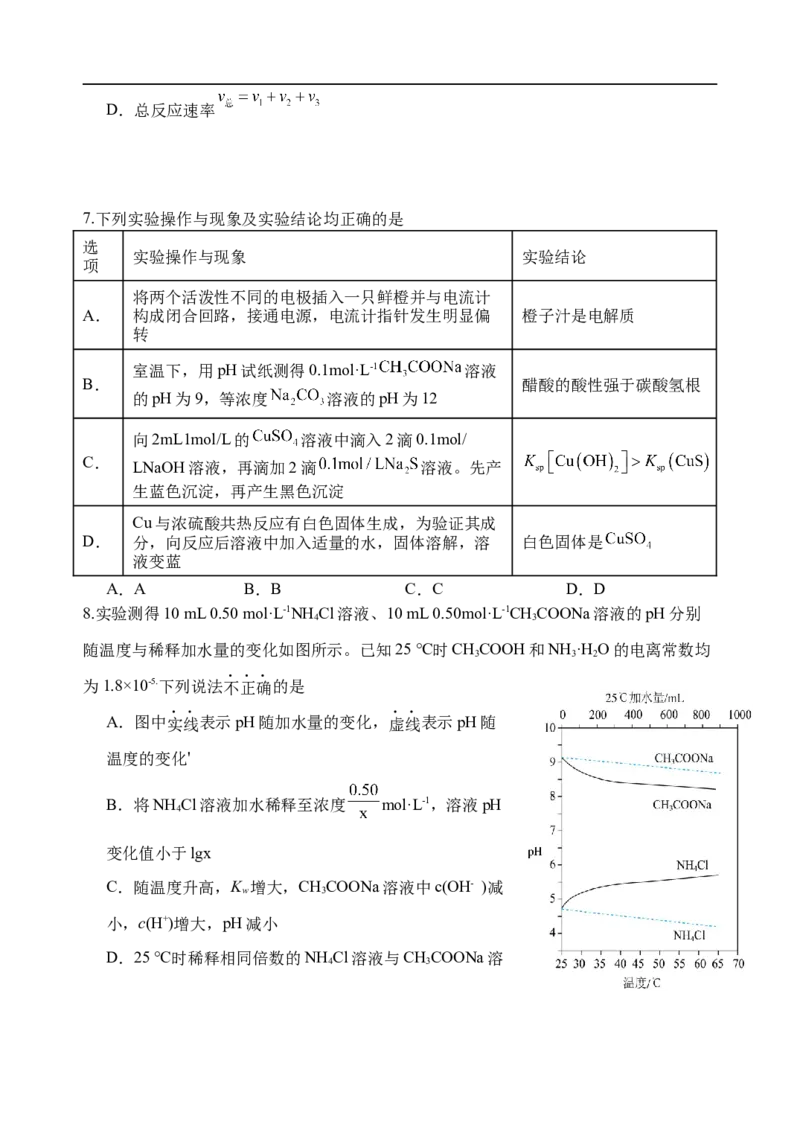
8.实验测得10 mL 0.50 mol·L-1NH Cl溶液、10 mL 0.50mol·L-1CHCOONa溶液的pH分别
4 3
随温度与稀释加水量的变化如图所示。已知25 ℃时CHCOOH和NH ·H O的电离常数均
3 3 2
为1.8×10-5.下列说法不正确的是
A.图中实线表示pH随加水量的变化,虚线表示pH随
温度的变化'
B.将NH Cl溶液加水稀释至浓度 mol·L-1,溶液pH
4
变化值小于lgx
C.随温度升高,K 增大,CHCOONa溶液中c(OH- )减
w 3
小,c(H+)增大,pH减小
D.25 ℃时稀释相同倍数的NH Cl溶液与CHCOONa溶
4 3液中:c(Na+ )-c(CHCOO- )=c(Cl-)-c(NH )
3
9.实验室制取乙炔时常混有 气体,可以依次通过①NaOH溶液将其除去,② 溶
液检验 是否除尽。已知常温下: , ,
,设 表示阿伏加德罗常数的值,下列说法正确的是
A.反应 的
B. 溶液中存在
C.常温下,用NaOH溶液吸收 时,若恰好生成NaHS溶液,则其pH<7
D.若NaOH溶液足量,①中离子方程式为
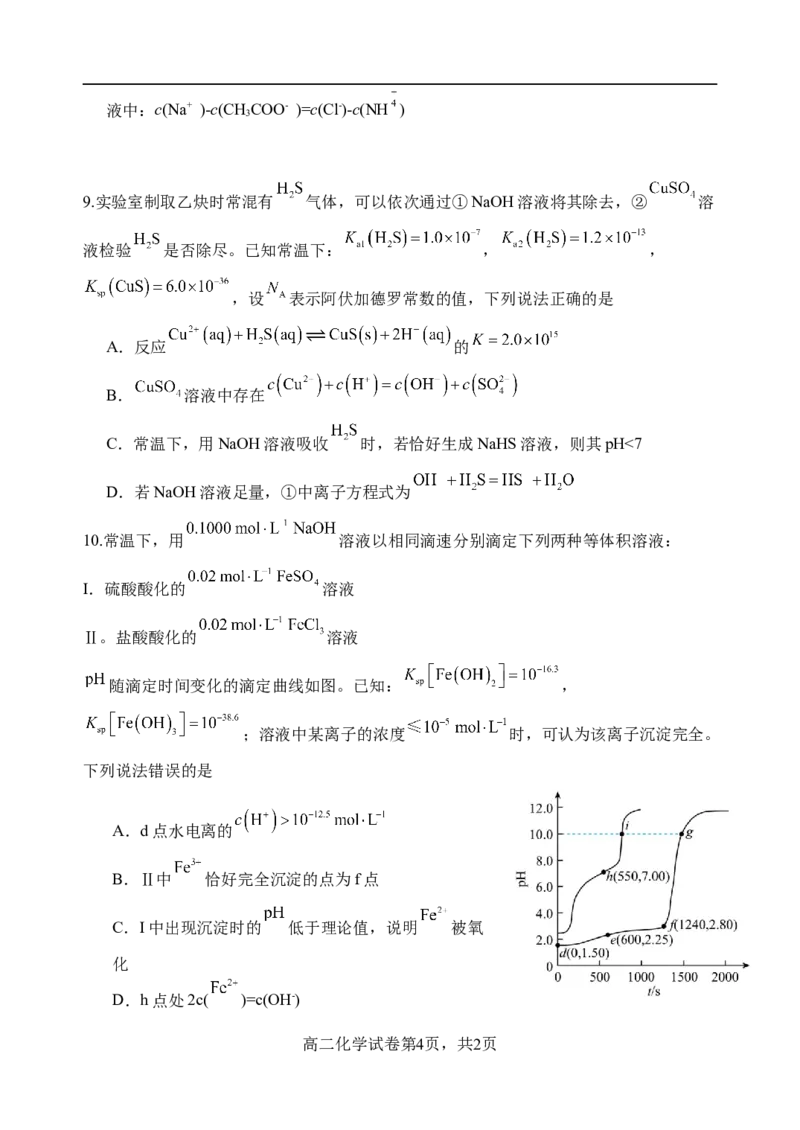
10.常温下,用 溶液以相同滴速分别滴定下列两种等体积溶液:
I.硫酸酸化的 溶液
Ⅱ。盐酸酸化的 溶液
随滴定时间变化的滴定曲线如图。已知: ,
;溶液中某离子的浓度 时,可认为该离子沉淀完全。
下列说法错误的是
A.d点水电离的
B.Ⅱ中 恰好完全沉淀的点为f点
C.I中出现沉淀时的 低于理论值,说明 被氧
化
D.h点处2c( )=c(OH-)
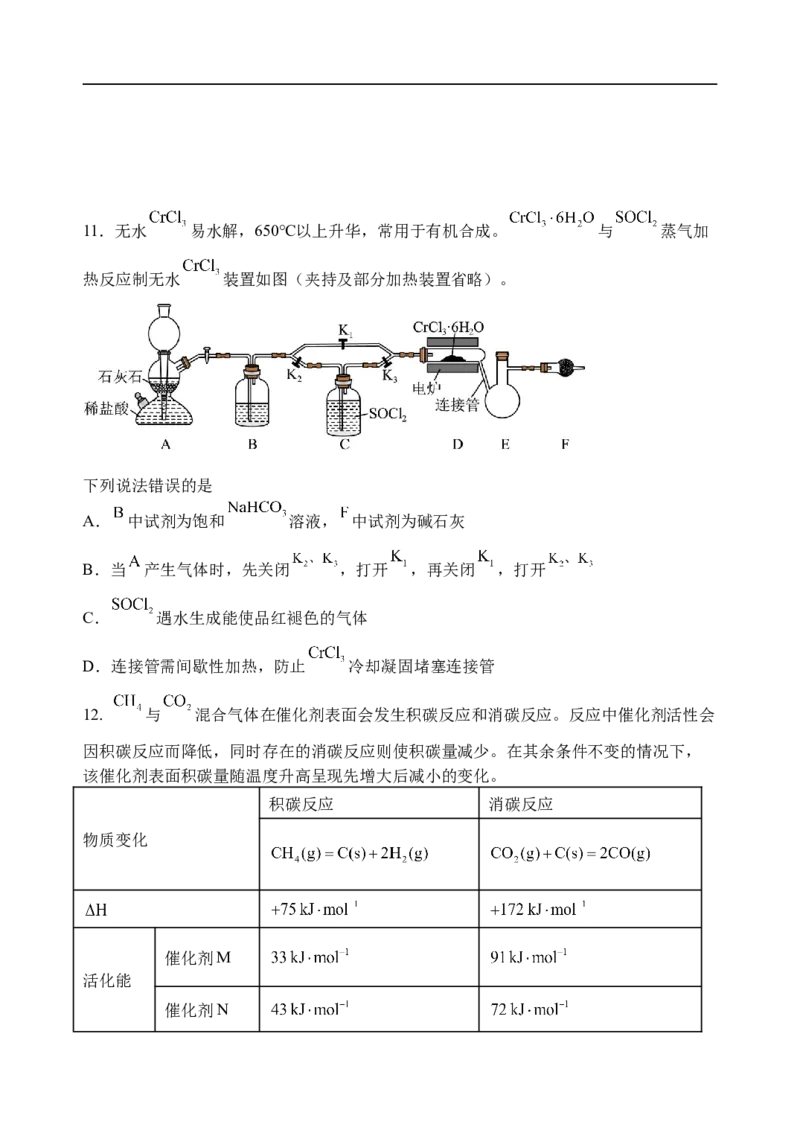
高二化学试卷第4页,共2页11.无水 易水解,650℃以上升华,常用于有机合成。 与 蒸气加
热反应制无水 装置如图(夹持及部分加热装置省略)。
下列说法错误的是
A. 中试剂为饱和 溶液, 中试剂为碱石灰
B.当 产生气体时,先关闭 ,打开 ,再关闭 ,打开
C. 遇水生成能使品红褪色的气体
D.连接管需间歇性加热,防止 冷却凝固堵塞连接管
12. 与 混合气体在催化剂表面会发生积碳反应和消碳反应。反应中催化剂活性会
因积碳反应而降低,同时存在的消碳反应则使积碳量减少。在其余条件不变的情况下,
该催化剂表面积碳量随温度升高呈现先增大后减小的变化。
积碳反应 消碳反应
物质变化
催化剂M
活化能
催化剂N下列说法正确的是
A.升温, 增加、 减小 B.积碳反应和消碳反应均为高温自发反应
C.升温,v 增加的倍数比v 增加的倍数少 D.催化剂M优于催化剂N
消 积
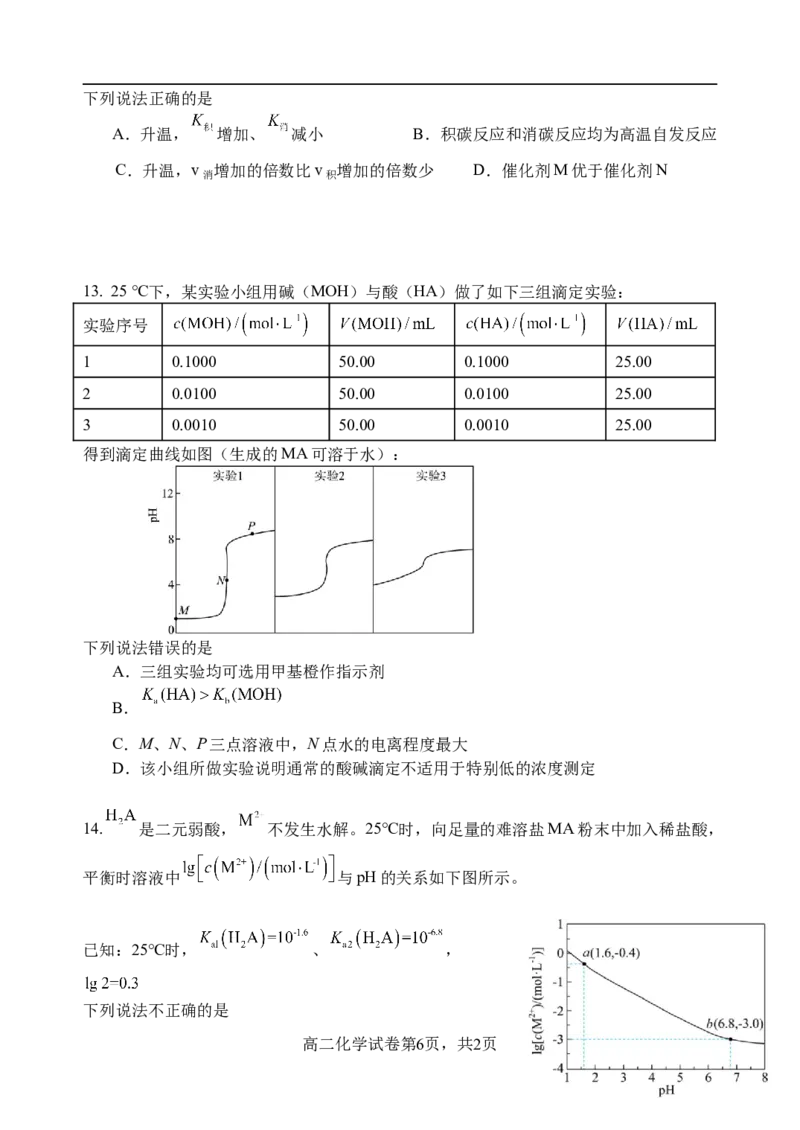
13. 25 ℃下,某实验小组用碱(MOH)与酸(HA)做了如下三组滴定实验:
实验序号
1 0.1000 50.00 0.1000 25.00
2 0.0100 50.00 0.0100 25.00
3 0.0010 50.00 0.0010 25.00
得到滴定曲线如图(生成的MA可溶于水):
下列说法错误的是
A.三组实验均可选用甲基橙作指示剂
B.
C.M、N、P三点溶液中,N点水的电离程度最大
D.该小组所做实验说明通常的酸碱滴定不适用于特别低的浓度测定
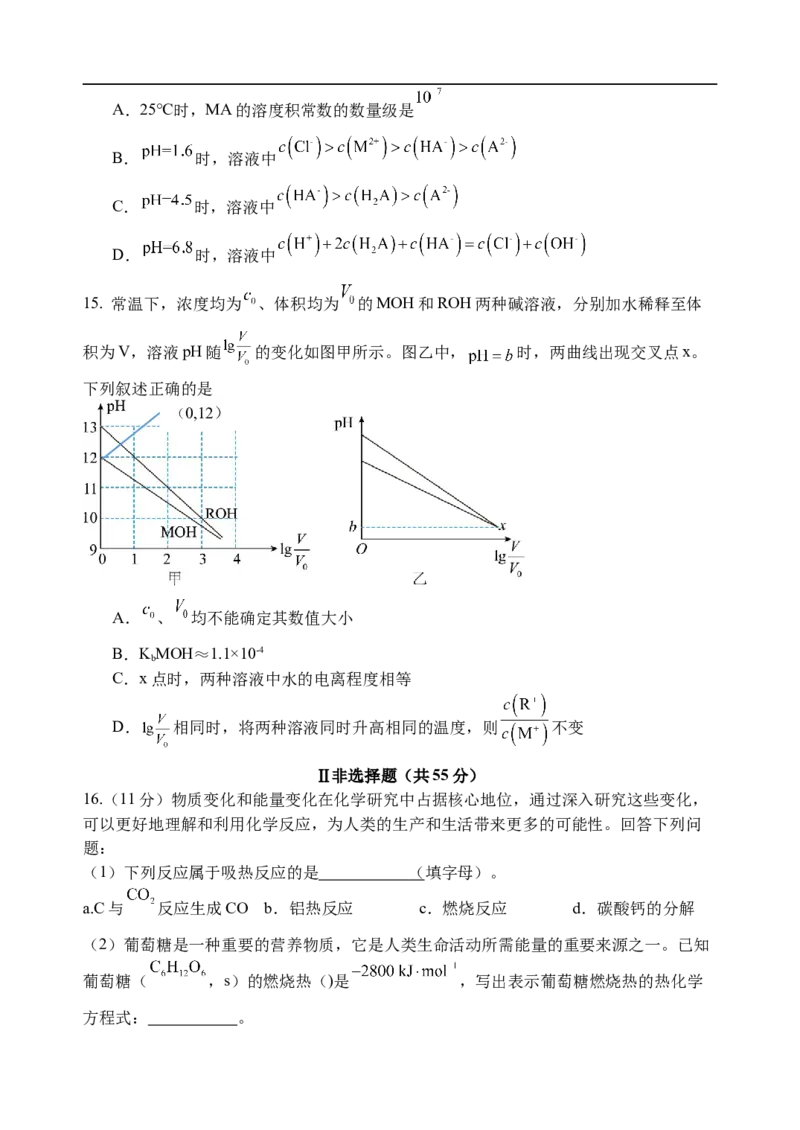
14. 是二元弱酸, 不发生水解。25℃时,向足量的难溶盐MA粉末中加入稀盐酸,
平衡时溶液中 与pH的关系如下图所示。
已知:25℃时, 、 ,
下列说法不正确的是
高二化学试卷第6页,共2页A.25℃时,MA的溶度积常数的数量级是
B. 时,溶液中
C. 时,溶液中
D. 时,溶液中
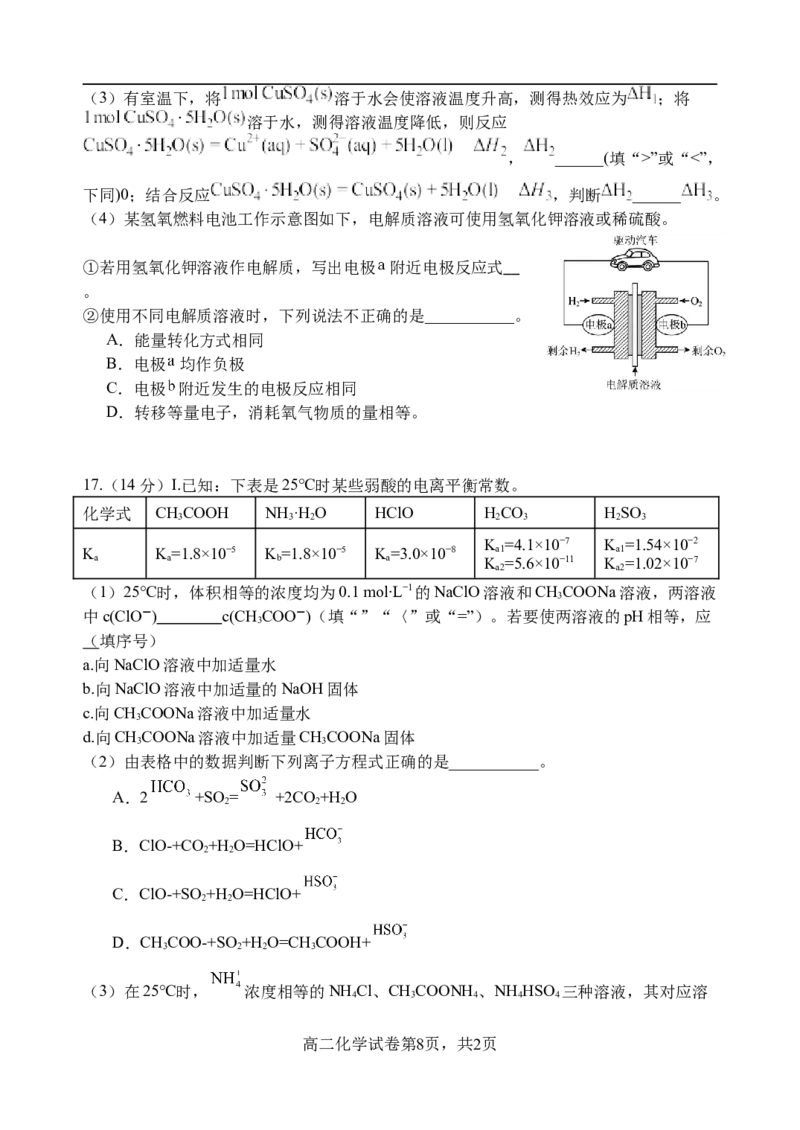
15. 常温下,浓度均为 、体积均为 的MOH和ROH两种碱溶液,分别加水稀释至体
积为V,溶液pH随 的变化如图甲所示。图乙中, 时,两曲线出现交叉点x。
下列叙述正确的是
(0,12)
A. 、 均不能确定其数值大小
B.KMOH≈1.1×10-4
b
C.x点时,两种溶液中水的电离程度相等
D. 相同时,将两种溶液同时升高相同的温度,则 不变
Ⅱ非选择题(共55分)
16.(11分)物质变化和能量变化在化学研究中占据核心地位,通过深入研究这些变化,
可以更好地理解和利用化学反应,为人类的生产和生活带来更多的可能性。回答下列问
题:
(1)下列反应属于吸热反应的是 ( 填字母)。
a.C与 反应生成CO b.铝热反应 c.燃烧反应 d.碳酸钙的分解
(2)葡萄糖是一种重要的营养物质,它是人类生命活动所需能量的重要来源之一。已知
葡萄糖( ,s)的燃烧热()是 ,写出表示葡萄糖燃烧热的热化学
方程式: 。(3)有室温下,将 溶于水会使溶液温度升高,测得热效应为 ;将
溶于水,测得溶液温度降低,则反应
, ______(填“>”或“<”,
下同)0;结合反应 ,判断 ______ 。
(4)某氢氧燃料电池工作示意图如下,电解质溶液可使用氢氧化钾溶液或稀硫酸。
①若用氢氧化钾溶液作电解质,写出电极 附近电极反应式
。
②使用不同电解质溶液时,下列说法不正确的是___________。
A.能量转化方式相同
B.电极 均作负极
C.电极 附近发生的电极反应相同
D.转移等量电子,消耗氧气物质的量相等。
17.(14分)I.已知:下表是25℃时某些弱酸的电离平衡常数。
化学式 CHCOOH NH ·H O HClO HCO HSO
3 3 2 2 3 2 3
K =4.1×10−7 K =1.54×10−2
K K=1.8×10−5 K=1.8×10−5 K=3.0×10−8 a1 a1
a a b a K =5.6×10−11 K =1.02×10−7
a2 a2
(1)25℃时,体积相等的浓度均为0.1 mol∙L−1的NaClO溶液和CHCOONa溶液,两溶液
3
中c(ClO-) c(CHCOO-)(填“”“〈”或“=”)。若要使两溶液的pH相等,应
3
(填序号)
a.向NaClO溶液中加适量水
b.向NaClO溶液中加适量的NaOH固体
c.向CHCOONa溶液中加适量水
3
d.向CHCOONa溶液中加适量CHCOONa固体
3 3
(2)由表格中的数据判断下列离子方程式正确的是___________。
A.2 +SO= +2CO +H O
2 2 2
B.ClO-+CO +H O=HClO+
2 2
C.ClO-+SO+H O=HClO+
2 2
D.CHCOO-+SO+H O=CHCOOH+
3 2 2 3
(3)在25℃时, 浓度相等的NH Cl、CHCOONH、NH HSO 三种溶液,其对应溶
4 3 4 4 4
高二化学试卷第8页,共2页液中溶质的物质的量浓度分别为a、b、c(单位为mol∙L−1),三者由大到小的顺序是
。
(4)在25℃下,将a mol∙L−1的氨水与0.01 mol∙L−1的盐酸等体积混合,充分反应后溶液
中c( )=c(Cl-),用含a的代数式表示NH ·H O的电离常数K= 。
3 2 b
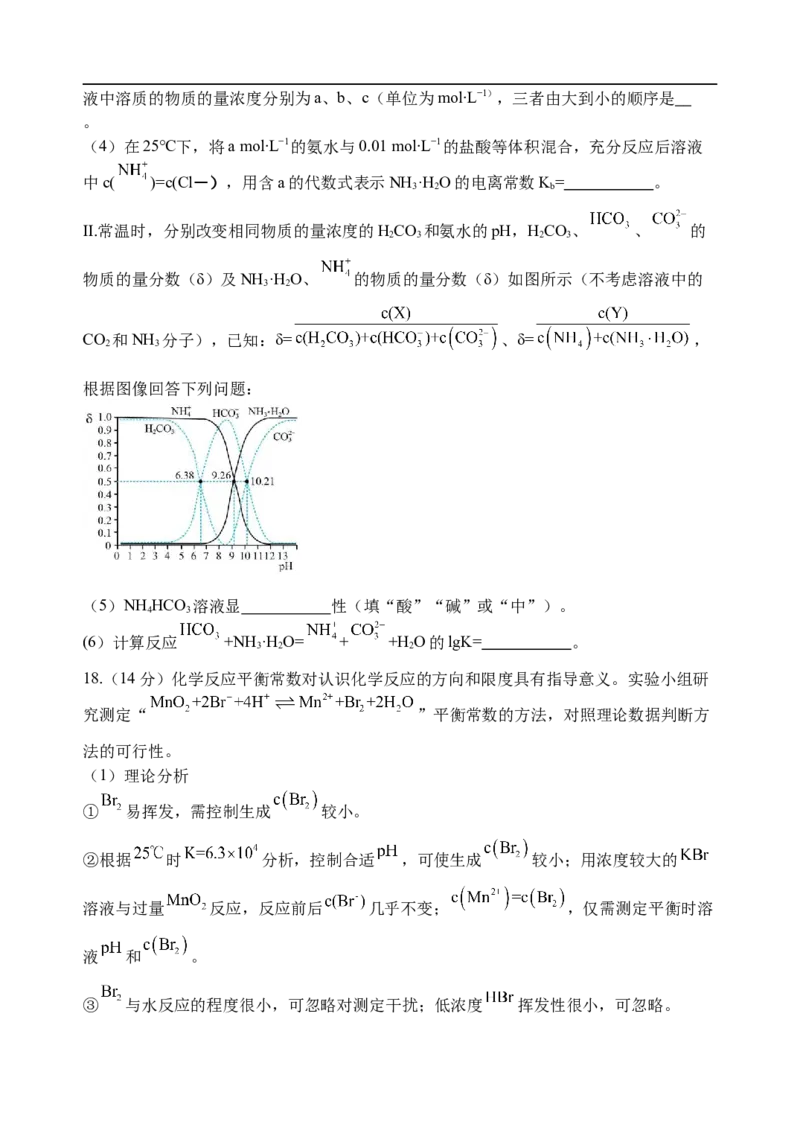
II.常温时,分别改变相同物质的量浓度的HCO 和氨水的pH,HCO、 、 的
2 3 2 3
物质的量分数(δ)及NH ·H O、 的物质的量分数(δ)如图所示(不考虑溶液中的
3 2
CO 和NH 分子),已知:δ= 、δ= ,
2 3
根据图像回答下列问题:
(5)NH HCO 溶液显 性(填“酸”“碱”或“中”)。
4 3
(6)计算反应 +NH·H O= + +H O的lgK= 。
3 2 2
18.(14分)化学反应平衡常数对认识化学反应的方向和限度具有指导意义。实验小组研
究测定“ ”平衡常数的方法,对照理论数据判断方
法的可行性。
(1)理论分析
① 易挥发,需控制生成 较小。
②根据 时 分析,控制合适 ,可使生成 较小;用浓度较大的
溶液与过量 反应,反应前后 几乎不变; ,仅需测定平衡时溶
液 和 。
③ 与水反应的程度很小,可忽略对测定干扰;低浓度 挥发性很小,可忽略。(2)实验探究
序
实验内容及现象
号
,将 溶液()与过量 混合,密闭并搅拌,充分反应后,
I
溶液变为黄色,容器液面上方有淡黄色气体。
,将 溶液()与过量 混合,密闭并搅拌,反应时间与I
Ⅱ
相同,溶液变为淡黄色,容器液面上方未观察到黄色气体。
测定I、Ⅱ反应后溶液的 ;取一定量反应后溶液,加入过量 固体,用
Ⅲ
标准溶液滴定,测定 。
已知: ; 和 溶液颜色均为无色。
①Ⅲ中,滴定时选用淀粉作指示剂,滴定终点时的现象是 。用离子方程式表示
的作用: 。
②I中,与反应前的溶液相比,反应后溶液的 ( 填“增大”“减小”或“不
变”)。平衡后,按 计算所得值小于的K值,是因为 挥发导致计算时
所用 的浓度小于其在溶液中实际浓度。
③Ⅱ中,按 计算所得值也小于的K值,可能原因是 。
(3)实验改进
分析实验I、Ⅱ中测定结果均偏小的原因,改变实验条件,再次实验。
控制反应温度为 ,其他条件与Ⅱ相同,经实验准确测得该条件下的平衡常数。
①判断该实验测得的平衡常数是否准确,应与 值比较。
②综合调控 和温度的目的是 。
19.(16分)硫酸锌主要用作制取颜料立德粉、锌钡白和其他含锌化合物的原料。利用某
工业废水(主要成分含有 、 、 及少量 、Fe2+、Fe3+)制备 溶液的流
程如下:
已知:室温下 , ,
高二化学试卷第10页,共2页K [Fe(OH) ]=4.9×10-17 。
SP 2
(1)加快“氧化”速率的措施有 ( 写两条);“氧化”时发生反应的离子方程
式为 。
(2)“除杂”需要过滤,实验室过滤所用到的玻璃仪器有 。
(3) 水溶液显 性(填“酸”“碱”或“中”);用离子方程式表示其原因:
;在 溶液中, 、 、 、 、 的物质的量浓度由大到小的顺序
是 。
(4)“调节 ”时,溶液中 mol/L。
(5)流程中先用 除杂,再用 深度除杂,不用 一步除杂的原因是