文档内容
湖北省 2025-2026 学年度上学期高二 10 月月考
高二化学试卷
本试卷共8页,19题。全卷满分100分。考试用时75分钟。
★祝考试顺利★
注意事项:
1. 答题前,先将自己的姓名、准考证号、考场号、座位号填写在试卷和答题卡上,并认真
核准准考证号条形码上的以上信息,将条形码粘贴在答题卡上的指定位置。
2. 请按题号顺序在答题卡上各题目的答题区域内作答,写在试卷、草稿纸和答题卡上的非
答题区域均无效。
3. 选择题用2B铅笔在答题卡上把所选答案的标号涂黑;非选择题用黑色签字笔在答题卡上
作答;字体工整,笔迹清楚。
4. 考试结束后,请将试卷和答题卡一并上交。
可能用到的相对原子质量:H1 C12 O16 Fe56
一、选择题:本题共15小题,每小题3分,共45分。在每个小题给出的四个选项中,只有一项
是符合题目要求的。
1. 化学与生产、生活、环境等密切相关,下列说法正确的是( )
A.推广使用可降解塑料制品是为了防止白色污染
B.传统的无机非金属材料多为硅酸盐材料,在硅酸盐中,Si和O构成了平面四边形
C.SO 有毒,不能用做食品添加剂
2
D.富勒烯、碳纳米管、石墨烯都属于有机高分子材料
2. 下列说法正确的是( )
A.常温下,5.6g铁与过量的浓硝酸反应,铁失去的电子数一定为0.3N
A
B.14g的乙烯和丙烯的混合物中所含碳原子数为2N
A
催化剂
C.硫酸工业中存在下列反应,2SO
2
(g)+O
2
(g)
加
热
2SO
3
(g),实际生产中通入过量的空
气,可以增大SO 的转化率
2
D.合成氨工业中,采用迅速冷却的方法将氨气从平衡体系中分离,可加快反应速率并提高
反应的转化率
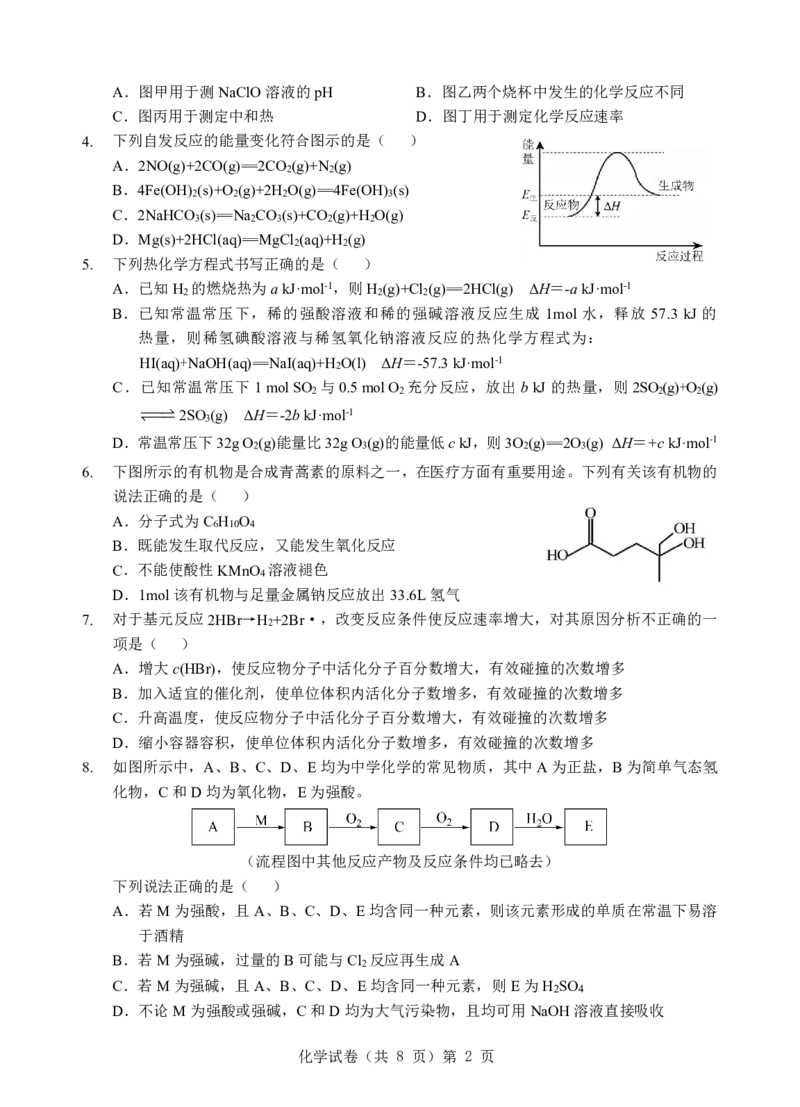
3. 下列有关图示的说法正确的是( )
甲: 乙: 丙: 丁:
化学试卷(共 8 页)第 1 页A.图甲用于测NaClO溶液的pH B.图乙两个烧杯中发生的化学反应不同
C.图丙用于测定中和热 D.图丁用于测定化学反应速率
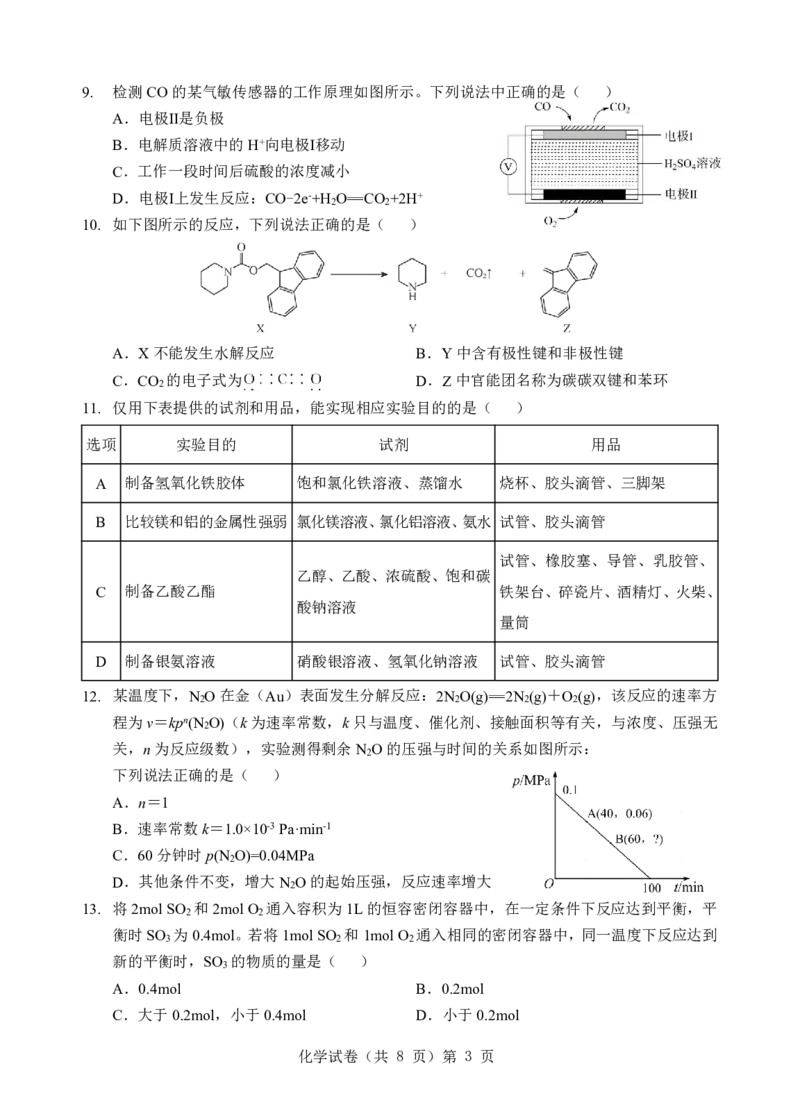
4. 下列自发反应的能量变化符合图示的是( )
A.2NO(g)+2CO(g)=2CO (g)+N (g)
2 2
B.4Fe(OH) (s)+O (g)+2H O(g)=4Fe(OH) (s)
2 2 2 3
C.2NaHCO (s)=Na CO (s)+CO (g)+H O(g)
3 2 3 2 2
D.Mg(s)+2HCl(aq)=MgCl (aq)+H (g)
2 2
5. 下列热化学方程式书写正确的是( )
A.已知H 的燃烧热为akJ·mol-1,则H (g)+Cl (g)=2HCl(g) ΔH=-akJ·mol-1
2 2 2
B.已知常温常压下,稀的强酸溶液和稀的强碱溶液反应生成 1mol 水,释放 57.3 kJ 的
热量,则稀氢碘酸溶液与稀氢氧化钠溶液反应的热化学方程式为:
HI(aq)+NaOH(aq)=NaI(aq)+H O(l) ΔH=-57.3kJ·mol-1
2
C.已知常温常压下1 molSO 与0.5molO 充分反应,放出bkJ 的热量,则2SO(g)+O(g)
2 2 2 2
2SO
3
(g) ΔH=-2bkJ·mol-1
D.常温常压下32gO (g)能量比32gO (g)的能量低ckJ,则3O (g)=2O (g) ΔH=+ckJ·mol-1
2 3 2 3
6. 下图所示的有机物是合成青蒿素的原料之一,在医疗方面有重要用途。下列有关该有机物的
说法正确的是( )
A.分子式为C H O
6 10 4
B.既能发生取代反应,又能发生氧化反应
C.不能使酸性KMnO 溶液褪色
4
D.1mol该有机物与足量金属钠反应放出33.6L氢气
7. 对于基元反应2HBr→H +2Br·,改变反应条件使反应速率增大,对其原因分析不正确的一
2
项是( )
A.增大c(HBr),使反应物分子中活化分子百分数增大,有效碰撞的次数增多
B.加入适宜的催化剂,使单位体积内活化分子数增多,有效碰撞的次数增多
C.升高温度,使反应物分子中活化分子百分数增大,有效碰撞的次数增多
D.缩小容器容积,使单位体积内活化分子数增多,有效碰撞的次数增多
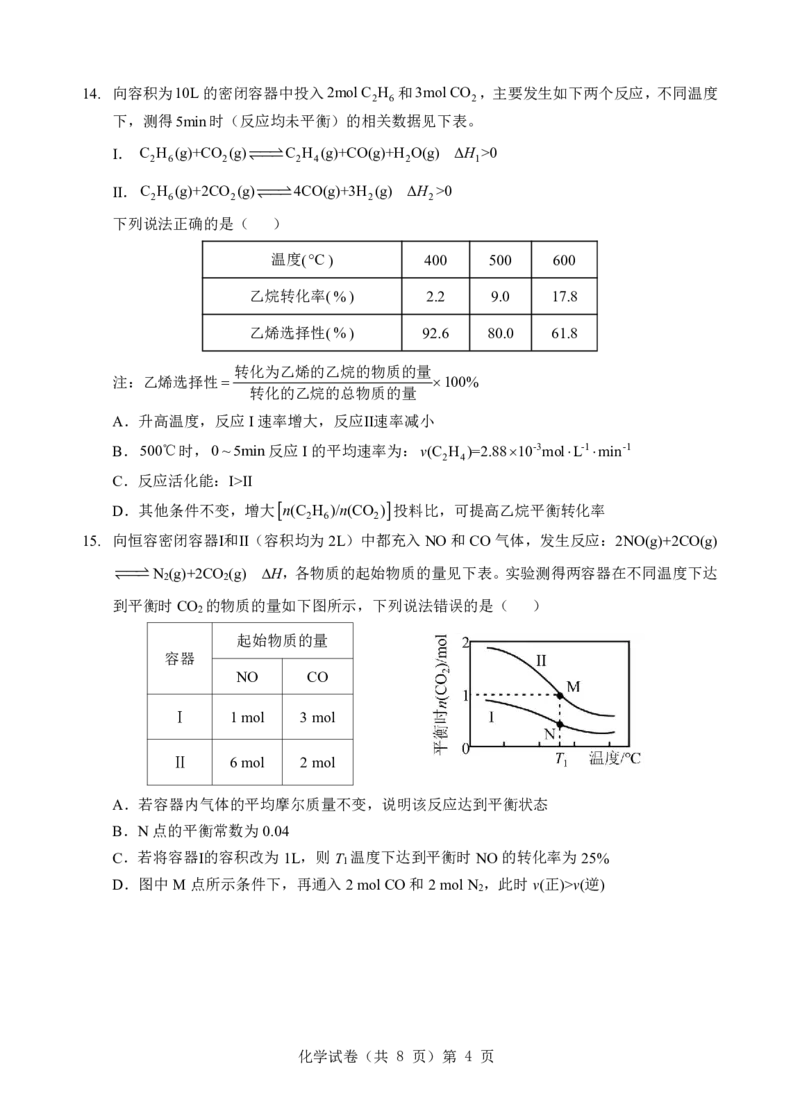
8. 如图所示中,A、B、C、D、E均为中学化学的常见物质,其中A为正盐,B为简单气态氢
化物,C和D均为氧化物,E为强酸。
(流程图中其他反应产物及反应条件均已略去)
下列说法正确的是( )
A.若M为强酸,且A、B、C、D、E均含同一种元素,则该元素形成的单质在常温下易溶
于酒精
B.若M为强碱,过量的B可能与Cl 反应再生成A
2
C.若M为强碱,且A、B、C、D、E均含同一种元素,则E为H2SO4
D.不论M为强酸或强碱,C和D均为大气污染物,且均可用NaOH溶液直接吸收
化学试卷(共 8 页)第 2 页9. 检测CO的某气敏传感器的工作原理如图所示。下列说法中正确的是( )
A.电极Ⅱ是负极
B.电解质溶液中的H+向电极Ⅰ移动
C.工作一段时间后硫酸的浓度减小
D.电极Ⅰ上发生反应:CO-2e-+H O=CO +2H+
2 2
10. 如下图所示的反应,下列说法正确的是( )
A.X不能发生水解反应 B.Y中含有极性键和非极性键
C.CO 的电子式为 D.Z中官能团名称为碳碳双键和苯环
2
11. 仅用下表提供的试剂和用品,能实现相应实验目的的是( )
选项 实验目的 试剂 用品
A 制备氢氧化铁胶体 饱和氯化铁溶液、蒸馏水 烧杯、胶头滴管、三脚架
B 比较镁和铝的金属性强弱 氯化镁溶液、氯化铝溶液、氨水 试管、胶头滴管
试管、橡胶塞、导管、乳胶管、
乙醇、乙酸、浓硫酸、饱和碳
C 制备乙酸乙酯 铁架台、碎瓷片、酒精灯、火柴、
酸钠溶液
量筒
D 制备银氨溶液 硝酸银溶液、氢氧化钠溶液 试管、胶头滴管
12. 某温度下,N O在金(Au)表面发生分解反应:2N O(g)=2N (g)+O (g),该反应的速率方
2 2 2 2
程为v=kpn(N O)(k为速率常数,k只与温度、催化剂、接触面积等有关,与浓度、压强无
2
关,n为反应级数),实验测得剩余N O的压强与时间的关系如图所示:
2
下列说法正确的是( )
A.n=1
B.速率常数k=1.0×10-3Pa·min-1
C.60分钟时p(N O)=0.04MPa
2
D.其他条件不变,增大N O的起始压强,反应速率增大
2
13. 将2molSO 和2molO 通入容积为1L的恒容密闭容器中,在一定条件下反应达到平衡,平
2 2
衡时SO 为0.4mol。若将1molSO 和1molO 通入相同的密闭容器中,同一温度下反应达到
3 2 2
新的平衡时,SO 的物质的量是( )
3
A.0.4mol B.0.2mol
C.大于0.2mol,小于0.4mol D.小于0.2mol
化学试卷(共 8 页)第 3 页14. 向容积为10L的密闭容器中投入2mol C H 和3mol CO ,主要发生如下两个反应,不同温度
2 6 2
下,测得5min时(反应均未平衡)的相关数据见下表。
I. C
2
H
6
(g)+CO
2
(g)C
2
H
4
(g)+CO(g)+H
2
O(g) ΔH
1
>0
II.C
2
H
6
(g)+2CO
2
(g)4CO(g)+3H
2
(g) ΔH
2
>0
下列说法正确的是( )
温度(C) 400 500 600
乙烷转化率(%) 2.2 9.0 17.8
乙烯选择性(%) 92.6 80.0 61.8
转化为乙烯的乙烷的物质的量
注:乙烯选择性 100%
转化的乙烷的总物质的量
A.升高温度,反应I速率增大,反应Ⅱ速率减小
B.500℃时,0~5min反应I的平均速率为:v(C H )=2.8810-3molL-1min-1
2 4
C.反应活化能:Ⅰ>Ⅱ
D.其他条件不变,增大
n(C H )/n(CO )
投料比,可提高乙烷平衡转化率
2 6 2
15. 向恒容密闭容器Ⅰ和Ⅱ(容积均为2L)中都充入NO和CO气体,发生反应:2NO(g)+2CO(g)
N
2
(g)+2CO
2
(g) ∆H,各物质的起始物质的量见下表。实验测得两容器在不同温度下达
到平衡时CO 的物质的量如下图所示,下列说法错误的是( )
2
起始物质的量
容器
NO CO
Ⅰ 1mol 3mol
Ⅱ 6mol 2mol
A.若容器内气体的平均摩尔质量不变,说明该反应达到平衡状态
B.N点的平衡常数为0.04
C.若将容器Ⅰ的容积改为1L,则T 温度下达到平衡时NO的转化率为25%
1
D.图中M点所示条件下,再通入2molCO和2molN ,此时v(正)>v(逆)
2
化学试卷(共 8 页)第 4 页二、非选择题:本题共4小题,共55分。
16. (13分)
C H OH、CH COOH、CO 、CH 、Fe都是日常生活中常见物质。
2 5 3 2 4
(1)常温常压下已知23g乙醇在氧气中完全燃烧放出683.4kJ的热量,请写出乙醇燃烧热的
热化学方程式______________________________________________________。
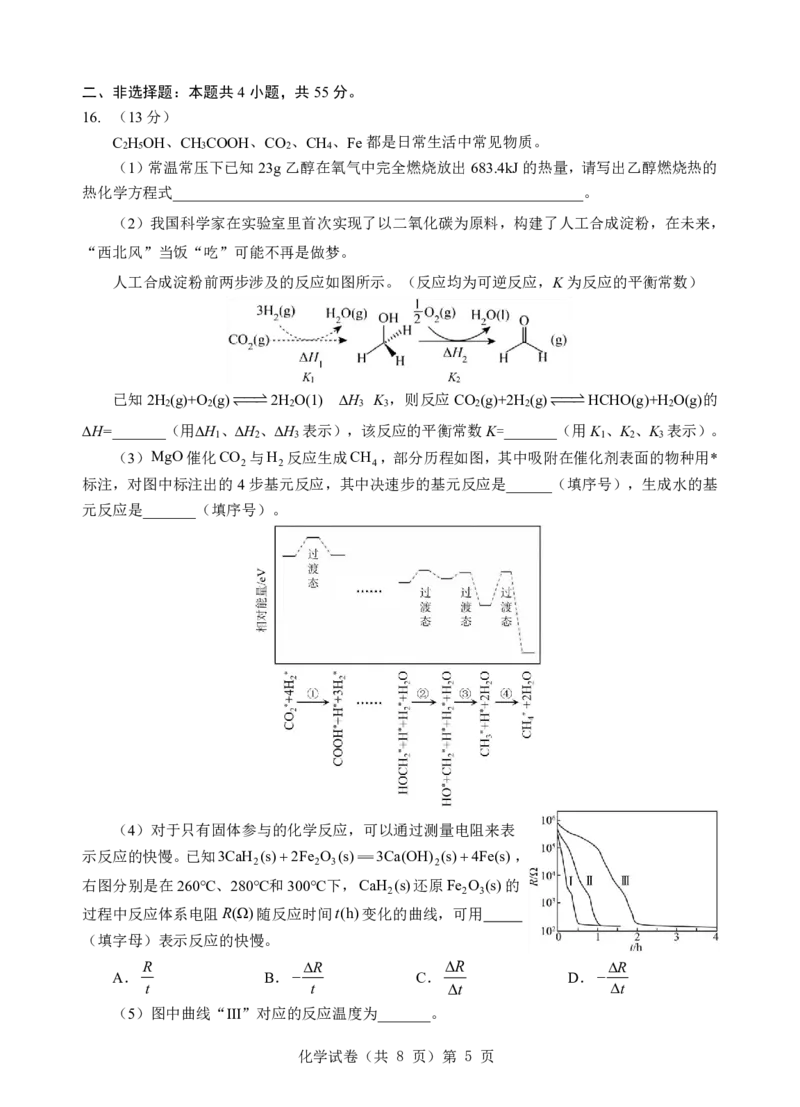
(2)我国科学家在实验室里首次实现了以二氧化碳为原料,构建了人工合成淀粉,在未来,
“西北风”当饭“吃”可能不再是做梦。
人工合成淀粉前两步涉及的反应如图所示。(反应均为可逆反应,K为反应的平衡常数)
已知2H
2
(g)+O
2
(g)2H
2
O(1) ∆H
3
K
3
,则反应CO
2
(g)+2H
2
(g)HCHO(g)+H
2
O(g)的
∆H=_______(用∆H 、∆H 、∆H 表示),该反应的平衡常数K=_______(用K 、K 、K 表示)。
1 2 3 1 2 3
(3)MgO催化CO 与H 反应生成CH ,部分历程如图,其中吸附在催化剂表面的物种用*
2 2 4
标注,对图中标注出的4步基元反应,其中决速步的基元反应是______(填序号),生成水的基
元反应是_______(填序号)。
(4)对于只有固体参与的化学反应,可以通过测量电阻来表
示反应的快慢。已知3CaH (s)2Fe O (s)=3Ca(OH) (s)4Fe(s) ,
2 2 3 2
右图分别是在260℃、280℃和300℃下,CaH (s)还原Fe O (s)的
2 2 3
过程中反应体系电阻R(Ω)随反应时间t(h)变化的曲线,可用
(填字母)表示反应的快慢。
R R R R
A. B. C. D.
t t t t
(5)图中曲线“Ⅲ”对应的反应温度为_______。
化学试卷(共 8 页)第 5 页17. (14分)
Cu(Ⅱ)盐(Ⅱ指元素在化合物中的价态)在水溶液中的颜色十分丰富,某课外小组对其进行探究:
探究一 温度对CuCl 溶液颜色的影响。
2
在CuCl 溶液中存在如下平衡:
2
[Cu(H
2
O)
4
]2++4Cl﹣ [CuCl
4
]2-+4H
2
O ΔH>0
蓝色 黄色
【实验预测】温度升高,溶液变成黄色;温度降低,溶液变成蓝色。
【实验操作及现象分析】
取两支试管,分别加入2mL0.5mol/LCuCl 溶液,将其中一支试管先加热,然后置于冷水中,
2
观察并记录实验现象,与另一支试管对比。
同学们观察到一开始溶液呈蓝色,加热试管,溶液变成黄绿色;将试管置于冷水中,溶液又
由黄绿色变成蓝绿色。
(1)甲同学认为随着温度的变化,溶液颜色随之变化,得出温度对化学平衡的影响是:在
其他条件一定时,温度升高,平衡向_____(填“放热”或“吸热”)方向移动;反之则向相反
方向移动。
(2)乙同学认为实验现象与预测有一定出入,推测是温度变化太小导致的,于是对CuCl 溶
2
液加热到较高温度,但仍未观察到[CuCl ]2-的黄色,认为其原因是溶液中存在大量[Cu(H O) ]2+,
4 2 4
导致观察不到溶液的黄色,这说明在其他条件不变时,温度的改变对该平衡移动的影响______(填
“较小”或“较大”)。
(3)综上所述同学们得出结论:温度的变化会导致平衡移动,但该反应的______(填“内
因”或“外因”)决定了平衡移动的程度。
探究二 CuCl 与Na S O 溶液反应的颜色变化。
2 2 2 3
已知:ⅰ.2S O2-+Cu2+ [Cu(S O ) ]2- (绿色) 2S O2-+Cu+ [Cu(S O ) ]3- (无色);
2 3 2 3 2 2 3 2 3 2
ⅱ.S O2-易被氧化为S O2-,Cu+在水溶液中不稳定。
2 3 4 6
【实验预测】同学们根据资料认为Cu(Ⅱ)盐与Na S O 可能会发生两种反应:
2 2 3
假设1:Cu2+与S O2-在溶液中发生络合反应生成[Cu(S O ) ]2-;
2 3 2 3 2
假设2:Cu(Ⅱ)有氧化性,与S O2-在溶液中发生氧化还原反应。
2 3
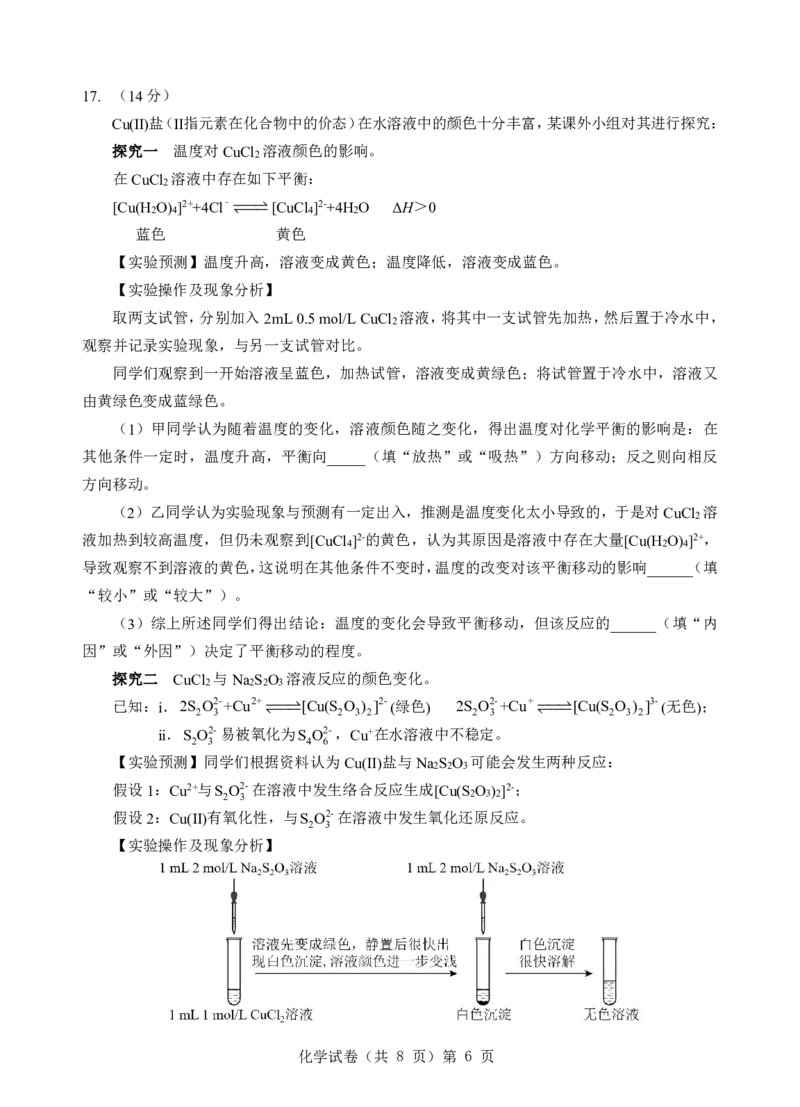
【实验操作及现象分析】
化学试卷(共 8 页)第 6 页(4)甲同学认为实验现象能证明假设1和2均成立,他的理由是_______________________。
(5)乙同学认为Cu(Ⅱ)盐与Na S O 在溶液中的反应与多种因素有关,并得出实验结论:
2 2 3
①Cu(Ⅱ)与S O2-反应时,络合反应速率____氧化还原反应速率。(填“>”“<”或“=”)
2 3
②随n(S O2-):n(Cu2+)的增大,络合反应的趋势____氧化还原反应的趋势。(填“>”“<”
2 3
或“=”)
(6)经检验证实最终无色溶液中大量存在S O2-。写出Cu2+与S O2-发生反应得到无色溶液
4 6 2 3
的离子方程式:____________________________________________________________。
18. (14分)
一定条件下,M与N发生催化反应,反应如下:
反应Ⅰ:M(g)+N(g)X(g) ∆H
1
<0
反应Ⅱ:M(g)+N(g)Y(g) ∆H
2
<0
反应Ⅲ:Y(g)X(g) ∆H
3
<0
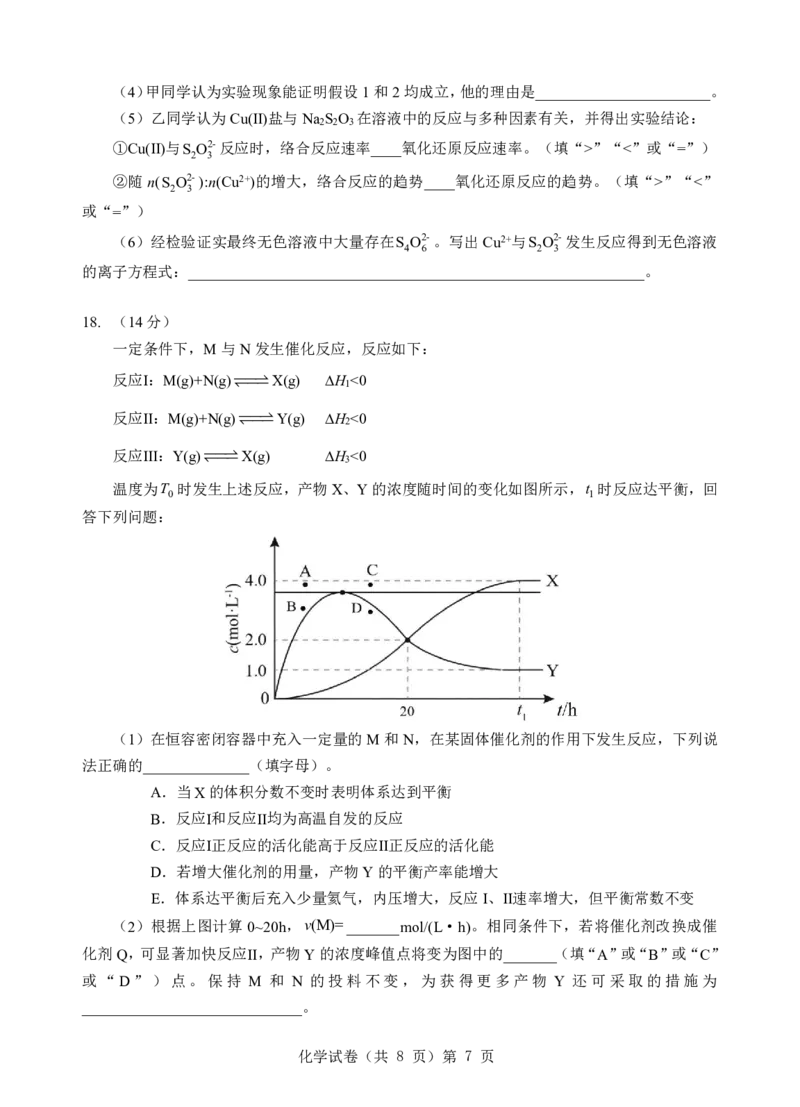
温度为T 时发生上述反应,产物X、Y的浓度随时间的变化如图所示,t 时反应达平衡,回
0 1
答下列问题:
(1)在恒容密闭容器中充入一定量的M和N,在某固体催化剂的作用下发生反应,下列说
法正确的______________(填字母)。
A.当X的体积分数不变时表明体系达到平衡
B.反应Ⅰ和反应Ⅱ均为高温自发的反应
C.反应Ⅰ正反应的活化能高于反应Ⅱ正反应的活化能
D.若增大催化剂的用量,产物Y的平衡产率能增大
E.体系达平衡后充入少量氦气,内压增大,反应I、Ⅱ速率增大,但平衡常数不变
(2)根据上图计算0~20h,v(M)=_______mol/(L·h)。相同条件下,若将催化剂改换成催
化剂Q,可显著加快反应Ⅱ,产物Y的浓度峰值点将变为图中的_______(填“A”或“B”或“C”
或“D”)点。保持 M 和 N 的投料不变,为获得更多产物 Y 还可采取的措施为
_____________________________。
化学试卷(共 8 页)第 7 页(3)控制温度为T ,若向容积为2L的恒容密闭容器中加入1mol的M和2mol的N,测得
0
M的平衡转化率为50%,则平衡体系中X的物质的量为_______mol,反应Ⅰ的平衡常数K=______
(用分数表示)。
(4)从图中可知平衡产物中X的浓度高于Y,从能量的角度分析可知X的能量_______Y
的能量。(填“低于”或“高于”)
19. (14分)
Ⅰ.(1)水果罐头中添加抗坏血酸(即维生素C)主要是用作_______(填字母)。
a.营养强化剂 b.抗氧化剂 c.增味剂
(2)甲基丙烯酸甲酯[CH =C(CH )COOCH ]是合成有机玻璃的单体,其含氧官能团的结构式
2 3 3
为_______________,其加聚反应产物有机玻璃的结构简式为_______________。
Ⅱ.恒压下,向某密闭容器中充入一定量的CH OH(g)和CO(g),发生如下反应:
3
主反应:CH OH(g)CO(g)CH COOH(g) H <0
3 3 1
副反应:CH
3
OH(g)CH
3
COOH(g)CH
3
COOCH
3
(g)H
2
O(g) H
2
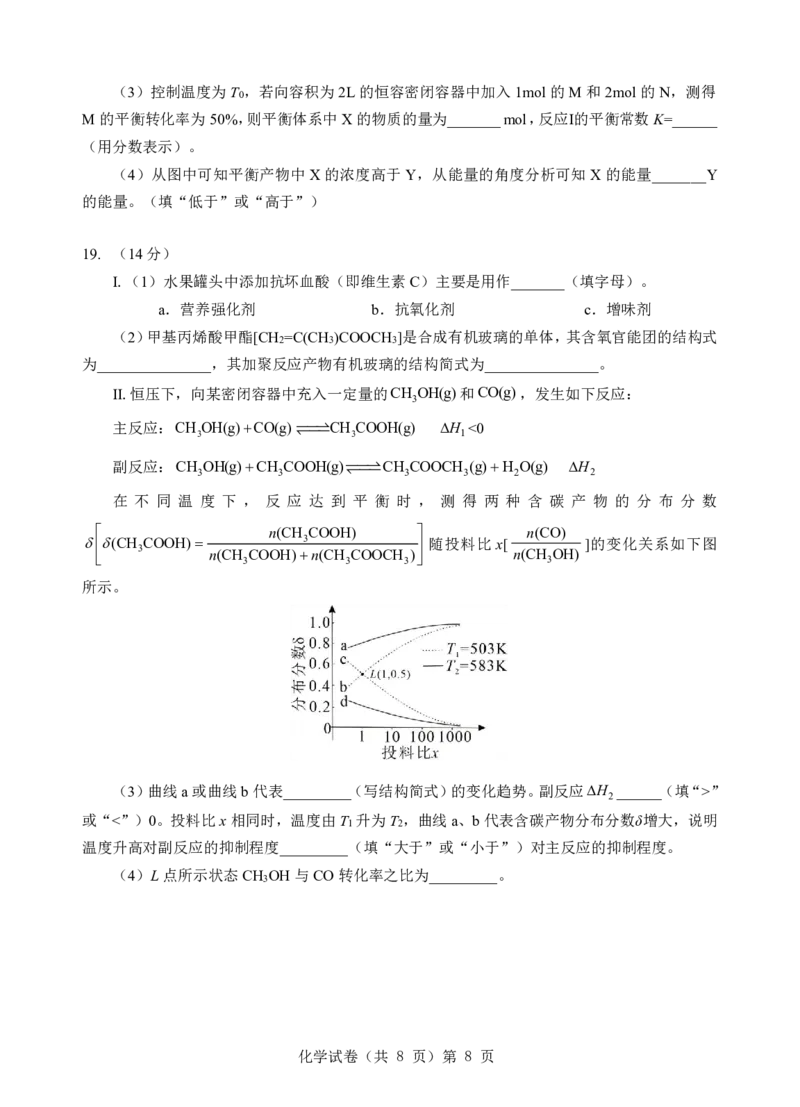
在 不 同 温 度 下 , 反 应 达 到 平 衡 时 , 测 得 两 种 含 碳 产 物 的 分 布 分 数
n(CH COOH) n(CO)
(CH COOH) 3 随投料比 x[ ]的变化关系如下图
3 n(CH 3 COOH)n(CH 3 COOCH 3 ) n(CH 3 OH)
所示。
(3)曲线a或曲线b代表_________(写结构简式)的变化趋势。副反应H ______(填“>”
2
或“<”)0。投料比x相同时,温度由T 升为T ,曲线a、b代表含碳产物分布分数δ增大,说明
1 2
温度升高对副反应的抑制程度_________(填“大于”或“小于”)对主反应的抑制程度。
(4)L点所示状态CH OH与CO转化率之比为_________。
3
化学试卷(共 8 页)第 8 页