文档内容
连城⼀中 2025—2026学年上期⾼⼆年级⽉考 2化学试题
满分:100分 考试时间:75分钟
第Ⅰ卷(选择题,共 40分)
可能⽤到的相对原⼦质量:Cu 64
⼀、选择题。(本⼤题共10⼩题,每⼩题4分,共40分。在每⼩题列出的四个选项中,只有
⼀项是最符合题⽬要求的。)
1.我国古代的⽣产和⽣活中蕴含着丰富的化学知识,⽽化学知识也⼴泛应⽤于现代⽣产、⽣活
中。下列有关说法不正确的是( )
A.明矾和⼆氧化氯⽤于净⽔时的原理相同
B.⼯业上⽤电解熔融氯化镁制备⾦属镁
C.实验室中常⽤排饱和⻝盐⽔的⽅法收集Cl
2
D.“暖宝宝贴”是利⽤原电池原理加快铁的腐蚀放热
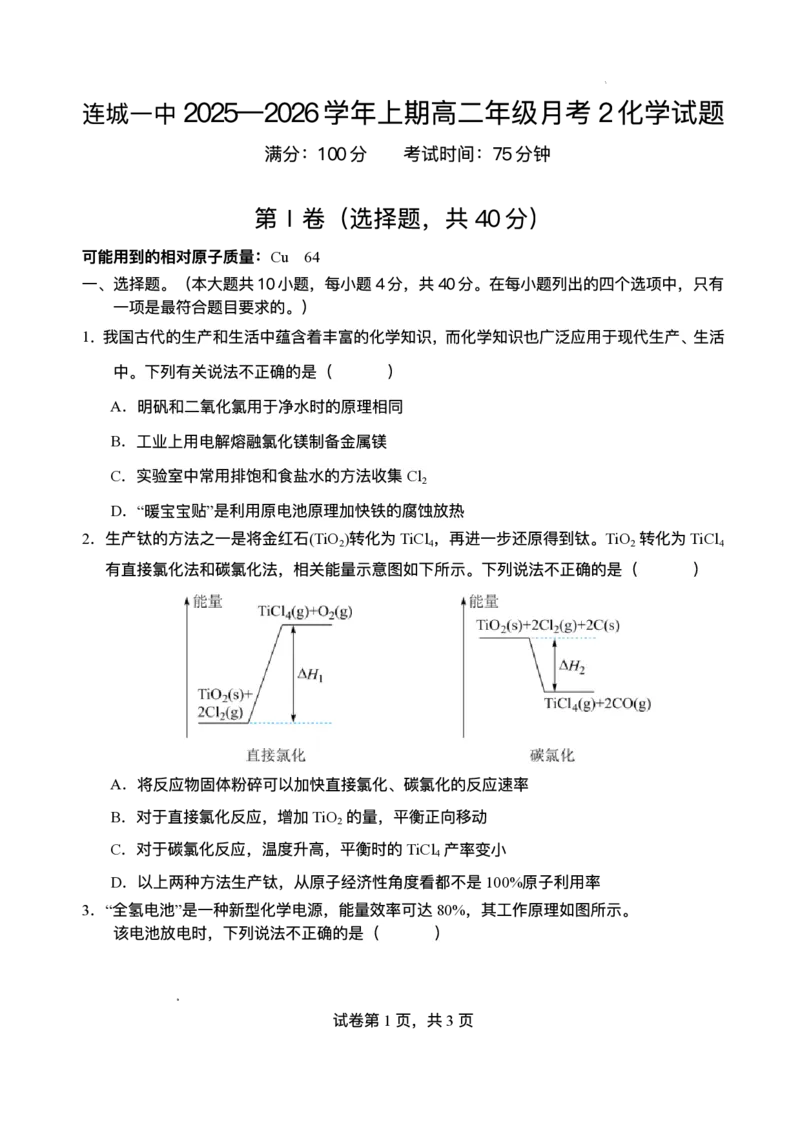
2.⽣产钛的⽅法之⼀是将⾦红⽯(TiO )转化为TiCl ,再进⼀步还原得到钛。TiO 转化为TiCl
2 4 2 4
有直接氯化法和碳氯化法,相关能量示意图如下所示。下列说法不正确的是( )
A.将反应物固体粉碎可以加快直接氯化、碳氯化的反应速率
B.对于直接氯化反应,增加TiO 的量,平衡正向移动
2
C.对于碳氯化反应,温度升⾼,平衡时的TiCl 产率变⼩
4
D.以上两种⽅法⽣产钛,从原⼦经济性⻆度看都不是100%原⼦利⽤率
3.“全氢电池”是⼀种新型化学电源,能量效率可达80%,其⼯作原理如图所示。
该电池放电时,下列说法不正确的是( )
试卷第1⻚,共3⻚
学科⽹(北京)股份有限公司A. 主要作⽤是提⾼溶液的导电性
B. 通过离⼦交换膜由左向右移动
C.吸附层A为负极,其电极反应为
D.电池总反应为
4.乳酸是⼀种重要的化⼯原料,可⽤于制备聚乳酸(PLA)⽣物可降解性塑料。已知常温下,乳
酸的电离常数 。下列有关说法正确的是( )
A.乳酸稀溶液加⽔稀释的过程中,溶液中 减⼩
B.在乳酸稀溶液中滴加少量盐酸,乳酸的电离平衡逆向移动, 变⼩
C.恒温下,在乳酸稀溶液中滴加少量 溶液,乳酸的电离常数
D.常温下,体积为 的醋酸溶液和乳酸溶液分别加⽔稀释⾄1000mL,若稀释后
溶液的pH:醋酸<乳酸,则电离常数:醋酸<乳酸
5.下列有关实验探究⽅案设计合理的是( )
选项 实验⽅案 实验⽬的
向等体积等浓度的H O 溶液中分别加⼊5滴等浓度
A 2 2 ⽐较Cu2+和Fe3+的催化效果
的CuSO 和FeCl 溶液,观察⽓体产⽣的速率
4 3
中和同体积同pH的HA溶液和CH COOH溶液,
B 3 判断HA是⼀种弱酸
前者所需的NaOH的物质的量较多
⽤洁净的玻璃棒蘸取少许84消毒液滴在pH试纸上,
C 测定84消毒液的pH
变⾊稳定后与标准⽐⾊卡对照
在 平衡体系中加
D 探究离⼦浓度对平衡移动的影响
⼊KCl晶体,观察并⽐较实验现象
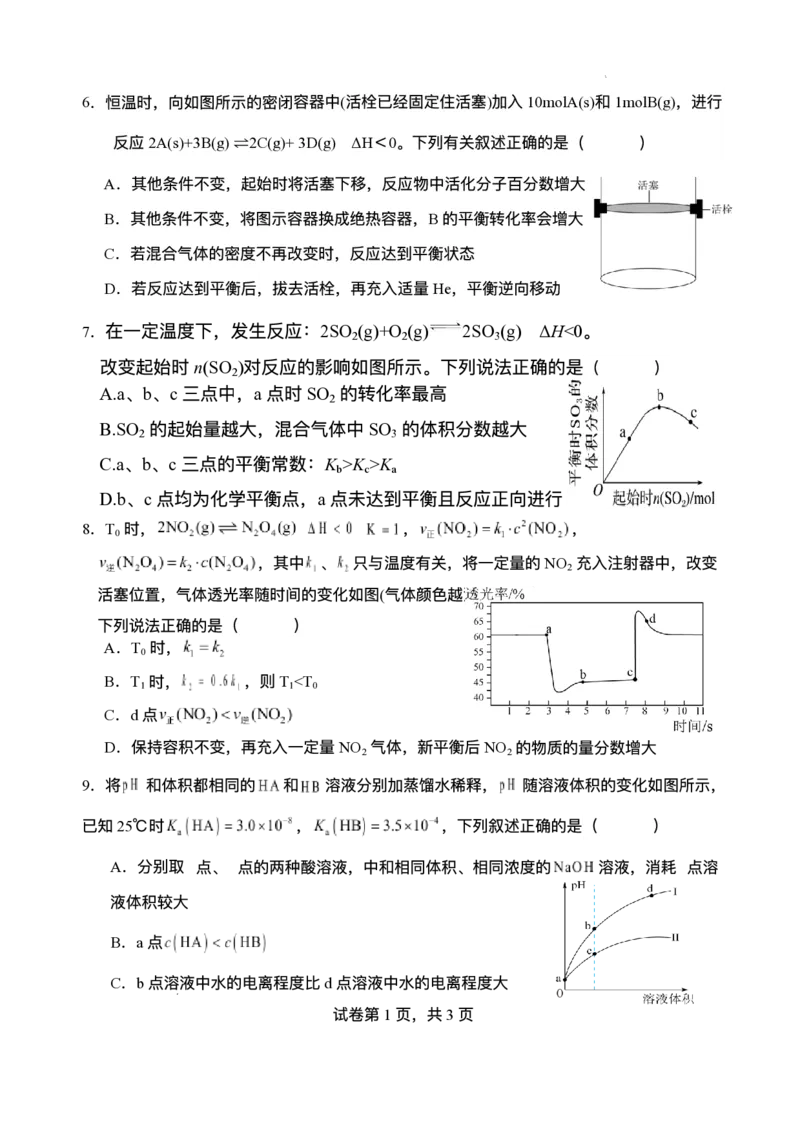
试卷第1⻚,共3⻚6.恒温时,向如图所示的密闭容器中(活栓已经固定住活塞)加⼊10molA(s)和1molB(g),进⾏
反应2A(s)+3B(g)⇌2C(g)+3D(g) ΔH<0。下列有关叙述正确的是( )
A.其他条件不变,起始时将活塞下移,反应物中活化分⼦百分数增⼤
B.其他条件不变,将图示容器换成绝热容器,B的平衡转化率会增⼤
C.若混合⽓体的密度不再改变时,反应达到平衡状态
D.若反应达到平衡后,拔去活栓,再充⼊适量He,平衡逆向移动
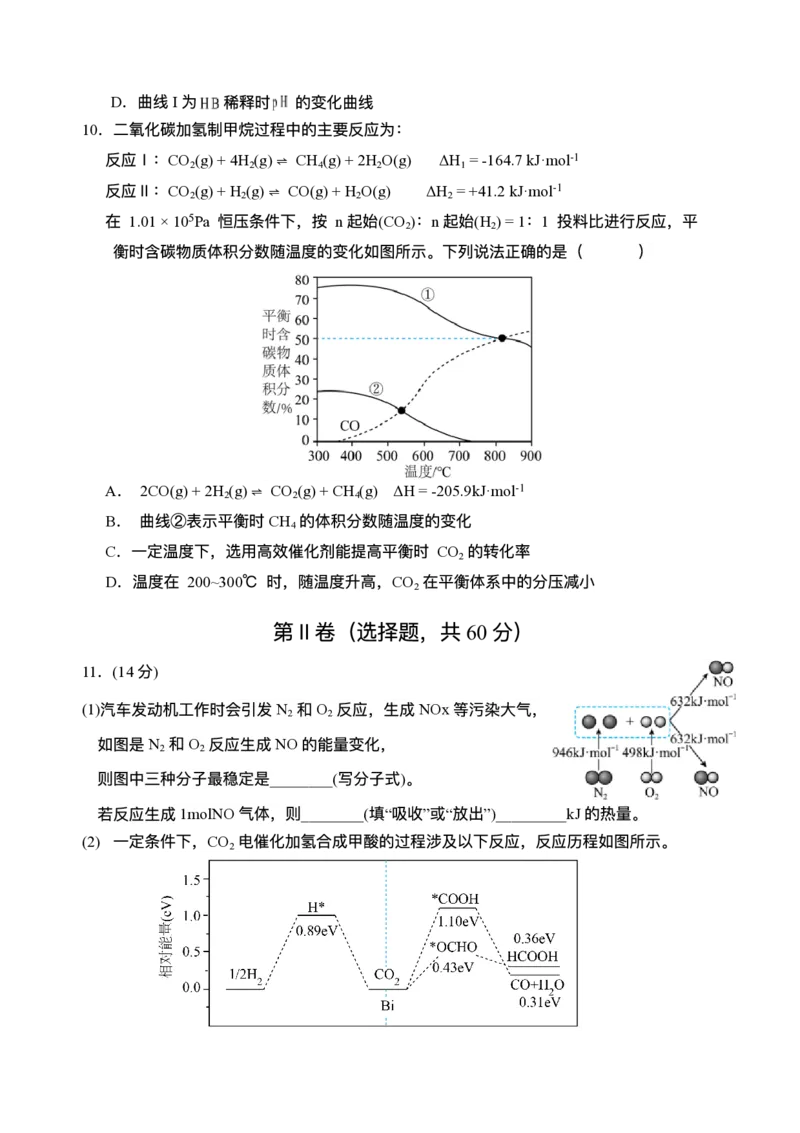
7.在⼀定温度下,发⽣反应:2SO (g)+O (g) 2SO (g) ΔH<0。
2 2 3
改变起始时 n(SO )对反应的影响如图所示。下列说法正确的是( )
2
A.a、b、c 三点中,a 点时 SO 的转化率最⾼
2
B.SO 的起始量越⼤,混合⽓体中 SO 的体积分数越⼤
2 3
C.a、b、c 三点的平衡常数:K >K >K
b c a
D.b、c 点均为化学平衡点,a 点未达到平衡且反应正向进⾏
8.T 时, , ,
0
,其中 、 只与温度有关,将⼀定量的NO 充⼊注射器中,改变
2
活塞位置,⽓体透光率随时间的变化如图(⽓体颜⾊越深,透光率越低),
下列说法正确的是( )
A.T 时,
0
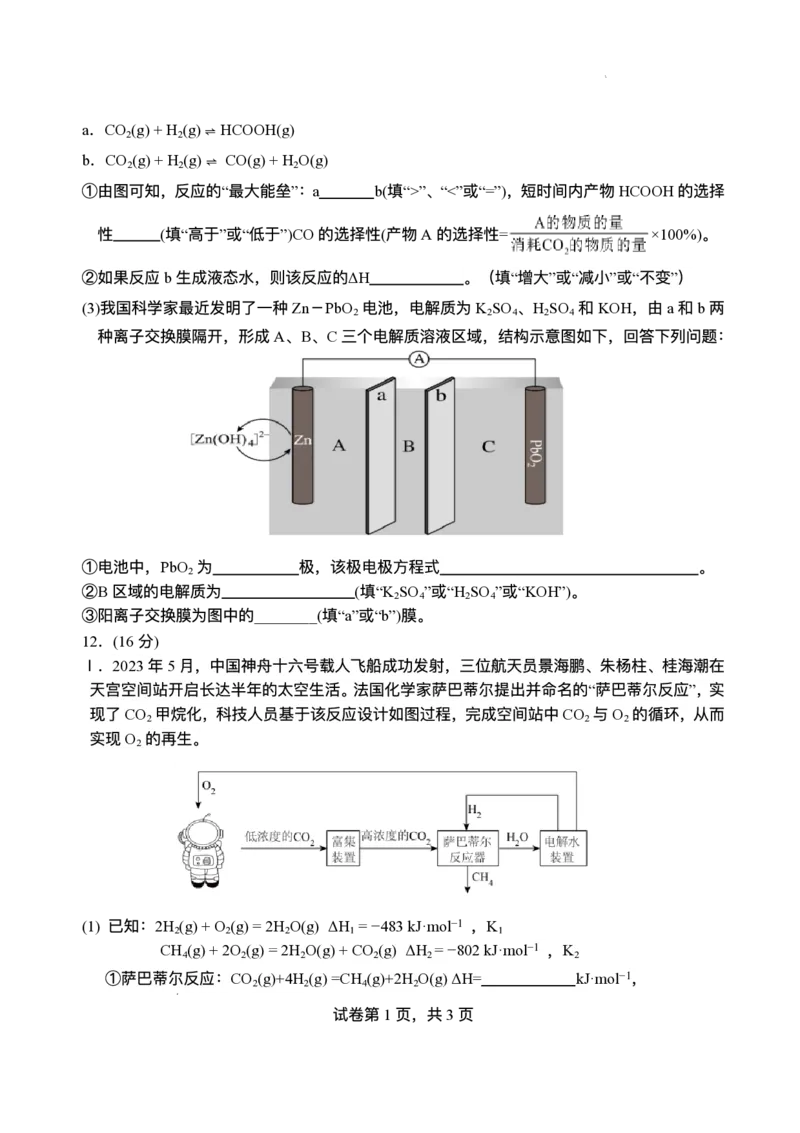
B.T 时, ,则T ”、“<”或“=”),短时间内产物HCOOH的选择
性 (填“⾼于”或“低于”)CO的选择性(产物A的选择性= ×100%)。
②如果反应b⽣成液态⽔,则该反应的ΔH 。(填“增⼤”或“减⼩”或“不变”)
(3)我国科学家最近发明了⼀种Zn-PbO 电池,电解质为K SO 、H SO 和KOH,由a和b两
2 2 4 2 4
种离⼦交换膜隔开,形成A、B、C三个电解质溶液区域,结构示意图如下,回答下列问题:
①电池中,PbO 为 极,该极电极⽅程式 。
2
②B区域的电解质为 (填“K SO ”或“H SO ”或“KOH”)。
2 4 2 4
③阳离⼦交换膜为图中的________(填“a”或“b”)膜。
12.(16分)
Ⅰ.2023年5⽉,中国神⾈⼗六号载⼈⻜船成功发射,三位航天员景海鹏、朱杨柱、桂海潮在
天宫空间站开启⻓达半年的太空⽣活。法国化学家萨巴蒂尔提出并命名的“萨巴蒂尔反应”,实
现了CO 甲烷化,科技⼈员基于该反应设计如图过程,完成空间站中CO 与O 的循环,从⽽
2 2 2
实现O 的再⽣。
2
(1) 已知:2H (g)+O (g)=2H O(g) ΔH =−483kJ·mol−1 ,K
2 2 2 1 1
CH (g)+2O (g)=2H O(g)+CO (g) ΔH =−802kJ·mol−1 ,K
4 2 2 2 2 2
①萨巴蒂尔反应:CO (g)+4H (g)=CH (g)+2H O(g)ΔH= kJ·mol−1,
2 2 4 2
试卷第1⻚,共3⻚
学科⽹(北京)股份有限公司K = (⽤K 和K 表示)
3 1 2
②“ 萨巴蒂尔反应” 在________(选填“⾼温”或“低温”或“ 任何温度” )下能⾃发进⾏。
(2)下列关于“ 萨巴蒂尔反应” 的说法中,正确的是_______。
a.输送进⼊萨巴蒂尔反应器的是电解⽔装置的阴极产物
b.采⽤⾼压和合适催化剂均有利于提⾼萨巴蒂尔反应中CO 平衡转化率
2
c.恒温恒压下, 增⼤,可提⾼萨巴蒂尔反应中CO 平衡转化率
2
d.应该在萨巴蒂尔反应器的前端维持较⾼温度,后端维持较低温度
Ⅱ.异丙醇 催化脱⽔⽣成丙烯 ,有关反应如下:
反应①: =+52kJ·mol−1;
反应②: 。
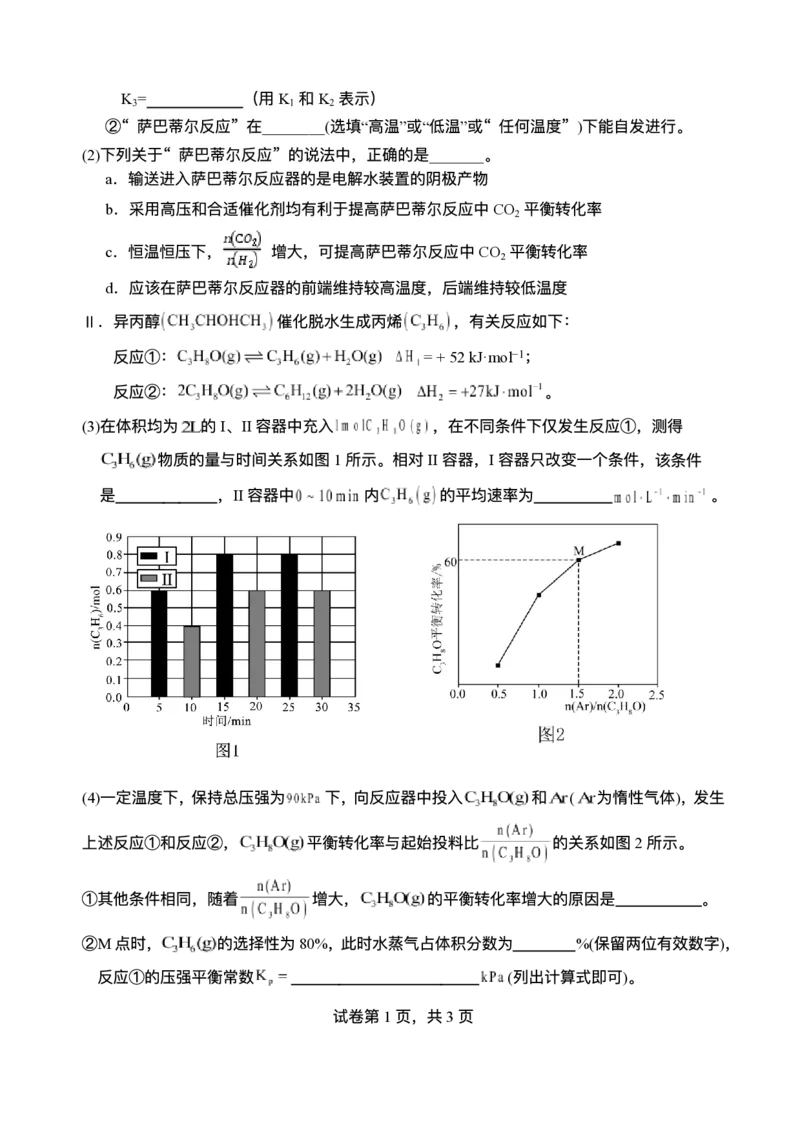
(3)在体积均为 的I、II容器中充⼊ ,在不同条件下仅发⽣反应①,测得
物质的量与时间关系如图1所示。相对II容器,I容器只改变⼀个条件,该条件
是 ,II容器中 内 的平均速率为 。
(4)⼀定温度下,保持总压强为 下,向反应器中投⼊ 和 ( 为惰性⽓体),发⽣
上述反应①和反应②, 平衡转化率与起始投料⽐ 的关系如图2所示。
①其他条件相同,随着 增⼤, 的平衡转化率增⼤的原因是 。
②M点时, 的选择性为80%,此时⽔蒸⽓占体积分数为 %(保留两位有效数字),
反应①的压强平衡常数 (列出计算式即可)。
试卷第1⻚,共3⻚[已知 的选择性 ]
13.(16分)
Ⅰ.绝⼤部分氰化物因能强烈抑制细胞呼吸⽽极具毒性,但它并⾮只存在于实验室中。苦杏仁、
⽊薯、苹果种⼦等天然⻝物中均含微量氰化物;⼯业上,它更是⻩⾦提炼和某些药物合成
的重要原料。已知 时的电离平衡常数:
化学式 HCN H CO CH COOH
2 3 3
K =4.3×10-7
电离平衡常数 6.2×10-10 1 1.8×10-5
K =5.6×10-11
2
(1) 向HCN溶液加⽔稀释过程中,下列说法正确的是 。
A.溶液中导电能⼒减弱 B.HCN电离程度增⼤,c(H+)也增⼤
C.溶液中 增⼤ D.溶液中 增⼤
(2)物质的量浓度均为0.1mol·L-1NaCN溶液和Na CO 溶液,⽐较pH:NaCN Na CO
2 3 2 3
(填“ <” 或“ >” )。
(3)下列离⼦⽅程式中⼀定错误的是____________。
A. B.
C. D.
(4)25℃时,将amol·L-1醋酸与bmol·L-1NaOH等体积混合,反应后溶液恰好显中性,⽤a、b
表示醋酸的电离平衡常数为___________________。
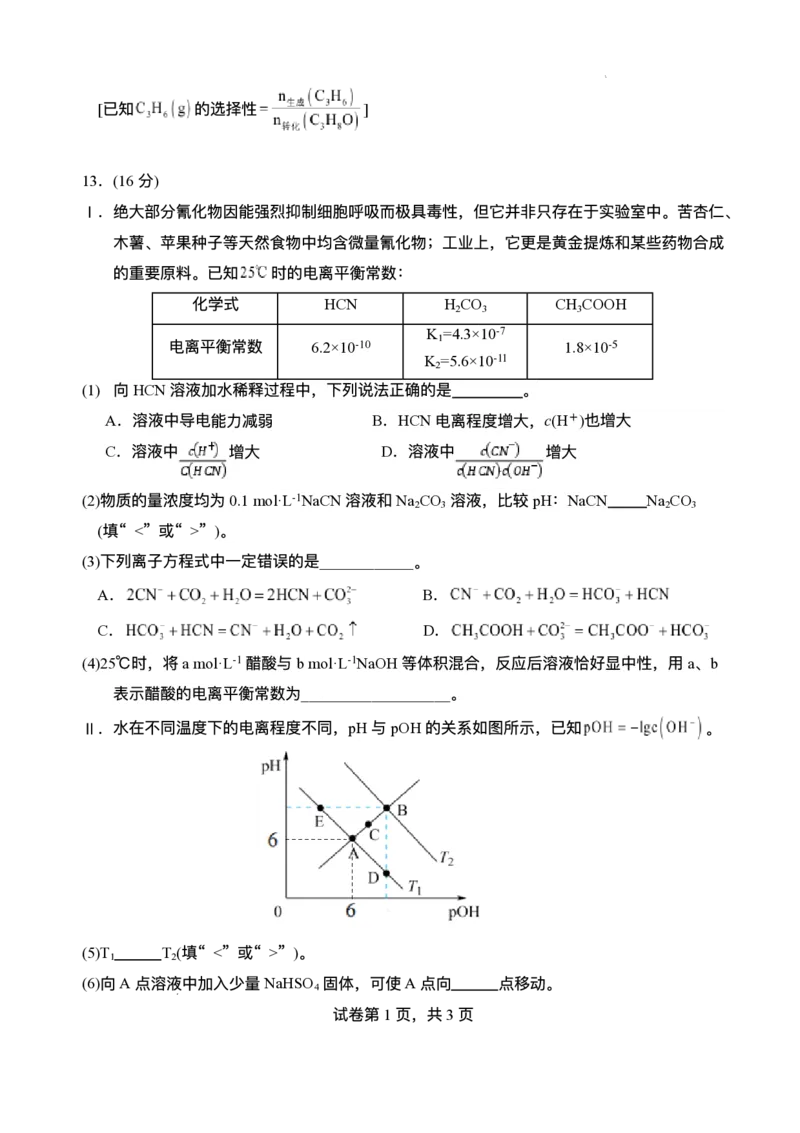
Ⅱ.⽔在不同温度下的电离程度不同,pH与pOH的关系如图所示,已知 。
(5)T T (填“ <” 或“ >” )。
1 2
(6)向A点溶液中加⼊少量NaHSO 固体,可使A点向 点移动。
4
试卷第1⻚,共3⻚
学科⽹(北京)股份有限公司(7)T 时,0.1mol·L-1HA溶液中 ,HA是 (填“强酸”或“弱酸”)。
1
(8)T 时,V LpH=1的H SO 与V LpH=12的NaOH溶液等体积混合后,若所得混合溶液的
1 1 2 4 2
pH=10,则V :V = 。
1 2
14.(14分)
某实验⼩组通过以下实验,探究镀件表⾯镀铜的最佳条件。回答下列问题:
【查阅资料】① ;
② 在溶液中不稳定,容易发⽣歧化。
【实验设计】⽤ 、 (焦磷酸钠)、添加剂配制⼀定浓度的电镀液,
分别⽤纯铜和镀件作为两极材料,探究电镀液的pH、电流密度、电极板间距对镀层的影响。
(1)镀件表⾯的油污可⽤热的纯碱溶液清洗,原因是 (填离⼦⽅程式)。
(2)电镀时阴极上发⽣的主要反应的电极反应式为 。
【实验结果与数据分析】
i.其他条件不变时,电镀10min,pH对电镀的影响如下表:
实验序号 pH值 镀膜质量/g 镀层外观
1 3 0.0136 表⾯斑驳
2 7 0.0258 光亮,不光滑
3 8.5 0.0352 光亮,光滑
4 10 0.0216 表⾯部分斑驳
(3)实验3中,铜镀层的沉积速率 mol/min。
(4)实验1和实验4中,酸性或碱性较强时,镀层出现斑驳的可能原因是 。
ii.电流密度、电极板间距与镀膜质量的关系如图所示:
试卷第1⻚,共3⻚(5)本实验电镀的最佳条件是pH为8.5、电流密度为 、电极板间距为 cm。
(6)使⽤最佳条件电镀时,会有部分Cu+⽣成。在阳极附近的电镀液中出现红⾊固体沉积物,其
可能原因是 (填离⼦⽅程式),通空⽓搅拌可防⽌红⾊固体沉积物形成。
连城⼀中 2025—2026学年上期⾼⼆年级⽉考 2化学答案
题号 1 2 3 4 5 6 7 8 9 10
答案 A B C D B C A C D B
11.(14分)
(1)N (1分) 吸收(1分) 90(2分)
2
(2)①<(1分) ⾼于 (1分) ②减⼩ (2分)
(3)①正(1分) PbO +SO2-4+2e-+4H+===PbSO +2H O(2分)
2 4 2
②K SO (2分) ③a(1分)
2 4
12.(16分)
(1)①−164(2分) (2分) ②低温(1分)
(2)ad(2分) (3)升温(1分) 0.02 (2分)
(4)①投料⽐增⼤,平衡体系分压减⼩,平衡向正反应⽅向移动,异丙醇平衡转化率增⼤(2分
)
②20 (2分) ③ (2分)
13.(16分)
(1) AC(2分) (2)<(2分) (3)AC(2分) (4) (2分)
试卷第1⻚,共3⻚
学科⽹(北京)股份有限公司(5)>(2分) (6)D(2分) (7)弱酸 (2分) (8)9:1(2分)
14.(14分)
(1) (2分)
(2) (2分)
(3)5.5×10-5(2分)
(4)pH=3酸性强,H+放电产⽣氢⽓,pH=10碱性强,易⽣成氢氧化铜沉淀均影响镀件上铜的沉
积(2分)
(5)0.5~0.75(区间任意⼀个数值也可以)(2分) 1.5(2分)
(6)2Cu++H O=Cu O+2H+或2Cu++2OH-=Cu O+H O或2Cu+=Cu+Cu2+(2分)
2 2 2 2
试卷第1⻚,共3⻚