文档内容
2025-2026 学年度高二第一学期 10 月学业水平质量监测
化学试题
注意事项
1.本试卷共10页,满分为100分,考试时间为75分钟。考试结束后,请将答题卡交回。
2.答题前,请务必将自己的姓名、考试号等用0.5毫米黑色墨水的签字笔填写在答题卡的规
定位置。
3.作答选择题,必须用2B铅笔将答题卡上对应选项的方框涂满、涂黑;如需改动,请用橡皮
擦干净后,再选涂其他答案。作答非选择题,必须用0.5毫米黑色墨水的签字笔在答题卡上
的指定位置作答,在其他位置作答一律无效。
一、单项选择题(共13小题 满分39分)
1.化学和生活、科技、社会发展息息相关,下列说法正确的是
A.铁制品表面镀上铜保护层,是利用牺牲阳极法的阴极保护法
B.载人飞船上的太阳能电池板直接将化学能转化为电能
C.我国发射的“北斗”组网卫星所使用的碳纤维,是一种新型无机非金属材料
D.“朱雀二号”遥二火箭成为全球首枚成功入轨的液氧甲烷运载火箭,甲烷作助燃剂
2.下列实验装置,能达到实验目的的是
A.用装置甲设计铜锌原电池
B.用装置乙定量测定 的分解速率
C.用装置丙采集到的压强数据判断铁钉发生析氢腐蚀还是吸氧腐蚀
D.用装置丁制备 并能较长时间观察其颜色
3.下列有关化学用语表示正确的是
A.潮湿空气中铁钉发生吸氧腐蚀时的负极反应为B.电解精炼铜时,阴极的电极反应式为
C. 在 中完全燃烧,生成2mol ,放出571.6kJ的热量,表示 燃
烧热的热化学方程式为
D.情性电极电解氯化镁溶液的离子方程式为
4.我国科学家研发出一种乙醇(沸点78.5℃)绿色制氢新途径,并实现高附加值乙酸(沸点
118℃)的生产,反应为: 。一定条件下,
在恒容密闭容器中发生该反应,下列说法正确的是
A.降低温度,v(正)减小,v(逆)增大
B.向容器中通入氦气,(正)、(逆)均增大
C.当v (HO)=2v (H),说明该反应达到平衡状态
正 2 逆 2
D.当混合气体的平均摩尔质量不变,说明该反应达到平衡状态
5.在给定条件下,下列选项所示的物质间转化均能一步实现的是
A.
B.
C.
D.
6. 转化为 的反应为 。在有、
无催化剂条件下 氧化成 过程中能量的变化如图所示。450℃、 催化时,该反
应机理为:
反应①
反应②
下列说法正确的是
高二化学试题 第2页 共3页A.反应1的△S>0
B. 催化时,反应②的速率大于反应①
C.其他条件相同,增大 , 的转化率下降
D.
7.水煤气变换反应为 。我国学者结合实验与计算机模拟
结果,研究了在金催化剂表面上水煤气变换的反应历程,如图所示,其中吸附在金催化剂
表面上的物种用*标注。下列说法错误的是
A.水煤气变换反应的
B.步骤②存在 键的形成
C.该反应的决速步是
D.步骤⑤的化学方程式为:
8.通过电解废旧锂电池中的 可获得难溶性的 和 ,电解示意图如下
(其中滤布的作用是阻挡固体颗粒,但离子可自由通过。电解过程中溶液的体积变化忽略不
计)。下列说法正确的是A.电极A为阳极,发生氧化反应
B.电极B的电极反应:
C.电解一段时间后溶液中Mn2+浓度保持不变
D.电解结束,可通过调节 除去Mn2+,再加入 溶液以获得
9.某学习小组为探究影响酸性高锰酸钾溶液与 溶液反应速率的因素,该小组设计
如表实验方案。
实验 溶 混合溶液褪色时间/min
溶液/mL 溶液/mL 液/mL 溶液/mL
1 3.0 2.0 1.0 0 2.0 8
2 3.0 2.0 2.0 0 a 6
3 4.0 2.0 2.0 0 0 4
4 3.0 2.0 1.0 0.5 b 3
下列说法不正确的是
A.该反应的离子方程式为
B. 、
C.实验3从反应开始到反应结束这段时间内反应速率
D.实验4与实验1相比,说明 可能是该反应的催化剂
10.钠离子电池使用的电极材料主要是钠盐,相较于锂盐而言储量更丰富,价格更低廉。
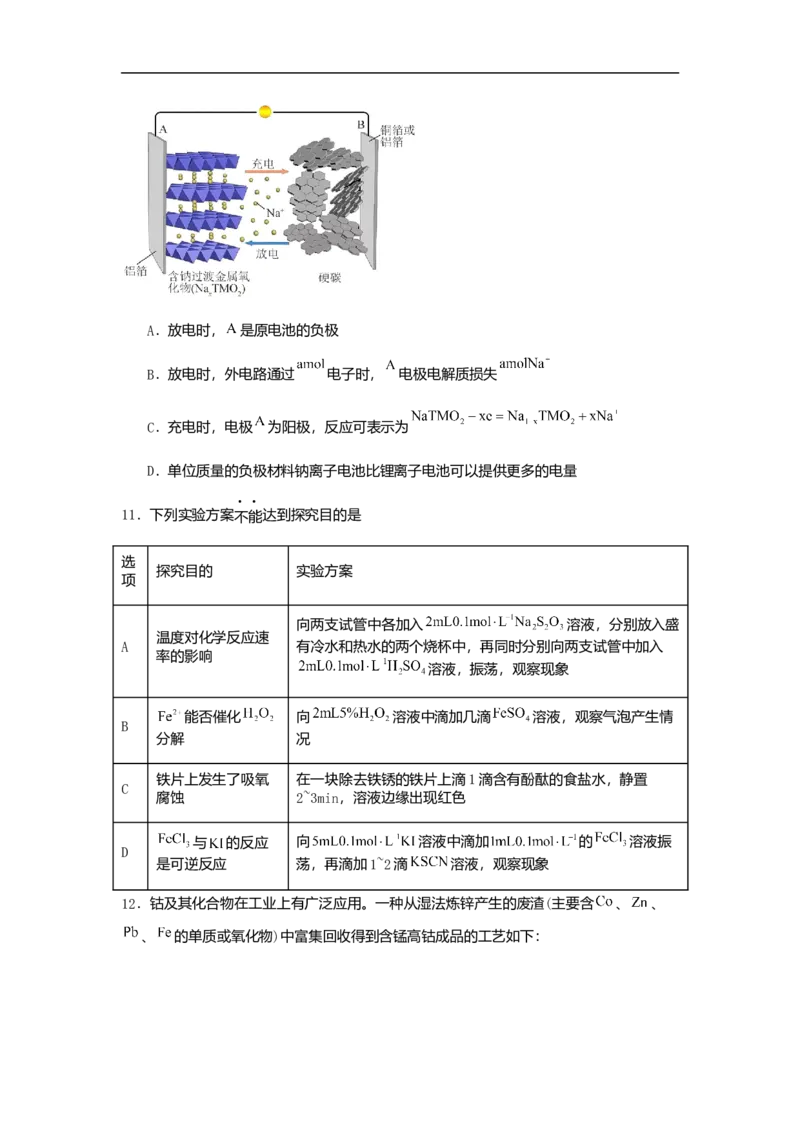
某钠离子电池结构如图所示,电极 为含钠过渡金属氧化物 ,电极 为硬碳,
充电时 得电子成为 嵌入硬碳中。下列说法正确的是
高二化学试题 第4页 共3页A.放电时, 是原电池的负极
B.放电时,外电路通过 电子时, 电极电解质损失
C.充电时,电极 为阳极,反应可表示为
D.单位质量的负极材料钠离子电池比锂离子电池可以提供更多的电量
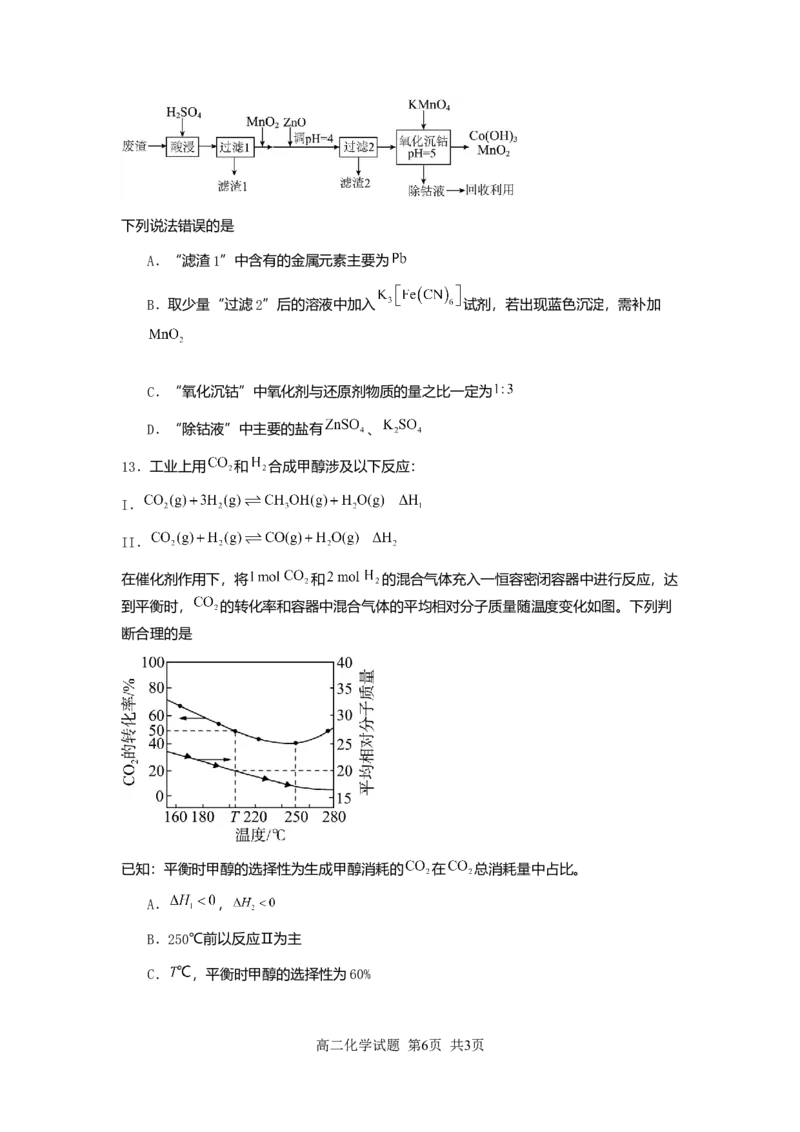
11.下列实验方案不能达到探究目的是
选
探究目的 实验方案
项
向两支试管中各加入 溶液,分别放入盛
温度对化学反应速
A 有冷水和热水的两个烧杯中,再同时分别向两支试管中加入
率的影响
溶液,振荡,观察现象
能否催化 向 溶液中滴加几滴 溶液,观察气泡产生情
B
分解 况
铁片上发生了吸氧 在一块除去铁锈的铁片上滴1滴含有酚酞的食盐水,静置
C
腐蚀 2~3min,溶液边缘出现红色
与 的反应 向 溶液中滴加 的 溶液振
D
是可逆反应 荡,再滴加1~2滴 溶液,观察现象
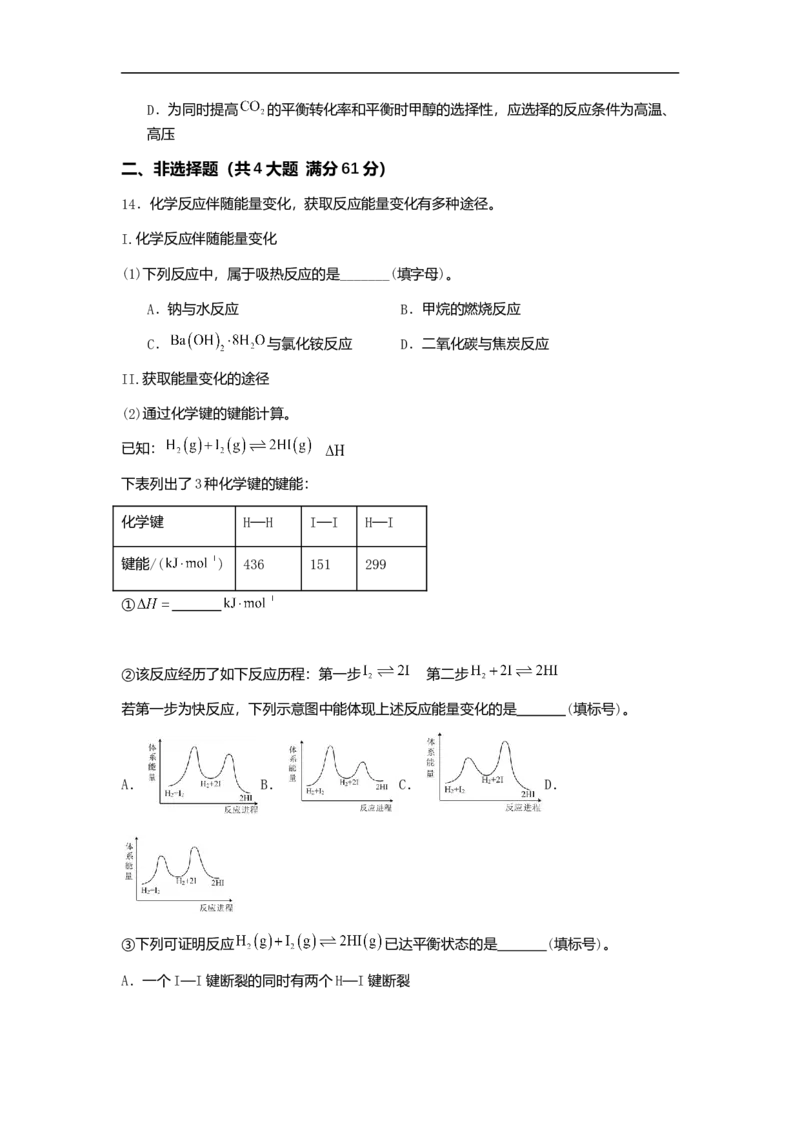
12.钴及其化合物在工业上有广泛应用。一种从湿法炼锌产生的废渣(主要含 、 、
、 的单质或氧化物)中富集回收得到含锰高钴成品的工艺如下:下列说法错误的是
A.“滤渣1”中含有的金属元素主要为
B.取少量“过滤2”后的溶液中加入 试剂,若出现蓝色沉淀,需补加
C.“氧化沉钴”中氧化剂与还原剂物质的量之比一定为
D.“除钴液”中主要的盐有 、
13.工业上用 和 合成甲醇涉及以下反应:
I.
II.
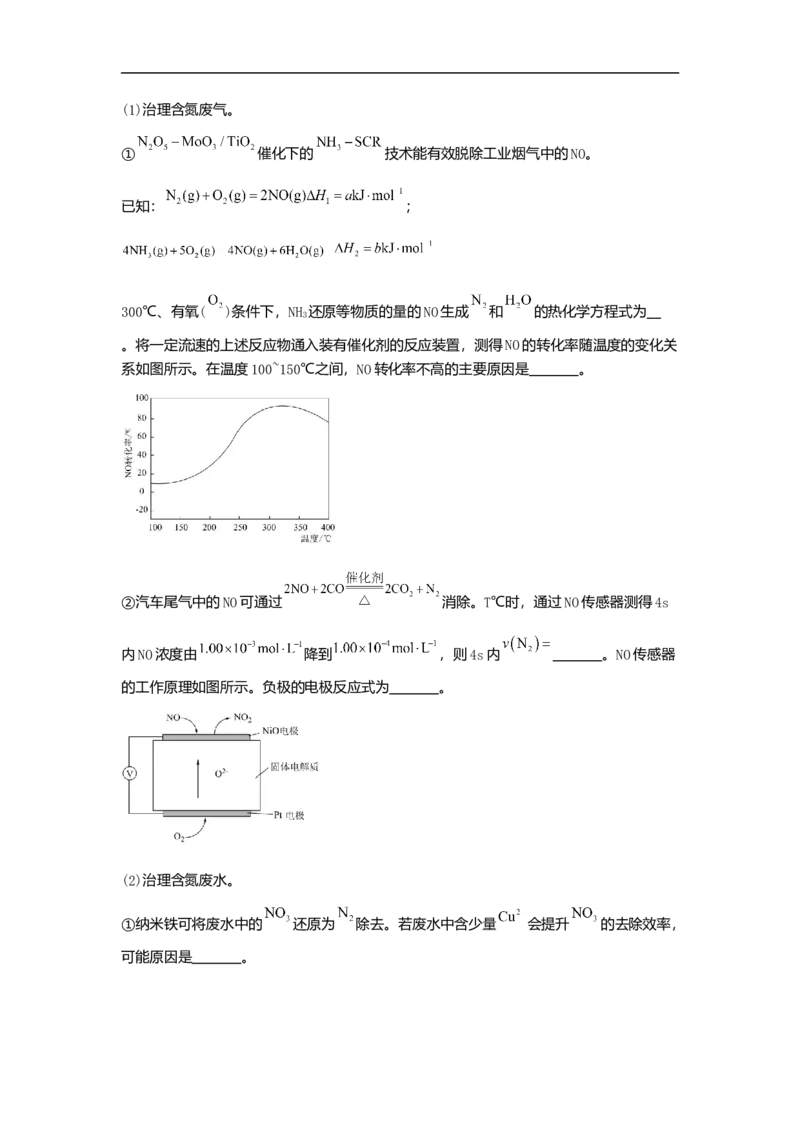
在催化剂作用下,将 和 的混合气体充入一恒容密闭容器中进行反应,达
到平衡时, 的转化率和容器中混合气体的平均相对分子质量随温度变化如图。下列判
断合理的是
已知:平衡时甲醇的选择性为生成甲醇消耗的 在 总消耗量中占比。
A. ,
B.250℃前以反应Ⅱ为主
C. ,平衡时甲醇的选择性为60%
高二化学试题 第6页 共3页D.为同时提高 的平衡转化率和平衡时甲醇的选择性,应选择的反应条件为高温、
高压
二、非选择题(共4大题 满分61分)
14.化学反应伴随能量变化,获取反应能量变化有多种途径。
I.化学反应伴随能量变化
(1)下列反应中,属于吸热反应的是_______(填字母)。
A.钠与水反应 B.甲烷的燃烧反应
C. 与氯化铵反应 D.二氧化碳与焦炭反应
II.获取能量变化的途径
(2)通过化学键的键能计算。
已知:
下表列出了3种化学键的键能:
化学键 H—H I—I H—I
键能/( ) 436 151 299
①
②该反应经历了如下反应历程:第一步 第二步
若第一步为快反应,下列示意图中能体现上述反应能量变化的是 (填标号)。
A. B. C. D.
③下列可证明反应 已达平衡状态的是 (填标号)。
A.一个I—I键断裂的同时有两个H—I键断裂B.反应速率
C.温度和体积一定时,混合气体颜色不再变化
D.条件一定时,混合气体的平均相对分子质量不再变化
(3)通过盖斯定律可计算。
甲醇既是重要的化工原料,又可作为燃料。利用合成气(主要成分为CO、 和 )在催
化剂作用下可合成甲醇,发生的主要反应如下
i.
ii.
iii.
。
(4)将2.0mol 和3.0mol 通入容积为3L的恒容密闭容器中,在一定条件下发生反应
ii,测得 的平衡转化率与温度的关系如图所示。
①100℃时反应ii达到平衡所需的时间为5min,则反应从起始至5min内,用 表示该反
应的平均反应速率为 。
②100℃时,反应ii的平衡常数K= 。
③已知:反应ii的瞬时速率表达式为 , (k
为速率常数,只与温度有关)]。温度由100℃升高到300℃,活化分子百分数 (填“增
大”“减小”或“不变”)。300℃时, (填“大于”“小于”或“等
于”)K(100℃)。
15.研究治理含氮化合物对空气、水源的污染问题,对保护环境有重要意义。
高二化学试题 第8页 共3页(1)治理含氮废气。
① 催化下的 技术能有效脱除工业烟气中的NO。
已知: ;
300℃、有氧( )条件下,NH 还原等物质的量的NO生成 和 的热化学方程式为
3
。将一定流速的上述反应物通入装有催化剂的反应装置,测得NO的转化率随温度的变化关
系如图所示。在温度100~150℃之间,NO转化率不高的主要原因是 。
②汽车尾气中的NO可通过 消除。T℃时,通过NO传感器测得4s
内NO浓度由 降到 ,则4s内 。NO传感器
的工作原理如图所示。负极的电极反应式为 。
(2)治理含氮废水。
①纳米铁可将废水中的 还原为 除去。若废水中含少量 会提升 的去除效率,
可能原因是 。②电解法可去除废水中的氨氮( 或 )。用惰性电极电解含 、NaCl
的溶液模拟工业去除氨氮,电解过程中生成的 能将 氧化为 。若电解液的初始
过大,则电解后 明显降低,但溶液中氮元素浓度变化不大,其原因是
。
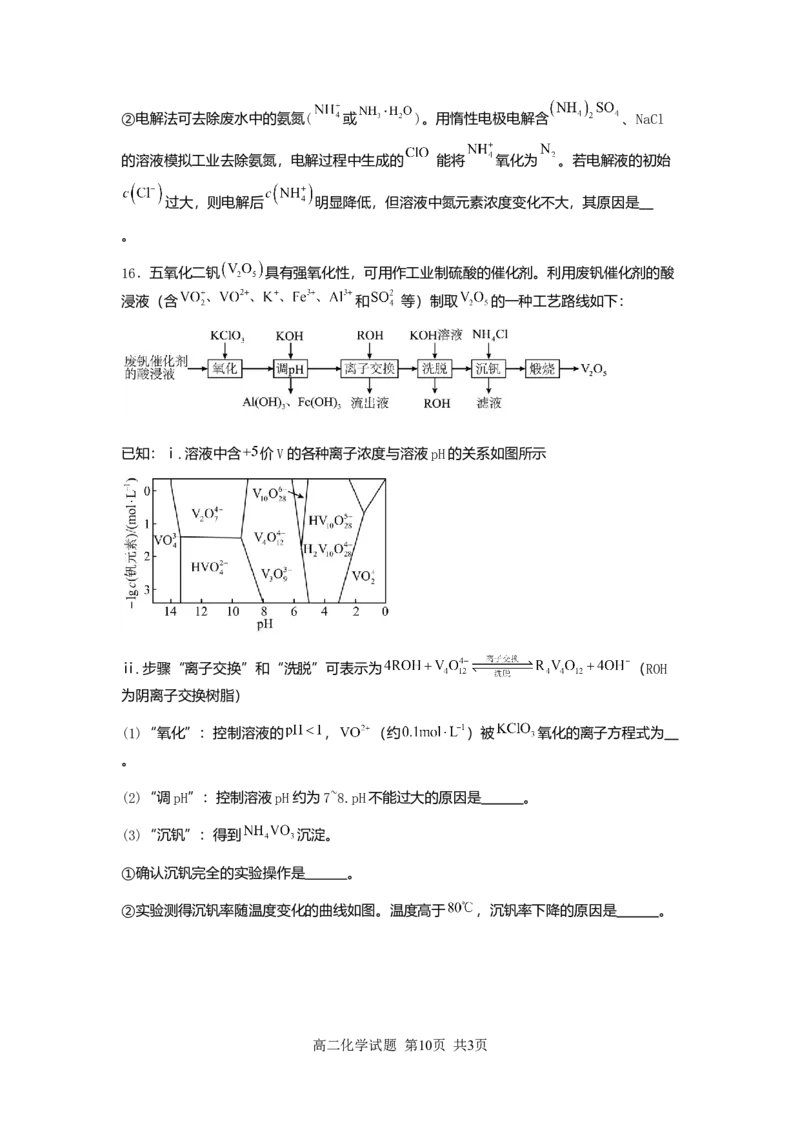
16.五氧化二钒 具有强氧化性,可用作工业制硫酸的催化剂。利用废钒催化剂的酸
浸液(含 和 等)制取 的一种工艺路线如下:
已知:ⅰ.溶液中含 价V的各种离子浓度与溶液pH的关系如图所示
ⅱ.步骤“离子交换”和“洗脱”可表示为 (ROH
为阴离子交换树脂)
(1)“氧化”:控制溶液的 , (约 )被 氧化的离子方程式为
。
(2)“调pH”:控制溶液pH约为7~8.pH不能过大的原因是 。
(3)“沉钒”:得到 沉淀。
①确认沉钒完全的实验操作是 。
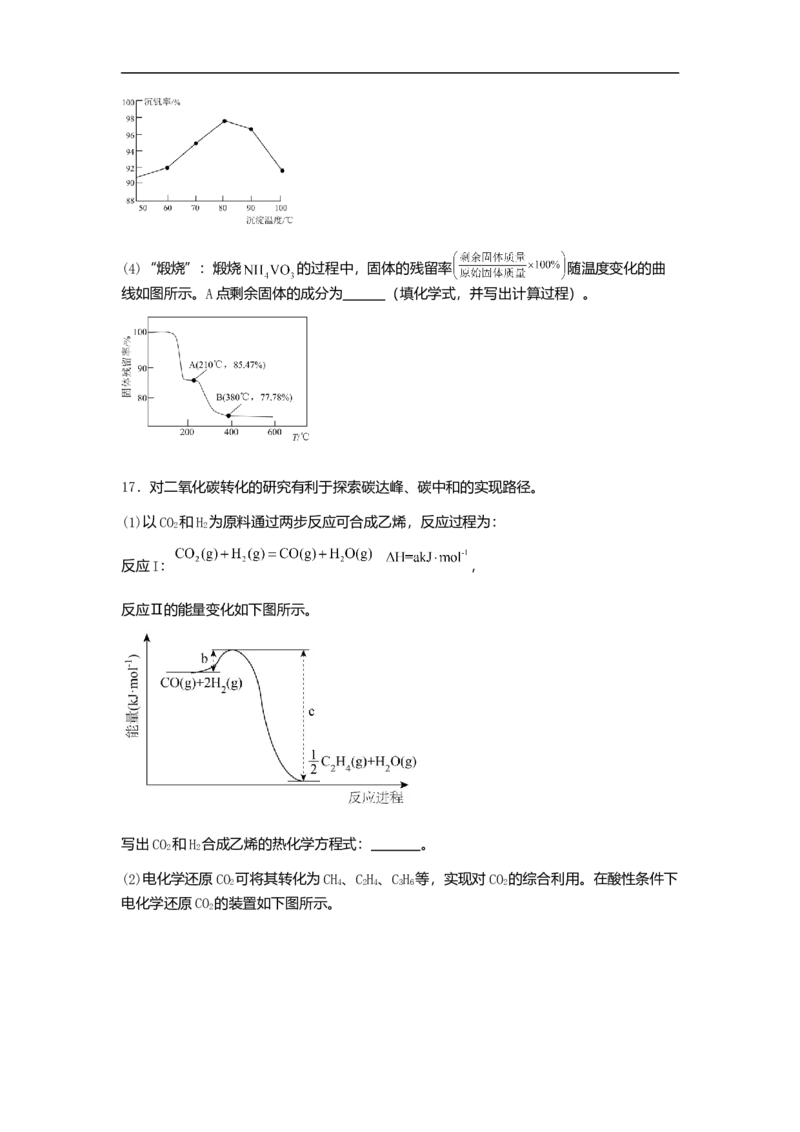
②实验测得沉钒率随温度变化的曲线如图。温度高于 ,沉钒率下降的原因是 。
高二化学试题 第10页 共3页(4)“煅烧”:煅烧 的过程中,固体的残留率 随温度变化的曲
线如图所示。A点剩余固体的成分为 (填化学式,并写出计算过程)。
17.对二氧化碳转化的研究有利于探索碳达峰、碳中和的实现路径。
(1)以CO 和H 为原料通过两步反应可合成乙烯,反应过程为:
2 2
反应I: ,
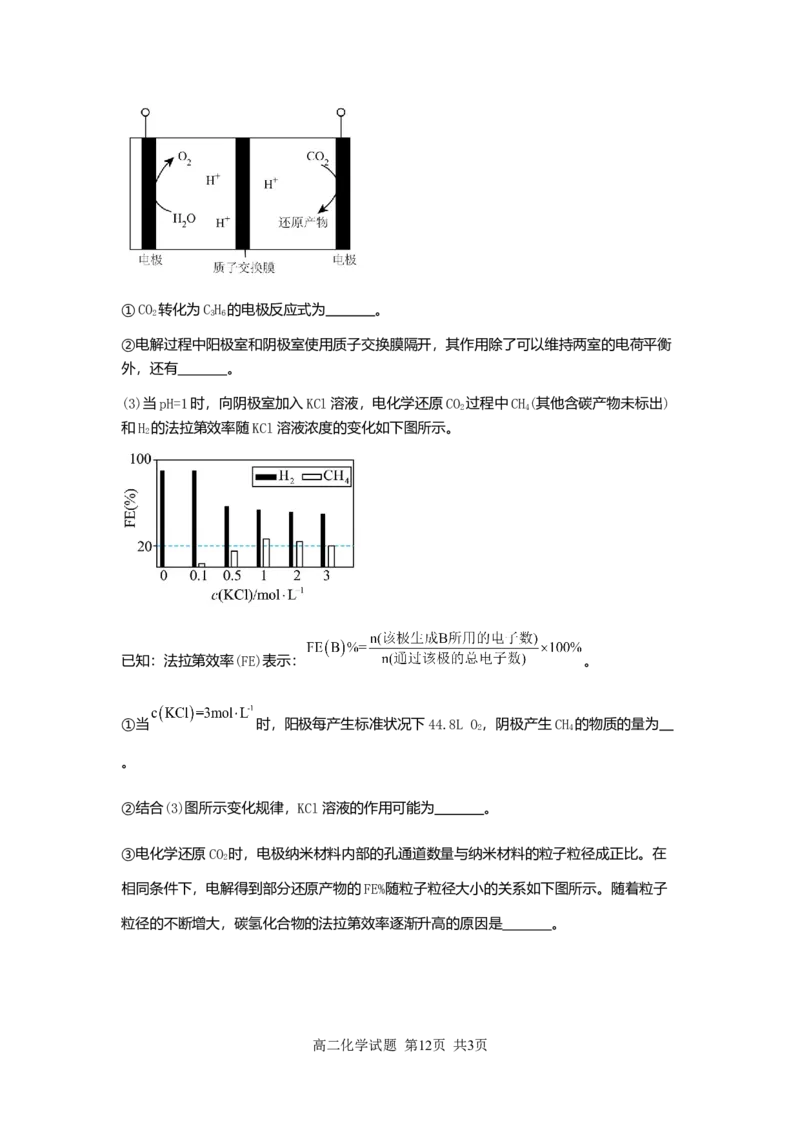
反应Ⅱ的能量变化如下图所示。
写出CO 和H 合成乙烯的热化学方程式: 。
2 2
(2)电化学还原CO 可将其转化为CH、CH、CH 等,实现对CO 的综合利用。在酸性条件下
2 4 2 4 3 6 2
电化学还原CO 的装置如下图所示。
2①CO 转化为CH 的电极反应式为 。
2 3 6
②电解过程中阳极室和阴极室使用质子交换膜隔开,其作用除了可以维持两室的电荷平衡
外,还有 。
(3)当pH=1时,向阴极室加入KCl溶液,电化学还原CO 过程中CH(其他含碳产物未标出)
2 4
和H 的法拉第效率随KCl溶液浓度的变化如下图所示。
2
已知:法拉第效率(FE)表示: 。
①当 时,阳极每产生标准状况下44.8L O,阴极产生CH 的物质的量为
2 4
。
②结合(3)图所示变化规律,KCl溶液的作用可能为 。
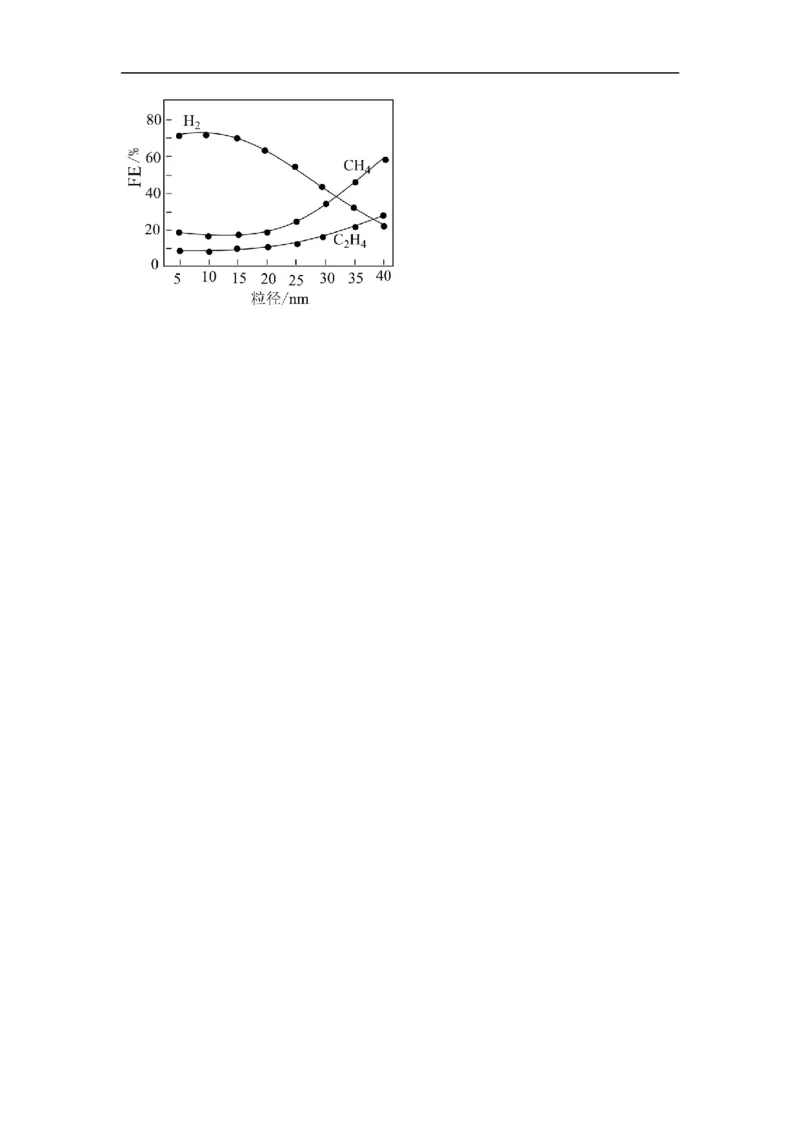
③电化学还原CO 时,电极纳米材料内部的孔通道数量与纳米材料的粒子粒径成正比。在
2
相同条件下,电解得到部分还原产物的FE%随粒子粒径大小的关系如下图所示。随着粒子
粒径的不断增大,碳氢化合物的法拉第效率逐渐升高的原因是 。
高二化学试题 第12页 共3页