文档内容
玉溪一中 2024—2025 学年下学期高二年级期中考
化学学科试卷
总分:100分,考试时间:75分钟 命题人:李娇 段翠红 审题人:梁兵
可能用到的相对原子质量:H-1 C-12 O-16 N-14 Na-23 P-31 S-32 Cu-64 Hg-201
一、单项选择题:本题共14小题,每小题3分,共42分,在每小题给出的四个选项中,只有一
个选项是正确的。
1.劳动有利于“知行合一”。下列对劳动项目的有关解释合理的是( )
A.船厂研学:轮船船体镶嵌镁合金,只与镁的导电性有关
B.农业劳动:石膏改良盐碱土壤,与硫酸钙溶液显酸性有关
C.水厂帮工:明矾净化生活用水,与明矾具有氧化性有关
D.家务劳动:食醋清除水壶中的少量水垢,与醋酸和碳酸的酸性有关
2.N 为阿伏加德罗常数的值。下列说法正确的是( )
A
A.27g HCN 分子中含有σ 键数目为 N
A
B.1mol K[Fe(CN) ] 的中心离子的配位键数目为6 N
3 6 A
C.常温常压下,1mol甲苯含碳碳双键的数目为3N
A
D.在粗铜精炼中,阳极减少64g时理论上转移电子数为2N
A
3.下列化学用语正确的是( )
A.铜原子( )的电子排布式:1s22s22p63s23p63d94s2
B.轨道表示式: 违背了泡利原理
C.NH Cl电子式为
4
D.二氧化硅的分子式为SiO
2
4.下列化学方程式或离子方程式书写正确的是( )
A.金属锂在 中加热
B.能证明亚硫酸酸性强于次氯酸的离子方程式:
C.含氟牙膏防治龋齿:
第 1 页 共 9 页D.用石灰乳除去工业尾气中的
5.下列说法正确的是( )
A.键线式为 的物质的名称:2,2,4-三甲基戊烷
B.C H 只有3种属于芳香烃的同分异构体
8 10
C.乙烯分子中碳原子杂化轨道示意图:
D.空间填充模型 可以表示甲烷分子或四氯化碳分子
6.下列关于有机物分离提纯所用试剂和方法有不正确的是(括号中物质为少量杂质)( )
选项 混合物 试剂 分离提纯的方法
A 甲烷(乙烯) 酸性KMnO 溶液 洗气
4
B 乙醇(水) CaO 蒸馏
C 粗苯甲酸 水 重结晶
D 溴苯(Br) NaOH溶液 分液
2
A.A B.B C.C D.D
7.《哪吒2之魔童闹海》中太乙真人使用藕粉为哪吒和敖丙重塑肉身。尼克酸是藕的主要成分
之一,其结构如图所示 ( 与苯环相似)。下列说法错误的是( )
A.尼克酸能与NaHCO 反应产生CO B.尼克酸的分子式为C HNO
3 2 6 5 2
C.尼克酸能发生取代、加成和氧化反应 D.尼克酸分子中碳原子有两种杂化方式
8.下列分子中属于既含有极性键和又含有非极性键的非极性分子的是( )
A.BF B.C H C.COCl D.HO
3 2 4 2 2 2
9.A、B、C、D、E是原子序数依次增大的短周期主族元素。基态A原子L层的电子有两种不
同的空间运动状态;基态 原子的未成对电子在同周期中数目最多;与 同周期的元素中,第
一电离能大于 的只有一种; 与 同主族。下列说法错误的是( )
A.电负性:D>C>B
B.简单氢化物的熔沸点:D>C>B
C.ECl 为离子晶体,熔融状态下可以导电
3
D.AD -中,中心原子最外层满足8电子稳定结构
4
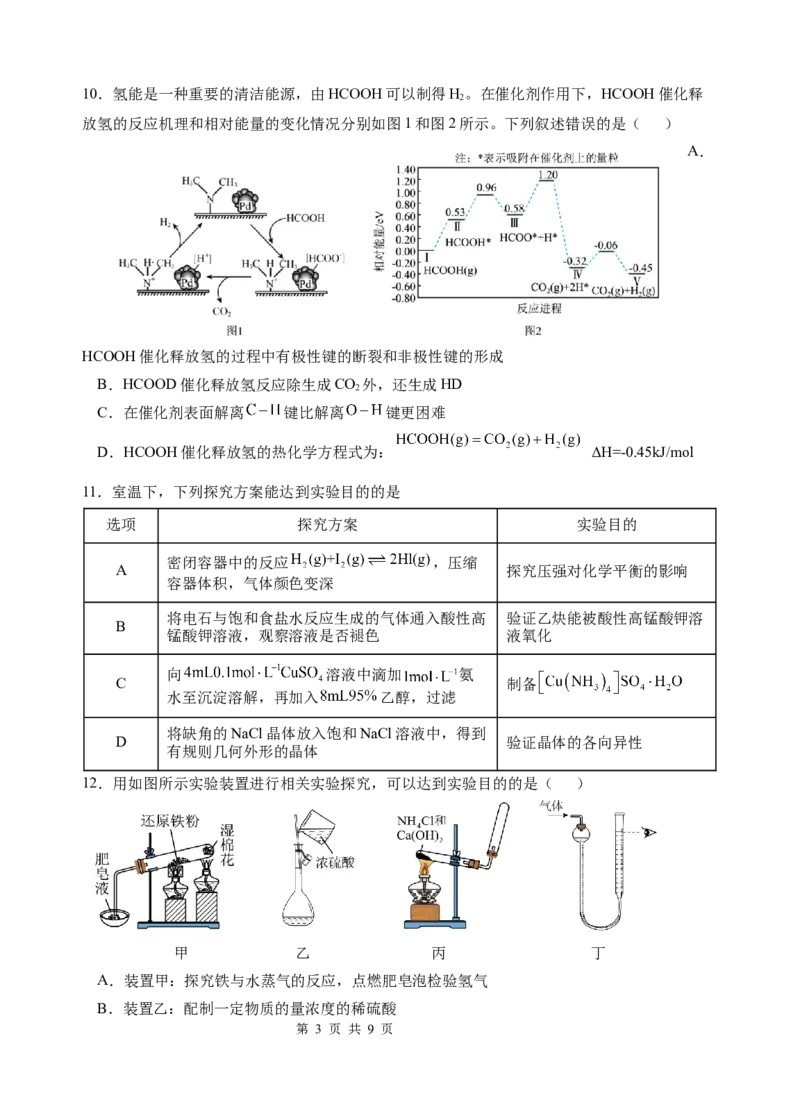
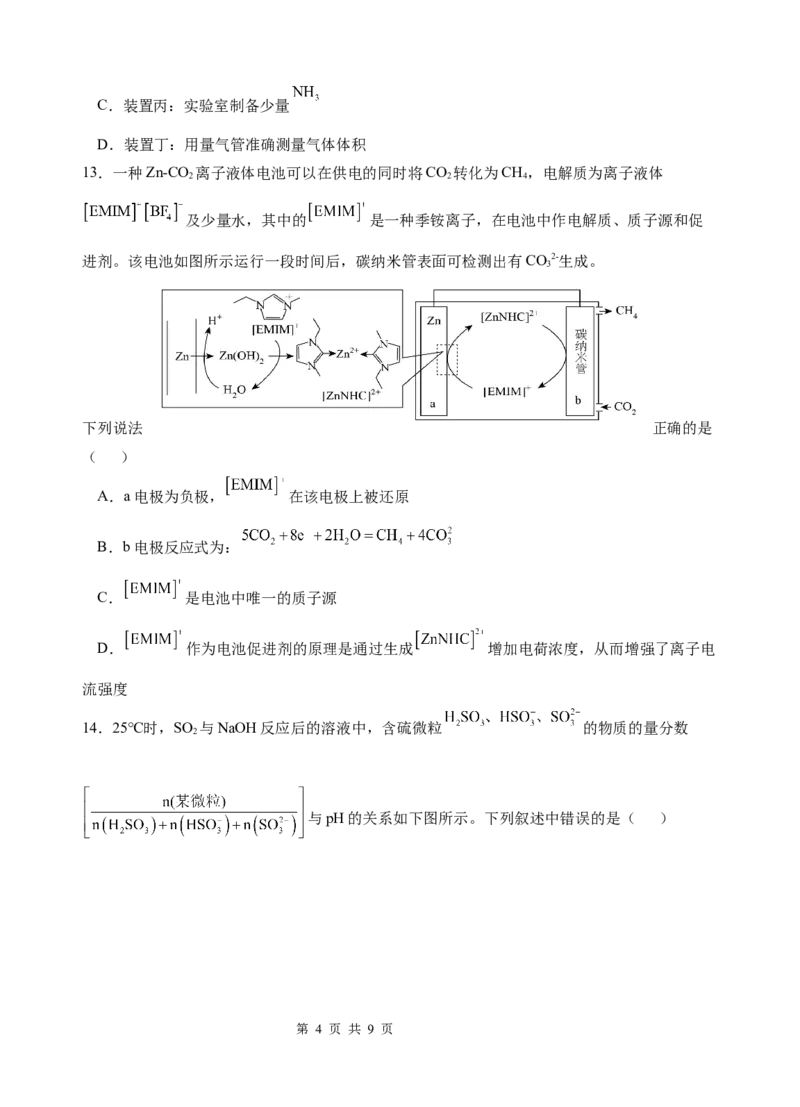
第 2 页 共 9 页10.氢能是一种重要的清洁能源,由HCOOH可以制得H。在催化剂作用下,HCOOH催化释
2
放氢的反应机理和相对能量的变化情况分别如图1和图2所示。下列叙述错误的是( )
A.
HCOOH催化释放氢的过程中有极性键的断裂和非极性键的形成
B.HCOOD催化释放氢反应除生成CO 外,还生成HD
2
C.在催化剂表面解离 键比解离 键更困难
D.HCOOH催化释放氢的热化学方程式为: ΔH=-0.45kJ/mol
11.室温下,下列探究方案能达到实验目的的是
选项 探究方案 实验目的
密闭容器中的反应 ,压缩
A 探究压强对化学平衡的影响
容器体积,气体颜色变深
将电石与饱和食盐水反应生成的气体通入酸性高 验证乙炔能被酸性高锰酸钾溶
B
锰酸钾溶液,观察溶液是否褪色 液氧化
向 溶液中滴加 氨
C 制备
水至沉淀溶解,再加入 乙醇,过滤
将缺角的NaCl晶体放入饱和NaCl溶液中,得到
D 验证晶体的各向异性
有规则几何外形的晶体
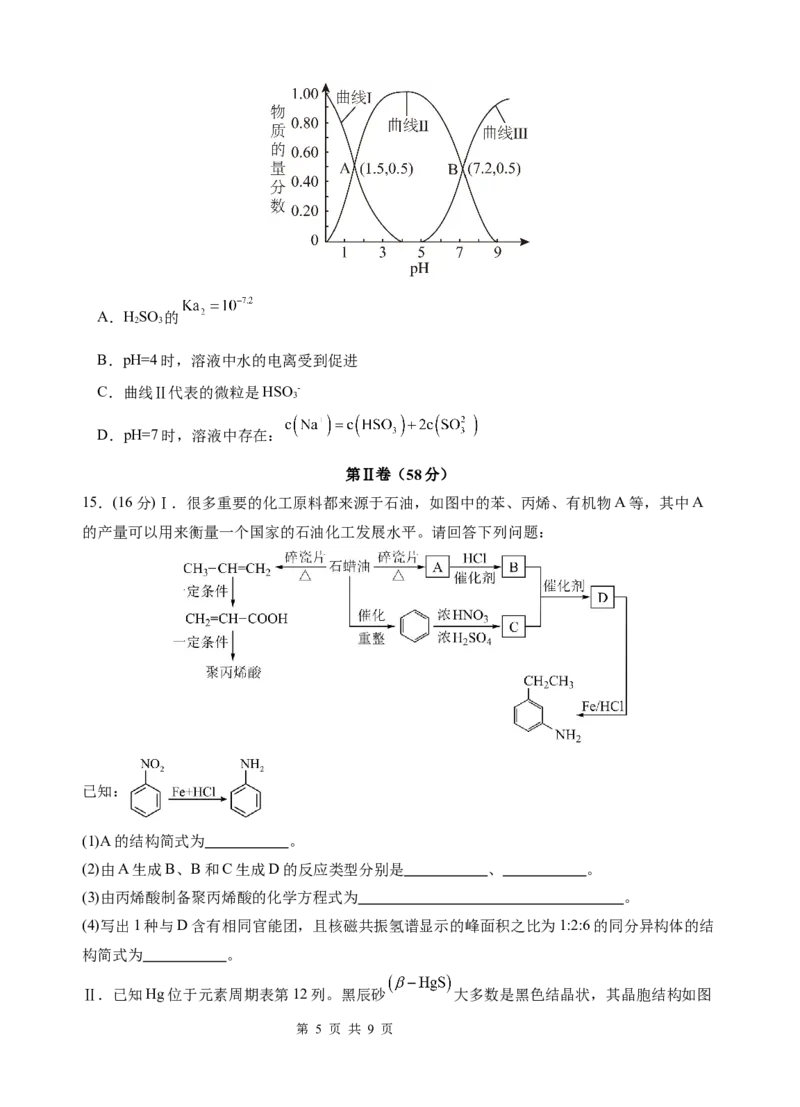
12.用如图所示实验装置进行相关实验探究,可以达到实验目的的是( )
甲 乙 丙 丁
A.装置甲:探究铁与水蒸气的反应,点燃肥皂泡检验氢气
B.装置乙:配制一定物质的量浓度的稀硫酸
第 3 页 共 9 页C.装置丙:实验室制备少量
D.装置丁:用量气管准确测量气体体积
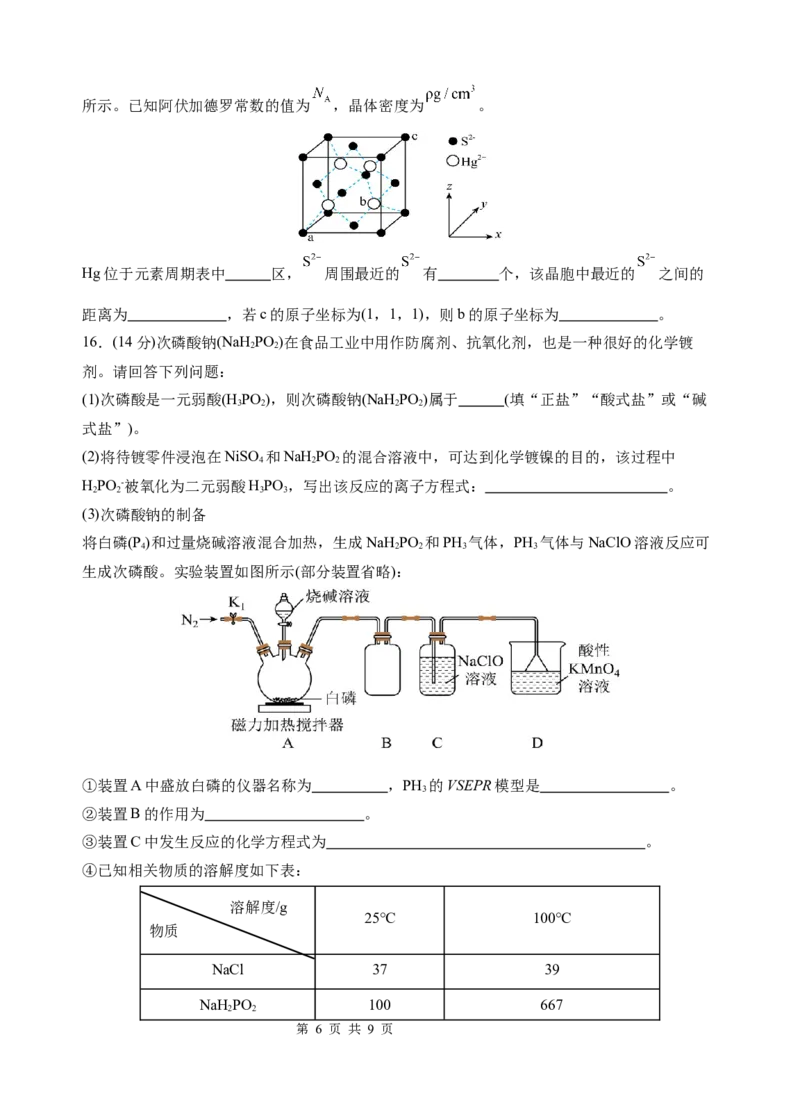
13.一种Zn-CO 离子液体电池可以在供电的同时将CO 转化为CH,电解质为离子液体
2 2 4
及少量水,其中的 是一种季铵离子,在电池中作电解质、质子源和促
进剂。该电池如图所示运行一段时间后,碳纳米管表面可检测出有CO2-生成。
3
下列说法 正确的是
( )
A.a电极为负极, 在该电极上被还原
B.b电极反应式为:
C. 是电池中唯一的质子源
D. 作为电池促进剂的原理是通过生成 增加电荷浓度,从而增强了离子电
流强度
14.25℃时,SO 与NaOH反应后的溶液中,含硫微粒 的物质的量分数
2
与pH的关系如下图所示。下列叙述中错误的是( )
第 4 页 共 9 页A.HSO 的
2 3
B.pH=4时,溶液中水的电离受到促进
C.曲线Ⅱ代表的微粒是HSO -
3
D.pH=7时,溶液中存在:
第Ⅱ卷(58分)
15.(16分)Ⅰ.很多重要的化工原料都来源于石油,如图中的苯、丙烯、有机物A等,其中A
的产量可以用来衡量一个国家的石油化工发展水平。请回答下列问题:
已知:
(1)A的结构简式为 。
(2)由A生成B、B和C生成D的反应类型分别是 、 。
(3)由丙烯酸制备聚丙烯酸的化学方程式为 。
(4)写出1种与D含有相同官能团,且核磁共振氢谱显示的峰面积之比为1:2:6的同分异构体的结
构简式为 。
Ⅱ.已知Hg位于元素周期表第12列。黑辰砂 大多数是黑色结晶状,其晶胞结构如图
第 5 页 共 9 页所示。已知阿伏加德罗常数的值为 ,晶体密度为 。
Hg位于元素周期表中 区, 周围最近的 有 个,该晶胞中最近的 之间的
距离为 ,若c的原子坐标为(1,1,1),则b的原子坐标为 。
16.(14分)次磷酸钠(NaH PO )在食品工业中用作防腐剂、抗氧化剂,也是一种很好的化学镀
2 2
剂。请回答下列问题:
(1)次磷酸是一元弱酸(HPO ),则次磷酸钠(NaH PO )属于 (填“正盐”“酸式盐”或“碱
3 2 2 2
式盐”)。
(2)将待镀零件浸泡在NiSO 和NaH PO 的混合溶液中,可达到化学镀镍的目的,该过程中
4 2 2
HPO -被氧化为二元弱酸HPO ,写出该反应的离子方程式: 。
2 2 3 3
(3)次磷酸钠的制备
将白磷(P)和过量烧碱溶液混合加热,生成NaH PO 和PH 气体,PH 气体与NaClO溶液反应可
4 2 2 3 3
生成次磷酸。实验装置如图所示(部分装置省略):
①装置A中盛放白磷的仪器名称为 ,PH 的VSEPR模型是 。
3
②装置B的作用为 。
③装置C中发生反应的化学方程式为 。
④已知相关物质的溶解度如下表:
溶解度/g
25℃ 100℃
物质
NaCl 37 39
NaH PO 100 667
2 2
第 6 页 共 9 页充分反应后,将A、C中溶液混合,将混合液(含极少量NaOH)蒸发浓缩,有大量杂质晶体析
出,然后 ,得到含NaH PO 的粗产品溶液,进一步处理得到粗产品。
2 2
(4)产品纯度的计算
取1.00g粗产品配成100mL溶液,取25.00mL于锥形瓶中,酸化后加入30.00ml 0.1mol/L碘
水,充分反应,然后以淀粉溶液作指示剂,用0.100mol/L NaSO 溶液滴定至终点,消耗
2 2 3
NaSO 溶液10.00mL,相关反应的方程式为 、
2 2 3
,则产品纯度为 。
17.(14分)钕铁硼废料中一般含有30%的稀土元素和少量的钴、锰、镍等金属。稀土元素经萃
取分离后萃余液化学成分有Ca2+、Mg2+、Co2+、Mn2+、Ni2+、Fe3+,从萃余液中回收氧化钴的工艺
流程如下:
已知:常温时相关物质的溶度积
化学式
回答下列问题:
(1)Co元素在周期表中的位置 ,Co2+价层电子的电子排布图为
。
(2)已知“滤液1”中 ,则滤液1中 的浓度为 。
(3)已知“滤渣”的主要成分为S,写出“酸分解”时 发生反应的离子方程式
。
第 7 页 共 9 页(4)反萃取的目的是 。
(5)“沉钴”后需将沉淀洗净,检验沉淀已洗净的方法是
。
(6)“煅烧”可在纯氩气中进行,写出煅烧反应的化学方程式
。
18.(14分)丙烯是一种重要的化工原料,工业上常用丙烷无氧脱氢制备丙烯:
。
(1)已知几种共价键键能如下表所示:
共价键
键能 a b c d
。
(2)一定温度下,向5L恒容密闭容器中充入2 C H 发生反应,测得平衡时气体压强是开始时
3 8
的1.75倍。
①下列能说明该反应达到平衡状态的是 (填字母)。
A. 分解速率与 生成速率相等 B. 保持不变
C. D.混合气的平均摩尔质量保持不变
②C H 的平衡转化率为 。
3 8
(3) 若在恒温、恒压的密闭容器中充入丙烷和氩气发生脱氢反应,起始n(氩气)/n(丙烷)越大,丙
烷的平衡转化率 (填“增大”“减小”或“不变”)
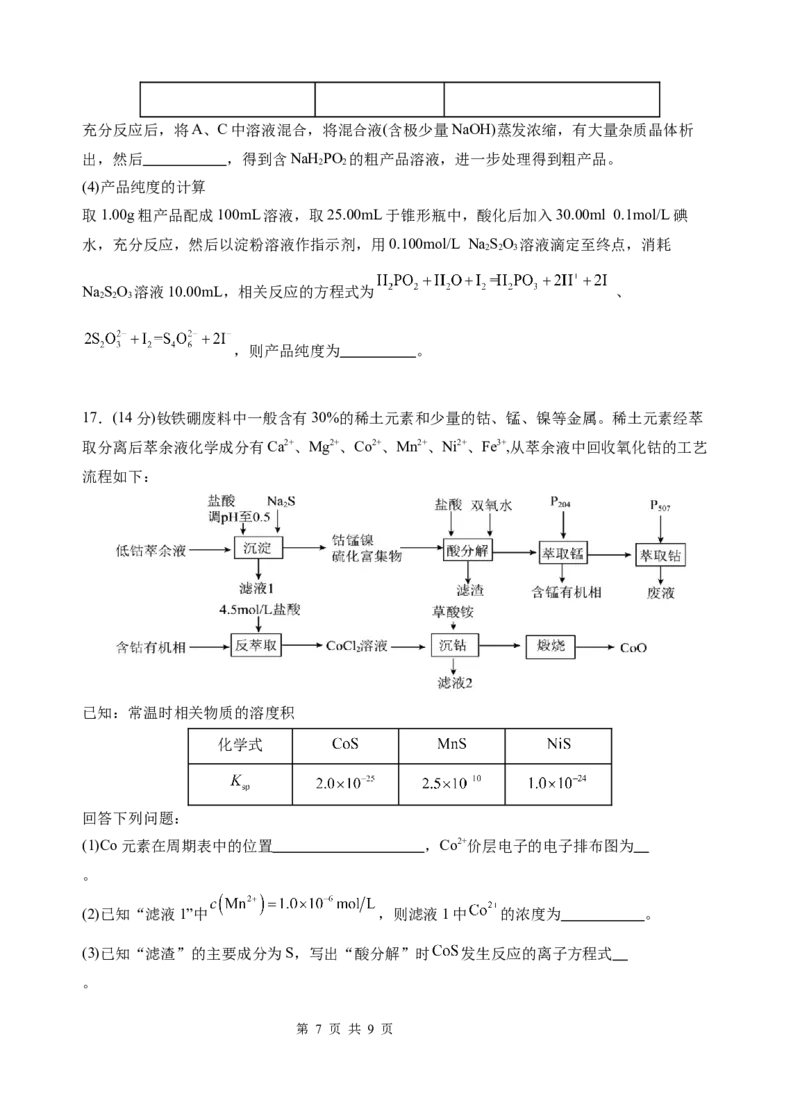
(4)总压强分别为P、P 时,上述反应在不同温度下达到平衡,测得丙烷和丙烯的物质的量分数
1 2
分别如图所示:压强:P P(填“>”或“<”)。
1 2
第 8 页 共 9 页在压强P 条件下,起始时充入一定量丙烷发生反应,计算Q点对应温度下该反应的压强平衡常
1
数Kp= (用P 表示)。(用各气体的平衡分压代替其物质的量浓度计算,可表示压
1
强平衡常数,分压=总压×物质的量分数)
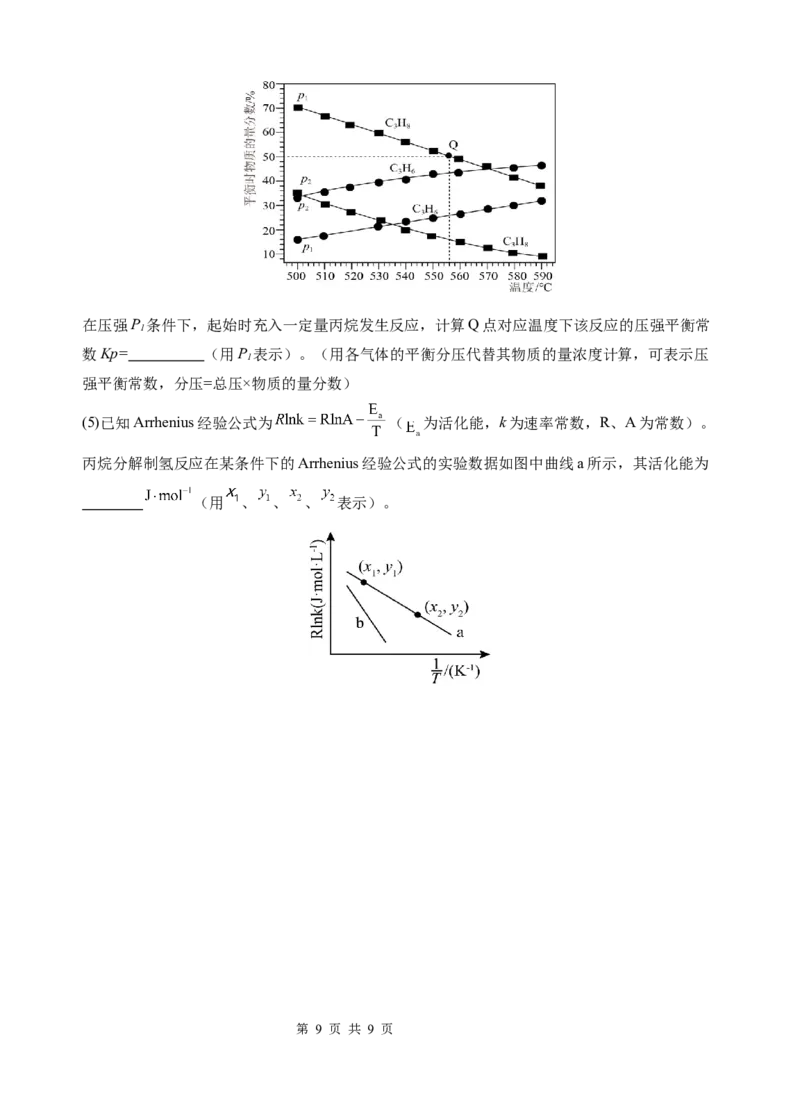
(5)已知Arrhenius经验公式为 ( 为活化能,k为速率常数,R、A为常数)。
丙烷分解制氢反应在某条件下的Arrhenius经验公式的实验数据如图中曲线a所示,其活化能为
(用 、 、 、 表示)。
第 9 页 共 9 页