文档内容
密
封
学 号 线 : 白银市第八中学2025届高三1月阶段性考试试卷 D. 溶液中滴加足量 溶液:
年 级 :
考生答题
班 级 :
不得超过
科目:高三化学 命题人:梁鹏业
姓 名 :
此密封线
考场:
一、单选题(每题3分,共14题,共42分.在给出的四个选项中,只有一个是符合题目要求
的.)
4.(本题3分)下列化学用语表述正确的是( )
1.(本题3分)高速铁路、量子计算机、移动支付、共享单车被称为中国新“四大发明”,
下列说法正确的是( )
A.激发态氮原子轨道表示式:
B.氢化钙的电子式:
A B C D C. 的VSEPR模型:
A.高铁列车的受电弓和接触导线之间涂抹石墨主要是利用了石墨的润滑性和导电性
B.量子计算机计算精度高、能力强,其芯片主要材质是
D. 形成 键的过程:
C.手机保护壳通常是纳米硅胶材料,优点是防滑抗震性好,硅胶还常用作食品抗氧化剂
D.共享单车用到的聚四氟乙烯材料含有 键和 键,能使溴水褪色 5.(本题3分) 的 溶液称为奈斯勒(Nessler)试剂,其制备流程及特色反应如图
2.(本题3分)天然方沸石是一种含有结晶水的盐,其分子式为 。其中 、 所示。
、 和 为短周期元素,且原子序数依次增大。 的某种单质可滤除大气中的大量紫外线,
保护地球生物, 的第一电离能小于元素周期表中与之紧邻的左侧元素,基态 原子未成对电
子数为2个,其单质及氧化物均为常见的共价晶体。下列说法正确的是( )
下列说法错误的是( )
A. 位于元素周期表的 区 B.电负性:
A.反应①的离子方程式为:
C.简单离子半径: D.W的氧化物具有两性
3.(本题3分)下列各情境中对应的方程式正确的是( )
B.由反应②可知,用 溶液可除去 中的
A.利用酸性重铬酸钾溶液检测酒驾:
C.反应③中消耗的 和 的物质的量之比为1:4
B.甲烷和 在光照条件下发生反应:
D.可用奈斯勒试剂检验 中微量的
C.泡沫灭火器灭火原理:
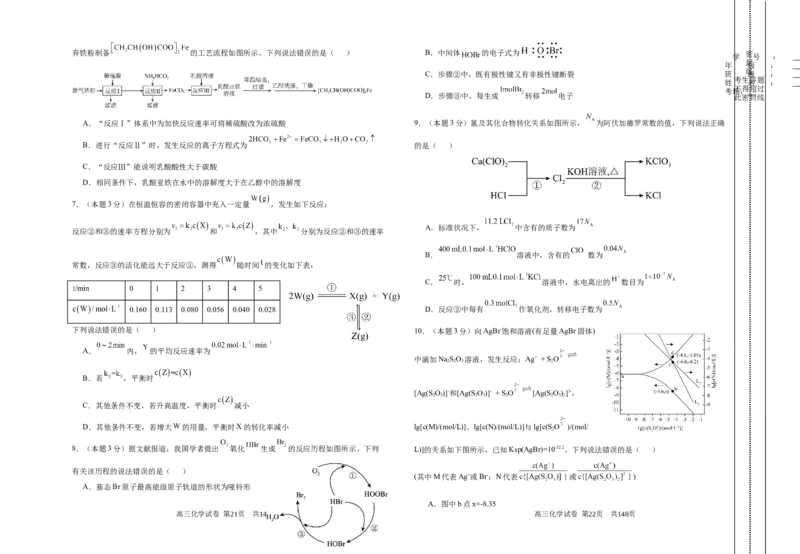
6.(本题3分)乳酸亚铁是一种常用的食品添加剂和营养强化剂。学习小组在实验室中由废
高三化学试卷 第11页 共148页 高三化学试卷 第12页 共148页
学科网(北京)股份有限公司弃铁粉制备 的工艺流程如图所示。下列说法错误的是( ) B.中间体 的电子式为 密
学 号 :
封
年 级 :
线
C.步骤②中,既有极性键又有非极性键断裂 班 级 :
考生答题
姓 名 :
不得超过
考场:
D.步骤③中,每生成 转移 电子 此密封线
A.“反应Ⅰ”体系中为加快反应速率可将稀硫酸改为浓硫酸 9.(本题3分)氯及其化合物转化关系如图所示, 为阿伏加德罗常数的值,下列说法正确
B.进行“反应Ⅱ”时,发生反应的离子方程式为 的是( )
C.“反应Ⅲ”能说明乳酸酸性大于碳酸
D.相同条件下,乳酸亚铁在水中的溶解度大于在乙醇中的溶解度
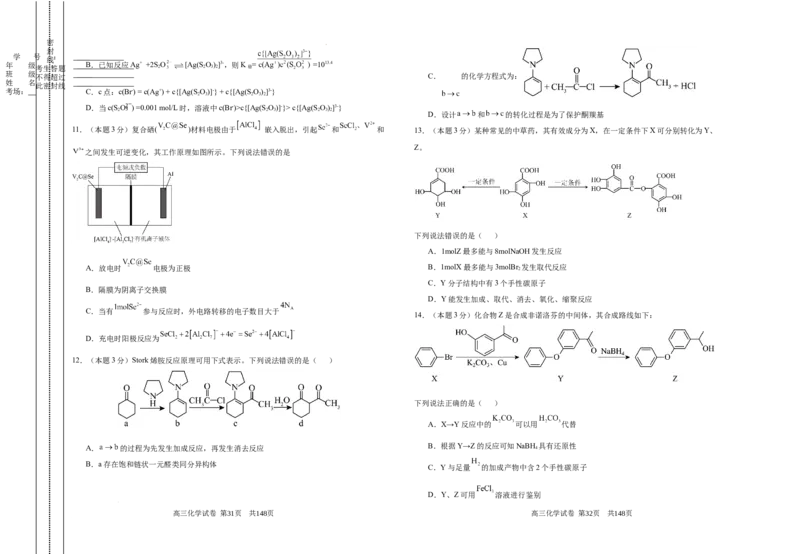
7.(本题3分)在恒温恒容的密闭容器中充入一定量 ,发生如下反应:
A.标准状况下, 中含有的质子数为
反应②和③的速率方程分别为 和 ,其中 分别为反应②和③的速率
B. 溶液中,含有的 数为
常数,反应③的活化能远大于反应②,测得 随时间 的变化如下表:
C. 时, 溶液中,水电离出的 数目为
0 1 2 3 4 5
0.160 0.113 0.080 0.056 0.040 0.028 D.反应②中每有 作氧化剂,转移电子数为
下列说法错误的是( ) 10.(本题3分)向AgBr饱和溶液(有足量AgBr固体)
A. 内, 的平均反应速率为
中滴加NaSO 溶液,发生反应:Ag+ + S O
2 2 3 2
B.若 ,平衡时
[Ag(S O)]-和[Ag(S O)]- + S O [Ag(S O)]3-,
2 3 2 3 2 2 3 2
C.其他条件不变,若升高温度,平衡时 减小
D.其他条件不变,若增大 的用量,平衡时 的转化率减小 lg[c(M)/(mol/L)]、lg[c(N)/(mol/L)]与lg[c(S O )/(mol/
2
8.(本题3分)据文献报道,我国学者提出 氧化 生成 的反应历程如图所示。下列 L)]的关系如下图所示,已知Ksp(AgBr)=10-12.2。下列说法错误的是( )
有关该历程的说法错误的是( )
(其中M代表Ag+或Br-;N代表 或 )
A.基态Br原子最高能级原子轨道的形状为哑铃形
A.图中b点x=-8.35
高三化学试卷 第21页 共148页 高三化学试卷 第22页 共148页密
封
学 号 :
线
年 级 : B.已知反 应Ag+ +2S O [Ag(S O)]3-,则K = =1013.4
考生答题 2 2 3 2 稳
班 级 :
不得超过 C. 的化学方程式为:
姓 名 :
此密封线
考场: C.c点:c(Br-) = c(Ag+) + c{[Ag(S O)]-} + c{[Ag(S O)]3-}
2 3 2 3 2
D.当c(SO ) =0.001 mol/L时,溶液中c(Br-)>c{[Ag(S O)]-}> c{[Ag(S O)]3-}
2 2 3 2 3 2
D.设计 和 的转化过程是为了保护酮羰基
11.(本题3分)复合硒( )材料电极由于 嵌入脱出,引起 和 和 13.(本题3分)某种常见的中草药,其有效成分为X,在一定条件下X可分别转化为Y、
Z。
之间发生可逆变化,其工作原理如图所示。下列说法错误的是
下列说法错误的是( )
A.1molZ最多能与8molNaOH发生反应
A.放电时 电极为正极 B.1molX最多能与3molBr 发生取代反应
2
C.Y分子结构中有3个手性碳原子
B.隔膜为阴离子交换膜
D.Y能发生加成、取代、消去、氧化、缩聚反应
C.当有 参与反应时,外电路转移的电子数目大于
14.(本题3分)化合物Z是合成非诺洛芬的中间体,其合成路线如下:
D.充电时阳极反应为
12.(本题3分)Stork烯胺反应原理可用下式表示。下列说法错误的是( )
下列说法正确的是( )
A.X→Y反应中的 可以用 代替
B.根据Y→Z的反应可知NaBH 具有还原性
A. 的过程为先发生加成反应,再发生消去反应 4
B.a存在饱和链状一元醛类同分异构体
C.Y与足量 的加成产物中含2个手性碳原子
D.Y、Z可用 溶液进行鉴别
高三化学试卷 第31页 共148页 高三化学试卷 第32页 共148页
学科网(北京)股份有限公司二、解答题(共58分)
(3)“调节 ”时, 不能过高的原因是 。(2分) 密
学 号 :
15.(本题11分)一种利用炼锌渣(主要含 、一定量的 、不溶 年 封 级 :
线
班 级 :
(4)室温时, 考生答题
姓 名 :
性杂质)为原料制备硫化锌及高纯镓的流程如图所示: 不得超过
考场:
此密封线
。计算反应 的平衡常数
。
(5)直接电解“沉锌”后的溶液可制备镓,阴极的电极反应式为 。(2分)
已知:①电解制取镓时,溶液中的氯离子会影响镓的析出。 (6)在沉铁前可以加入铁氰化钾检验 是否被完全氧化,若 未被完全氧化,则会产生蓝色
② 。
的 沉淀,每个 晶胞含 个 。
③ 与 的各物种的分布分数随 的变化如图1所示。
16.(本题13分)利用物质的结构与性质进行研究,有助于我们更好地掌握知识。
④ 晶胞可以看成是由8个图2所示的小立方体堆积成大立方体以后, 占据四
(1)基态砷原子中,共有 种空间运动状态不同的电子。
个互不相邻的小立方体的体心得到的结构。
(2) 键角大小: (填“>”、“=”或“<”),其原因是 。(3分)
(3)有关 晶体的下列说法正确的是_______。(3分)
A.超分子都是通过配位键相互作用形成的
B. 的焰色试验呈绿色,是电子由激发态跃迁至基态时吸收能量产生的
C. 中含有 键的数目为
D.对该晶体进行加热时,配体 比 更容易失去
(1)黄钠铁矾的化学式为 ,晶体颗粒大、易沉降。
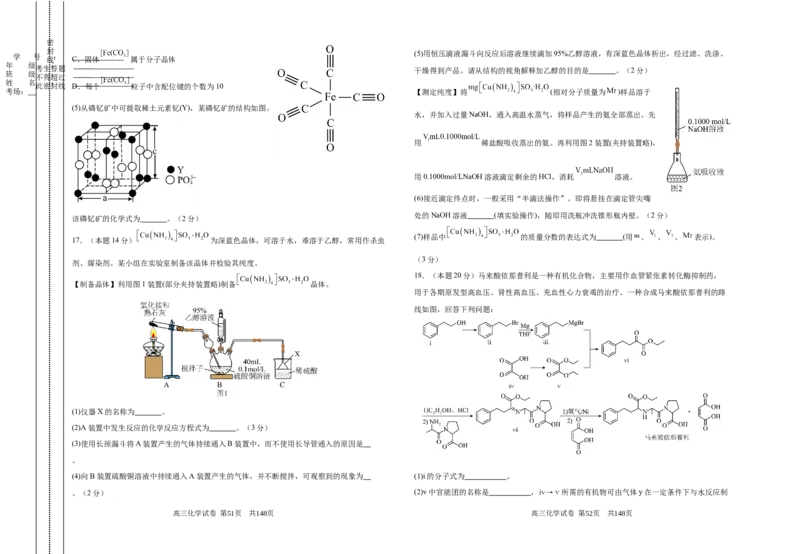
(4)配合物 是一种具有三角双锥结构的黄色黏稠状液体,可用于制备纯铁,结构如图所
①“沉铁”时生成黄钠铁矾的离子方程式为 。(2分)
②不采用调节 的方式沉铁,从制备或分离的角度分析可能的原因是: 。(2
示。已知熔点为 ,沸点为 。下列关于 的说法错误的是_______。(3分)
分)
(2)“还原除杂”时先向溶液中加入一定量的铜粉,反应一段时间后再向溶液中加入稍过量 粉, A. 中 原子以 杂化方式与 成键
滤渣的成分除了 、 粉外,还有 。
B.五羰基铁不溶于水,易溶于苯
高三化学试卷 第41页 共148页 高三化学试卷 第42页 共148页密
封
(5)用恒压滴液漏斗向反应后溶液继续滴加95%乙醇溶液,有深蓝色晶体析出,经过滤、洗涤、
学 号 :
线 C.固体 属于分子晶体
年 级 :
考生答题 干燥得到产品。请从结构的视角解释加乙醇的目的是 。(2分)
班 级 :
不得超过
姓 名 :
此密封线 D.每个 粒子中含配位键的个数为10
考场: 【测定纯度】将 (相对分子质量为 )样品溶于
(5)从磷钇矿中可提取稀土元素钇(Y),某磷钇矿的结构如图。
水,并加入过量NaOH,通入高温水蒸气,将样品产生的氨全部蒸出。先
用 稀盐酸吸收蒸出的氨。再利用图2装置(夹持装置略),
用0.1000mol/LNaOH溶液滴定剩余的HCl,消耗 溶液。
(6)接近滴定终点时,一般采用“半滴法操作”。即将悬挂在滴定管尖嘴
处的NaOH溶液 (填实验操作),随即用洗瓶冲洗锥形瓶内壁。(2分)
该磷钇矿的化学式为 。(2分)
(7)样品中 的质量分数的表达式为 (用 、 、 、 表示)。
17.(本题14分) 为深蓝色晶体,可溶于水,难溶于乙醇,常用作杀虫
(3分)
剂、媒染剂。某小组在实验室制备该晶体并检验其纯度。
18.(本题20分)马来酸依那普利是一种有机化合物,主要用作血管紧张素转化酶抑制药,
【制备晶体】利用图1装置(部分夹持装置略)制备 晶体。
用于各期原发型高血压、肾性高血压、充血性心力衰竭的治疗。一种合成马来酸依那普利的路
线如图,回答下列问题:
(1)仪器X的名称为 。
(2)A装置中发生反应的化学反应方程式为 。(3分)
(3)使用长颈漏斗将A装置产生的气体持续通入B装置中,而不使用长导管通入的原因是
。
(4)向B装置硫酸铜溶液中持续通入A装置产生的气体,并不断搅拌,可观察到的现象为 (1)ⅰ的分子式为 。
。(2分) (2)ⅴ中官能团的名称是 ,ⅳ→ⅴ所需的有机物可由气体y在一定条件下与水反应制
高三化学试卷 第51页 共148页 高三化学试卷 第52页 共148页
学科网(北京)股份有限公司备,该制备反应是理想的绿色化学反应,y的名称是 。
密
学 号 :
(3)根据化合物ⅵ的结构特征,分析预测其可能的化学性质,完成下表。 封
年 级 :
线
班 级 :
序号 反应试剂、条件 反应形成的新官能团 反应类型 姓 考生 名 答题 :
不得超过
考场:
此密封线
a (2分) (侧链)加成(或还原)反应
参考答案
题号 1 2 3 4 5 6 7 8 9 10
b (2分) -COOH和 (酸性条件下)水解反应
答案 A C D D B A D D A D
题号 11 12 13 14
(4)下列关于ⅵ→ⅶ→马来酸依那普利的叙述正确的是___________(填标号)。(4分)
答案 D B B B
A.ⅵ→ⅶ中,断裂了 中 键和 键
1.A
B.ⅵ→ⅶ中,形成了 键和 键
【详解】A.石墨是能导电的非金属单质,具有润滑性的优良性能,所以高铁列车的受电弓和
C.ⅶ分子中N原子都采用 杂化
接触导线之间涂抹石墨主要是利用了石墨的润滑性和导电性,故A正确;
D.马来酸依那普利中存在氢键 B.芯片主要材质是单晶硅,不是二氧化硅,故B错误;
C.硅胶的主要成分二氧化硅没有还原性,不能用作食品抗氧化剂,故C错误;
(5)X是ⅵ的同分异构体,X能与 反应,也能发生银镜反应,X的苯环上含有3个取代
D.聚四氟乙烯中不含有碳碳双键,不可能含有π键,也不能与溴水发生加成反应使溴水褪色,
基,且含氧官能团直接连在苯环上,符合条件的X共有 种。
故D错误;
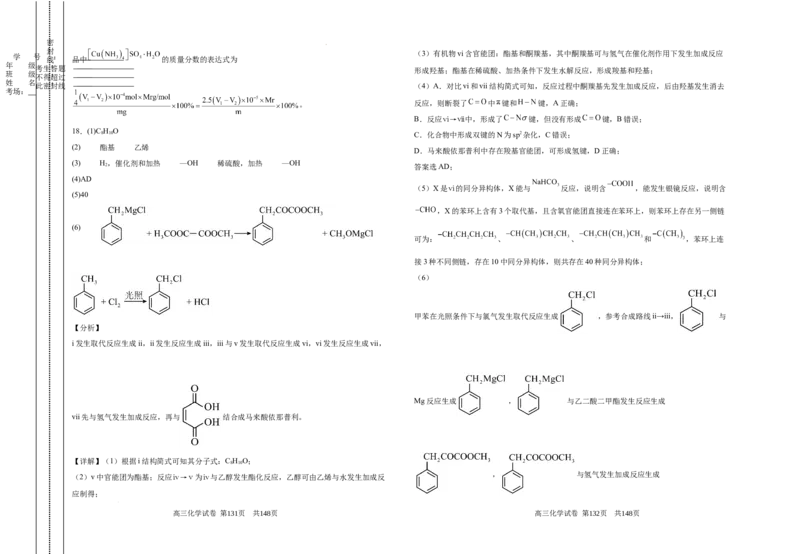
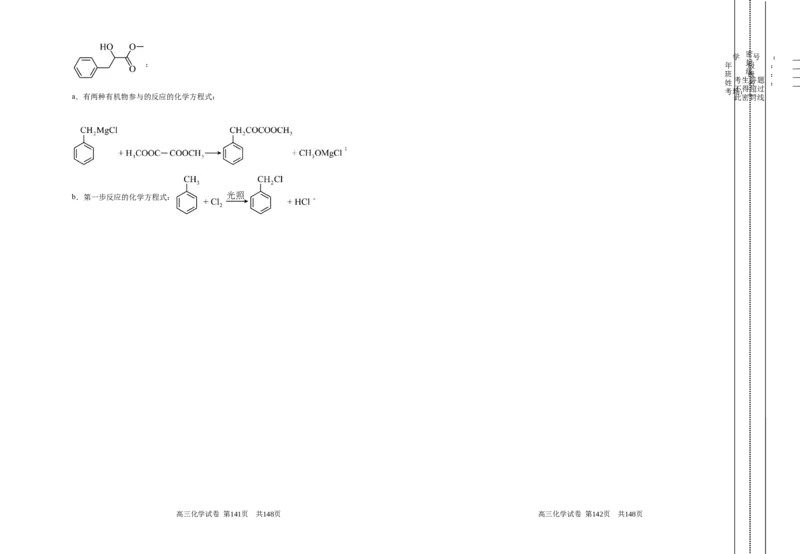
(6)以甲苯、乙二酸二甲酯为碳源,参照上述相关原理合成ⅷ,ⅷ的结构简式如图所示。
故选A。
a.有两种有机物参与的反应的化学方程式为 。(3分)
2.C
b.第一步反应的化学方程式为 (标明反应条件)。(3分)
【分析】 的某种单质可滤除大气中的大量紫外线,保护地球生物,此单质应为臭氧,因此
为O元素;基态 原子未成对电子数为2个,其单质及氧化物均为常见的共价晶体,因此
为Si元素; 的第一电离能小于元素周期表中与之紧邻的左侧元素,则 为ⅢA或ⅥA族元素,
又因为 、 、 和 为短周期元素,且原子序数依次增大,得Z为Al元素;根据分子式
得Y为Na元素。
【详解】A.Na的价层电子排布式为3s1,位于元素周期表的s区,A错误;
B.同周期从左往右,电负性依次增强,同主族同上到下,电负性依次减弱,因此电负性:
,即 ,B错误;
C.比较粒子半径大小:电子层数相同时,核电荷数越大,半径越小,因此简单离子半径:
,C正确;
高三化学试卷 第61页 共148页 高三化学试卷 第62页 共148页密
封
D.W的氧化物为SiO,为酸性氧化物,D错误; 故选D。
学 号 : 2
线
年 级 :
考生答题 答案选C。 5.B
班 级 :
不得超过
姓 名 :
此密封线 3.D 【分析】
考场:
【详解】A.酸性重铬酸钾溶液将乙醇氧化成乙酸,离子方程式应为: 根据制备流程可看出,汞和过量的稀硝酸反应生成硝酸汞,再和过量的碘化钾溶液反应生成
,A错误; , 再 加 入 氢 氧 化 钾 溶 液 和 微 量 的 反 应 生 成 红 色 沉 淀
B.甲烷和 在光照条件下反应生成一氯甲烷和氯化氢,反应方程式应为:
,B错误;
。
C.泡沫灭火器中盛放的是硫酸铝和碳酸氢钠溶液,离子方程式应为:
,C错误;
【详解】A.反应①为汞和过量的稀硝酸反应生成硝酸汞、一氧化氮和水,离子方程式为
D. 溶液中外界的氯离子可以电离,滴加足量 溶液,化学方程式为:
,A项正确;
,D正确;
B. 溶液与 能发生反应 ,故不能用 溶液除去 中的 ,
答案选D。
B项错误;
4.D
【详解】
C.反应③离子方程式为 ,消
A. 是基态氮原子的轨道表示式,不是激发态,A错误;
B.氢化钙中钙离子和H-离子个数比为1:2,B错误;
耗的 和 的物质的量之比为1:4,C项正确;
C. 的VSEPR模型应该是四面体形, 是 分子空间模型,C错误;
D.根据反应③可知,奈斯勒试剂即 与 混合溶液,和微量的 反应可生成红
D. 形成 键的过程: ,D
正确;
高三化学试卷 第71页 共148页 高三化学试卷 第72页 共148页
学科网(北京)股份有限公司为放热反应,升高温度,反应②平衡向逆反应方向移动,平衡时Z的浓度减小,C正确;
密
学 号 :
D.过程①是完全反应,过程②是可逆反应,其他条件不变,若增大 的用量,生成的X量增 封
年 级 :
线
色沉淀 ,故可用奈斯勒试剂检验 中微量的 ,D项正 班 级 :
多,相当于增大了体系的压强,但反应②为气体分子数不变的反应,改变压强对平衡无影响, 考生答题
姓 名 :
不得超过
考场:
故平衡时 的转化率不变,D错误; 此密封线
答案选D。
确;
8.D
答案选B。
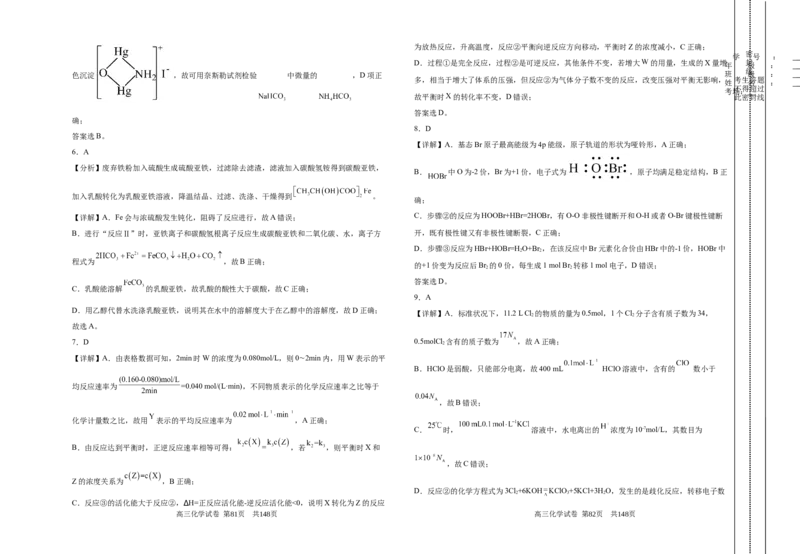
【详解】A.基态Br原子最高能级为4p能级,原子轨道的形状为哑铃形,A正确;
6.A
【分析】废弃铁粉加入硫酸生成硫酸亚铁,过滤除去滤渣,滤液加入碳酸氢铵得到碳酸亚铁,
B. 中O为-2价,Br为+1价,电子式为 ,原子均满足稳定结构,B正
加入乳酸转化为乳酸亚铁溶液,降温结晶、过滤、洗涤、干燥得到 。
确;
【详解】A.Fe会与浓硫酸发生钝化,阻碍了反应进行,故A错误; C.步骤②的反应为HOOBr+HBr=2HOBr,有O-O非极性键断开和O-H或者O-Br键极性键断
B.进行“反应Ⅱ”时,亚铁离子和碳酸氢根离子反应生成碳酸亚铁和二氧化碳、水,离子方 开,既有极性键又有非极性键断裂,C正确;
D.步骤③反应为HBr+HOBr=H O+Br ,在该反应中Br元素化合价由HBr中的-1价,HOBr中
2 2
程式为 ,故B正确;
的+1价变为反应后Br 的0价,每生成1 mol Br 转移1 mol电子,D错误;
2 2
答案选D。
C.乳酸能溶解 的乳酸亚铁,故乳酸的酸性大于碳酸,故C正确;
9.A
D.用乙醇代替水洗涤乳酸亚铁,说明其在水中的溶解度大于在乙醇中的溶解度,故D正确;
【详解】A.标准状况下,11.2 L Cl 的物质的量为0.5mol,1个Cl 分子含有质子数为34,
2 2
故选A。
7.D 0.5molCl 含有的质子数为 ,故A正确;
2
【详解】A.由表格数据可知,2min时W的浓度为0.080mol/L,则0∼2min内,用W表示的平
B.HClO是弱酸,只能部分电离,故400 mL HClO溶液中,含有的 数小于
均反应速率为 =0.040 mol/(L·min),不同物质表示的化学反应速率之比等于
,故B错误;
化学计量数之比,故用 表示的平均反应速率为 ,A正确;
C. 时, 溶液中,水电离出的 浓度为10-7mol/L,其数目为
B.由反应达到平衡时,正逆反应速率相等可得: = ,若 ,则平衡时X和
,故C错误;
Z的浓度关系为 ,B正确;
D.反应②的化学方程式为3Cl+6KOH KClO+5KCl+3H O,发生的是歧化反应,转移电子数
2 3 2
C.反应③的活化能大于反应②,∆H=正反应活化能-逆反应活化能<0,说明X转化为Z的反应
高三化学试卷 第81页 共148页 高三化学试卷 第82页 共148页密
封 为 5,即每消耗3molCl 转移5mol电子,在3molCl 中,只有2.5mol为氧化剂,故0.25molCl D.根据图像,当c(SO ) =0.001 mol/L时,溶液中c(Br-)> c{[Ag(S O)]3-}>c{[Ag(S O)]-},故
学 号 : 2 2 2 2 2 3 2 2 3
线
年 级 :
考生答题 D错误;
班 级 :
不得超过
姓 名 : 作 氧化剂时转移 电子数为 ,0.3molCl 作氧化剂时转移电子数为0.6N ,故D错误;
此密封线 2 A 选D。
考场:
故选A。 11.D
10.D 【分析】由图示可知,该电池放电时, 为负极,电极反应式为
【分析】溴化银的饱和溶液中溴离子浓度和银离子浓度相等,向饱和溶液中滴加硫代硫酸钠溶
, 为正极, 发生的反应为
液时,溶液中银离子浓度减小、溴离子浓度增大,则b点所在曲线表示银离子浓度与硫代硫酸
根离子浓度变化的关系、d点所在曲线表示溴离子与硫代硫酸根离子浓度变化的关系;溴化银
, 发生的反应为 ;充电时, 为阴
与硫代硫酸钠溶液开始反应时,溴化银主要转化为[Ag(S O)]−,溶液中 小于
2 3
极,电极反应式为 , 为阳极, 发生的反应为
, 发生的反应为 。
,则L 表示 随lg[c(S O )变化的关系、直线L 表示
1 2 2
【详解】A.由分析可知,放电时 电极为正极,A项正确;
B.放电时 通过离子交换膜进行移动,隔膜为阴离子交换膜,B项正确;
随lg[c(S O )变化的关系。
2
C.当有 参与反应时, 也在同时发生反应,外电路转移的电子数目大 ,C项正
【详解】A.Ksp(AgBr)=10-12.2,d点代表lgc(Br-)=-3.85、b点代表lgc(Ag+)=x,则10-3.85×10x=10-
12.2,x=-8.35,故A正确; 确;
D.充电时,阳极应失去电子,发生氧化反应, D项错误;
B.根据Ag+ + S O [Ag(S O)]-和[Ag(S O)]- + S O [Ag(S O)]3-,得Ag+ + 2S O
2 2 3 2 3 2 2 3 2 2
故选D。
12.B
【详解】A. 的过程可看作先发生酮羰基与亚氨基上H原子的加成反应生成羟基,然后
[Ag(S O)]3-。根据c点数据,c(SO ) =10-4.6时, 、 都等于10-
2 3 2 2
羟基再发生消去反应生成碳碳双键,A项正确;
B.a中含一个酮羰基和一个环,不饱和度为2,而饱和链状一元醛类的不饱和度为1,a不可
能存在饱和链状一元醛类同分异构体,B项错误;
4.2,反应Ag+ +2S O [Ag(S O)]3-,则K = = ,故B正确;
2 2 3 2 稳
C.根据物料守恒,c点c(Br-) = c(Ag+) + c{[Ag(S O)]-} + c{[Ag(S O)]3-},故C正确;
2 3 2 3 2
高三化学试卷 第91页 共148页 高三化学试卷 第92页 共148页
学科网(北京)股份有限公司密
学 号 :
C.Y与足量 的加成产物( )中含3个手性碳原子,C错误; 年 封 级 :
C. 发生取代反应,产物除了 还有HCl生成,所给化学方程式正确,C项 线
班 级 :
考生答题
姓 名 :
不得超过
考场:
此密封线
D.Y、Z均不具有酚羟基,所以不可用 溶液进行鉴别,D错误;
正确;
D. 的过程是酮羰基的反应,c→d又重新生成酮羰基,故设计 和 的转化过程 故选B。
是为了保护酮羰基,D项正确;
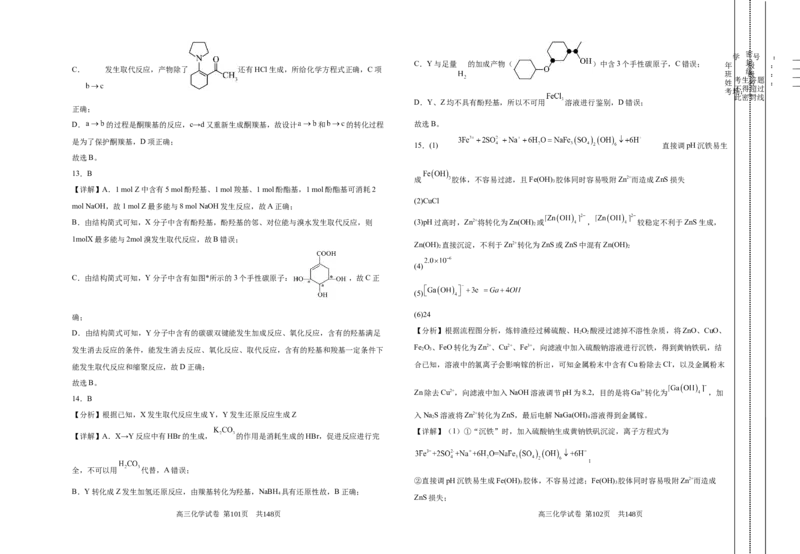
15.(1) 直接调pH沉铁易生
故选B。
13.B
成 胶体,不容易过滤,且Fe(OH) 胶体同时容易吸附Zn2+而造成ZnS损失
3
【详解】A.1 mol Z中含有5 mol酚羟基、1 mol羧基、1 mol酚酯基,1 mol酚酯基可消耗2
(2)CuCl
mol NaOH,故1 mol Z最多能与8 mol NaOH发生反应,故A正确;
B.由结构简式可知,X分子中含有酚羟基,酚羟基的邻、对位能与溴水发生取代反应,则 (3)pH过高时,Zn2+将转化为Zn(OH) 或 , 较稳定不利于ZnS生成,
2
1molX最多能与2mol溴发生取代反应,故B错误;
Zn(OH) 直接沉淀,不利于Zn2+转化为ZnS或ZnS中混有Zn(OH)
2 2
(4)
C.由结构简式可知,Y分子中含有如图*所示的3个手性碳原子: ,故C正
(5)
(6)24
确;
【分析】根据流程图分析,炼锌渣经过稀硫酸、HO 酸浸过滤掉不溶性杂质,将ZnO、CuO、
D.由结构简式可知,Y分子中含有的碳碳双键能发生加成反应、氧化反应,含有的羟基满足 2 2
Fe O、FeO转化为Zn2+、Cu2+、Fe3+,向滤液中加入硫酸钠溶液进行沉铁,得到黄钠铁矾,结
发生消去反应的条件,能发生消去反应、氧化反应、取代反应,含有的羟基和羧基一定条件下 2 3
合已知,溶液中的氯离子会影响镓的析出,可知金属粉末中含有Cu粉除去Cl-,以及金属粉末
能发生取代反应和缩聚反应,故D正确;
故选B。
Zn除去Cu2+,向滤液中加入NaOH溶液调节pH为8.2,目的是将Ga3+转化为 ,加
14.B
【分析】根据已知,X发生取代反应生成Y,Y发生还原反应生成Z 入NaS溶液将Zn2+转化为ZnS,最后电解NaGa(OH) 溶液得到金属镓。
2 4
【详解】(1)①“沉铁”时,加入硫酸钠生成黄钠铁矾沉淀,离子方程式为
【详解】A.X→Y反应中有HBr的生成, 的作用是消耗生成的HBr,促进反应进行完
;
全,不可以用 代替,A错误;
②直接调pH沉铁易生成Fe(OH) 胶体,不容易过滤;Fe(OH) 胶体同时容易吸附Zn2+而造成
3 3
B.Y转化成Z发生加氢还原反应,由羰基转化为羟基,NaBH 具有还原性故,B正确;
4
ZnS损失;
高三化学试卷 第101页 共148页 高三化学试卷 第102页 共148页密
封
键角更小
学 号 线 : ( 2)加入铜 粉的目的是:除去Cl-,发生的反应为 ,故滤渣的成分除
年 级 :
考生答题 (3)C
班 级 :
不得超过
姓 名 : 了 、 粉外 ,还有CuCl;
此密封线 (4)A
考场:
(3)根据图示可得知,当pH过高时,Zn2+将转化为Zn(OH) 或 , 较
2 (5)
稳定不利于ZnS生成,Zn(OH)
2
直接沉淀,不利于Zn2+转化为ZnS或ZnS中混有Zn(OH)
2
; 【详解】(1)基态As原子的核外电子排布式为:1s22s22p63s23p63d104s24p3,共有18个原子轨
道,故基态As原子的核外电子有18种不同的空间运动状态。
(4)由反应方程式 的平衡常数K =
1
(2) 中的N原子存在的孤电子对数为 ,价层电子对数=1+3=4,氨分子为三角
,结合 K=1.0×1034,可知K =
1
锥结构, 中的N原子形成3个普通的N-H,还有1个配位键,价层电子对数为
4,且均为成键电子对,氨分子为三角锥结构,则 键角大小: > ,因
=
为 中的N原子的价层电子对均为成键电子对,而 中的N原子存在一对孤电
子对,孤电子对与成键电子对的斥力比成键电子对之间的斥力更大,所以 中的键角更小。
(3)A.超分子是两种或两种以上的分子通过分子间相互作用形成的分子聚合体。超分子定义
= =1×10-35×1×1034×2.0×10-5=2.0×10-6;
中的分子是广义的,包括离子。分子以什么样的作用形成超分子?说法很纷繁,有人将它概括
为非共价键,有人则将其限于分子间作用力。超分子这种分子集合体,有的是有限的,有的是
(5)电解NaGa(OH) 溶液得到金属镓,阴极的反应为 ;
4
无限伸展的。故超分子不可能都是通过配位键相互作用形成的,A错误;
(6)K+占据四个互不相邻的小立方体(晶胞的 部分)的体心,所以晶胞中含有4个K+,化学式 B. 的焰色试验呈绿色,是电子由激发态跃迁至基态或者能量更低的激发态时释放能量产生
的,B错误;
为KFe[Fe(CN) ],则每个KFe[Fe(CN) ]晶胞含有CN-的个数是24。
6 6
16.(1)18 C. 中的每个N原子形成3个普通的N-H,还有1个配位键,都是 键,故1个
(2) > 中的N原子的价层电子对均为成键电子对,而 中的N原子存
中含有4×4=16个 键,键的数目为 中含有 键的数目为 ,
在一对孤电子对,孤电子对与成键电子对的斥力比成键电子对之间的斥力更大,所以 中的
C正确;
D.对该晶体进行加热时,先失结晶水,内界的氨气不易失去,D错误;
高三化学试卷 第111页 共148页 高三化学试卷 第112页 共148页
学科网(北京)股份有限公司选C。 【分析】装置A中生成氨气,反应产生的氨气通入B中,先产生氢氧化铜蓝色沉淀,继续向B
密
学 号 :
(4)A.由图可知,一氧化碳分子中的碳原子提供孤电子对,铁原子提供空轨道,则每个 中通入氨气,氢氧化铜溶解,生成硫酸四氨合铜,再滴入95%的乙醇析出 年 封 级 :
线
班 级 :
考生答题
姓 名 :
不得超过
粒子中含Fe-C配位键的个数为5,则 中 原子有5个杂化轨道,不可能以 ,分离出 ,溶解后和氢氧化钠反应释放出氨气被考场:
此密封线
稀盐酸吸收,通过滴定剩余盐酸溶质的量可以计算生成氨气的量,进而计算硫酸四氨合铜晶体
杂化方式与 成键,具有三角双锥结构,为sp3d杂化,A错误;
的纯度。
【详解】(1)根据装置图,仪器X的名称为普通漏斗;
B.已知配合物 熔点为 ,沸点为 ,则固体 属于分子晶体,按相似
(2)A装置制备氨气,氯化铵和氢氧化钙反应生成氯化钙、氨气、水,发生反应的化学反应
相溶原理,五羰基铁不溶于水,易溶于苯,B正确;
方程式为 ;
C.已知配合物 熔点为 ,沸点为 ,则固体 属于分子晶体,C正确;
(3)氨气极易溶于水,氨气溶于水易发生倒吸,使用长颈漏斗将A装置产生的气体持续通入
D.由图可知,一氧化碳分子中的碳原子提供孤电子对,铁原子提供空轨道,则每个
B装置中,而不使用长导管通入的原因是防倒吸。
粒子中含5个Fe-C配位键,每个一氧化碳分子内,氧和碳原子间还有1个配位键,则每个 (4)向B装置硫酸铜溶液中持续通入A装置产生的气体,并不断搅拌,先生成氢氧化铜沉淀,
氢氧化铜继续和氨气反应生成硫酸四氨合铜,可观察到的现象为:先生成蓝色沉淀,后蓝色沉
粒子中含配位键的个数为10,D正确;
淀消失,溶液变为深蓝色。
选A。 (5)水分子的极性大于乙醇分子的极性,加入乙醇能降低溶剂的极性,利于
(5)晶胞中含Y的个数是: ,含磷酸根的个数是: ,二者的
结晶析出,所以滴加95%乙醇溶液,有深蓝色晶体析出。
个数比是1:1,故该磷钇矿的化学式为YPO 。
4 (6)接近滴定终点时,一般采用“半滴法操作”,即将悬挂在滴定管尖嘴处的NaOH溶液轻
17.(1)普通漏斗
轻靠一下锥形瓶内壁,随即用洗瓶冲洗锥形瓶内壁。
(2) (7)根据滴定原理,样品产生的氨气和滴定用的氢氧化钠共消耗
(3)防倒吸
HCl,则氨气消耗的氯化氢为
(4)先生成蓝色沉淀,后蓝色沉淀逐渐溶解,溶液变为深蓝色
(5)降低溶剂的极性,利于 结晶析出
,n(NH )= ,根据
3
(6)轻轻靠一下锥形瓶内壁
~~4NH , 的物质的量为 ,样
3
(7)
高三化学试卷 第121页 共148页 高三化学试卷 第122页 共148页密
封
(3)有机物vi含官能团:酯基和酮羰基,其中酮羰基可与氢气在催化剂作用下发生加成反应
学 号 :
线 品中 的质量分数的表达式为
年 级 :
考生答题 形成羟基;酯基在稀硫酸、加热条件下发生水解反应,形成羧基和羟基;
班 级 :
不得超过
姓 名 :
此密封线 (4)A.对比vi和vii结构简式可知,反应过程中酮羰基先发生加成反应,后由羟基发生消去
考场:
。 反应,则断裂了 中 键和 键,A正确;
B.反应ⅵ→ⅶ中,形成了 键,但没有形成 键,B错误;
18.(1)C H O
8 10 C.化合物中形成双键的N为sp2杂化,C错误;
(2) 酯基 乙烯
D.马来酸依那普利中存在羧基官能团,可形成氢键,D正确;
(3) H ,催化剂和加热 —OH 稀硫酸,加热 —OH
2 答案选AD;
(4)AD
(5)X是ⅵ的同分异构体,X能与 反应,说明含 ,能发生银镜反应,说明含
(5)40
,X的苯环上含有3个取代基,且含氧官能团直接连在苯环上,则苯环上存在另一侧链
(6)
可为: 、 、 和 ,苯环上连
接3种不同侧链,存在10中同分异构体,则共存在40种同分异构体;
(6)
甲苯在光照条件下与氯气发生取代反应生成 ,参考合成路线ii→iii, 与
【分析】
i发生取代反应生成ii,ii发生反应生成iii,iii与v发生取代反应生成vi,vi发生反应生成vii,
Mg反应生成 , 与乙二酸二甲酯发生反应生成
vii先与氢气发生加成反应,再与 结合成马来酸依那普利。
【详解】(1)根据i结构简式可知其分子式:C H O;
8 10
, 与氢气发生加成反应生成
(2)v中官能团为酯基;反应ⅳ→ⅴ为ⅳ与乙醇发生酯化反应,乙醇可由乙烯与水发生加成反
应制得;
高三化学试卷 第131页 共148页 高三化学试卷 第132页 共148页
学科网(北京)股份有限公司密
学 号 :
; 年 封 级 :
线
班 级 :
考生答题
姓 名 :
不得超过
考场:
a.有两种有机物参与的反应的化学方程式: 此密封线
;
b.第一步反应的化学方程式: 。
高三化学试卷 第141页 共148页 高三化学试卷 第142页 共148页