文档内容
重庆市长寿中学校 2024-2025 学年高二上第三学月测试
化学试题
注意事项:
1.答卷前,考生务必将自己的姓名、准考证号填写在答题卡上。
2.回答选择题时,选出每小题答案后,用铅笔把答题卡对应题目的答案标号涂黑;如需改动,
用橡皮擦干净后,再选涂其他答案标号。回答非选择题时,将答案写在答题卡上,写在试卷
上无效。
3.考试结束后,本试卷和答题卡一并交回。
第I卷(选择题)
一、单选题:本大题共14小题,共42分。
1.煤的液化可以合成甲醇。下列有关说法正确的是( )
①“气化”: ;
②催化液化I: ;
③催化液化II: ;
A.催化液化I中使用催化剂,反应的活化能 、 都减小
B.反应
C.
D. 为电解质溶液的甲醇燃料电池中负极的电极反应为:
2.氯酸钾和亚硫酸氢钾溶液能发生氧化还原反应: 。已知该反应的速
率随 的增大而加快。如图为用 在单位时间内物质的量浓度变化表示的该反应 图。下列说
法中不正确的是( )A.反应开始时速率增大,可能是 增大所致
B.纵坐标为 的 曲线与图中曲线完全重合
C.图中阴影部分的面积表示 时间内 的物质的量的减少量
D.后期反应速率下降的主要原因是反应物浓度减小
3.下列说法正确的是( )
A.固体的溶解过程与熵变无关
B.常温下,冰融化成水是自发的,说明水的混乱度大于冰
C.放热反应都是自发的,吸热反应都是非自发的
D.反应焓变是决定反应能否自发进行的唯一因素
4.合成氨 的工业化生产是化工领域的突出成就,其生产流程如下图。下列说法错误的是( )
A.净化原料气的主要目的是防止催化剂“中毒”
B.加压至 ,既加快反应速率,也提高了平衡转化率
C.工业上不用常温而选择400℃~500℃的高温,符合勒夏特列原理
D.冷却分离出 ,利于平衡正向移动,提高产率
5.在生产、生活中,酸碱中和及溶液的酸碱性研究具有十分重要的意义。常温下,将两种一元酸分别和
溶液等体积混合,实验数据如下:
组
C(一酸) 混和溶液的
别
甲
乙
下列说法中正确的是( )
A.乙组混合液中:B.乙组实验所得混合溶液中由水电离出的 为
C.相同体积时, 溶液和 溶液中 浓度相同
D.相同体积时, 溶液和 溶液分别与足量的镁反应,产生氢气的速率和总量
均不同
6.常温下,用 溶液分别滴定浓度均为 溶液和 溶液各
,得到2条滴定曲线,如图所示。下列叙述正确的是( )
A.由图可推知, 是弱酸,而 是强酸
B.滴定 溶液时,应该选择甲基橙作为指示剂
C.滴定至 点时,溶液中
D.若 、 两点对应溶液的 分别为1、9,则两点处水电离出的 之比为
7.下列说法正确的是( )
A.中和滴定实验时,滴定管需用待装液润洗2~3次
B.中和滴定实验时,用待测液润洗锥形瓶
C.图I中滴定管可准确量取 酸性 溶液
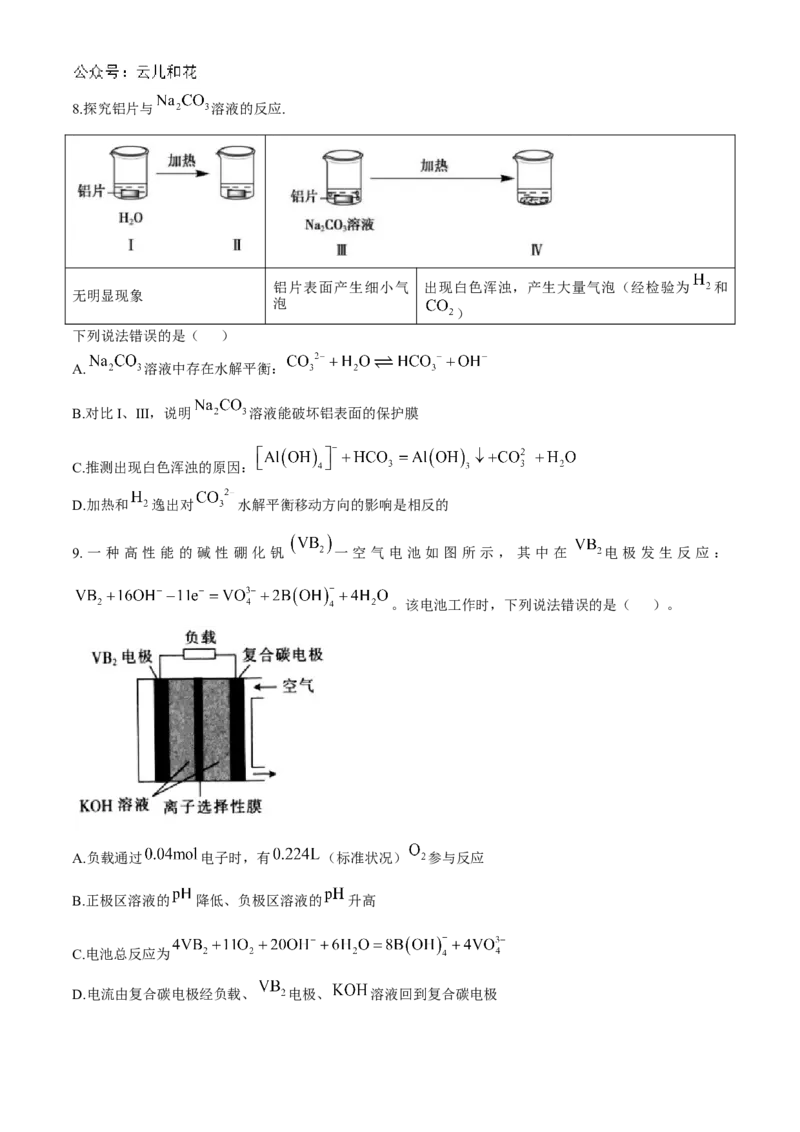
D.图II为用已知浓度的氢氧化钠溶液滴定未知浓度盐酸的实验8.探究铝片与 溶液的反应.
铝片表面产生细小气 出现白色浑浊,产生大量气泡(经检验为 和
无明显现象
泡
)
下列说法错误的是( )
A. 溶液中存在水解平衡:
B.对比I、III,说明 溶液能破坏铝表面的保护膜
C.推测出现白色浑浊的原因:
D.加热和 逸出对 水解平衡移动方向的影响是相反的
9. 一 种 高 性 能 的 碱 性 硼 化 钒 一 空 气 电 池 如 图 所 示 , 其 中 在 电 极 发 生 反 应 :
。该电池工作时,下列说法错误的是( )。
A.负载通过 电子时,有 (标准状况) 参与反应
B.正极区溶液的 降低、负极区溶液的 升高
C.电池总反应为
D.电流由复合碳电极经负载、 电极、 溶液回到复合碳电极10.荣获2019年诺贝尔化学奖的吉野彰是最早开发具有商业价值的锂离子电池的日本科学家,他设计的锂
充电电池的工作原理示意图如图所示。该可充电电池的放电反应为 。
表示阿伏加德罗常数的值。下列说法错误的是( )
A.若初始两电极质量相等,当转移 个电子时,两电极质量差为
B.充电时,阴极反应为
C.该电池用于电动汽车可有效减少光化学烟雾污染
D.充电时, 由B极移向A极
11.关于下列几个装置叙述正确的是( )
A B C D
利用此装置电解
离子导体可更换为 X为锌或锡均可减缓钢闸
铁既发生吸氧腐蚀又发生析氢腐蚀 精炼铜,粗铜做
溶液 门的腐蚀
b极
A.A B.B C.C D.D
12.利用双离子交换膜电解法可以处理含 的工业废水,原理如图所示。下列叙述错误的是( )A. 由 室向 室迁移
B. 室得到的混合气体是 和
C.阳极反应式为
D.理论上外电路中通过 电子,可处理工业废水中
13.某温度时,反应 在2L恒容密闭容器中进行,X和Z的浓度
随时间变化如图所示,下列说法正确的是( )
A. 内,X的平均反应速率为
B. 内,反应放出的热量为
C.第 后,X的生成速率与Y的生成速率相等且保持不变
D.第 时,该反应未达到平衡状态
14.用某浓度的钠盐 溶液处理一定量的 固体,测得加入 溶液的体积与溶液中 的关系如图所示。已知 。下列说法错误的是( )
A. 、 两点均为 的饱和溶液
B. 点表示 还未溶解完全
C.
D.该 溶液的浓度约为
第II卷(非选择题)
二、实验题:本大题共2小题,共26分。
15. ( 12 分 ) 目 前 , 常 利 用 催 化 技 术 将 汽 车 尾 气 中 的 和 进 行 下 列 转 化 :
。为研究如何增大该化学反应的速率,某课题组进行了以下实验探究。
【查阅资料】使用等质量的同种催化剂,催化剂比表面积对催化效率有影响。
【实验设计】实验数据如表所示。
编号 /℃
催化剂的比表面积
I 280 80
II 120.0
III 360 80.0
【图像分析】三组实验中 的浓度随时间的变化如图所示(曲线I表示实验I)。(1)实验数据表格中, _____; _____。
(2)第I组实验中,从反应开始到达到平衡用时 ,用 表示该反应在此段时间内的反应速率为
_____。
(3)要得出催化剂的比表面积对催化效率的影响,应比较曲线_____和曲线_____(填“I”、“ ”或“
”)。
(4)从化学平衡角度分析,该反应正方向为_____(填“放热”或“吸热”)反应。
16.(14分)25℃时,三种弱酸的电离平衡常数如下表所示。
名称 醋酸 亚硝酸
化学式
电离平衡常数
(1)将 和体积均相同的 溶液和 溶液分别稀释,其 随加水体积的变化如图。
①曲线I代表溶液_____(填" "或" ")。
②图中, 点水的电离程度_____(填“大于”、“小于”或“等于”) 点水的电离程度。
(2)某学习小组用 标准溶液来滴定未知物质的量浓度的盐酸时,选择酚酞作指示剂。
请回答下列问题:
①进行滴定时,将锥形瓶置于滴定管下方,眼睛应注视_____
②若滴定开始和结束时,该仪器中溶液读数如图所示,所用 标准溶液的体积为_____ 。(3)判断滴定终点的现象:_____。
(4)在上述实验过程中,出现了以下操作(其他操作均正确),其中会造成测定结果(待测液浓度值)
偏高的有_____(填字母)。
A.量取标准液的碱式滴定管未润洗
B.锥形瓶水洗后直接装待测液
C.酸式滴定管水洗后未用待测稀盐酸润洗
D.滴定到达终点时,俯视液面读数
E.碱式滴定管尖嘴部分有气泡,滴定后消失
(5)某学生根据3次实验分别记录有关数据如表所示:
滴 定 次 标准 溶液体积 滴定次数
待测盐酸的体积/
数
滴定前的刻度/
第一次 25.00 0.06 第一次
第二次 25.00 1.56 第二次
第三次 25.00 0.22 第三次
依据表中数据计算该盐酸的物质的量浓度为_____ (保留四位有效数字)
三、简答题:本大题共2小题,共32分。
17.(20分)完成下列问题。
(1)我国科研团队设计了一种表面锂掺杂的锡纳米粒子催化剂 可提高电催化制甲酸盐的产率,
同时释放电能,实验原理如图所示。
①放电时,正极的电极反应为_____。若使用铅蓄电池为该装置充电,产生 ,则铅蓄电池的正极质量_____(填“增加”或“减少”)_____g。
②研究发现,使用催化剂 或者 均能有效减少副产物 的生成,其原因是__________。
(2)电化学法也可合成氨。下图是用低温固体质子导体作为电解质,用 作阴极催化剂电解
和 合成 的原理示意图如下图所示。
① 电极反应产生 的电极反应式_____。
②实验研究表明,当外加电压超过一定值以后,发现阴极产物中氨气的体积分数随着电压的增大而减小,
分析其可能原因_____。
③该装置使用甲醇 燃料电池(电解质溶液为 )作为电源,写出负极的电极反应_____。
(3)某学习小组设想利用A装置电解制备绿色硝化剂 ,装置如下 、 为惰性电极)。
已知:无水硝酸可在液态 中发生微弱电离。
① 装置中通入 一极的电极反应式为_____。
②写出生成 的电极反应式_____。18.(12分)由于盐的水解,盐溶液不一定呈中性,如 溶液呈酸性, 溶液呈碱性,
溶液呈中性。已知A、B、C、D、E五种溶液分别是 、 、 、
、 中的一种。常温下进行下列实验:① 、 均能与 的 溶液反应,当它们以等
物质的量混合时均能恰好反应,反应后得到的溶液前者呈酸性,后者呈中性;②浓度均为 与
溶液等体积混合,溶液呈酸性。
回答下列问题:
(1) 是_____, 是_____(填写化学式);
(2)用水稀释 时,溶液中随着水量的增加而减小的是_____(填写序号)
a. c. d.
(3) 相同的等体积的两份溶液 和 ,分别与镁粉反应,若最后仅有一份溶液中存在镁粉,且放出
氢气的质量相同,则下列说法正确的是_____(填写序号)
a.参加反应的镁粉物质的量
b.开始反应时的速率
c.反应所需要的时间
d. 溶液里有镁粉剩余
(4)将等体积、等物质的量浓度 和 混合后溶液,升高温度(溶质不会分解)溶液 随温度变化如
下图中_____曲线(填写序号)。
(5)室温下,向 溶液中滴加 溶液至中性,得到的溶液中所有离子的物质的
量浓度由大到小的顺序为_____。
化学答案
1-5.BCBCB 6-10.CADBA 11-14.BDDB15.(1)280℃;
(2) ;
(3)I; ;
(4)放热。
16.(1)① ②大于
(2)①.锥形瓶内溶液颜色的变化②26.10
(3)当滴入最后半滴氢氧化钠标准液时溶液由无色变为浅红色,且半分钟内不褪色
(4)
(5)0.1044
17.(1)① ;增加;128
②使用催化剂后,生成 的活化能较生成 的活化能高,前者反应速率慢,相同时间内更有利于
的生成
(2)
②电压加大后发生副反应 ,而且该反应速率比生成氨气的反应速率更快,故氨气的体积
分数下降
③
(3) ②
18.(1) ; ;
(2) ;
(3) ;
(4)④;
(5) 。