文档内容
2025-2026学年度第一学期福九联盟(高中)期中联考 3. 已知化合物A与H O在一定条件下反应生成化合物B与HCOO−,其反应历程如图所
2
示,其中TS表示过渡态,Ⅰ表示中间体。下列说法正确的是( )
高中二年化学科试卷
A. 该历程中有6个基
元反应
B. 化合物A与H O之
完卷时间:75分钟 满 分:100分 2
间的碰撞均为有效碰撞
可能用到的相对原子质量:H-1 C-12 N-14 O-16 Cu-64
C. 该历程中的最大活
第I卷(选择题)
化能
一、单选题(每题3分,共45分。每小题只有一项符合题目要求)
E =18.86 kJ·mol-1
正
1. 化学与生产、生活、科技密切相关。下列有关说法不正确的是( ) D. 决定总反应速率快慢的步骤是最后一个基元反应
A. “月落乌啼霜满天,江枫渔火对愁眠”涉及的化学变化是放热反应
4. 二氧化硫空气质子交换膜燃料电池可以利用大气所含的SO 快速启动,下图为其装
2
B. 绿氢”燃料电池客车投入“冰丝带”:光伏电解水制氢可作为“绿氢”
置示意图。以下说法正确的是( )
的主要来源
A. 质子
C. “曾青得铁则化为铜”,湿法炼铜产物纯度不高,电解精炼铜时,粗铜
流动方向Y→X
应该与外接电源的正极相连
B. 负极
D. 将桥墩钢铁与外接电源负极相连的方法,称为牺牲阳极的阴极保护法
区有硫酸生成
2. 下列关于热化学反应方程式的描述正确的是( )
C. 正极反应物为SO
2
A. 若2H (g)+O (g)=2H O(g) ΔH ;2H (g)+O (g)=2H O(l) ΔH ,则
2 2 2 1 2 2 2 2
D. 离子导体为O2-
ΔH <ΔH
1 2
5. 下列叙述正确的是( )
B. 若C(金刚石,s)=C(石墨,s) ΔH= -1.9 kJ·mol-1,则石墨比金刚石更稳定
A. 在恒温恒压的密闭容器中发生反应:2NH (g) ⇌ N (g)+3H (g),向其中
C. 若H+(aq)+OH-(aq)=H O(l) ΔH= -57.3 kJ·mol-1 ,则NaOH固体和HCl反 3 2 2
2
通入氩气,反应速率减慢
应的反应热 ΔH= -57.3 kJ·mol-1
B. 已知反应H (g)+I (g) ⇌ 2HI(g)平衡常数为K,则2H (g)+2I (g) ⇌
D. 若C H (g)的燃烧热ΔH= -1299.6 kJ·mol-1,则乙炔燃烧的热化学方程式 2 2 2 2
2 2
4HI(g)的平衡常数为2K
为:2C H (g)+5O (g)=4CO (g)+2H O(g) ΔH= -2599.2 kJ·mol-1
2 2 2 2 2C. 已知反应2A(g)=C(g)+3D(g)低温时不反应,高温时自发进行,则该反应
加入2mL 5%H O 溶液,浓度大的试管冒出气泡的速 反应物浓度,化学反应速
2 2
的 <0 率更快 率加快
D. 对可逆反应4NH +5O ⇌ 4NO+6H O,增大c(O ),活化分子百分数增 取1 mL 0.1 mol·L-1 KI溶液于试管中,加入5 mL
3 2 2 2
KI与FeCl 的反应是可逆反
B 0.1 mol·L-1 FeCl 溶液,滴入5滴15% KSCN溶液, 3
大,有效碰撞几率增加,反应速率增大 3 应
溶液变血红色
6. 反应N (g)+3H (g) ⇌ 2NH (g) ,若在恒容绝热容器中发生,下列能判断该
2 2 3
催化剂改变反应历程,降
反应已经达到化学平衡的标志的是( ) C 5%的双氧水中加入二氧化锰粉末,分解速率迅速加快
低焓变,反应速率加快
①相同时间内,断开H-H键的数目和生成N-H键的数目相等
其他条件相同,Na S O 溶液与稀硫酸反应时, 其他条件相同时,反应物
D 2 2 3
②3v 正 (H 2 ) = 2v 逆 (NH 3 ) ③该反应的ΔH不再变化 ④容器内的温度不再变化 Na 2 S 2 O 3 溶液浓度越大,析出S沉淀所需时间越短 浓度越大,反应速率越快
⑤混合气体的密度不再变化 ⑥该反应的平衡常数K不再变化 9. 钌(Ru)是极好的催化剂,常用于氢化、异构化、氧化等重要反应。用钌基催化剂催化
CO (g)和H (g)的反应时,每生成92 g液态HCOOH
A.④⑥ B.③④ C.①⑤ D.②③ 2 2
时放出62.4 kJ的热量,反应机理如图所示,下列说
7. 浓差电池是利用物质的浓度差产生电势的一种装置。将两个完全相同的电极浸入两个
法正确的是( )
溶质相同但浓度不同的电解质溶液中构成的浓差电池,称为双液浓差电池。模拟工业上
电渗析法实现海水(用氯化钠溶液代替)淡化的装置如图所示。下列说法错误的是 A. 该反应的热化学方程式为
( )
H (g)+CO (g)=HCOOH(g) ΔH= - 31.2 kJ·mol-1
2 2
A.Cu(2)极发生还原反应
B. 该反应的活化能为
B.膜2为阴离子交换膜 62.4kJ·mol-1
C.C(2)极反应:
C. 图示中物质Ⅰ为该反应
2H O+2e-= 2OH-+H ↑ 的催化剂
2 2
D. 当电路中转移1 mol电子时,1 mol Cl-通过膜1向左移动 D. 图示中参与循环的物质只有H 2 O
10. 某全固态薄膜锂离子电池的工作示意图如
下,电极 a为锂硅合金,电极 b为镍钴锰三
8.下列现象及解释均正确的是( )
元材料(Li Ni Co Mn O ),电解质选用固
1-x 0.8 0.1 0.1 2
态Li PS Cl,下列说法中错误的是( )
现象 解释 6 5
A. 放电时电极a电势低于电极b
A 向2支盛有5mL不同浓度NaHSO 溶液的试管中同时 当其他条件不变时,增大
3
高二化学 -2** 错误的表达式 **- (共8页) 高二化学 -2** 错误的表达式 **- (共8页)电势 13. 电浮选凝聚法处理酸性污水的工作原理如
图所示,下列说法不正确的是( )
B. 放电时通过电路0.5mol电子 物质的量(n/mol)
时间
时,电解质Li PS Cl增加0.5molLi+ A. 为了增强污水的导电能力,
6 5 (t/min)
n(A) n(B) n(C)
可向污水中加入适量KCl
C. 充电时电极a连接电源的负
0 2.0 2.4 0
极 B. 铁电极的电极反应式为Fe
- 2e-=Fe2+
D. 充电时阳极反应为: 5 0.8
LiNi Co Mn O - xe- = Li C. 若左池石墨电极产生44.8L气体,则消耗0.5mol甲烷
0.8 0.1 0.1 2 1-
10 1.6
Ni Co Mn O + xLi+
x 0.8 0.1 0.1 2 D. 通入甲烷的石墨的电极反应式为:
15 1.6
11.已知NaNO +NH Cl=NaCl+2H O+N ↑的
2 4 2 2 CH + 4CO 2- - 8e- = 5CO + 2H O
4 3 2 2
速率方程为v ,为探究反应速率与反应物浓度的关系,进行
如下实验:向锥形瓶中加入一定体积(V)的 2.0 mol·L-1 NaNO 溶液、2.0 mol·L-1
2
V/mL
NH Cl溶液、1.0mol·L-1醋酸和水,充分搅拌,保持体系温度为36℃,测定反应初始速
4 实
反应初始速率v(mmol·L-1·s-1)
率v,实验数据如下表(忽略水溶液体系中其他平衡对离子浓度的影响)。下列说法正确 验 醋
NaNO 溶液 NH Cl溶液 水
的是( ) 2 4 酸
A.V 1 =4.0,V 2 =8.0 B.速率方程中m=2,n=2 1 4.0 V 1 4.0 12.0 4v
C.醋酸不参与反应,其浓度不会影响反应速率 D.实验4中,v'约为36v
2 6.0 4.0 4.0 10.0 9v
12.催化剂Ⅰ和Ⅱ均能催化反应R(g) P(g)。反应历程(下图)中,M为中间产物。其
3 4.0 V 4.0 0 32v
2
它条件相同时,下列说法不正确的是( )
⇌
4 12.0 4.0 4.0 V v'
A. 使用Ⅰ和Ⅱ,反应历程都分4步进行 3
B. 若不加催化剂,则正反应的活化能比逆反应的
小
C. 达到平衡所需要的时间:催化剂II<催化剂I
14. 一定温度下,在1 L的恒容密闭容器中发生反应A(g)+2B(g) 4C(g),反应过程中
D. 使用Ⅰ时,反应过程中M所能达到的最高浓度
的部分数据如下表所示。下列说法不正确的是( )
更大 ⇌
A. 0~5 min用A表示的平均反应速率为0.04 mol·L-1·min-1B. 物质A的平衡转化率约为20% (2)乙炔加氢可除去乙烯中少量乙炔杂质。该过程包括以下两个主要反应:
C. 该反应需经历十分钟才能建立平衡状态 反应1:C H (g)+H (g)=C H (g) ΔH = -175 kJ·mol-1(25℃,101kPa)
2 2 2 2 4 1
D. 当反应达平衡时,物质C的体积分数约为33% 反应2:C H (g)+2H (g)=C H (g) ΔH = -312 kJ·mol-1(25℃,101kPa)
2 2 2 2 6 2
15.T ℃,压力为P 时,向2L密闭容器中充入10 mol H 和3 mol SO 发生反应: 25℃,101kPa时,反应C H (g)+H (g)=C H (g) ΔH= 。
1 1 2 2 2 4 2 2 6
Ⅱ、手持技术测定中和反应反应热的装置和测定结果如图。
3H (g)+SO (g) H S(g)+2H O(g) ΔH <0。部分
2 2 2 2
⇌
物质的物质的量 随时间t变化如图中实线所
示。下列说法正确的是( )
A. 实线a代表n(H O)随时间变化的
2
曲线
B. min时,v (H ) > 3v (H S)
正 2 逆 2
C. 若该反应在T ℃,P (P >P )时进行,则虚线b可表示n(SO )的变化
1 2 2 1 2
D. 该反应的平衡常数 L mol-1
⋅
(3)磁子表面的聚四氟乙烯 (填“能”或“不能”)换成铁,原因是 。
第Ⅱ卷(非选择题)
(4)根据上图所示,计算本次实验中测定的中和反应反应热为 kJ/mol (精确至
二、填空题(共4题,共55分)。
0.01)。[已知:混合溶液的密度为1 g·cm-3,比热容为4.18 J·g-1·℃-1。忽略水以外各物
16.(13分)Ⅰ、化学反应伴随着能量变化,根据所学知识,回答下列问题:
质吸收的热量]
(1)已知N 2 (g)+3H 2 (g) ⇌ 2NH 3 (g) ΔH= - 92 kJ/mol。根据下表中的键能数据。 (5)测定稀盐酸和稀氢氧化钠中和热(中和热为57.3 kJ/mol)的实验装置如上图所示。实验
数值结果小于57.3 kJ/mol,原因可能是_______(填字母)。
共价键 N≡N H-H H-N
A.读取混合液的最高温度记为终点温度
键能(kJ/mol) 946 436 a
B.用量筒量取盐酸时仰视读数
则表中a= 。
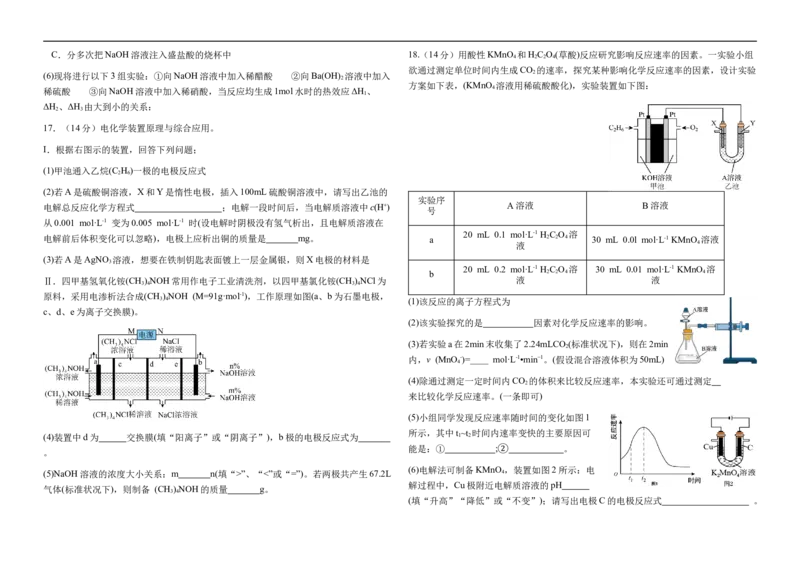
高二化学 -4** 错误的表达式 **- (共8页) 高二化学 -4** 错误的表达式 **- (共8页)C.分多次把NaOH溶液注入盛盐酸的烧杯中 18.(14分)用酸性KMnO 和H C O (草酸)反应研究影响反应速率的因素。一实验小组
4 2 2 4
欲通过测定单位时间内生成CO 的速率,探究某种影响化学反应速率的因素,设计实验
(6)现将进行以下3组实验:①向NaOH溶液中加入稀醋酸 ②向Ba(OH) 溶液中加入 2
2
方案如下表,(KMnO 溶液用稀硫酸酸化),实验装置如下图:
稀硫酸 ③向NaOH溶液中加入稀硝酸,当反应均生成1mol水时的热效应ΔH 、 4
1
ΔH 、ΔH 由大到小的关系:
2 3
17.(14分)电化学装置原理与综合应用。
I.根据右图示的装置,回答下列问题;
(1)甲池通入乙烷(C H )一极的电极反应式
2 6
(2)若A是硫酸铜溶液,X和Y是惰性电极,插入100mL硫酸铜溶液中,请写出乙池的
实验序
电解总反应化学方程式 ;电解一段时间后,当电解质溶液中c(H+) A溶液 B溶液
号
从0.001 mol·L-1 变为0.005 mol·L-1 时(设电解时阴极没有氢气析出,且电解质溶液在
20 mL 0.1 mol·L-1 H C O 溶
电解前后体积变化可以忽略),电极上应析出铜的质量是 mg。 a 2 2 4 30 mL 0.0l mol·L-1 KMnO 溶液
液 4
(3)若A是AgNO 溶液,想要在铁制钥匙表面镀上一层金属银,则X电极的材料是
3
20 mL 0.2 mol·L-1 H C O 溶 30 mL 0.01 mol·L-1 KMnO 溶
b 2 2 4 4
Ⅱ.四甲基氢氧化铵(CH ) NOH常用作电子工业清洗剂,以四甲基氯化铵(CH ) NCl为 液 液
3 4 3 4
原料,采用电渗析法合成(CH ) NOH (M=91g·mol-1),工作原理如图(a、b为石墨电极,
3 4 (1)该反应的离子方程式为
c、d、e为离子交换膜)。
(2)该实验探究的是 因素对化学反应速率的影响。
(3)若实验a在2min末收集了2.24mLCO (标准状况下),则在2min
2
内,v (MnO -)=____ mol·L-1•min−1。(假设混合溶液体积为50mL)
4
(4)除通过测定一定时间内CO 的体积来比较反应速率,本实验还可通过测定
2
来比较化学反应速率。(一条即可)
(5)小组同学发现反应速率随时间的变化如图1
所示,其中t ~t 时间内速率变快的主要原因可
(4)装置中d为 交换膜(填“阳离子”或“阴离子”),b极的电极反应式为 1 2
能是:① ; 。
。
(6)电解法可制备KMnO②,装置如图2所示:电
(5)NaOH溶液的浓度大小关系:m n(填“>”、“<”或“=”)。若两极共产生67.2L 4
解过程中,Cu极附近电解质溶液的pH
气体(标准状况下),则制备 (CH ) NOH的质量 g。
3 4
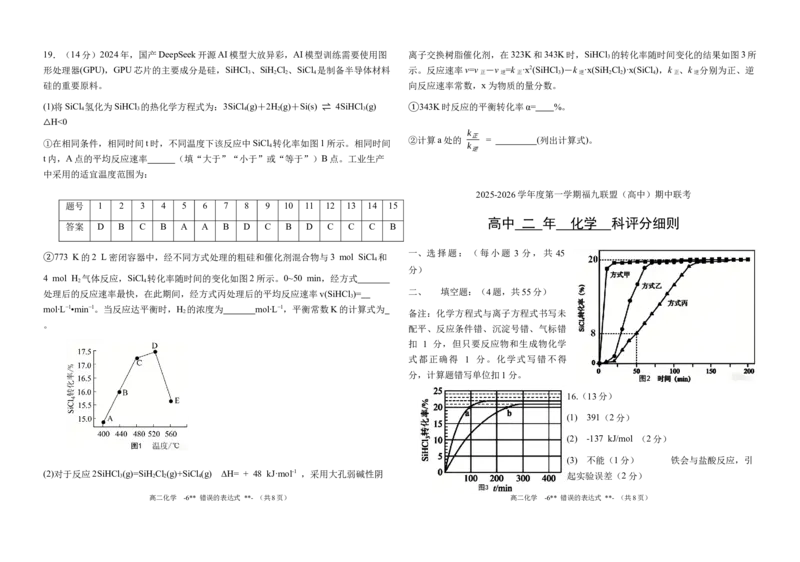
(填“升高”“降低”或“不变”);请写出电极C的电极反应式 。19.(14分)2024年,国产DeepSeek开源AI模型大放异彩,AI模型训练需要使用图 离子交换树脂催化剂,在323K和343K时,SiHCl 的转化率随时间变化的结果如图3所
3
形处理器(GPU),GPU芯片的主要成分是硅,SiHCl 、SiH Cl 、SiCl 是制备半导体材料 示。反应速率v=v -v =k ·x2(SiHCl )-k ·x(SiH Cl )·x(SiCl ),k 、k 分别为正、逆
3 2 2 4 正 逆 正 3 逆 2 2 4 正 逆
硅的重要原料。 向反应速率常数,x为物质的量分数。
(1)将SiCl 氢化为SiHCl 的热化学方程式为:3SiCl (g)+2H (g)+Si(s) ⇌ 4SiHCl (g) 343K时反应的平衡转化率α= %。
4 3 4 2 3
H<0
①
k
②计算a处的 正 = (列出计算式)。
△①在相同条件,相同时间t时,不同温度下该反应中SiCl 转化率如图1所示。相同时间
4 k
逆
t内,A点的平均反应速率 (填“大于”“小于”或“等于”)B点。工业生产
中采用的适宜温度范围为:
2025-2026学年度第一学期福九联盟(高中)期中联考
题号 1 2 3 4 5 6 7 8 9 10 11 12 13 14 15
高中 二 年 化学 科评分细则
答案 D B C B A A B D C B D C C C B
一、选择题:(每小题 3 分,共 45
773 K的2 L密闭容器中,经不同方式处理的粗硅和催化剂混合物与3 mol SiCl 和
4
分)
②4 mol H 气体反应,SiCl 转化率随时间的变化如图2所示。0~50 min,经方式
2 4
处理后的反应速率最快,在此期间,经方式丙处理后的平均反应速率v(SiHCl )=
二、 填空题:(4题,共55分)
3
mol‧L−1•min−1。当反应达平衡时,H 的浓度为 mol‧L−1,平衡常数K的计算式为
2 备注:化学方程式与离子方程式书写未
。
配平、反应条件错、沉淀号错、气标错
扣 1 分,但只要反应物和生成物化学
式都正确得 1 分。化学式写错不得
分,计算题错写单位扣1分。
16.(13分)
(1) 391(2分)
(2) -137 kJ/mol (2分)
(3) 不能(1分) 铁会与盐酸反应,引
(2)对于反应2SiHCl 3 (g)=SiH 2 Cl 2 (g)+SiCl 4 (g) ΔH= + 48 kJ·mol-1 ,采用大孔弱碱性阴 起实验误差(2分)
高二化学 -6** 错误的表达式 **- (共8页) 高二化学 -6** 错误的表达式 **- (共8页)(4) ﹣55.18 (2分)
(2) ① 22(2分) ② (2分)
(5) C(2分)
(6) ΔH >ΔH >ΔH (2分)
1 3 2
17.(14分)
(1) C H + 18OH- - 14e- = 2CO 2-+12H O(2分)
2 6 3 2
(2) 2CuSO + 2H O 2Cu + O ↑+ 2H SO (2分) 12.8(2分)
4 2 2 2 4
(3) Ag(银) (1分)
(4) 阴离子(1分) (2分)
(5) > (2分) 364(2分)
18.(14分)
(1) 2MnO - + 5H C O + 6H+ = 2Mn2+ + 10 CO ↑ + 8H O(2分)
4 2 2 4 2 2
(2) 草酸浓度(1分)
(3) 0.0002(2×10—4)(2分)
(4) KMnO 溶液完全褪色所需时间或产生相同体积气体所需的时间(2分)
4
(5) 该反应放热(2分) 产物Mn2+是反应的催化剂(2分)
(6) 升高(1分) MnO 2- - e- = MnO - (2分)
4 4
19.(14分)
(1) 小于(1分) 480~520°C(2分)
①
②甲(1分) 3.2×10−3(2分) 1.8 (2分) (2
分)