文档内容
宜昌市部分省级示范高中 2025 春季学期高二年级
期中考试化学试卷
考试时间:75分钟 满分:100分
可能用到的相对原子质量:H 1 C 12 N 14 O 16 S 32 Cl 35.5 K 39 Fe 56 Zn 65
一、选择题:本题共15小题,每小题3分,共45分。在每小题给出的四个选项中,只有一项是
符合题目要求的。
1. 传统节日美食承载着中华文化。下列说法错误的是( )
A. 元宵食汤圆——汤圆中的淀粉属于多糖
B. 端午尝粽子——肉粽中的瘦肉所含蛋白质可水解
C. 中秋品月饼——月饼包装中的铁粉作脱氧剂
D. 冬至吃饺子——饺子馅中的油脂属于有机高分子
2. 我国战略高技术领域迎来新跨越,如“嫦娥”揽月、“天问”探火、“天和”驻空及“地壳
一号”挺进地球深处。下列说法正确的是( )
A.“嫦娥六号”采集样本中所含的Ca、O元素均位于元素周期表p区
B.“天问一号”在火星大气中探测出的12CO 和13CO 互为同位素
2 2
C.“天和一号”铝基复合材料中所含的碳化硅属于共价晶体
D.“地壳一号”在万米深处钻出的石油和天然气均属于可再生能源
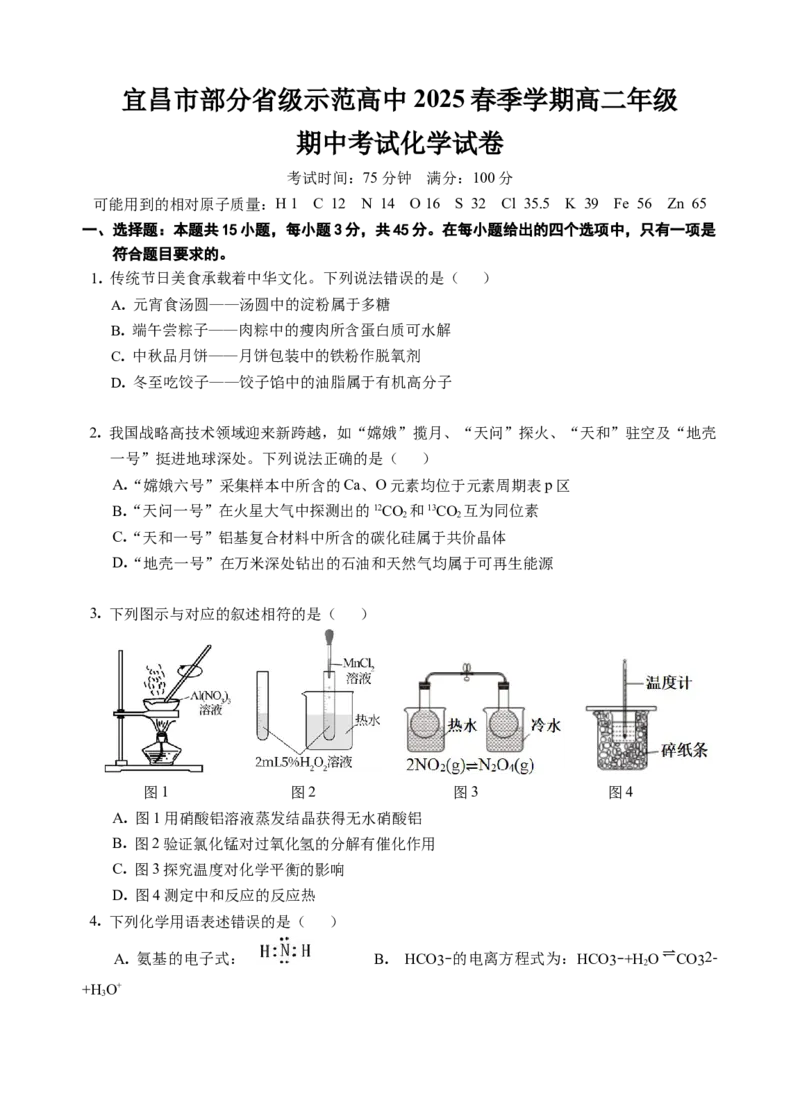
3. 下列图示与对应的叙述相符的是( )
图1 图2 图3 图4
A. 图1用硝酸铝溶液蒸发结晶获得无水硝酸铝
B. 图2验证氯化锰对过氧化氢的分解有催化作用
C. 图3探究温度对化学平衡的影响
D. 图4测定中和反应的反应热
4. 下列化学用语表述错误的是( )
A. 氨基的电子式: B. HCO3-的电离方程式为:HCO3-+H O⇌CO32-
2
+H O+
3C. CO
2
分子的空间填充模型: D. p-p π键的形成:
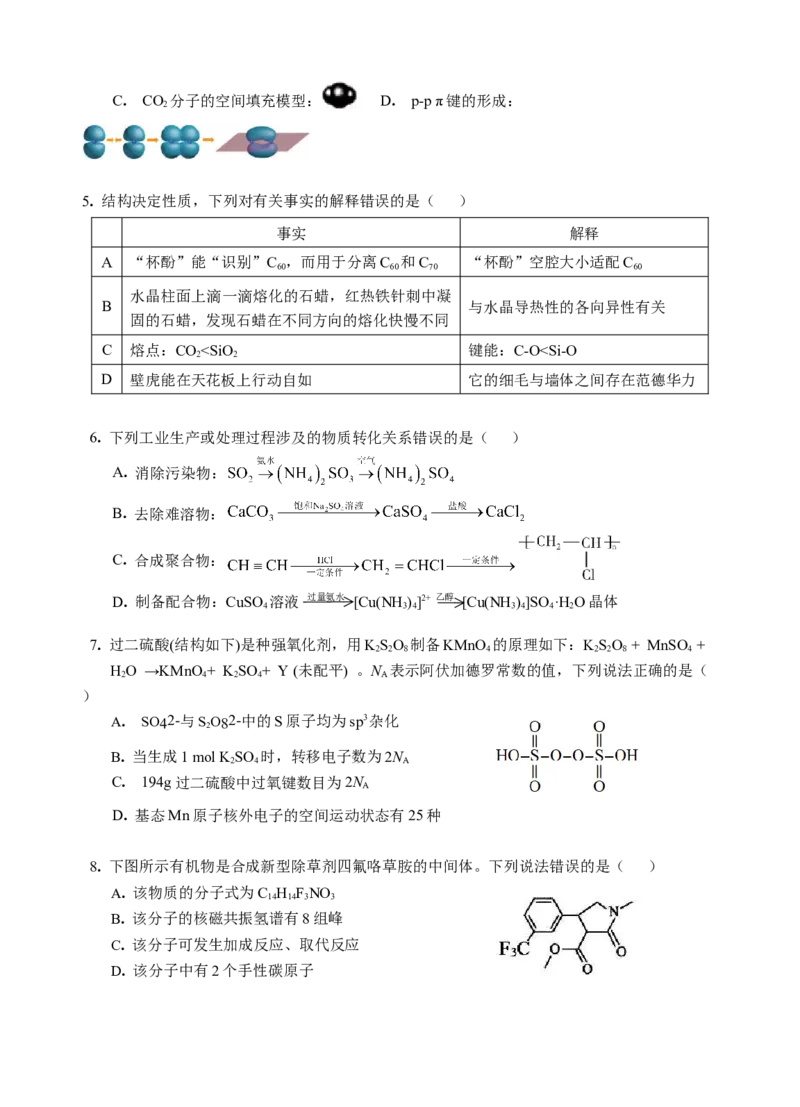
5. 结构决定性质,下列对有关事实的解释错误的是( )
事实 解释
A “杯酚”能“识别”C ,而用于分离C 和C “杯酚”空腔大小适配C
60 60 70 60
水晶柱面上滴一滴熔化的石蜡,红热铁针刺中凝
B 与水晶导热性的各向异性有关
固的石蜡,发现石蜡在不同方向的熔化快慢不同
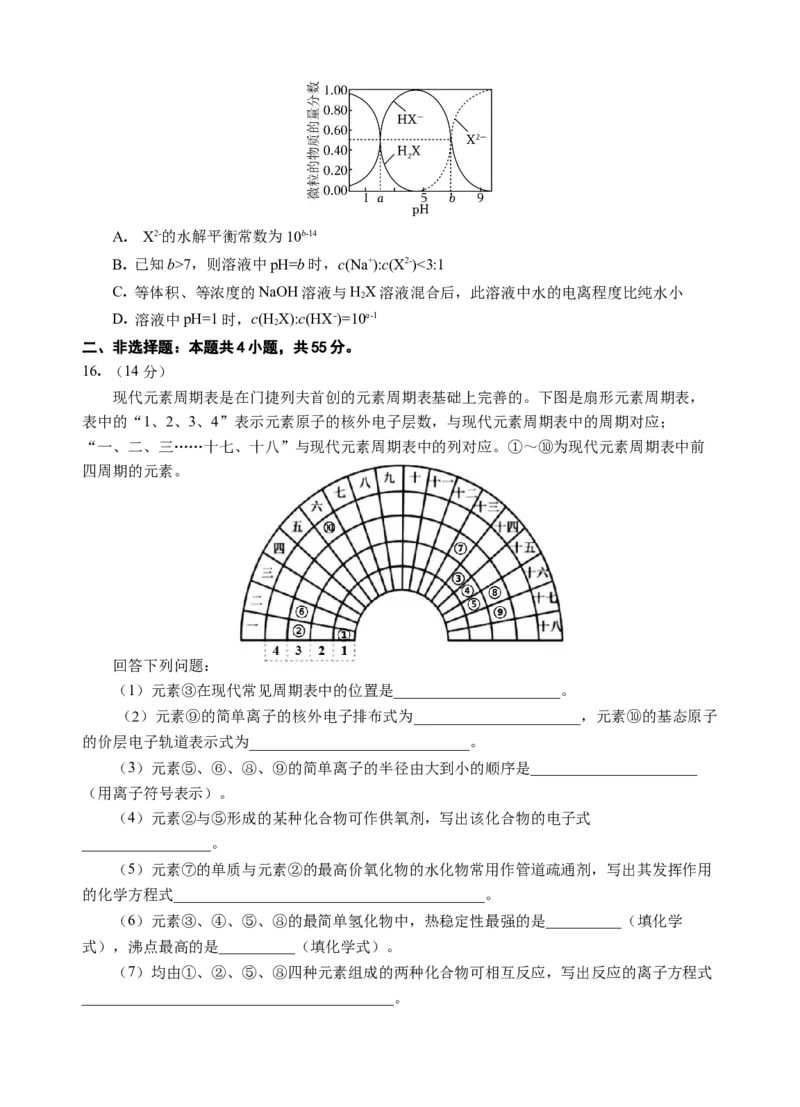
C 熔点:COX
B. 第一电离能:X7,则溶液中pH=b时,c(Na+):c(X2-)<3:1
C. 等体积、等浓度的NaOH溶液与HX溶液混合后,此溶液中水的电离程度比纯水小
2
D. 溶液中pH=1时,c(HX):c(HX-)=10a-1
2
二、非选择题:本题共4小题,共55分。
16. (14分)
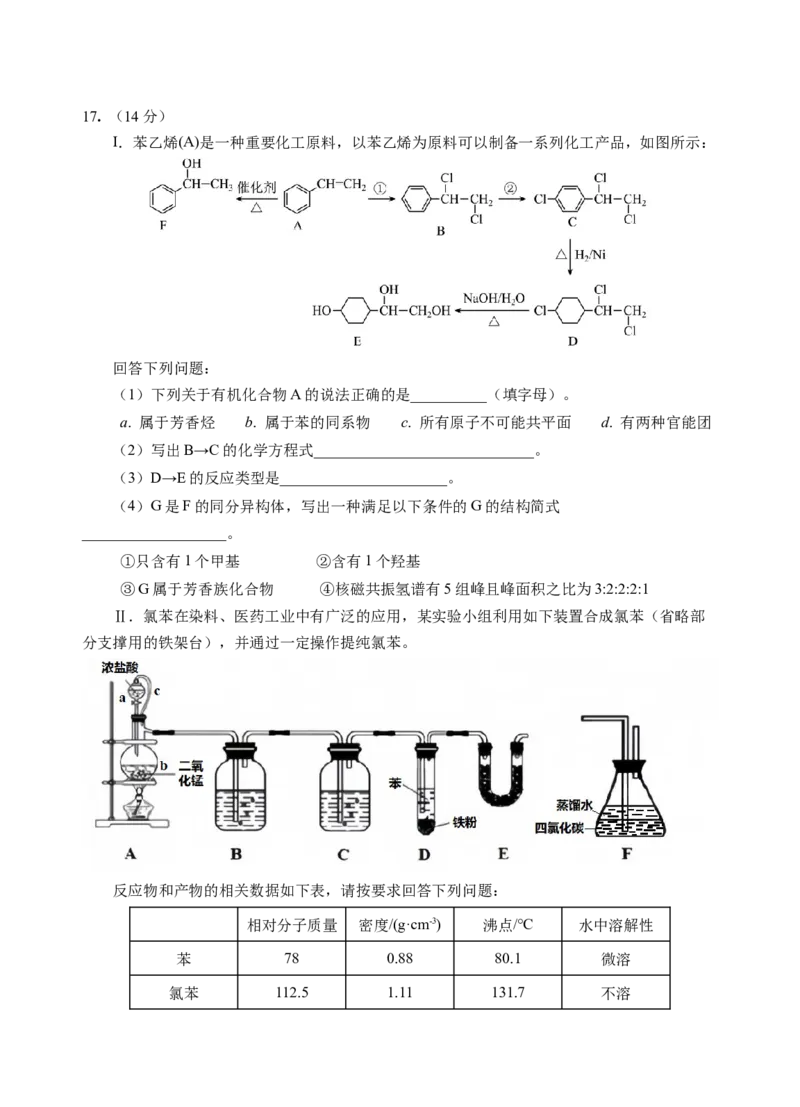
现代元素周期表是在门捷列夫首创的元素周期表基础上完善的。下图是扇形元素周期表,
表中的“1、2、3、4”表示元素原子的核外电子层数,与现代元素周期表中的周期对应;
“一、二、三……十七、十八”与现代元素周期表中的列对应。①~⑩为现代元素周期表中前
四周期的元素。
回答下列问题:
(1)元素③在现代常见周期表中的位置是______________________。
(2)元素⑨的简单离子的核外电子排布式为______________________,元素⑩的基态原子
的价层电子轨道表示式为_____________________________。
(3)元素⑤、⑥、⑧、⑨的简单离子的半径由大到小的顺序是______________________
(用离子符号表示)。
(4)元素②与⑤形成的某种化合物可作供氧剂,写出该化合物的电子式
_________________。
(5)元素⑦的单质与元素②的最高价氧化物的水化物常用作管道疏通剂,写出其发挥作用
的化学方程式_________________________________________。
(6)元素③、④、⑤、⑧的最简单氢化物中,热稳定性最强的是__________(填化学
式),沸点最高的是__________(填化学式)。
(7)均由①、②、⑤、⑧四种元素组成的两种化合物可相互反应,写出反应的离子方程式
_________________________________________。17. (14分)
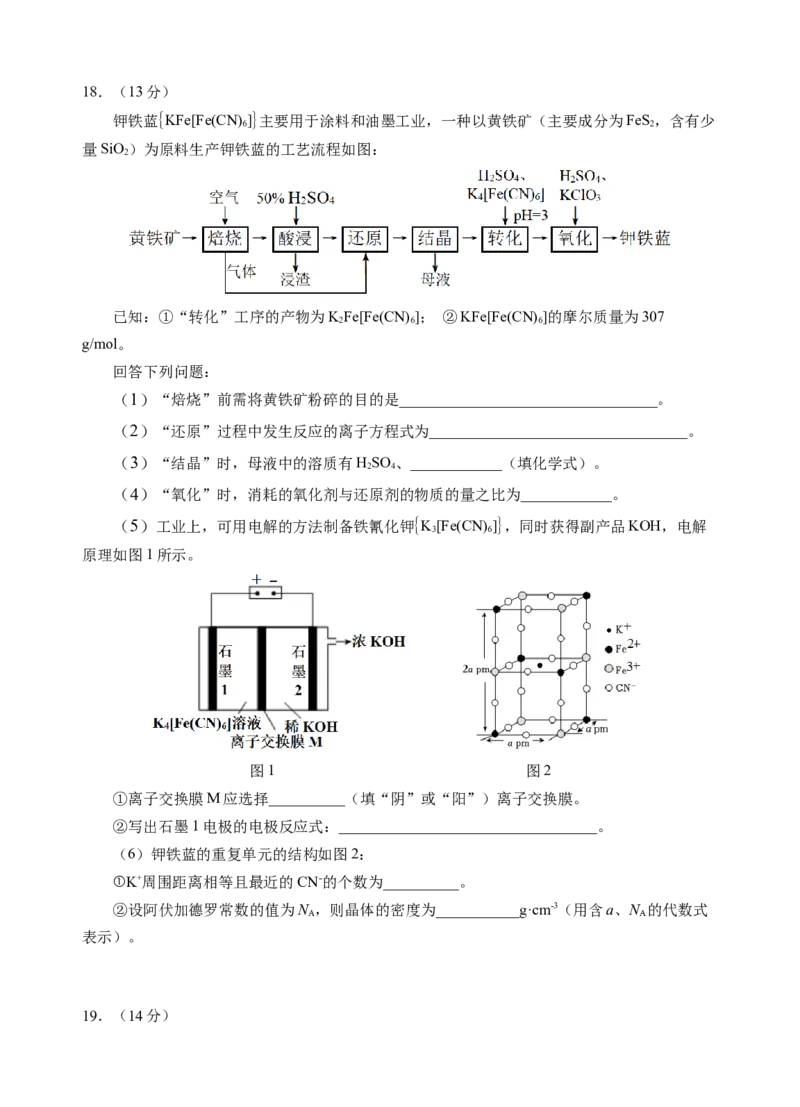
I.苯乙烯(A)是一种重要化工原料,以苯乙烯为原料可以制备一系列化工产品,如图所示:
回答下列问题:
(1)下列关于有机化合物A的说法正确的是__________(填字母)。
a. 属于芳香烃 b. 属于苯的同系物 c. 所有原子不可能共平面 d. 有两种官能团
(2)写出B→C的化学方程式_____________________________。
(3)D→E的反应类型是______________________。
(4)G是F的同分异构体,写出一种满足以下条件的G的结构简式
___________________。
①只含有1个甲基 ②含有1个羟基
③G属于芳香族化合物 ④核磁共振氢谱有5组峰且峰面积之比为3:2:2:2:1
Ⅱ.氯苯在染料、医药工业中有广泛的应用,某实验小组利用如下装置合成氯苯(省略部
分支撑用的铁架台),并通过一定操作提纯氯苯。
反应物和产物的相关数据如下表,请按要求回答下列问题:
相对分子质量 密度/(g·cm-3) 沸点/℃ 水中溶解性
苯 78 0.88 80.1 微溶
氯苯 112.5 1.11 131.7 不溶(5)装置A是实验室中常见的气体制备装置:
①A中橡胶管c的作用是______________________________________;
②A中发生反应的离子方程式为______________________________________。
(6)为证明氯气和苯发生的是取代而不是加成反应,该小组将装置F置于D、E间,F中
CCl 的作用是______________________,证明该结论还需使用的试剂是
4
______________________。
(7)若A中产生足量Cl,D中加入7.8 mL苯,经提纯后收集到氯苯6.6 g,则氯苯的产
2
率为__________%(保留三位有效数字)。18.(13分)
钾铁蓝{KFe[Fe(CN) ]}主要用于涂料和油墨工业,一种以黄铁矿(主要成分为FeS,含有少
6 2
量SiO)为原料生产钾铁蓝的工艺流程如图:
2
已知:①“转化”工序的产物为KFe[Fe(CN) ]; ②KFe[Fe(CN) ]的摩尔质量为307
2 6 6
g/mol。
回答下列问题:
(1)“焙烧”前需将黄铁矿粉碎的目的是__________________________________。
(2)“还原”过程中发生反应的离子方程式为__________________________________。
(3)“结晶”时,母液中的溶质有HSO 、____________(填化学式)。
2 4
(4)“氧化”时,消耗的氧化剂与还原剂的物质的量之比为____________。
(5)工业上,可用电解的方法制备铁氰化钾{K[Fe(CN) ]},同时获得副产品KOH,电解
3 6
原理如图1所示。
图1 图2
①离子交换膜M应选择__________(填“阴”或“阳”)离子交换膜。
②写出石墨1电极的电极反应式:__________________________________。
(6)钾铁蓝的重复单元的结构如图2:
①K+周围距离相等且最近的CN-的个数为__________。
②设阿伏加德罗常数的值为N ,则晶体的密度为___________g·cm-3(用含a、N 的代数式
A A
表示)。
19.(14分)我国在应对气候变化工作中取得显著成效,并向国际社会承诺 2030年实现“碳达峰”,
2060年实现“碳中和”。因此将CO 转化为高附加值化学品成为科学家研究的重要课题。
2
已知利用CO 合成甲醇过程中主要发生以下反应:
2
主反应I:CO
2
(g)+3H
2
(g)⇌CH
3
OH(g)+H
2
O(g) △H
1
=-49.4 kJ·mol-1
副反应II:CO
2
(g)+H
2
(g)⇌CO(g)+H
2
O(g) △H
2
=+41.2 kJ·mol-1
回答下列问题:
(1)反应CO(g)+2H
2
(g)⇌CH
3
OH(g)的△H
3
=_________________。
(2)主反应I自发进行的条件是__________(填“高温”或“低温”)。
(3)保持1.8 MPa、400℃不变,CO 和H 按体积比1:3充入反应器,同时发生上述两个反
2 2
应,下列可作为反应(反应I和反应II)达到平衡状态的判据是__________(填字母)。
a. 体系压强不再变化 b. 气体的密度不再改变
c. v正 (CO
2
)=3v逆 (H
2
) d. 各物质浓度不再改变
(4)为 了提 高 CO 的平衡 转化率和增大甲醇 的选择 性( CHOH 的选择 性
2 3
n(CH OH)
= 3 生成 ×100%),可采取的措施是_______________________________(任写一
n(CO )
2 消耗
种)。
(5)保持温度恒定,向某恒容容器中按体积比 1:3:1充入CO 、H 和Ar,起始压强为5
2 2
MPa。发生上述平行反应,达到平衡后压强为 3.8 MPa。已知达到平衡时CHOH的选择性为
3
75%。则:
①CO 的转化率为__________;
2
②该条件下反应I的压强平衡常数K 为__________(MPa)-2(用分压表示,分压=总压×物质
p
的量分数)。
E
(6)已知Arrhenius经验公式为RLnk= − a +C(E 为活化能,k为速率常数,R和C为常
T a
数),为探究m、n两种催化剂对反应I的催化效能,进行了实验探究,依据实验数据获得下
图。在m催化剂作用下,该反应的活化能E=__________kJ/mol,从图中信息获知催化性能较高
a
的催化剂是__________(填“m”或“n”)。