文档内容
2025~2026 学年高二上学期 10 月考试
化 学 试 题
考生注意:
1.本试卷分选择题和非选择题两部分。满分100分,考试时间75分钟。
2.答题前,考生务必用直径0.5毫米黑色墨水签字笔将密封线内项目填写清楚。
3.考生作答时,请将答案答在答题卡上。选择题每小题选出答案后,用2B铅笔把答题卡上对应题目
的答案标号涂黑;非选择题请用直径 0.5毫米黑色墨水签字笔在答题卡上各题的答题区域内作
答,超出答题区域书写的答案无效,在试题卷、草稿纸上作答无效。
4.本卷命题范围:苏教版选择性必修1专题1-专题2。
5.可能用到的相对原子质量:H1 C12 N14 O16 Na 23 S32 Cl 35.5 Fe 56 Cu 64 Zn 65
一、选择题(本题共 14小题,每小题3分,共42分。在每小题给出的四个选项中,只有一项是符合题目
要求的)
1.下列过程中,主要将电能转化为化学能的是
2.2025年受台风竹节草的影响,某些地区狂降暴雨。下列有关水蒸气变成雨水的过程中焓变和熵变的判
断正确的是
A.△H<0、△S<0 B.△H>0、△S<0
C.△H>0、△S>0 D.△H<0、△S>0
3.2025年9月3日大阅兵中惊雷-1、巨浪-3、东风61等导弹震撼亮相,彰显大国实力。肼( (N H )可
2 4
用作导弹发射的燃料。已知 0.5m ol液态肼与NO₂(g)完全反应生成 H O(g)、N (g),,放出283.5
2 2
kJ 热量,则表示该反应的热化学方程式正确的是
A.2N H (1)+2NO (g)=3N (g)+4H O(g)△H=−1134.0kJ·mol-1
2 4 2 2 2
B.2N₂H₄(1)+2NO₂(g)══3N₂(g)+4H₂O(g) ΔH=+283.5 kJ·mol⁻¹
C.2N H +2NO =3N +4H O△H=−283.5kJ·mol−1
2 4 2 2 2
D.2N₂H₄(g)+2NO₂(g)══3N₂(g)+4H₂O(l) △H=—1134.0kJ·mol⁻¹
4.反应 4N H (g)+5O (g)=4NO(g)+6H O(g))在2 L密闭容器中进行,5 min后, N H 的物质的量
3 2 2 3
减少了0.4m ol,则该反应在此5 min内的平均速率可表示为
A.v(N H )=0.08mol⋅L−1 ⋅min−1 B.v(O )=0.04mol⋅L−1 ⋅min−1
3 2
C.v(NO)=0.08mol⋅L−1 ⋅min−1 D.v(H O)=0.06mol⋅L−1 ⋅min−1
2
5.下图装置的烧杯中均盛有 0.2mol⋅L−1的稀盐酸,在铜电极上能产生气泡的是
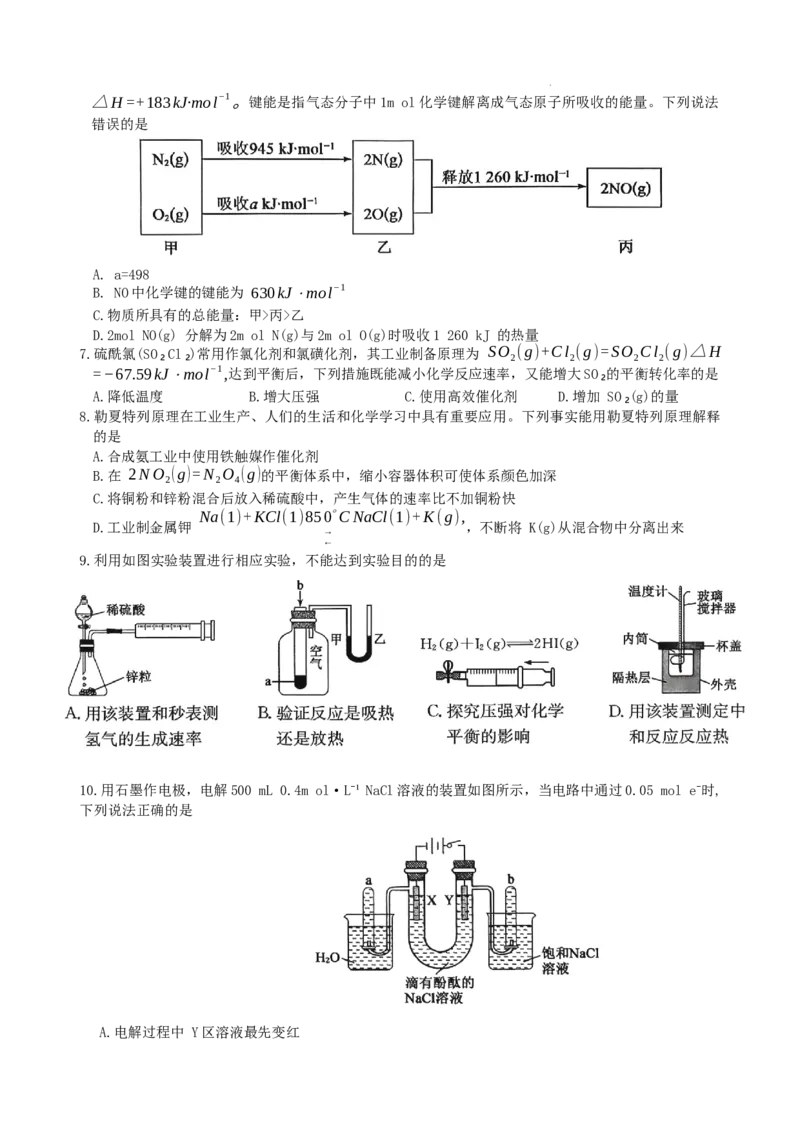
6.汽车发动机工作时会引发N₂和O₂反应,其能量变化示意图如图所示,已知 N (g)+O (g)=2NO(g)
2 2
学科网(北京)股份有限公司△H=+183kJ·mol−1 。键能是指气态分子中1m ol化学键解离成气态原子所吸收的能量。下列说法
错误的是
A. a=498
B. NO中化学键的键能为 630kJ⋅mol−1
C.物质所具有的总能量:甲>丙>乙
D.2mol NO(g) 分解为2m ol N(g)与2m ol O(g)时吸收1 260 kJ 的热量
7.硫酰氯(SO₂Cl₂)常用作氯化剂和氯磺化剂,其工业制备原理为 SO (g)+Cl (g)=SO Cl (g)△H
2 2 2 2
=−67.59kJ⋅mol−1,达到平衡后,下列措施既能减小化学反应速率,又能增大SO₂的平衡转化率的是
A.降低温度 B.增大压强 C.使用高效催化剂 D.增加 SO₂(g)的量
8.勒夏特列原理在工业生产、人们的生活和化学学习中具有重要应用。下列事实能用勒夏特列原理解释
的是
A.合成氨工业中使用铁触媒作催化剂
B.在 2NO (g)=N O (g)的平衡体系中,缩小容器体积可使体系颜色加深
2 2 4
C.将铜粉和锌粉混合后放入稀硫酸中,产生气体的速率比不加铜粉快
Na(1)+KCl(1)850∘CNaCl(1)+K(g),
D.工业制金属钾 ,不断将 K(g)从混合物中分离出来
→
←
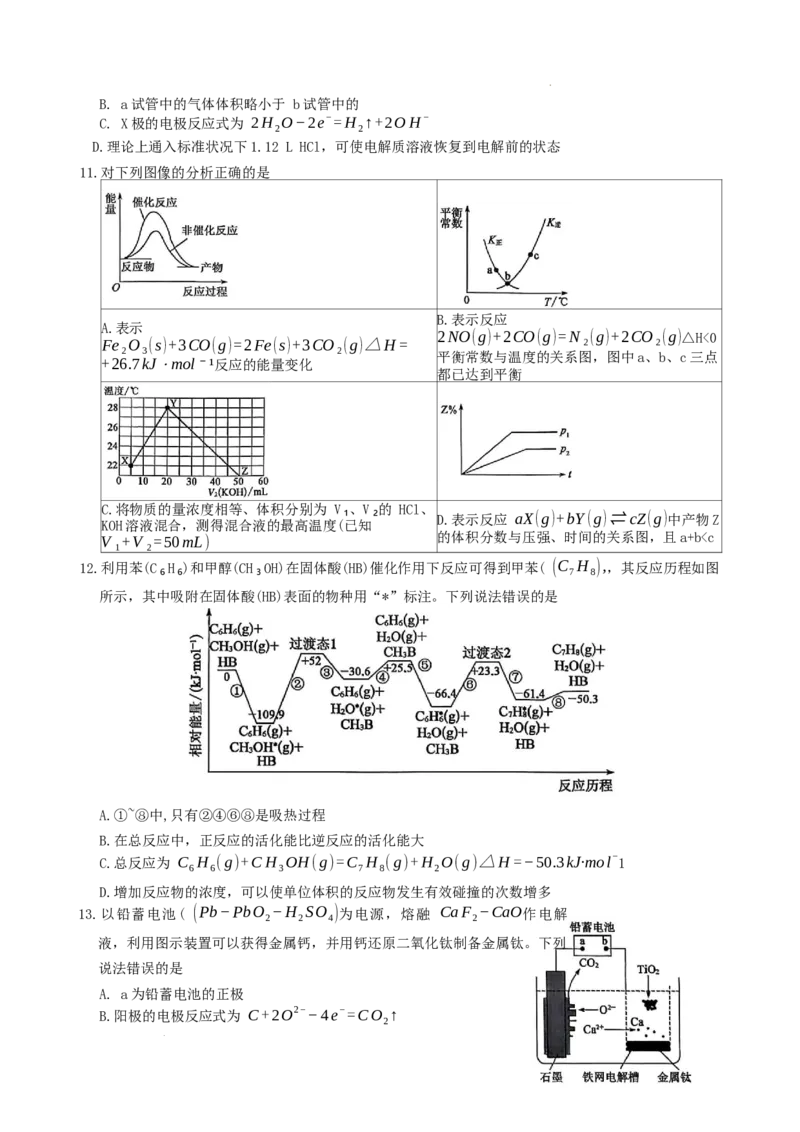
9.利用如图实验装置进行相应实验,不能达到实验目的的是
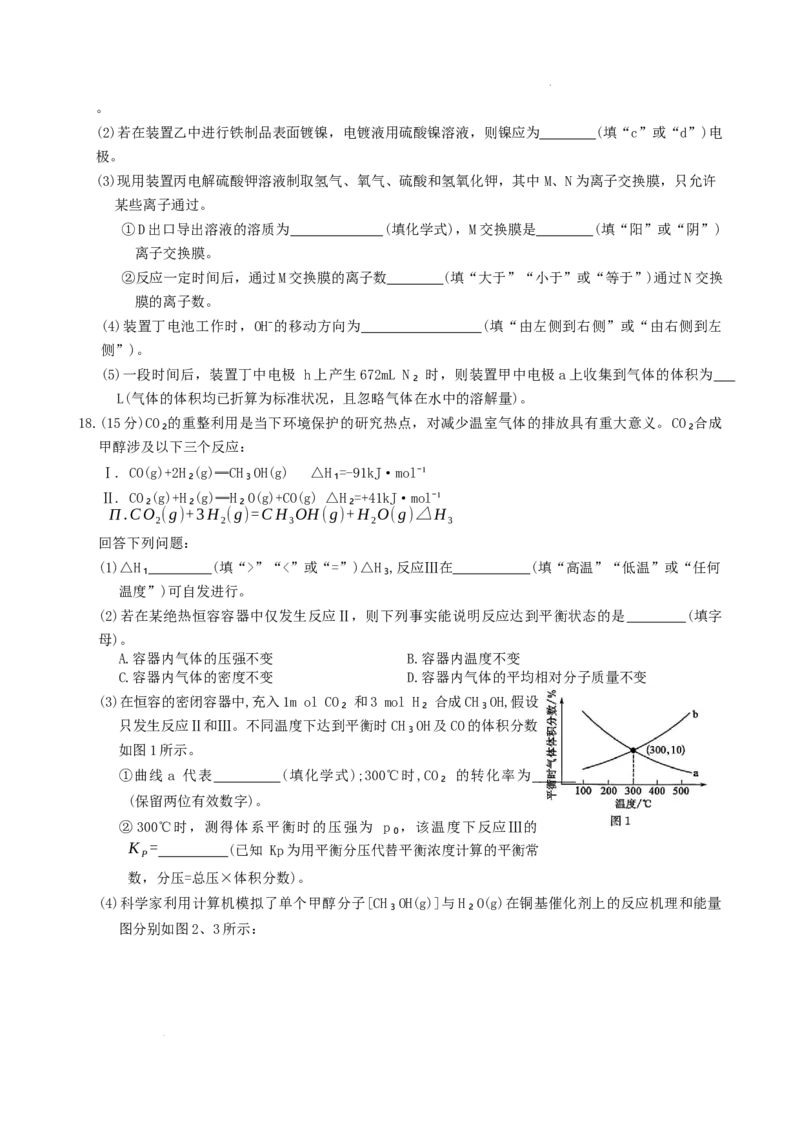
10.用石墨作电极,电解500 mL 0.4m ol·L⁻¹NaCl溶液的装置如图所示,当电路中通过0.05 mol e⁻时,
下列说法正确的是
A.电解过程中 Y区溶液最先变红
学科网(北京)股份有限公司B. a试管中的气体体积略小于 b试管中的
C. X极的电极反应式为 2H O−2e−=H ↑+2OH−
2 2
D.理论上通入标准状况下1.12 L HCl,可使电解质溶液恢复到电解前的状态
11.对下列图像的分析正确的是
B.表示反应
A.表示
2NO(g)+2CO(g)=N₂(g)+2CO₂(g)△H<0
Fe₂O₃(s)+3CO(g)=2Fe(s)+3CO₂(g)△H=
平衡常数与温度的关系图,图中a、b、c三点
+26.7kJ⋅mol⁻¹反应的能量变化
都已达到平衡
C.将物质的量浓度相等、体积分别为 V₁、V₂的 HCl、
D.表示反应 aX(g)+bY(g)⇌cZ(g)中产物Z
KOH溶液混合,测得混合液的最高温度(已知
V ₁+V ₂=50mL) 的体积分数与压强、时间的关系图,且a+bv(z)>v(x)
C. x点时,平衡常数K=2
D. x、y两点对应的平衡常数 K(x)=K(y)
二、非选择题(本题共4小题,共58分)
15.(14分)物质变化和能量变化在化学研究中占据核心地位,通过深入研究这些变化,可以更好地理解
和利用化学反应,为人类的生产和生活带来更多的可能性。回答下列问题:
(1)下列选项属于吸热反应的是 (填字母)。
a.干冰汽化 b. C与CO₂反应生成CO c.铝热反应 d.燃烧反应 e.碳酸钙的分解
(2)葡萄糖是一种重要的营养物质,它是人类生命活动所需能量的重要来源之一。已知葡萄糖(
(C H O ,s)的燃烧热(△H)是- −2800kJ⋅mol−1,写出表示葡萄糖燃烧热的热化学方程式:
6 12 6
。
(3)有机物M经过太阳光光照可转化成N,该转化过程如下:
△H=+88.6 kJ·mol⁻¹。M、N相比,较稳定的是 ( 填“M”或“N”),
该反应中1mol M的能量 (填“大于”或“小于”)1mol N 的能量。
(4)市场上出售的“热敷袋”,其主要成分是铁屑、炭粉、木屑与少量氯化钠等。某实验小组模
拟“热敷袋”原理设计了如下实验。将锥形瓶内壁用酸化的饱和食盐水润洗后,放入混合均匀的
铁粉和炭粉,塞紧瓶塞,同时用压强传感器测得锥形瓶内压强的变化如图所示。
①“热敷袋”放出的热量时铁屑作 (填“正”或“负”)极。
②0~t₁时,体系压强增大的原因是 。
学科网(北京)股份有限公司③t₁~t₂时,炭粉表面发生的电极反应式为 。
16.(14分)实验室模拟热气循环法合成尿素[CO(NH₂)₂],CO₂(g)与NH₃(g)在一定条件下发生反应:
CO (g)+2N H (g)=H O(g)+CO(N H ) (s)△H<0。为了探究温度和催化剂的载体结构对该
2 3 2 2 2
化学反应速率的影响,某课题组进行了以下实验:
NH₃初始浓度/
实验编号 T/℃ CO₂初始浓度/(mol·L⁻¹) 催化剂载体结构
/(mol⋅L⁻¹)
I 280 1.2×10⁻³ x 棒状
Ⅱ 280 1.2×10⁻³ 5.8×10⁻³ 层状
Ⅲ 280 1.2×10⁻³ 5.8×10⁻³ 蜂窝状 18
Ⅳ 300 y 5.8×10⁻³ 层状
V 350 1.2×10⁻³ 5.8×10⁻³ 层状
已知:实验Ⅰ~Ⅴ使用的催化剂种类和质量均相同;查阅资料可知,使用相同的催化剂,当催化剂质
量相同时,催化剂的比表面积(单位质量的物质所具有的总面积)越大,反应速率越快。回答下列问
题:
(1)表中x= ,y= 。
(2)课题组根据实验Ⅰ、Ⅱ、Ⅲ的相关数据,绘制了如图所示曲线图。
①由该图可知,其他条件均相同时,使用的催化剂载体结构为 (填“棒状”“层
状 ” 或 “ 蜂 窝 状 ” ) 的 情 况 下 该 反 应 的 化 学 反 应 速 率 最 快 , 解 释 其 原 因 :
。
②第Ⅲ组实验中,0~5s 内用CO₂表示的平均速率为 m o l \cdot L^{ - 1}\cdot s^{
- 1}。
(3)若上述反应在恒温密闭容器中进行,当压缩容器使容积减小时,v正将 (填“增大”“减
小”或“不变”,下同),v逆将 。
17.(15分)电化学知识在我们的生产、生活中的应用广泛。某同学设计的串联电化学装置如图所示。向
装置丁中通入NH₃、O₂一段时间后,装置甲a极有气体产生,b极处溶液逐渐变成紫红色,停止实验
观察到电极b明显变细,电解液仍然澄清。查阅资料:高铁酸根离子(FeO²⁻)在溶液中呈紫红色。回
答下列问题:
(1)电极 a 为 (填“正”“负”“阴”或“阳”)极,电极 b 发生的电极反应式为
学科网(北京)股份有限公司。
(2)若在装置乙中进行铁制品表面镀镍,电镀液用硫酸镍溶液,则镍应为 (填“c”或“d”)电
极。
(3)现用装置丙电解硫酸钾溶液制取氢气、氧气、硫酸和氢氧化钾,其中 M、N为离子交换膜,只允许
某些离子通过。
①D出口导出溶液的溶质为 (填化学式),M交换膜是 (填“阳”或“阴”)
离子交换膜。
②反应一定时间后,通过M交换膜的离子数 (填“大于”“小于”或“等于”)通过N交换
膜的离子数。
(4)装置丁电池工作时,OH⁻的移动方向为 (填“由左侧到右侧”或“由右侧到左
侧”)。
(5)一段时间后,装置丁中电极 h上产生672mL N₂ 时,则装置甲中电极a上收集到气体的体积为
L(气体的体积均已折算为标准状况,且忽略气体在水中的溶解量)。
18.(15分)CO₂的重整利用是当下环境保护的研究热点,对减少温室气体的排放具有重大意义。CO₂合成
甲醇涉及以下三个反应:
Ⅰ. CO(g)+2H₂(g)═CH₃OH(g) △H₁=-91kJ·mol⁻¹
Ⅱ. CO₂(g)+H₂(g)═H₂O(g)+CO(g) △H₂=+41kJ·mol⁻¹
Π.CO (g)+3H (g)=CH OH(g)+H O(g)△H
2 2 3 2 3
回答下列问题:
(1)△H₁ (填“>”“<”或“=”)△H₃,反应Ⅲ在 (填“高温”“低温”或“任何
温度”)可自发进行。
(2)若在某绝热恒容容器中仅发生反应Ⅱ,则下列事实能说明反应达到平衡状态的是 (填字
母)。
A.容器内气体的压强不变 B.容器内温度不变
C.容器内气体的密度不变 D.容器内气体的平均相对分子质量不变
(3)在恒容的密闭容器中,充入1m ol CO₂ 和3 mol H₂ 合成CH₃OH,假设
只发生反应Ⅱ和Ⅲ。不同温度下达到平衡时CH₃OH及CO的体积分数
如图1所示。
①曲线 a 代表 (填化学式);300℃时,CO₂ 的转化率为
(保留两位有效数字)。
② 300℃时,测得体系平衡时的压强为 p₀,该温度下反应Ⅲ的
K = (已知 Kp为用平衡分压代替平衡浓度计算的平衡常
P
数,分压=总压×体积分数)。
(4)科学家利用计算机模拟了单个甲醇分子[CH₃OH(g)]与H₂O(g)在铜基催化剂上的反应机理和能量
图分别如图2、3所示:
学科网(北京)股份有限公司已知 a、 b 、
c、d、e均表示能量值。
①由图 2、3 知反应 I 的△H (填“<”“>”或“=”)0;反应 II 的活化能为
kJ·mol⁻¹。
②决定反应速率快慢的步骤为 (填“反应Ⅰ”或“反应Ⅱ”)。
学科网(北京)股份有限公司