文档内容
★ 保密·启用前
★
吉林市普通高中2025—2026学年度高二年级阶段性调研测试
化 学 试 题
说明:1.答卷前,考生务必将自己的姓名、准考证号填写在答题卡上,贴好条形码。
2.答选择题时,选出每小题答案后,用 2B铅笔把答题卡对应题目的答案标号
涂黑。如需改动,用橡皮擦干净后,再选涂其他答案标号。答非选择题时,
用0.5毫米的黑色签字笔将答案写在答题卡上。字体工整,笔迹清楚。
3.请按题号顺序在答题卡相应区域作答,超出区域所写答案无效;在试卷上、
草纸上答题无效。
4.考试结束后,将本试卷和答题卡一并交回。
一、选择题:本题共15小题,每小题3分,共45分。在每小题给出的四个选项中,只有
一项符合题目要求。
1.下列物质溶解于水时,电离出的阴离子能使水的电离平衡向右移动的是
A.Na SO B.CH COONa C.NH Cl D.HSO
2 4 3 4 2 4
2.下列说法正确的是
A.能够自发进行的反应一定是放热反应
B.ΔH<0的反应均是自发进行的反应
C.能够自发进行的反应一定是熵增的过程
D.水凝结成冰的过程,ΔH<0、ΔS<0
3.已知4NH +5O =4NO+6H O,若反应速率分别用v (NH )、v (O )、v (NO)、v (H O)
3 2 2 3 2 2
表示,则正确的关系是
A. B.
C. D.
4.强碱MOH的溶液和等体积等物质的量浓度的弱酸HA的溶液混合后,溶液中有关离
子浓度的大小关系正确的是
A.c(M+)>c(A-)>c(OH-)>c(H+) B.c(M+)>c(A-)>c(H+)>c(OH-)
C.c(M+)>c(OH-)>c(A-)>c(H+) D.c(M+)+c(H+)>c(A-)+c(OH-)
5.合理利用某些盐能水解的性质,能解决许多生产、生活中的问题,下列叙述的事实与
盐水解的性质无关的是
A.金属焊接时可用NH Cl溶液作除锈剂
4
B.配制FeSO 溶液时,加入一定量Fe粉
4
C.长期施用铵态氮肥会使土壤酸化
D.向FeCl 溶液中加入CaCO 粉末后有气泡产生
3 36.向10 mL氨水中加入蒸馏水,将其稀释到1 L后,下列变化中错误的是
A.NH ·HO的电离程度增大 B.c(NH ·HO)增大
3 2 3 2
C.NH + 的数目增多 D. 增大
4
7.在一定条件下的密闭容器中发生反应:CH(g) CH(g)+H (g) ΔH>0。当达到平衡
2 6 2 4 2
时,下列各项措施中,不能提高乙烷转化率的是
A.等容下通入稀有气体 B.升高反应的温度
C.分离出部分氢气 D.增大容器的容积
8.向一个密闭容器中充入1 mol N 和3 mol H ,在一定条件下使其发生反应生成NH 。
2 2 3
达到平衡时,下列说法中正确的是
A.N、H 和NH 的物质的量浓度之比为1:3:2
2 2 3
B.N 完全转化为NH
2 3
C.正反应速率和逆反应速率都为零
D.单位时间内消耗a mol N,同时消耗2a mol NH
2 3
9.下列各组离子在指定溶液中一定能大量共存的是
A.常温下pH=11的溶液中: 、 、 、
B.常温下 的溶液中: 、 、 、
C.室温下 的溶液中: 、 、 、
D.滴加NaOH溶液能产生红褐色沉淀的溶液中: 、 、 、
10.下列说法正确的是
A.相同温度时,1 L 0.5 mol/L NH Cl溶液与2 L 0.25 mol/L NH Cl溶液含NH +物质
4 4 4
的量相同
B.将pH相同的盐酸和醋酸等体积混合,醋酸电离程度增大
C.将CH COONa溶液从20℃升温至30℃,溶液中 减小
3
D.某温度下,向含有AgCl固体的AgCl饱和溶液中加入少量稀盐酸,AgCl的溶解度
不变11.有关下列图像的分析错误的是
A.
图
①
表
示
用蒸馏水稀释温度相同、pH相同的盐酸和醋酸时溶液的pH变化曲线,其中溶液
的导电性: a>b>c
B.图②表示反应2SO (g)+O (g) 2SO (g) ΔH<0 ,若其他条件不变,O 的物质的
2 2 3 2
量一定,则a、b、c三点中,a点的SO 转化率最高
2
C.图③表示在恒温恒容的密闭容器中,按不同投料比充入CO和H 发生反应:
2
CO(g)+2H (g) CH OH(g),若平衡时CO和H 的转化率相等,则a=2
2 3 2
D.图④表示发生反应:mA(s)+nB(g) pC(g),若m+n>p,则a曲线一定使用了催
化剂
12.下列实验操作、现象及所得结论均正确的是
选
实验操作和现象 结论
项
相同条件下,分别测量0.1 mol·L-1和
A 0.01 mol·L-1醋酸溶液的导电性,前者 醋酸浓度越大,电离程度越大
的导电性强
向2mL 0.1 mol·L-1FeCl 溶液中滴加
3 加入KCl后,FeCl+3KSCN
B KSCN溶液后,溶液变红,再加入少量 3
KCl固体,红色变浅 Fe(SCN) +3KCl的平衡逆向移动
3
在2mL 0.1 mol·L-1Na S溶液中先滴入
2
几滴0.1 mol·L-1ZnSO 溶液有白色沉淀
C 4 K (CuS)HS-
2
pH,前者的pH大
A.A B.B C.C D.D
13.三甲胺N(CH ) 是重要的化工原料。我国科学家利用(CH)NCHO(简称DMF)在
3 3 3 2铜催化作用下发生可逆反应得到N(CH ),计算机模拟单个DMF分子在铜催化剂表
3 3
面的反应历程如图所示(*表示物质吸附在铜催化剂上),下列说法正确的是
A
. 恒
容 密
闭 容
器 中
减 小
压 强
可增大DMF的平衡转化率
B.若1mol DMF完全转化为三甲胺,则会释放1.02eV的能量
C.该历程的最大能垒(活化能)为1.19eV
D.该反应中铜催化剂可以加快化学反应速率,降低活化分子百分数
14. 室温下,用含少量Mg2+的MnSO 溶液制备MnCO 的过程如图所示。已知
4 3
K (MgF)=5.2×10-11,下列说法正确的是
sp 2
A. 0.1 mol·L-1NaF溶液中:
B.“除镁”得到的上层清液中:
C.0.1 mol·L-1NaHCO 溶液中:
3
D.“沉锰”后的滤液中:
15.常温下,用0.1000 mol·L-1的NaOH溶液滴定20.00mL未知浓度的二元酸HA溶液。
2溶液的pH、分布系数 随滴加NaOH溶液体积V[NaOH(aq)]的变化关系如图所示。
[比如A2−的分布系数: ]。下列叙述正确的是
A.曲线①代表 (H A),曲线②代表 (HA-)
2
B.该实验可选用酚酞或甲基橙为指示剂
C.V[NaOH(aq)]=30mL时,溶液中2c(A2-) + c(HA-) > c(Na+)
D.HA-的电离常数K =1.0×10-5
a
二、非选择题:本题共4道题,共55分。
16.(12分)平衡思想与生命活动、日常生活、工农业生产和环境保护等息息相关。请回
答以下问题。
(1)在饮用水、食物或牙膏中添加氟化物,氟离子能与釉质层(主要成分羟基磷灰石)
发生反应,生成氟磷灰石,能起到预防龋齿的作用。因为氟磷灰石的溶解度
羟基磷灰石的溶解度(填“大于”或“小于”)。
(2)明矾[化学式为KAl(SO )·12HO]溶液呈 性(填“酸”“碱”或“中”),
4 2 2
原因是
(用离子方程式表示)。
(3)草木灰与铵态氮肥不能混合施用,其原因是 。
(4)工业上处理废水时,Na S和FeS均可用于除去废水中的Hg2+,试解释原因(用离子
2
方程式表示) 、 。17.(15分)苯甲酸( )具有弱酸性,其能抑制微生物生长、延长产品保质期,在
医药、食品、化妆品等行业中作为酸化剂或防腐添加剂使用。
部分物质的电离常数如下表所示。
酸 电离平衡常数(25℃)
亚硫酸 K =1.4×10-2 K =6.0×10-8
a1 a2
苯甲酸 K =6.4×10-5
a
(1)足量的苯甲酸与亚硫酸钠溶液反应的离子方程式 。
(2)下列四种溶质能发生水解反应的是 (填标号,下同);常温下,
下列溶液中,由水电离出的c(H+)由小到大的排列顺序是 。
① 0.1 mol/L 苯甲酸钠溶液 ② 0.1 mol/L NaHSO 溶液
3
③ 0.1 mol/L Na SO 溶液 ④ 0.1 mol/L NaOH溶液
2 3
(3)兴趣小组为测定常温下饱和苯甲酸溶液的浓度,设计了酸碱中和滴定方法。
操作步骤:量取50.00 mL待测饱和苯甲酸溶液置于锥形瓶中,滴加2滴指示剂;将
0.1000 mol·L-1 NaOH溶液盛装于滴定管中进行滴定,达到滴定终点并记录 NaOH
溶液的最终读数,再重复滴定3次,记录数据如下:
滴定次数 1 2 3 4
V(苯甲酸)/mL 50.00 50.00 50.00 50.00
V[NaOH(aq)](消耗)/mL 14.95 14.00 14.02 13.98
①该滴定过程中应选用的指示剂为________(填“酚酞”或“甲基橙”)。
②滴定至终点的现象为____________________________________________________。
③滴定后所得溶液呈碱性的原因是_____________________(用离子方程式解释)。
④由上述滴定结果可计算得c(苯甲酸)=________mol·L-1。
⑤若出现下列情况,测定结果偏高的是________(填标号)。
A.用蒸馏水清洗滴定管后,未用NaOH标准液润洗
B.滴定前用蒸馏水冲洗锥形瓶
C.在振荡锥形瓶时不慎将瓶内溶液溅出
D.滴定至终点时,俯视读数18.(14分)Ⅰ.甲烷和二氧化碳重整是制取甲醇合成气(CO和H)的重要方法,主要反
2
应有:
① CH (g)+CO (g) 2CO(g)+2H (g) ΔH
4 2 2 1
② CO (g)+H (g) CO(g)+H O(g) ΔH
2 2 2 2
③ CH (g)+ H O(g) CO(g)+3H (g) ΔH
4 2 2 3
(1)已知反应①、②、③的化学平衡常数分别为K 、K 、K ,则K =
1 2 3 1
(用K 、K 表示)。
2 3
(2)恒温恒容条件下,可提高CH 转化率的措施有 (填标号)。
4
a.增加原料中CH 的量 b.增加原料中CO 的量 c.通入Ar气
4 2
(3)恒温恒压密闭容器中,投入不同物质的量之比的 CH /CO /Ar混合气发生反应,若
4 2
使平衡体系中n(H ):n(CO)的值增大,投料组成中 Ar含量应 (填“增
2
大”或“减小”)。
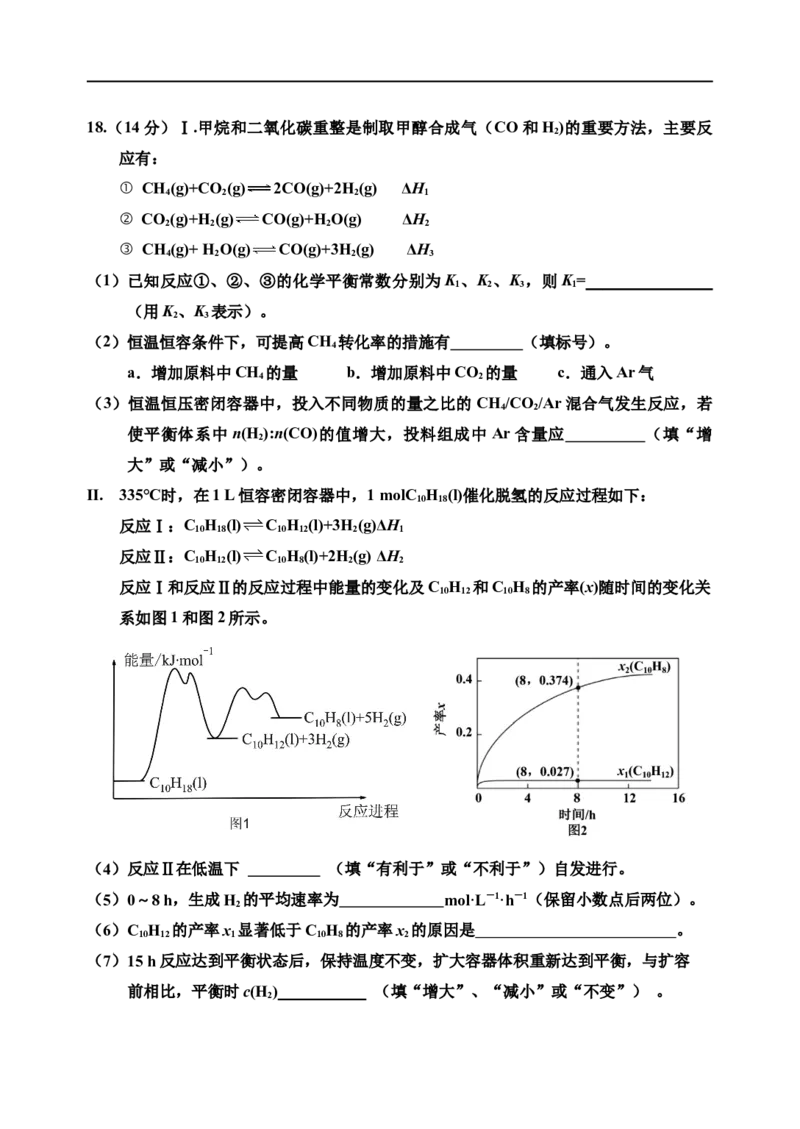
Ⅱ. 335℃时,在1 L恒容密闭容器中,1 molC H (l)催化脱氢的反应过程如下:
10 18
反应Ⅰ:C H (l) C H (l)+3H (g)ΔH
10 18 10 12 2 1
反应Ⅱ:C H (l) C H(l)+2H (g) ΔH
10 12 10 8 2 2
反应Ⅰ和反应Ⅱ的反应过程中能量的变化及C H 和C H 的产率(x)随时间的变化关
10 12 10 8
系如图1和图2所示。
(4)反应Ⅱ在低温下 (填“有利于”或“不利于”)自发进行。
(5)0~8 h,生成H 的平均速率为 mol·L-1·h-1(保留小数点后两位)。
2
(6)C H 的产率x 显著低于C H 的产率x 的原因是 。
10 12 1 10 8 2
(7)15 h反应达到平衡状态后,保持温度不变,扩大容器体积重新达到平衡,与扩容
前相比,平衡时c(H ) (填“增大”、“减小”或“不变”) 。
219.(14分)2025年8月成都世界运动会开幕式上的烟花表演,用珙桐树幻化的“和平
之花”惊艳世界。其中无硫复合还原剂W49的研发,在一定程度上缓解了燃放后的
烟雾弥漫和化学残留。制备W49用到的BaSO 源于重晶石(重晶石主要成分为硫酸
4
钡,内含硫酸锶等杂质)。BaSO 提纯工艺流程如下:
4
氨水、
碳酸氢铵
稀盐酸 稀硫酸
粉碎 滤渣
重晶石 溶浸 酸解 分离 SrCl2溶液
浸出液 BaSO4(s) BaSO4(s)
已知:Ⅰ:25 ℃时,K (SrSO ) =3.3×10-7、K (SrCO )=5.6×10-10、
sp 4 sp 3
K (BaSO ) =1.1×10-10、K (BaCO ) =2.6×10-9
sp 4 sp 3
Ⅱ:锶(Sr)为第五周期IIA族元素,其化合物六水氯化锶(SrCl ·6HO)晶体
2 2
在61℃时开始失去结晶水
(1)溶浸前需将重晶石粉碎,其目的是 。
(2) 溶浸在 65℃~80℃进行,碳酸氢铵的用量大于理论量,其原因可能是
。
(3)酸解中SrCO 与盐酸反应的离子方程式为 。
3
(4)向粉碎的重晶石中直接加入BaCl 溶液,SrSO 转化反应的离子方程式为 ;
2 4
该反应的平衡常数为 。
(5)分离时,当Ba2+沉淀完全(离子浓度小于1×10-5 mol·L-1时,认为沉淀完全)时,
此时溶液中c(Sr2+)不大于 mol·L-1。
(6)由SrCl 溶液制备SrCl ·6HO的过程中各步骤的说法,正确的是 。
2 2 2
A.用60℃的热水浴加热蒸发至有晶膜出现
B.冷却结晶过程中应通入HCl气体
C.干燥SrCl ·6HO晶体可以采用减压干燥
2 2
命题、校对:高二化学命题组