文档内容
哈尔滨市第九中学 2024—2025 学年度上学期
十月月考高二化学考试试卷
(考试时间:75分钟 满分:100分)
第I卷(共45分)
一、选择题(本题共15小题,每小题3分,共45分,每小题只有一个选项符合题意)
1. 下列事实能用勒夏特列原理解释的是
A. 可用排饱和食盐水法收集 B. 将猪肉放入冰箱中冷藏
C. 平衡混合气体加压后颜色变深 D. 溶液中加少量 固体,促进 分
解
2. 反应 ,其反应速率方程为 。
下列措施能同时提高 平衡转化率和反应速率的是
A. 升高温度 B. 使用催化剂 C. 减小 的浓度 D. 增大容器体积
3. 向恒容密闭容器中充入一定体积的 ,发生反应 后达到平
衡。若保持温度不变,再充入相同体积的 ,达到新平衡后,与原平衡相比,下列值增大的是
A. B. 的转化率 C. 的体积分数 D.
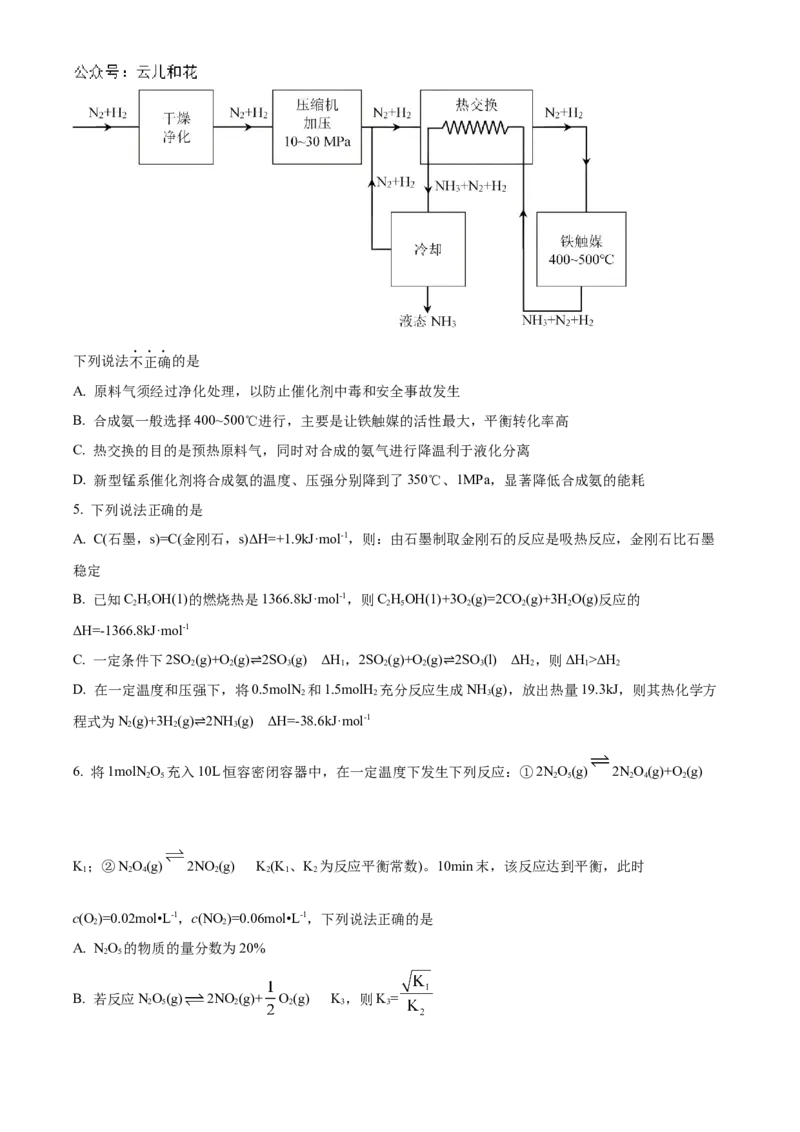
4. 氨对发展农业有着重要意义,也是重要的化工原料。合成氨的生产流程示意如下。下列说法不正确的是
A. 原料气须经过净化处理,以防止催化剂中毒和安全事故发生
B. 合成氨一般选择400~500℃进行,主要是让铁触媒的活性最大,平衡转化率高
C. 热交换的目的是预热原料气,同时对合成的氨气进行降温利于液化分离
D. 新型锰系催化剂将合成氨的温度、压强分别降到了350℃、1MPa,显著降低合成氨的能耗
5. 下列说法正确的是
A. C(石墨,s)=C(金刚石,s)ΔH=+1.9kJ·mol-1,则:由石墨制取金刚石的反应是吸热反应,金刚石比石墨
稳定
B. 已知C HOH(1)的燃烧热是1366.8kJ·mol-1,则C HOH(1)+3O (g)=2CO (g)+3HO(g)反应的
2 5 2 5 2 2 2
ΔH=-1366.8kJ·mol-1
C. 一定条件下2SO (g)+O(g) 2SO (g) ΔH ,2SO (g)+O(g) 2SO (l) ΔH,则ΔH>ΔH
2 2 3 1 2 2 3 2 1 2
D. 在一定温度和压强下,将⇌0.5molN
2
和1.5molH
2
充分反应生⇌成NH
3
(g),放出热量19.3kJ,则其热化学方
程式为N(g)+3H(g) 2NH (g) ΔH=-38.6kJ·mol-1
2 2 3
⇌
6. 将1molN O 充入10L恒容密闭容器中,在一定温度下发生下列反应:①2NO(g) 2NO(g)+O(g)
2 5 2 5 2 4 2
K;②NO(g) 2NO (g) K (K 、K 为反应平衡常数)。10min末,该反应达到平衡,此时
1 2 4 2 2 1 2
c(O )=0.02mol•L-1,c(NO )=0.06mol•L-1,下列说法正确的是
2 2
A. NO 的物质的量分数为20%
2 5
B. 若反应NO(g) 2NO (g)+ O(g) K ,则K=
2 5 2 2 3 3C. v(O )=0.02mol•L-1•min-1
2
.
D K•K=2×10-4
1 2
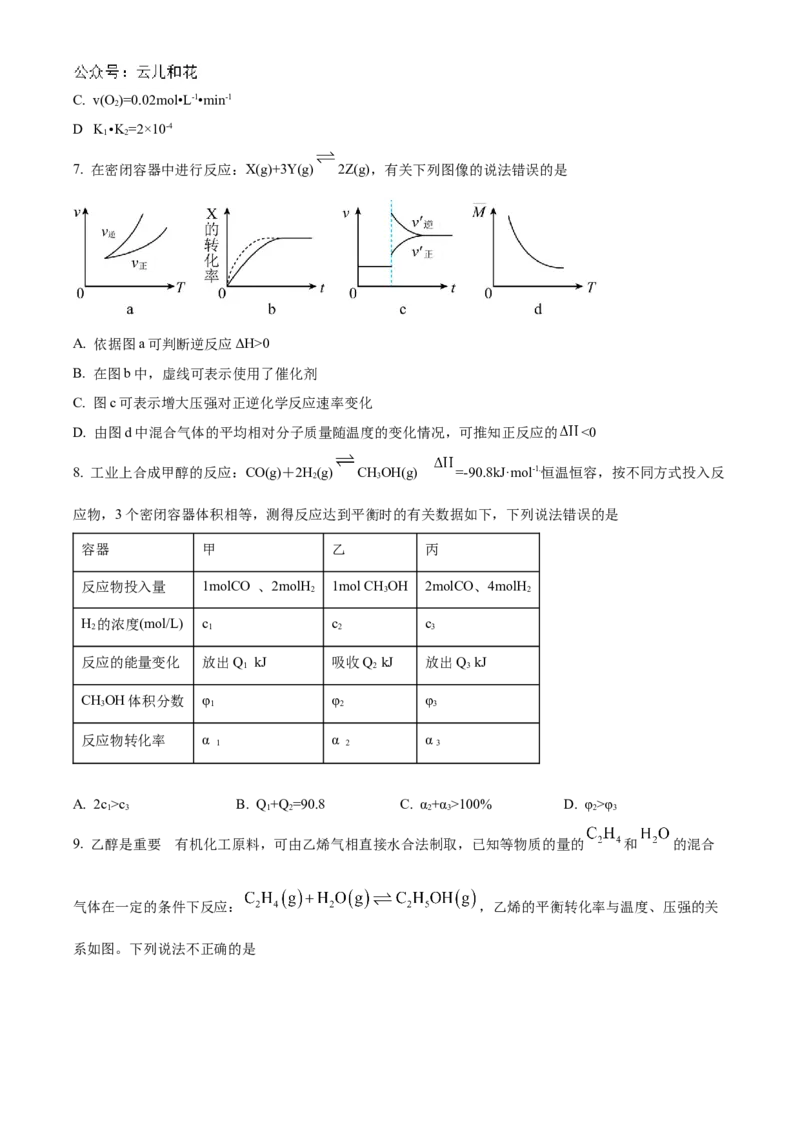
7. 在密闭容器中进行反应:X(g)+3Y(g) 2Z(g),有关下列图像的说法错误的是
A. 依据图a可判断逆反应ΔH>0
B. 在图b中,虚线可表示使用了催化剂
C. 图c可表示增大压强对正逆化学反应速率变化
D. 由图d中混合气体的平均相对分子质量随温度的变化情况,可推知正反应的 <0
8. 工业上合成甲醇的反应:CO(g)+2H(g) CHOH(g) =-90.8kJ·mol-1.恒温恒容,按不同方式投入反
2 3
应物,3个密闭容器体积相等,测得反应达到平衡时的有关数据如下,下列说法错误的是
容器 甲 乙 丙
反应物投入量 1molCO 、2molH 1mol CHOH 2molCO、4molH
2 3 2
H 的浓度(mol/L) c c c
2 1 2 3
反应的能量变化 放出Q kJ 吸收Q kJ 放出Q kJ
1 2 3
CHOH体积分数 φ φ φ
3 1 2 3
反应物转化率 α α α
1 2 3
A. 2c>c B. Q+Q =90.8 C. α +α >100% D. φ>φ
1 3 1 2 2 3 2 3
的
9. 乙醇是重要 有机化工原料,可由乙烯气相直接水合法制取,已知等物质的量的 和 的混合
气体在一定的条件下反应: ,乙烯的平衡转化率与温度、压强的关
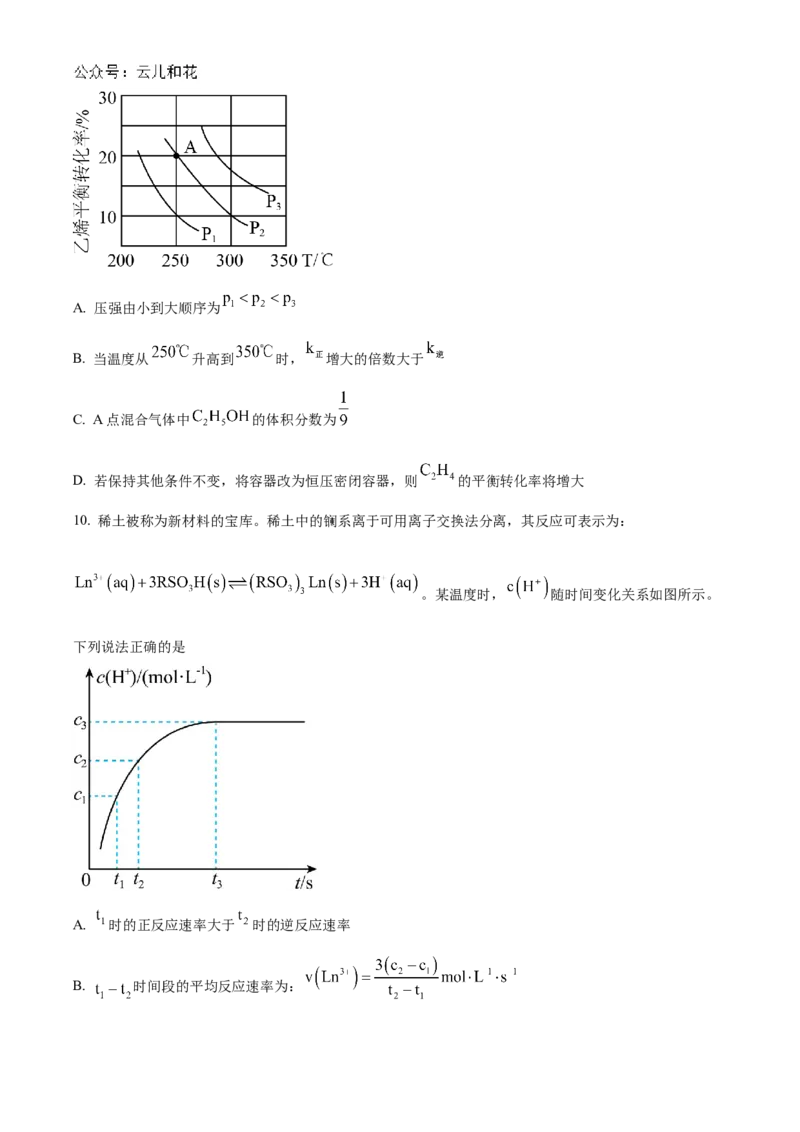
系如图。下列说法不正确的是A. 压强由小到大顺序为
B. 当温度从 升高到 时, 增大的倍数大于
C. A点混合气体中 的体积分数为
D. 若保持其他条件不变,将容器改为恒压密闭容器,则 的平衡转化率将增大
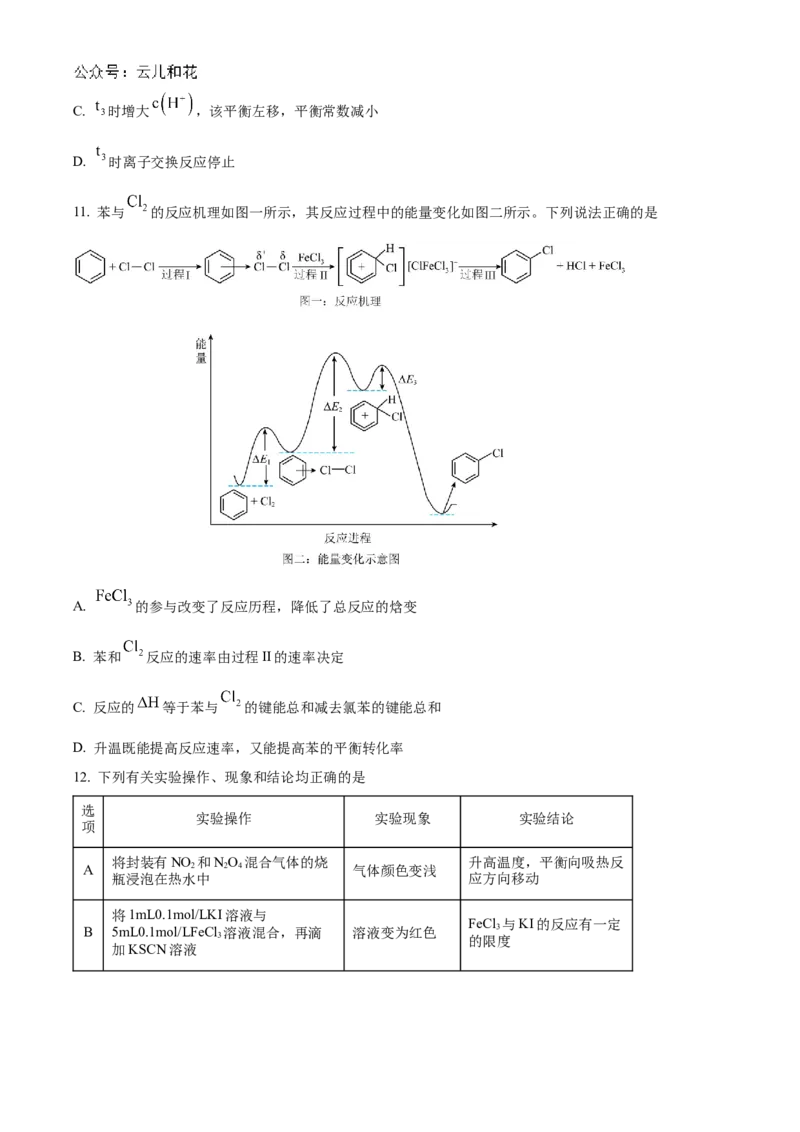
10. 稀土被称为新材料的宝库。稀土中的镧系离于可用离子交换法分离,其反应可表示为:
。某温度时, 随时间变化关系如图所示。
下列说法正确的是
A. 时的正反应速率大于 时的逆反应速率
B. 时间段的平均反应速率为:C. 时增大 ,该平衡左移,平衡常数减小
D. 时离子交换反应停止
11. 苯与 的反应机理如图一所示,其反应过程中的能量变化如图二所示。下列说法正确的是
A. 的参与改变了反应历程,降低了总反应的焓变
B. 苯和 反应的速率由过程II的速率决定
C. 反应的 等于苯与 的键能总和减去氯苯的键能总和
D. 升温既能提高反应速率,又能提高苯的平衡转化率
12. 下列有关实验操作、现象和结论均正确的是
选
实验操作 实验现象 实验结论
项
将封装有NO 和NO 混合气体的烧 升高温度,平衡向吸热反
A 2 2 4 气体颜色变浅
瓶浸泡在热水中 应方向移动
将1mL0.1mol/LKI溶液与
FeCl 与KI的反应有一定
B 5mL0.1mol/LFeCl 溶液混合,再滴 溶液变为红色 3
3 的限度
加KSCN溶液向两份等浓度、等体积的过氧化氢
前者产生气泡较
C 溶液中分别加入2滴等浓度的FeCl 催化效率:Fe3+>Cu2+
3 快
溶液和CuSO 溶液
4
分别取2mL0.5mol/LCuCl 溶液(绿 加热时溶液变为 其他条件不变时,升高温
2
色)加入两支试管中,将其中一支 黄绿色;置于冷 度,平衡向吸热反应方向
D
试管先加热,然后置于冷水中,与 水中,溶液由黄 移动;降低温度,平衡向
另一支试管的溶液颜色对比 绿色变为蓝绿色 放热反应方向移动
A. A B. B C. C D. D
13. T 时,向容积为5L的恒容密闭容器中充入一定量的A(g)和B(g),发生反应:
0
△H<0。反应过程中的部分数据如下表,下列说法错误的是
t/ n(A)/ n(B)/
min mol mol
0 4.0 2.0
5 2.0 1.0
10 2.0 1.0
A. 其他条件不变,温度变为T 时,平衡时测得C的浓度为0.8mol/L,则T>T
1 1 0
B. 8min时,该反应的 (正)= (逆)
C. 平衡时,D的体积分数约为14.3%
D. 5min时,向该容器中再充入4.0molA和2.0molB,达新平衡后,B的百分含量变大
14. 利用丙烷C H 在无氧条件下制备丙烯C H 的反应方程式为:
3 8 3 6
。向两个初始压强为0.1MPa的相同恒压容器Ⅰ、Ⅱ中都充入等物质的量的丙烷气体,
再向Ⅱ容器中充入一定量的水蒸气进行上述反应,达到化学平衡时,测得丙烷和丙烯的物质的量分数随温
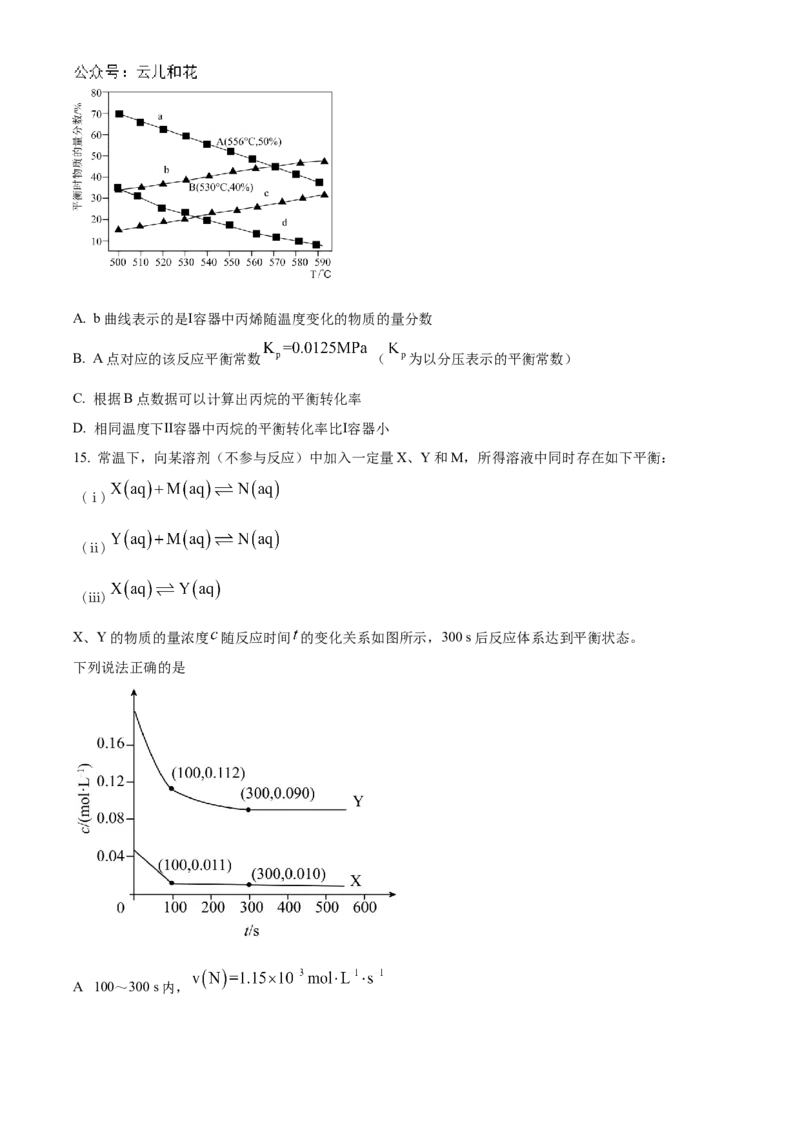
度变化如图所示,则下列说法正确的是A. b曲线表示的是Ⅰ容器中丙烯随温度变化的物质的量分数
B. A点对应的该反应平衡常数 ( 为以分压表示的平衡常数)
C. 根据B点数据可以计算出丙烷的平衡转化率
D. 相同温度下Ⅱ容器中丙烷的平衡转化率比Ⅰ容器小
15. 常温下,向某溶剂(不参与反应)中加入一定量X、Y和M,所得溶液中同时存在如下平衡:
(ⅰ)
(ⅱ)
(ⅲ)
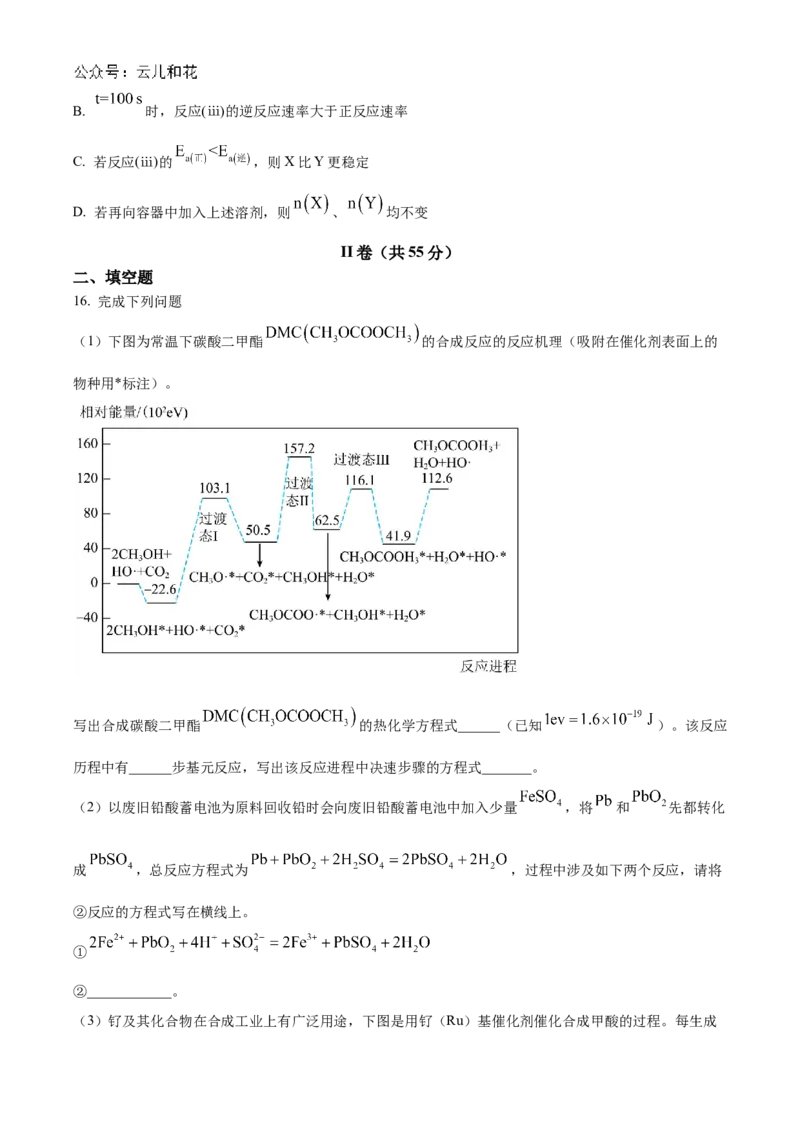
X、Y的物质的量浓度 随反应时间 的变化关系如图所示,300 s后反应体系达到平衡状态。
下列说法正确的是
.
A 100~300 s内,B. 时,反应(ⅲ)的逆反应速率大于正反应速率
C. 若反应(ⅲ)的 ,则X比Y更稳定
D. 若再向容器中加入上述溶剂,则 、 均不变
II卷(共55分)
二、填空题
16. 完成下列问题
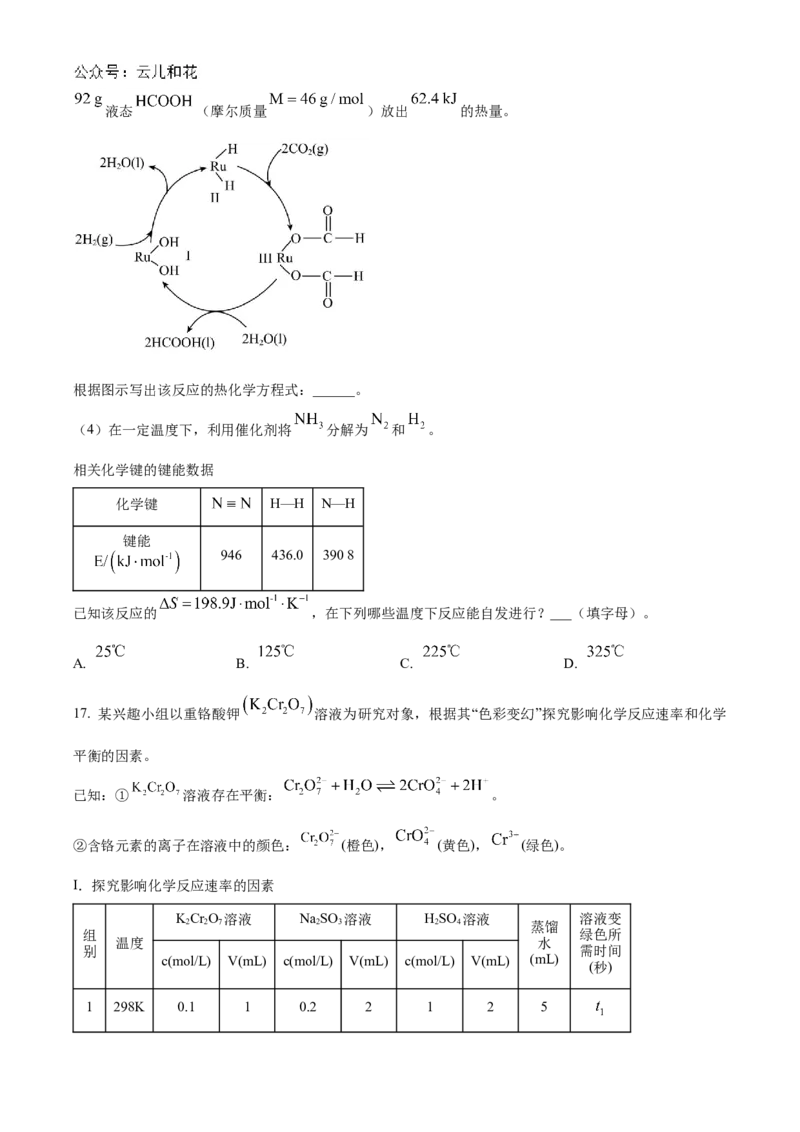
(1)下图为常温下碳酸二甲酯 的合成反应的反应机理(吸附在催化剂表面上的
物种用*标注)。
写出合成碳酸二甲酯 的热化学方程式______(已知 )。该反应
历程中有______步基元反应,写出该反应进程中决速步骤的方程式_______。
(2)以废旧铅酸蓄电池为原料回收铅时会向废旧铅酸蓄电池中加入少量 ,将 和 先都转化
成 ,总反应方程式为 ,过程中涉及如下两个反应,请将
②反应的方程式写在横线上。
①
②____________。
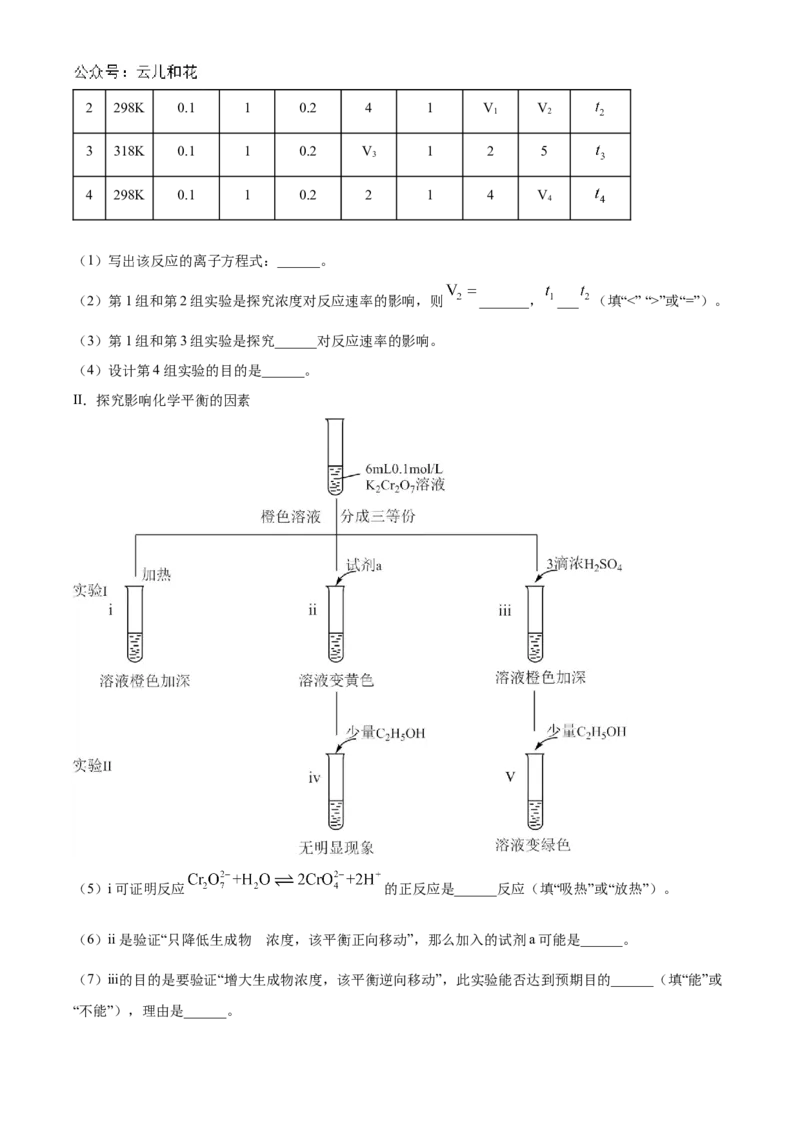
(3)钌及其化合物在合成工业上有广泛用途,下图是用钌(Ru)基催化剂催化合成甲酸的过程。每生成液态 (摩尔质量 )放出 的热量。
根据图示写出该反应的热化学方程式:______。
(4)在一定温度下,利用催化剂将 分解为 和 。
相关化学键的键能数据
化学键 H—H N—H
键能 .
946 436.0 3908
已知该反应的 ,在下列哪些温度下反应能自发进行?___(填字母)。
A. B. C. D.
17. 某兴趣小组以重铬酸钾 溶液为研究对象,根据其“色彩变幻”探究影响化学反应速率和化学
平衡的因素。
已知:① 溶液存在平衡: 。
②含铬元素的离子在溶液中的颜色: (橙色), (黄色), (绿色)。
I.探究影响化学反应速率的因素
KCr O 溶液 NaSO 溶液 HSO 溶液 溶液变
2 2 7 2 3 2 4 蒸馏
组 绿色所
温度 水
别 需时间
c(mol/L) V(mL) c(mol/L) V(mL) c(mol/L) V(mL) (mL)
(秒)
1 298K 0.1 1 0.2 2 1 2 52 298K 0.1 1 0.2 4 1 V V
1 2
3 318K 0.1 1 0.2 V 1 2 5
3
4 298K 0.1 1 0.2 2 1 4 V
4
(1)写出该反应的离子方程式:______。
(2)第1组和第2组实验是探究浓度对反应速率的影响,则 _______, ___ (填“<” “>”或“=”)。
(3)第1组和第3组实验是探究______对反应速率的影响。
(4)设计第4组实验的目的是______。
Ⅱ.探究影响化学平衡的因素
(5)i可证明反应 的正反应是______反应(填“吸热”或“放热”)。
的
(6)ii是验证“只降低生成物 浓度,该平衡正向移动”,那么加入的试剂a可能是______。
(7)ⅲ的目的是要验证“增大生成物浓度,该平衡逆向移动”,此实验能否达到预期目的______(填“能”或
“不能”),理由是______。(8)根据实验Ⅱ的现象,可得出结论:氧化性: ______ (填“>”、“<”或“=”)。
18. 一定条件下,水气变换反应 的中间产物是 。为探究该反应过程,研
究 的分解反应,常温下,在密封石英管内完全充满 水溶液,使 分
解,分解产物均完全溶于水。
I. Ⅱ.
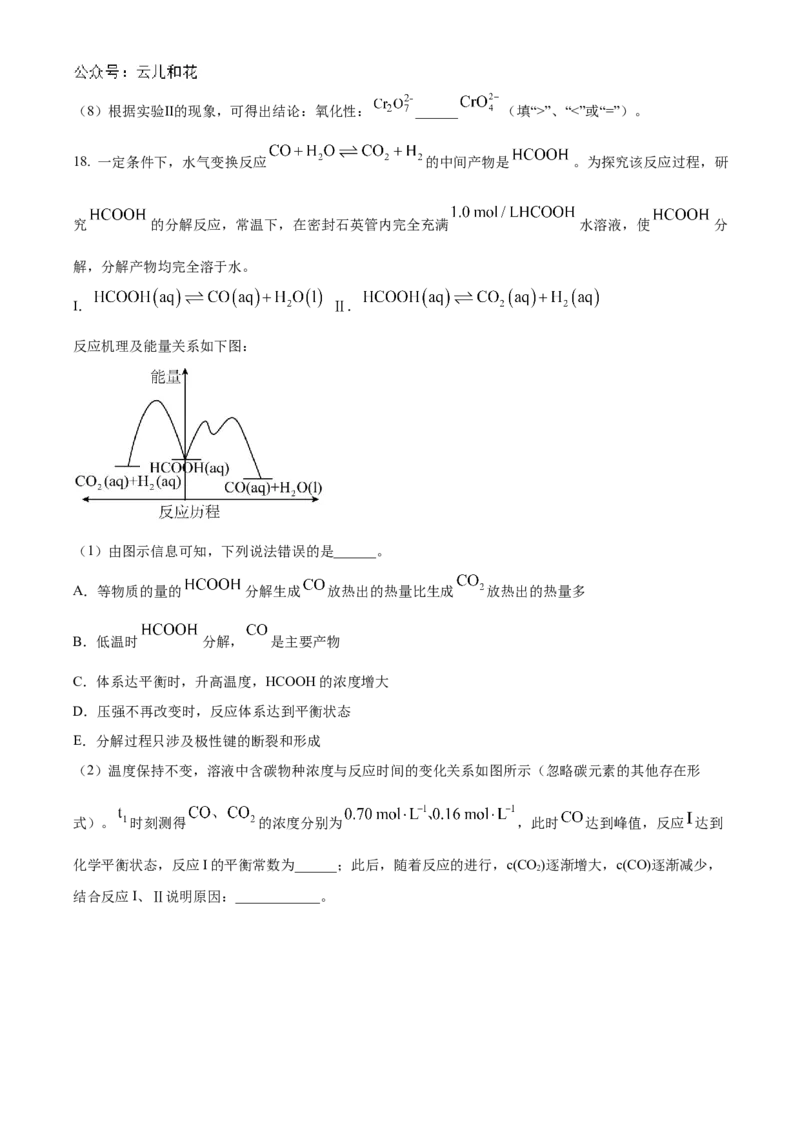
反应机理及能量关系如下图:
(1)由图示信息可知,下列说法错误的是______。
A.等物质的量的 分解生成 放热出的热量比生成 放热出的热量多
B.低温时 分解, 是主要产物
C.体系达平衡时,升高温度,HCOOH的浓度增大
D.压强不再改变时,反应体系达到平衡状态
E.分解过程只涉及极性键的断裂和形成
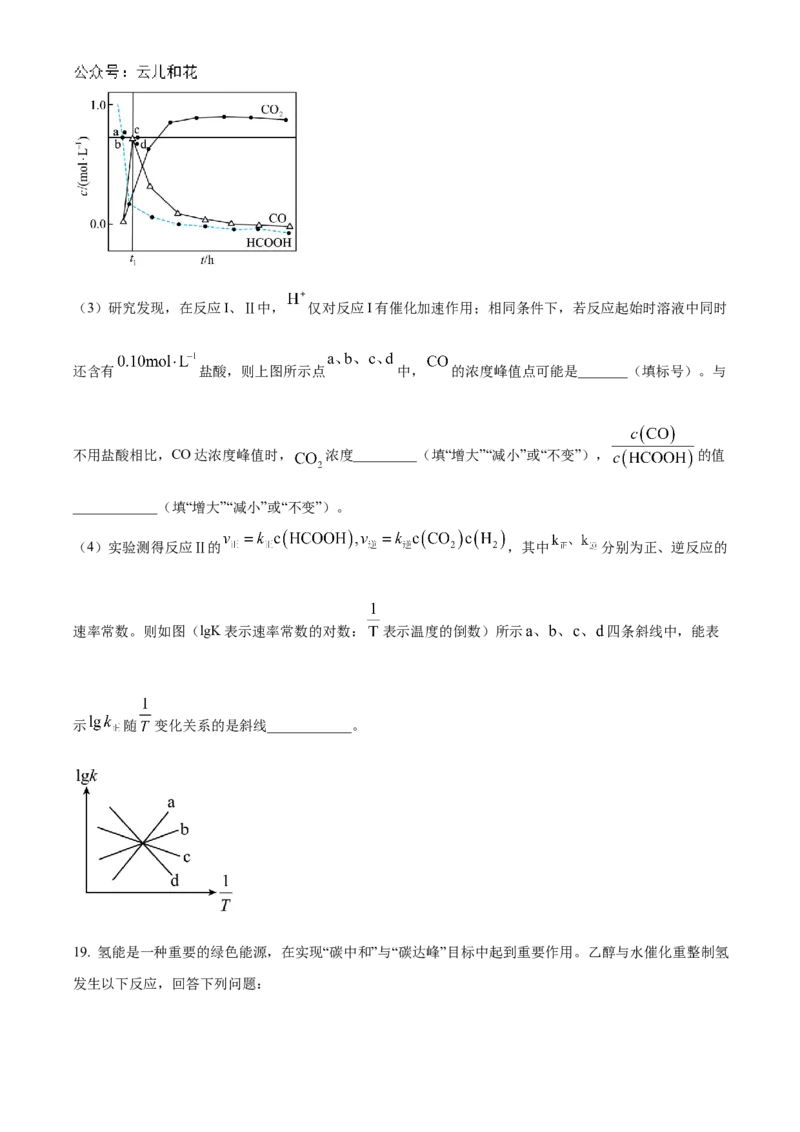
(2)温度保持不变,溶液中含碳物种浓度与反应时间的变化关系如图所示(忽略碳元素的其他存在形
式)。 时刻测得 的浓度分别为 ,此时 达到峰值,反应 达到
化学平衡状态,反应I的平衡常数为______;此后,随着反应的进行,c(CO)逐渐增大,c(CO)逐渐减少,
2
结合反应I、Ⅱ说明原因:____________。(3)研究发现,在反应I、Ⅱ中, 仅对反应I有催化加速作用;相同条件下,若反应起始时溶液中同时
还含有 盐酸,则上图所示点 中, 的浓度峰值点可能是_______(填标号)。与
不用盐酸相比,CO达浓度峰值时, 浓度_________(填“增大”“减小”或“不变”), 的值
____________(填“增大”“减小”或“不变”)。
(4)实验测得反应Ⅱ的 ,其中 分别为正、逆反应的
速率常数。则如图(lgK表示速率常数的对数: 表示温度的倒数)所示 四条斜线中,能表
示 随 变化关系的是斜线____________。
19. 氢能是一种重要的绿色能源,在实现“碳中和”与“碳达峰”目标中起到重要作用。乙醇与水催化重整制氢
发生以下反应,回答下列问题:反应I:
反应II:
(1)已知反应III:
则 __________(用含 和 的代数式表示)。
(2)将 和 加入容积为 的刚性密闭容器中,容器温度保持 ,下列不能表
示反应达到平衡的标志是____________(填编号)。
A. 的体积分数不再变 B.压强不再变化
C.混合气体的平均相对分子质量不再变化 D.混合气体密度不再变化
E. 不变
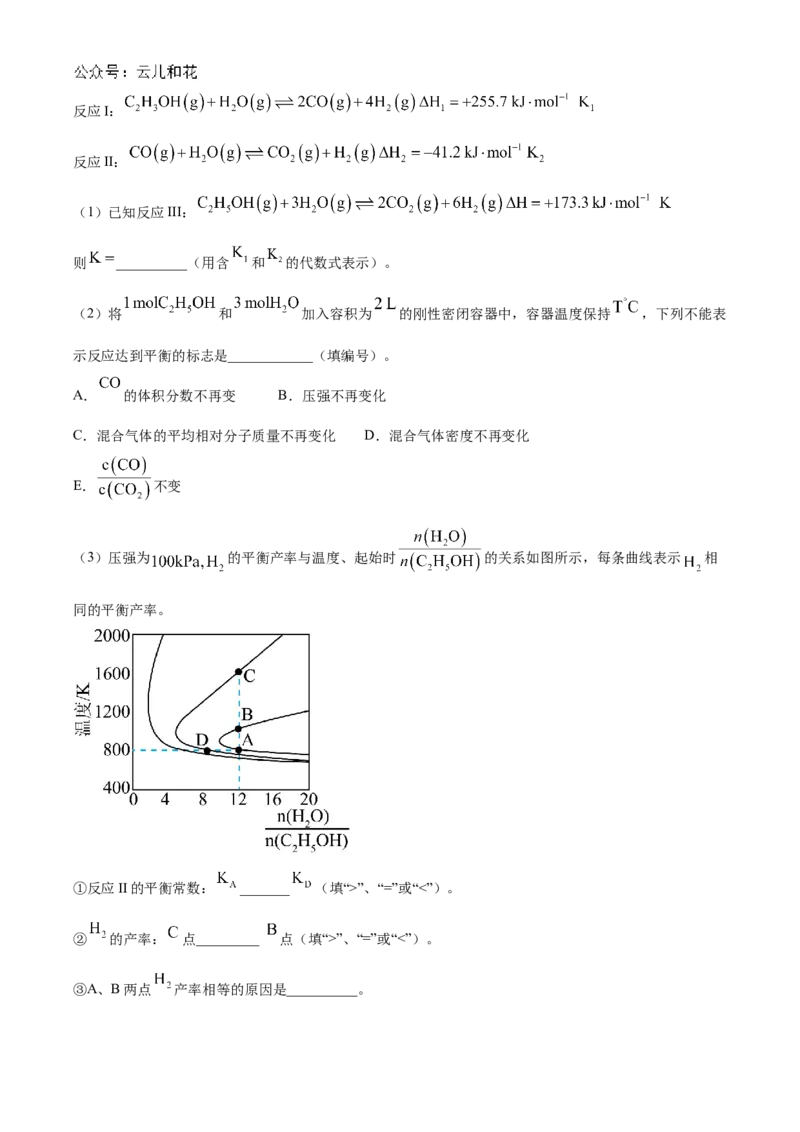
(3)压强为 的平衡产率与温度、起始时 的关系如图所示,每条曲线表示 相
同的平衡产率。
①反应II的平衡常数: _______ (填“>”、“=”或“<”)。
② 的产率: 点_________ 点(填“>”、“=”或“<”)。
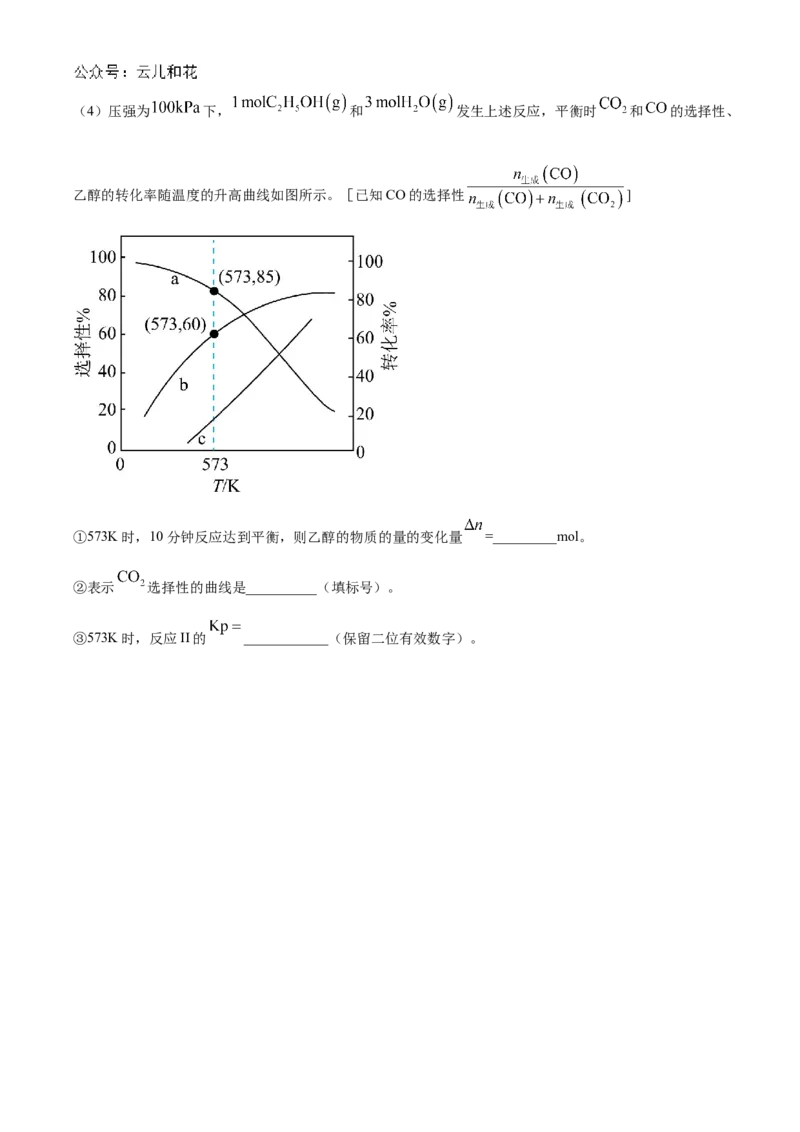
③A、B两点 产率相等的原因是__________。(4)压强为 下, 和 发生上述反应,平衡时 和 的选择性、
乙醇的转化率随温度的升高曲线如图所示。[已知CO的选择性 ]
①573K时,10分钟反应达到平衡,则乙醇的物质的量的变化量 =_________mol。
②表示 选择性的曲线是__________(填标号)。
③573K时,反应II的 ____________(保留二位有效数字)。哈尔滨市第九中学 2024—2025 学年度上学期
十月月考高二化学考试试卷
(考试时间:75分钟 满分:100分)
第I卷(共45分)
一、选择题(本题共15小题,每小题3分,共45分,每小题只有一个选项符合题意)
【1题答案】
【答案】A
【2题答案】
【答案】C
【3题答案】
【答案】A
【4题答案】
【答案】B
【5题答案】
【答案】C
【6题答案】
【答案】D
【7题答案】
【答案】C
【8题答案】
【答案】D
【9题答案】
【答案】B
【10题答案】
【答案】A
【11题答案】
【答案】B
【12题答案】
【答案】D
【13题答案】
【答案】A【14题答案】
【答案】B
【15题答案】
【答案】B
II卷(共55分)
二、填空题
【16题答案】
【答案】(1) ①. 2CHOH(l)+CO (g)= (l)+H O(l) ②. 3
3 2 2
③. CHOH*+HO·*=CH O·*+HO*
3 3 2
(2)
(3)H(g)+CO (g)= (g) (4)CD
2 2
【17题答案】
【答案】(1)
(2) ①. 3 ②. >
(3)温度 (4)探究相同条件下,硫酸溶液浓度对反应速率的影响
(5)放热 (6)KOH
(7) ①. 不能 ②. 加入浓硫酸,不但增加氢离子浓度平衡逆向移动的情况,同时考虑浓硫酸溶于
水放出大量的热的情况,浓硫酸溶于水放出大量的热,平衡也会逆向移动
(8)>
【18题答案】
【答案】(1)DE (2) ①. 5 ②. 反应I是快反应,达到平衡所需要的时间短,随着反应进行,
反应Ⅱ消耗HCOOH,使I的平衡逆向移动,c(CO)逐渐减少
(3) ①. b ②. 减小 ③. 不变
(4)c
【19题答案】
【答案】(1) ×
(2)D (3) ①. = ②. < ③. B点温度高于A点,升高温度,反应II逆向移动消耗氢气的
量与反应I、反应Ⅲ正向移动产生氢气的量相等(4) ①. 0.6 ②. a ③. 14.04