文档内容
2025 届高三第一学期阶段性检测卷(二)
化学
全卷满分100分,考试时间75分钟。
注意事项:
1.答题前,先将自己的姓名、准考证号填写在试卷和答题卡上,并将条形码粘贴在答题卡上
的指定位置。
2.请按题号顺序在答题卡上各题目的答题区域内作答,写在试卷、草稿纸和答题卡上的非答
题区域均无效。
3.选择题用2B铅笔在答题卡上把所选答案的标号涂黑;非选择题用黑色签字笔在答题卡上作
答;字体工整,笔迹清楚。
4.考试结束后,请将试卷和答题卡一并上交。
5.本卷主要考查内容:化学物质及其变化、物质的量、化学实验基础知识(60%),其余高考内
容(40%)。
可能用到的相对原子质量:H:1 Li:7 O:16 Mg:24 Zn:65 As:75
一、选择题:本题共14小题,每小题3分,共42分。在每小题给出的四个选项中,只有一
项是符合题目要求的。
1. 氧化还原反应广泛地存在于生产和生活之中。下列过程中不涉及氧化还原反应的是
A. 金属的冶炼 B. 金属的腐蚀 C. 食物的腐败 D. 煅烧石灰石
2. 下列关于物质分类的组合正确的是
碱性氧化
选项 碱 酸 盐 酸性氧化物
物
七氧化二
A 熟石灰 硫酸 小苏打 干冰
锰
B 烧碱 苯甲酸 氯化钠 氧化钠 一氧化碳
C 苛性钠 硝酸 碳酸钙 氧化铁 三氧化硫
D 石灰水 冰醋酸( ) 胆矾( ) 氧化钠 二氧化硫
A. A B. B C. C D. D
3. 《本草纲目》中记载了豆腐的造法:“水浸碎,滤去滓,煎成,以盐卤汁或山矾叶或酸浆、醋淀就釜收之。又有入缸内,以石膏末收者”。其中涉及胶体的有关知识,下列叙述错误的是
A. 豆浆中的分散质微粒直径的范围主要是
B. 用激光笔照射稀豆浆,会出现光亮的“通路”
C. 采用过滤操作对胶体进行提纯、精制
D. 豆浆凝聚成豆腐的原理与江河入海口形成“三角洲”类似
4. 下列反应的离子方程式正确的是
A. 向澄清石灰水中滴加碳酸钠溶液:
B. 氢氧化钡溶液与硫酸铜溶液混合:
C. 氢氧化镁溶于盐酸中:
D. Cu与 溶液反应:
5. 某化学兴趣小组进行如下实验:
实验① 向 晶体中滴加浓盐酸,产生黄绿色气体 ;
实验② 向 溶液中通入少量实验①中产生的 ,溶液变为黄色;
实验③ 取实验②中生成的溶液滴在淀粉KI试纸上,试纸变为蓝色。
下列判断正确的是
A. 上述实验证明氧化性:
B. 上述实验中,共有两个氧化还原反应
C. 不能使湿润的淀粉KI试纸变蓝
D. 实验②证明 既有氧化性又有还原性
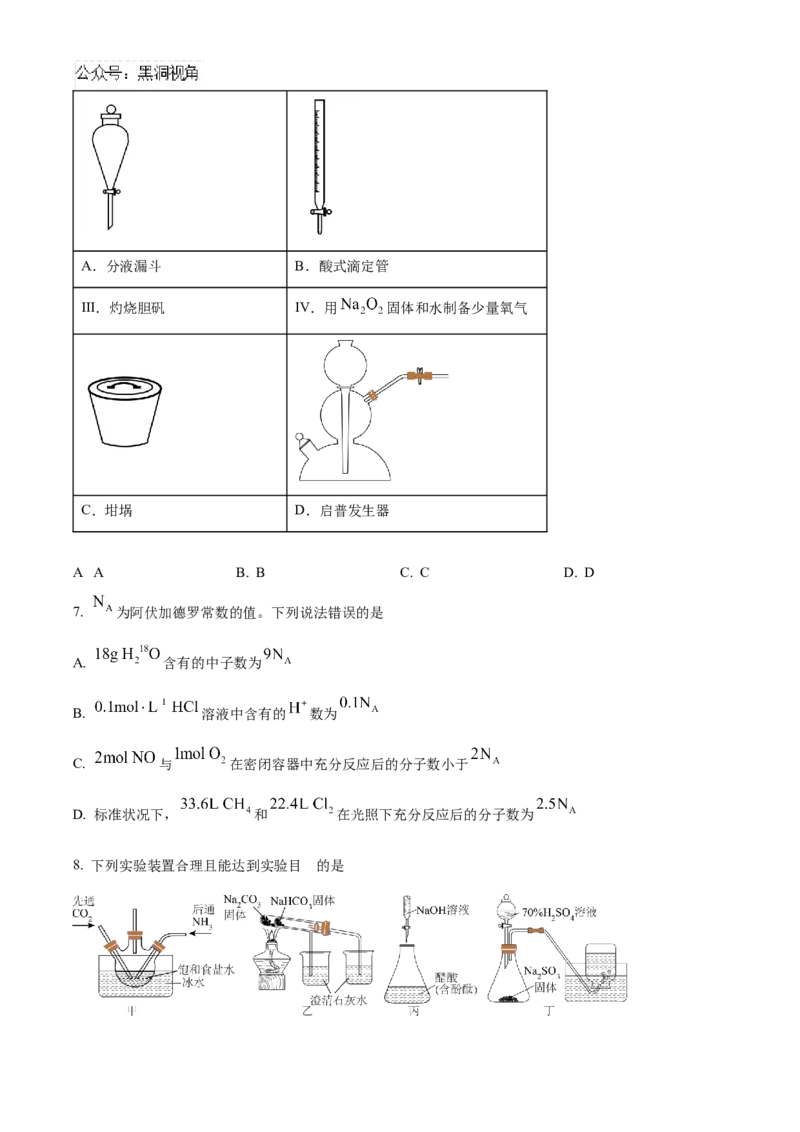
6. 实验室进行下列操作时,仪器选用错误的是
Ⅰ.用四氯化碳提取碘水中的碘 Ⅱ.量取一定体积的酸性 溶液A.分液漏斗 B.酸式滴定管
Ⅲ.灼烧胆矾 Ⅳ.用 固体和水制备少量氧气
C.坩埚 D.启普发生器
.
A A B. B C. C D. D
7. 为阿伏加德罗常数的值。下列说法错误的是
A. 含有的中子数为
B. 溶液中含有的 数为
C. 与 在密闭容器中充分反应后的分子数小于
D. 标准状况下, 和 在光照下充分反应后的分子数为
的
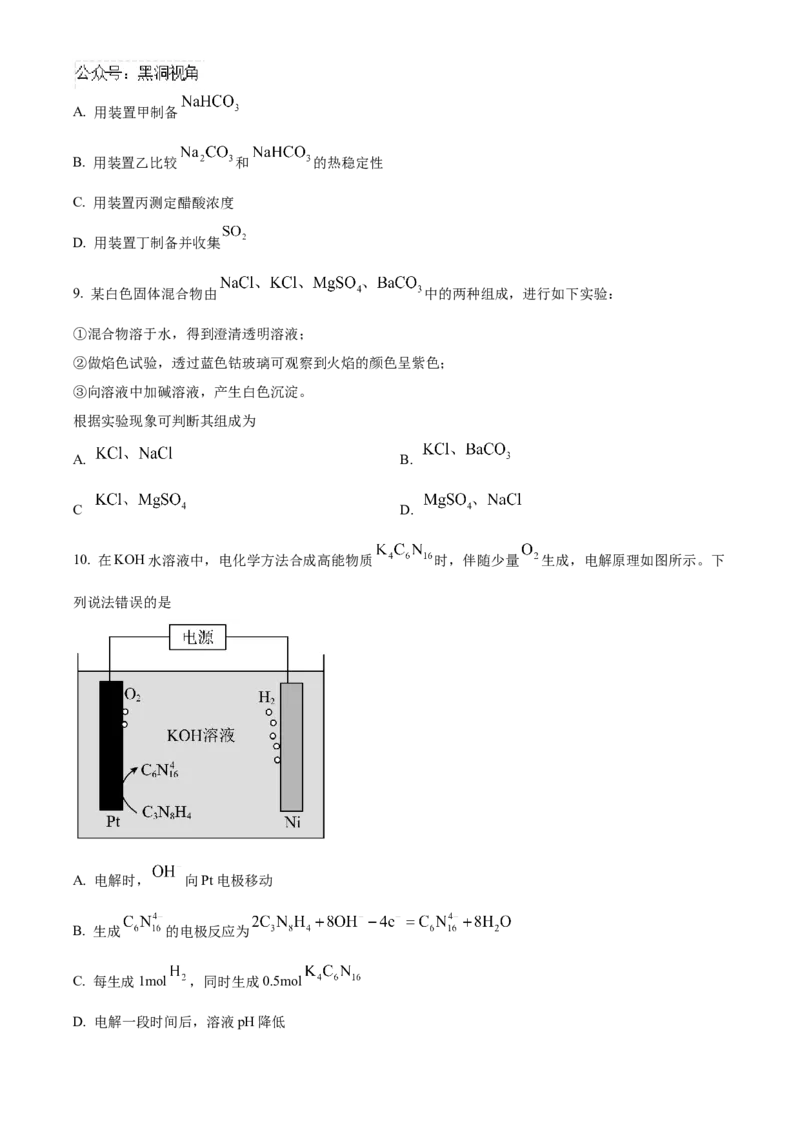
8. 下列实验装置合理且能达到实验目 的是A. 用装置甲制备
B. 用装置乙比较 和 的热稳定性
C. 用装置丙测定醋酸浓度
D. 用装置丁制备并收集
9. 某白色固体混合物由 中的两种组成,进行如下实验:
①混合物溶于水,得到澄清透明溶液;
②做焰色试验,透过蓝色钴玻璃可观察到火焰的颜色呈紫色;
③向溶液中加碱溶液,产生白色沉淀。
根据实验现象可判断其组成为
A. B.
.
C D.
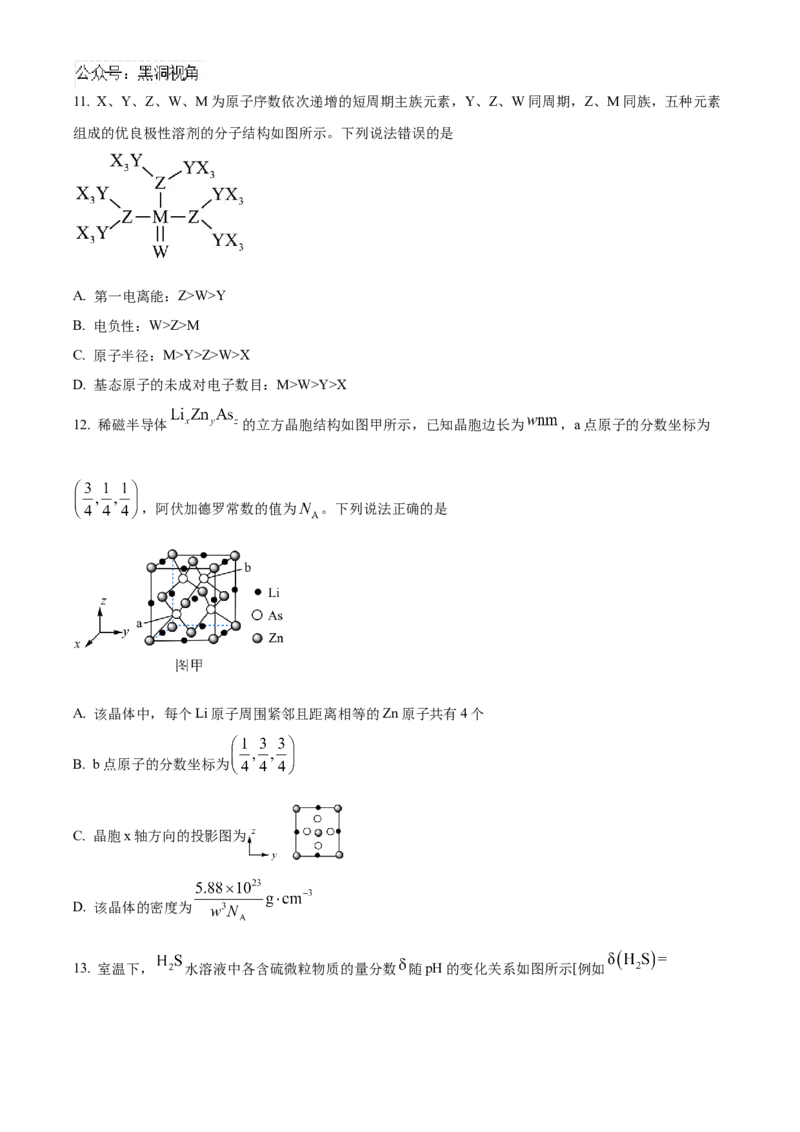
10. 在KOH水溶液中,电化学方法合成高能物质 时,伴随少量 生成,电解原理如图所示。下
列说法错误的是
A. 电解时, 向Pt电极移动
B. 生成 的电极反应为
C. 每生成1mol ,同时生成0.5mol
D. 电解一段时间后,溶液pH降低11. X、Y、Z、W、M为原子序数依次递增的短周期主族元素,Y、Z、W同周期,Z、M同族,五种元素
组成的优良极性溶剂的分子结构如图所示。下列说法错误的是
A. 第一电离能:Z>W>Y
B. 电负性:W>Z>M
C. 原子半径:M>Y>Z>W>X
D. 基态原子的未成对电子数目:M>W>Y>X
12. 稀磁半导体 的立方晶胞结构如图甲所示,已知晶胞边长为 ,a点原子的分数坐标为
,阿伏加德罗常数的值为 。下列说法正确的是
A. 该晶体中,每个Li原子周围紧邻且距离相等的Zn原子共有4个
B. b点原子的分数坐标为
C. 晶胞x轴方向的投影图为
D. 该晶体的密度为
13. 室温下, 水溶液中各含硫微粒物质的量分数 随pH的变化关系如图所示[例如]。已知:室温下, , ,
溶液中 的水解率为62%。下列说法错误的是
A. 室温下, 的 和 分别为 、 ;溶解度:FeS小于
B. 以酚酞为指示剂(变色的pH范围为8.2~10.0),用NaOH标准溶液可准确滴定 水溶液的浓度
C. 等物质的量浓度的 和NaHS混合溶液中存在关系:
D. 溶液中加入等体积 溶液,反应初始生成的沉淀是FeS和
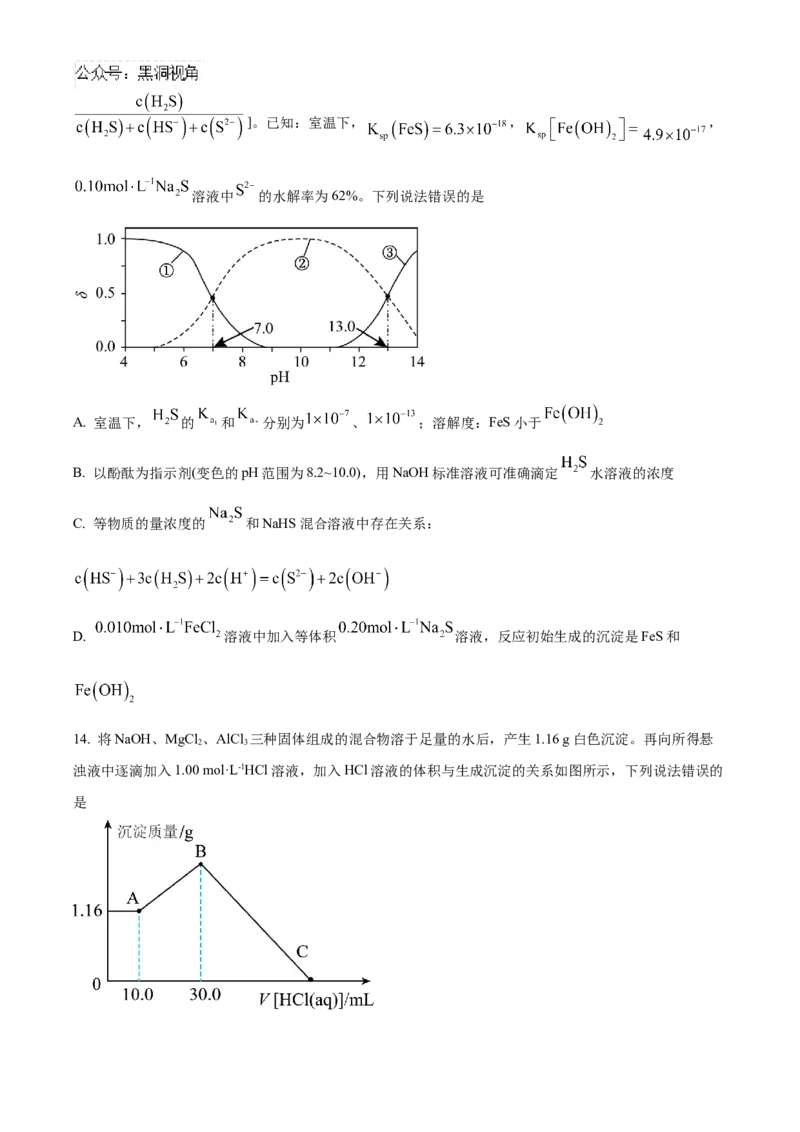
14. 将NaOH、MgCl 、AlCl 三种固体组成的混合物溶于足量的水后,产生1.16 g白色沉淀。再向所得悬
2 3
浊液中逐滴加入1.00 mol·L-1HCl溶液,加入HCl溶液的体积与生成沉淀的关系如图所示,下列说法错误的
是的
A. 1.16 g白色沉淀为Mg(OH) ,B点 沉淀为Mg(OH) 和Al(OH)
2 2 3
B. A点到B点发生反应的离子方程式为 +H++HO=Al(OH) ↓
2 3
C. C点时,加入HCl溶液的总体积为130 mL
D. 原混合物中MgCl 和AlCl 的物质的量之比为1:2
2 3
二、非选择题:本题共4小题,共58分。
15. 兴趣小组在课外实验中意外发现:将镁条放入 溶液中,快速产生较多气泡,有白色沉淀生成,
小组同学对此进行了系列探究活动。
探究1:反应产生的气体是什么?
【作出猜想】小组同学经查阅资料和讨论,作出如下猜想,气体可能是:①氢气;②二氧化碳;③氢气和
二氧化碳。
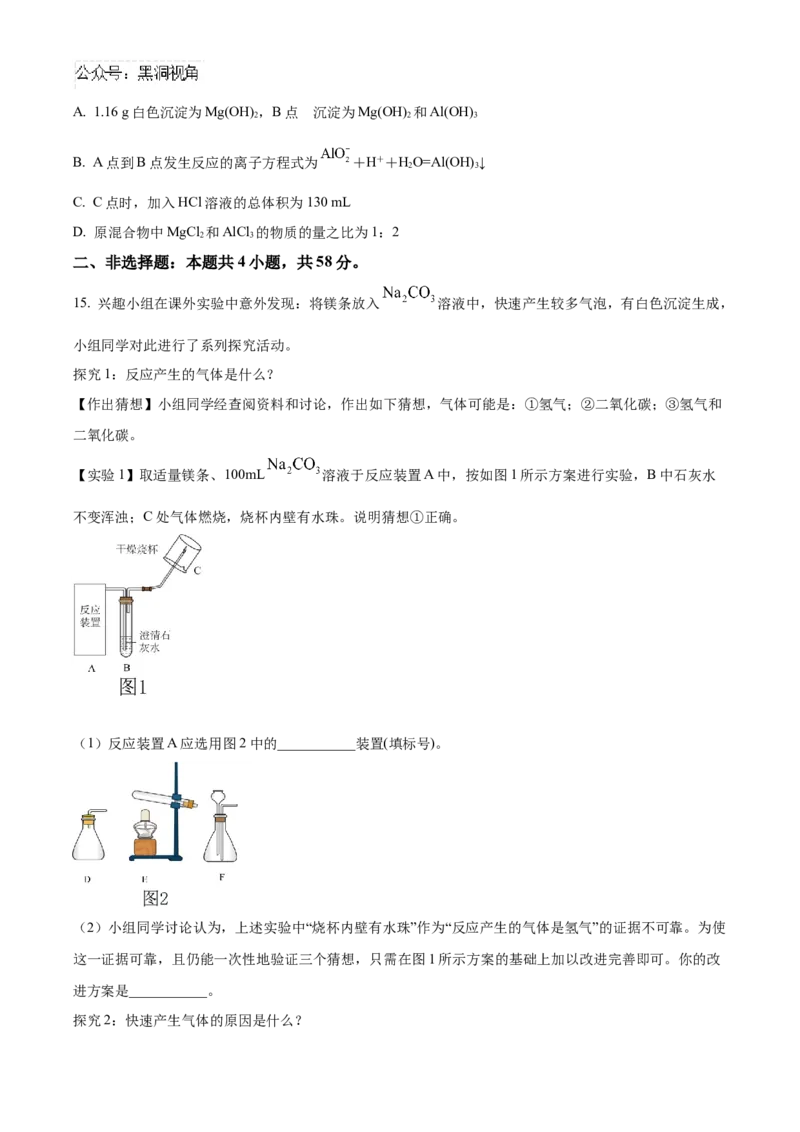
【实验1】取适量镁条、100mL 溶液于反应装置A中,按如图1所示方案进行实验,B中石灰水
不变浑浊;C处气体燃烧,烧杯内壁有水珠。说明猜想①正确。
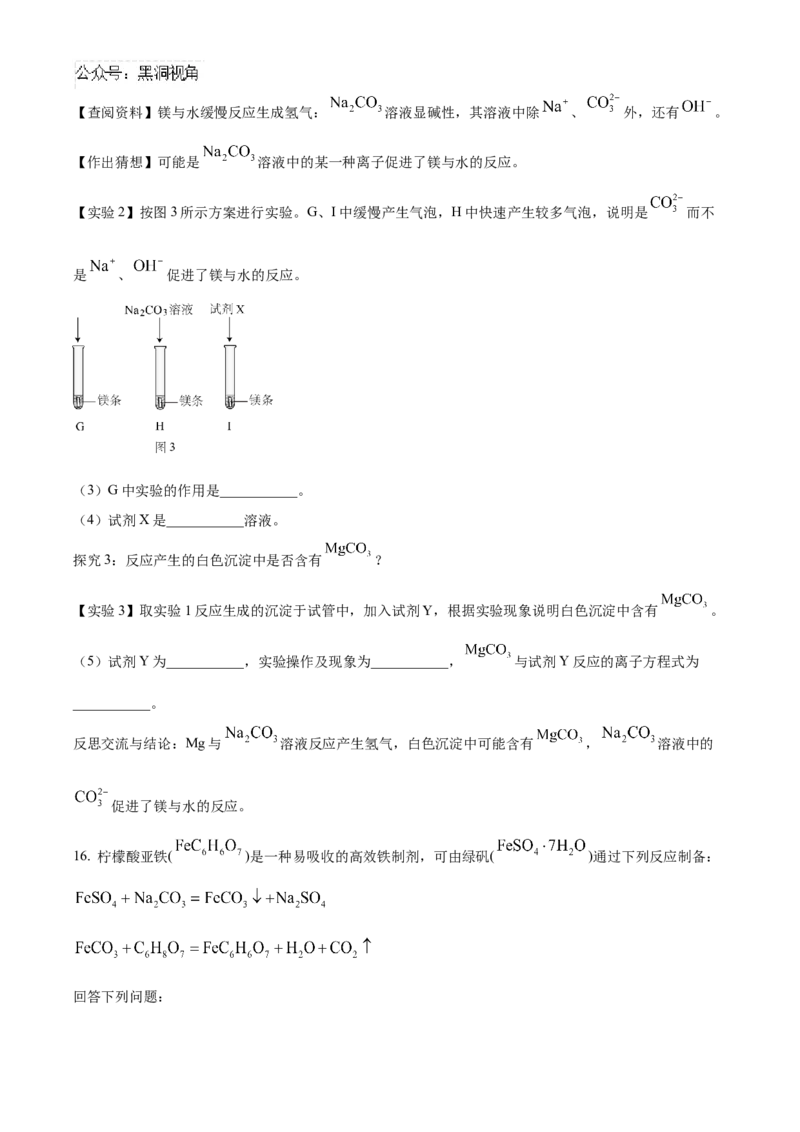
(1)反应装置A应选用图2中的___________装置(填标号)。
(2)小组同学讨论认为,上述实验中“烧杯内壁有水珠”作为“反应产生的气体是氢气”的证据不可靠。为使
这一证据可靠,且仍能一次性地验证三个猜想,只需在图1所示方案的基础上加以改进完善即可。你的改
进方案是___________。
探究2:快速产生气体的原因是什么?【查阅资料】镁与水缓慢反应生成氢气: 溶液显碱性,其溶液中除 、 外,还有 。
【作出猜想】可能是 溶液中的某一种离子促进了镁与水的反应。
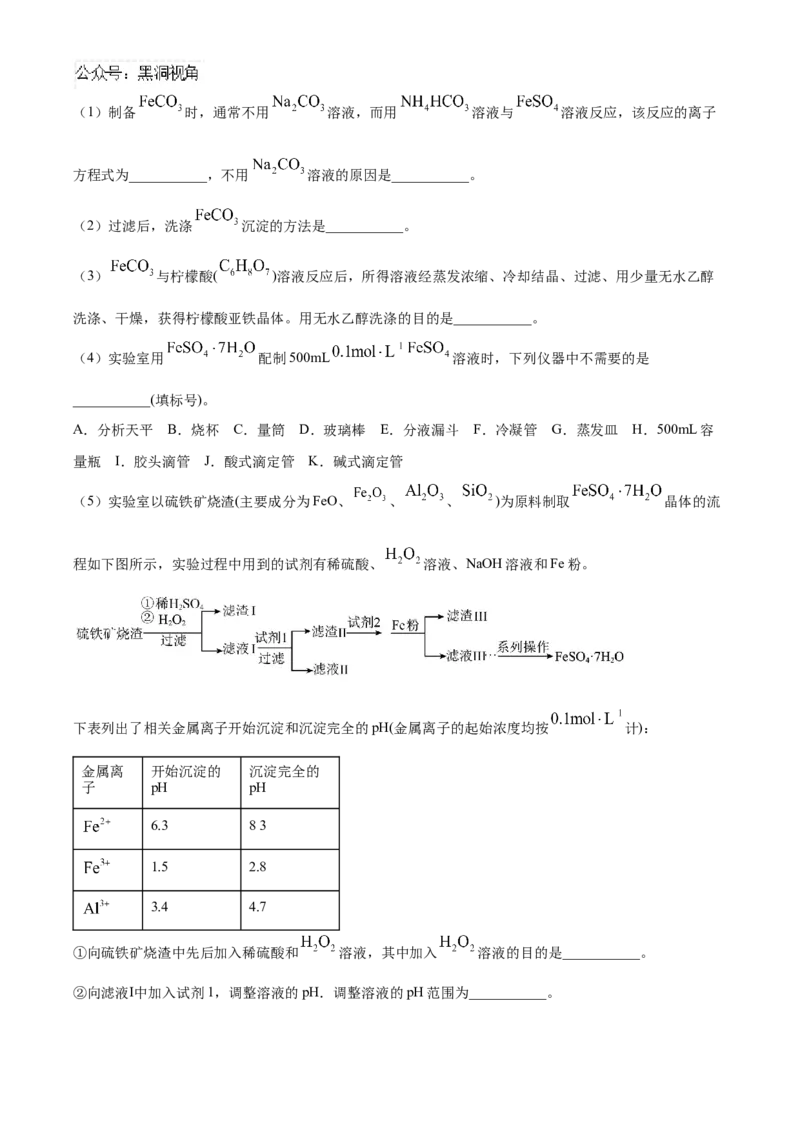
【实验2】按图3所示方案进行实验。G、I中缓慢产生气泡,H中快速产生较多气泡,说明是 而不
是 、 促进了镁与水的反应。
(3)G中实验的作用是___________。
(4)试剂X是___________溶液。
探究3:反应产生的白色沉淀中是否含有 ?
【实验3】取实验1反应生成的沉淀于试管中,加入试剂Y,根据实验现象说明白色沉淀中含有 。
(5)试剂Y为___________,实验操作及现象为___________, 与试剂Y反应的离子方程式为
___________。
反思交流与结论:Mg与 溶液反应产生氢气,白色沉淀中可能含有 , 溶液中的
促进了镁与水的反应。
16. 柠檬酸亚铁( )是一种易吸收的高效铁制剂,可由绿矾( )通过下列反应制备:
回答下列问题:(1)制备 时,通常不用 溶液,而用 溶液与 溶液反应,该反应的离子
方程式为___________,不用 溶液的原因是___________。
(2)过滤后,洗涤 沉淀的方法是___________。
(3) 与柠檬酸( )溶液反应后,所得溶液经蒸发浓缩、冷却结晶、过滤、用少量无水乙醇
洗涤、干燥,获得柠檬酸亚铁晶体。用无水乙醇洗涤的目的是___________。
(4)实验室用 配制500mL 溶液时,下列仪器中不需要的是
___________(填标号)。
A.分析天平 B.烧杯 C.量筒 D.玻璃棒 E.分液漏斗 F.冷凝管 G.蒸发皿 H.500mL容
量瓶 I.胶头滴管 J.酸式滴定管 K.碱式滴定管
(5)实验室以硫铁矿烧渣(主要成分为FeO、 、 、 )为原料制取 晶体的流
程如下图所示,实验过程中用到的试剂有稀硫酸、 溶液、NaOH溶液和Fe粉。
下表列出了相关金属离子开始沉淀和沉淀完全的pH(金属离子的起始浓度均按 计):
金属离 开始沉淀的 沉淀完全的
子 pH pH
.
6.3 83
1.5 2.8
3.4 4.7
①向硫铁矿烧渣中先后加入稀硫酸和 溶液,其中加入 溶液的目的是___________。
②向滤液Ⅰ中加入试剂1,调整溶液的pH.调整溶液的pH范围为___________。17. 、 常用于制造农药等,磷在氯气中燃烧生成这两种卤化磷。回答下列问题:
(1)已知:①
② ( )
则 _______ 。
(2)实验测得 的速率方程为 (k为速率常数,只
与温度、催化剂有关),速率常数k与活化能的经验关系式为 (R、C为常数, 为活化能,
T为热力学温度)。
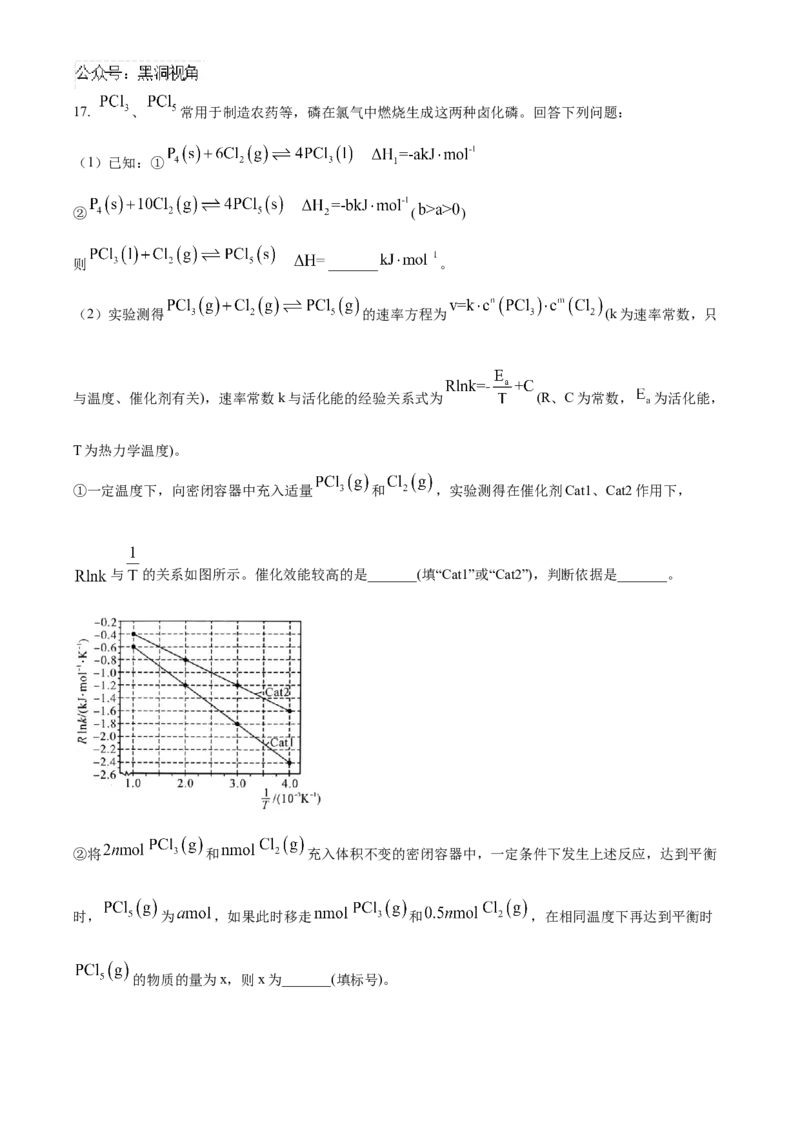
①一定温度下,向密闭容器中充入适量 和 ,实验测得在催化剂Cat1、Cat2作用下,
与 的关系如图所示。催化效能较高的是_______(填“Cat1”或“Cat2”),判断依据是_______。
②将 和 充入体积不变的密闭容器中,一定条件下发生上述反应,达到平衡
时, 为 ,如果此时移走 和 ,在相同温度下再达到平衡时
的物质的量为x,则x为_______(填标号)。A. B. C. D.
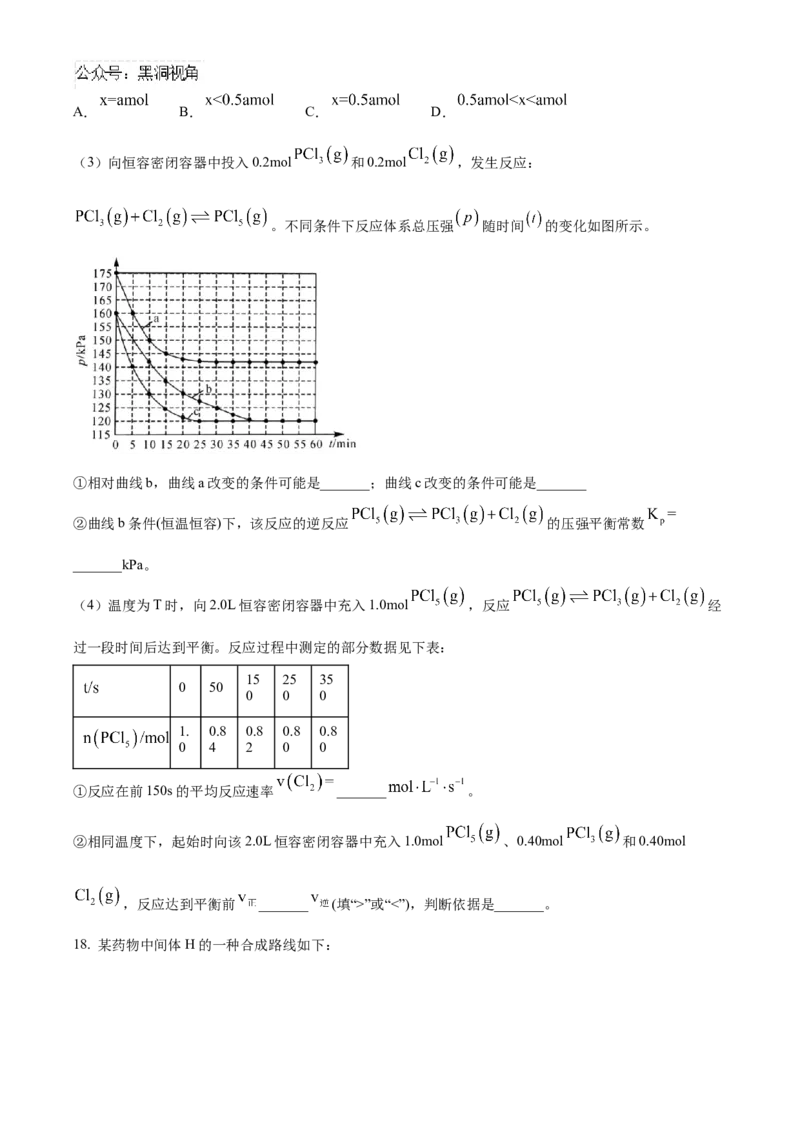
(3)向恒容密闭容器中投入0.2mol 和0.2mol ,发生反应:
。不同条件下反应体系总压强 随时间 的变化如图所示。
①相对曲线b,曲线a改变的条件可能是_______;曲线c改变的条件可能是_______
②曲线b条件(恒温恒容)下,该反应的逆反应 的压强平衡常数
_______kPa。
(4)温度为T时,向2.0L恒容密闭容器中充入1.0mol ,反应 经
过一段时间后达到平衡。反应过程中测定的部分数据见下表:
15 25 35
0 50
0 0 0
1. 0.8 0.8 0.8 0.8
0 4 2 0 0
①反应在前150s的平均反应速率 _______ 。
②相同温度下,起始时向该2.0L恒容密闭容器中充入1.0mol 、0.40mol 和0.40mol
,反应达到平衡前 _______ (填“>”或“<”),判断依据是_______。
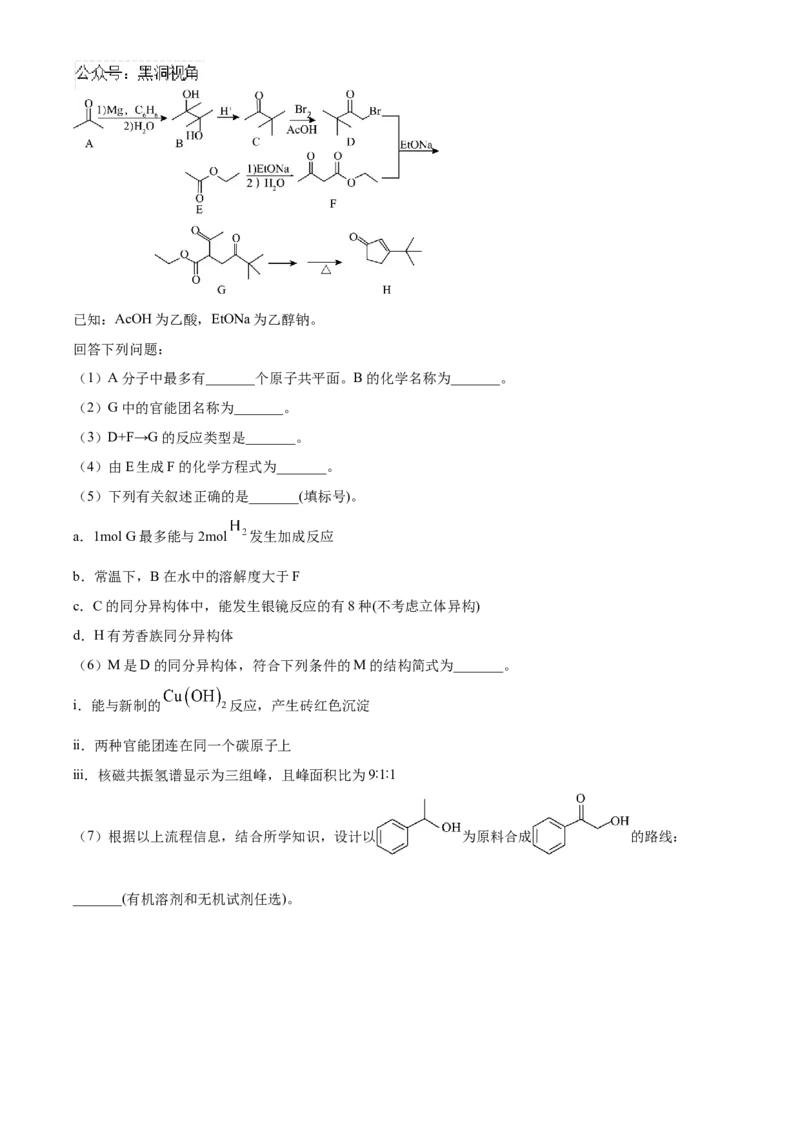
18. 某药物中间体H的一种合成路线如下:已知:AcOH为乙酸,EtONa为乙醇钠。
回答下列问题:
(1)A分子中最多有_______个原子共平面。B的化学名称为_______。
(2)G中的官能团名称为_______。
(3)D+F→G的反应类型是_______。
(4)由E生成F的化学方程式为_______。
(5)下列有关叙述正确的是_______(填标号)。
a.1mol G最多能与2mol 发生加成反应
b.常温下,B在水中的溶解度大于F
c.C的同分异构体中,能发生银镜反应的有8种(不考虑立体异构)
d.H有芳香族同分异构体
(6)M是D的同分异构体,符合下列条件的M的结构简式为_______。
ⅰ.能与新制的 反应,产生砖红色沉淀
ⅱ.两种官能团连在同一个碳原子上
ⅲ.核磁共振氢谱显示为三组峰,且峰面积比为9∶1∶1
(7)根据以上流程信息,结合所学知识,设计以 为原料合成 的路线:
_______(有机溶剂和无机试剂任选)。2025 届高三第一学期阶段性检测卷(二)
化学
全卷满分100分,考试时间75分钟。
注意事项:
1.答题前,先将自己的姓名、准考证号填写在试卷和答题卡上,并将条形码粘贴在答题卡上
的指定位置。
2.请按题号顺序在答题卡上各题目的答题区域内作答,写在试卷、草稿纸和答题卡上的非答
题区域均无效。
3.选择题用2B铅笔在答题卡上把所选答案的标号涂黑;非选择题用黑色签字笔在答题卡上作
答;字体工整,笔迹清楚。
4.考试结束后,请将试卷和答题卡一并上交。
5.本卷主要考查内容:化学物质及其变化、物质的量、化学实验基础知识(60%),其余高考内
容(40%)。
可能用到的相对原子质量:H:1 Li:7 O:16 Mg:24 Zn:65 As:75
一、选择题:本题共14小题,每小题3分,共42分。在每小题给出的四个选项中,只有一
项是符合题目要求的。
【1题答案】
【答案】D
【2题答案】
【答案】C
【3题答案】
【答案】C
【4题答案】
【答案】A
【5题答案】
【答案】A
【6题答案】
【答案】D
【7题答案】【答案】B
【8题答案】
【答案】B
【9题答案】
【答案】C
【10题答案】
【答案】C
【11题答案】
【答案】D
【12题答案】
【答案】D
【13题答案】
【答案】B
【14题答案】
【答案】D
二、非选择题:本题共4小题,共58分。
【15题答案】
【答案】(1)D (2)在装置B、C之间增加干燥装置
(3)作对比实验 (4)NaOH或氢氧化钠
(5) ①. 稀盐酸 ②. 取实验1反应生成的沉淀于试管中,加入稀盐酸,有(无色无味)气泡生成,
将气体通入澄清石灰水中,石灰水变浑浊 ③.
【16题答案】
【答案】(1) ①. ②. 溶液水解程度较大,
碱性较强,防止生成 沉淀
(2)向漏斗中的 沉淀上加蒸馏水至浸没沉淀,待水自然流下后,重复操作2~3次
(3)减少柠檬酸亚铁晶体因溶解而造成的损失,便于干燥
(4)EFGJK (5) ①. 将 氧化成 ②.【17题答案】
【答案】(1)
(2) ①. Cat2 ②. Cat2对应直线斜率更小活化能更低 ③. B
(3) ①. 升高温度 ②. 加入催化剂 ③. 40
(4) ①. ②. < ③. Q>K,则反应逆向进行
c
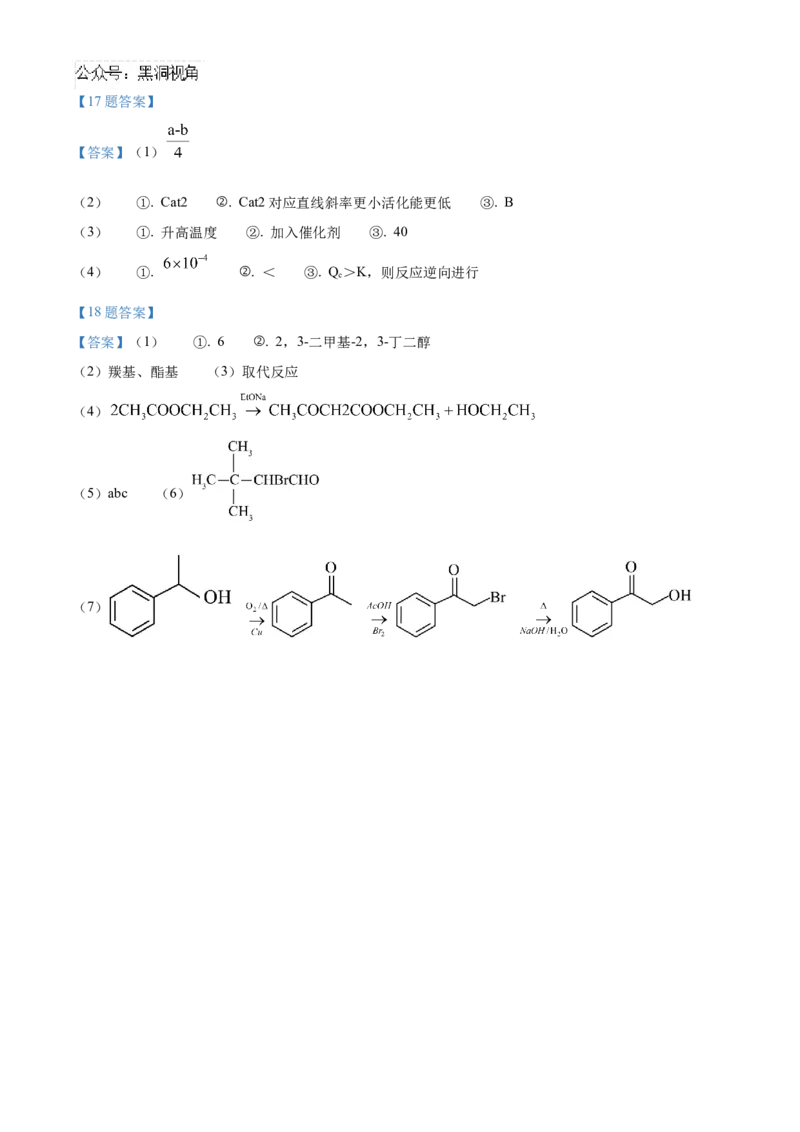
【18题答案】
【答案】(1) ①. 6 ②. 2,3-二甲基-2,3-丁二醇
(2)羰基、酯基 (3)取代反应
(4)
(5)abc (6)
(7)