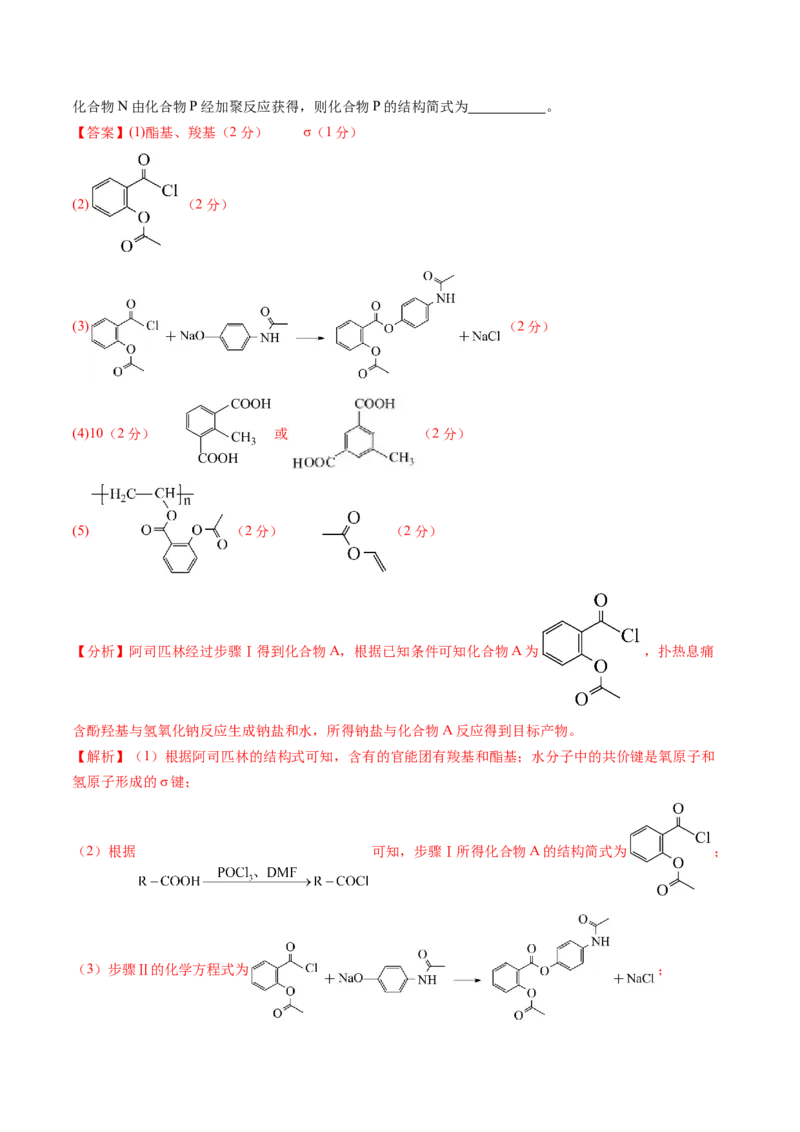
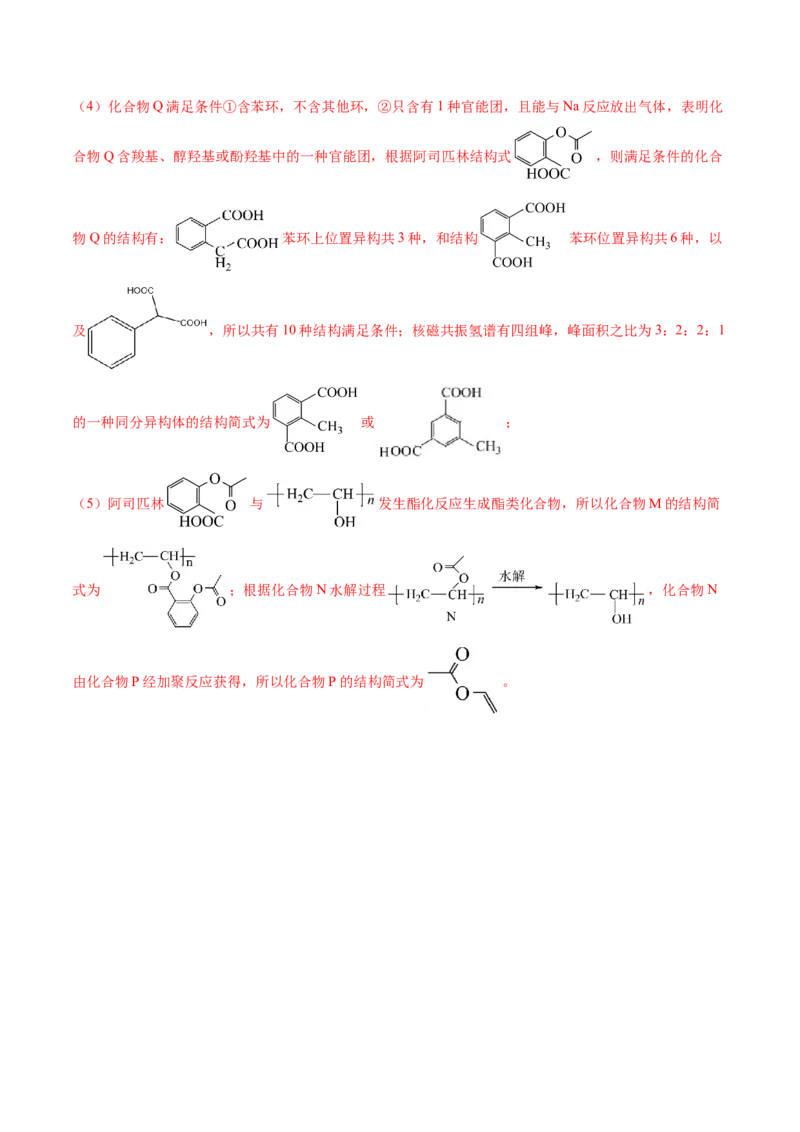
文档内容
2023-2024学年高三化学下学期开学摸底考(新高考七省专用)
(考试时间:75分钟 试卷满分:100分)
注意事项:
1.答卷前,考生务必将自己的姓名、准考证号等填写在答题卡和试卷指定位置上。
2.回答选择题时,选出每小题答案后,用铅笔把答题卡上对应题目的答案标号涂黑。如需改动,用橡皮
擦干净后,再选涂其他答案标号。回答非选择题时,将答案写在答题卡上。写在本试卷上无效。
3.考试结束后,将本试卷和答题卡一并交回。
4.测试范围:高考全部内容。
可能用到的相对原子质量:H 1 B 11 C 12 O 16 Fe 56
第Ⅰ卷
一、选择题:本题共14小题,每小题3分,共42分。在每小题给出的四个选项中,只有一项是符合题目
要求的。
1.化学促进了生活、生产、科研的发展,下列相关说法错误的是
A.在葡萄酒中添加SO 作为抗氧化剂食品保鲜,SO 在保鲜时体现了氧化性
2 2
B.华为Mate60手机高清镜头中使用的COC/COP(环状聚烯烃)是高分子化合物,也是混合物
C.中国自主研发的首个5G微基站射频芯片的主要材料是Si
D.高铁动车的车厢厢体由不锈钢和铝合金制成,不锈钢和铝合金均属于金属材料
【答案】A
【解析】A.SO 具有强还原性,具防腐和抗氧化等作用,可作为食品添加剂,SO 在保鲜时体现了还原性,
2 2
故A不正确;B.环状聚烯烃是高分子,是混合物,故B正确;C.电子芯片的材料主要是Si,射频芯片
也是电子芯片,故C正确;D.不锈钢是铁合金,铁合金与铝合金均属于金属材料,故D正确;答案选
A。
2.设N 为阿伏加德罗常数的值。下列说法正确的是
A
A.pH=2的硫酸溶液中,含氢离子数目为0.01N
A
B.在常温常压下,11.2LCO 分子中含氧原子数目小于N
2 A
C.21gC H 分子中含σ键数目一定是4N
3 6 A
D.在 中,每生成 ,转移的电子数为6N
A
【答案】B
【解析】A.pH=2的硫酸溶液中,未告知溶液的体积,无法计算溶液中氢离子数,故A不正确;B.在常温
常压下,V >22.4L/mol,11.2LCO 物质的量小于0.5mol,则含含氧原子数目小于N ,故B正确;C.
m 2 A
21gC H 分子的物质的量为0.5mol,但C H 有两种结构:丙烯(CHCH=CH)和环丙烷(△),前者含有
3 6 3 6 3 2
8个σ键,后者含有9个σ键,则0.5molC H 分子中含极性键数目不一定是4N ,故C不正确;D.在反应
3 6 A
中,KClO 中Cl的化合价降低了5价,转移了5个电子,故每生成 ,
3
转移的电子数为 ,故D不正确;答案选B。
3.甘草素是从甘草中提炼制成的甜味剂,其结构如图所示。下列说法正确的是
学科网(北京)股份有限公司A.不存在手性碳原子
B.分子中含有酯基
C.能与饱和溴水发生取代反应和加成反应
D.1mol甘草素最多能与2molNaOH反应
【答案】D
【解析】A.连接4个不同原子或原子团的碳原子为手性碳原子,甘草素中含有1个手性碳原子(
),故A不正确;B.甘草素分子结构中不含酯基,含酮基、醚键及羟基,故B不正确;
C.甘草素含有酚羟基,能与饱和溴水发生取代反应,但无碳碳双键,不能发生加成反应,故C不正确;
D.1mol甘草素含有2mol酚羟基,最多能与2molNaOH反应,故D正确;答案选D。
4.鎏金是古代常用的镀金工艺,将金汞合金涂于器物表面,加热使汞挥发,便形成一层光亮的金镀层。
下列关于青铜器鎏金工艺的说法不正确的是
A.用电化学方法也可实现铜上覆金
B.鎏金除了改善外观,还可保护青铜器,使其不易生锈
C.若表面的金镀层破损,暴露出的青铜表面会更易生锈
D.鎏金工艺的镀金过程是一种化学变化
【答案】D
【解析】A.用电解的方法,铜做阴极,电解液中含有可溶性的含金离子,则可实现铜上镀金,故A正确;
B.由题干信息可知,鎏金即在青铜器表面镀上一层金,由于金是一种很不活泼的金属,故除了改善外观,
还可保护青铜器,使其不易生锈,故B正确;C.由于金的活动性弱于Cu,故若表面的金镀层破损,暴露
出的青铜表面由于能形成电化学腐蚀,故会更易生锈,故C正确;D.鎏金工艺的镀金过程即将金汞合金
涂于器物表面,加热使汞挥发,便形成一层光亮的金镀层,故是一种物理变化,D错误;故选D。
5.室温下,下列各组离子在指定溶液中能大量共存的是
A. 的溶液中: 、 、 、
B.含有大量 的溶液中: 、 、 、
C. 的溶液中: 、 、 、
D.酚酞变红色的溶液中: 、 、 、
【答案】D
【解析】A. 会氧化 : ,A错误;B. 会与 发生双水
学科网(北京)股份有限公司解: ,B错误;C. 即 ; ,
C错误;D.“酚酞变红色”是碱性溶液,此时 不能氧化 ,D中的离子能共存,故D正确;故选:
D。
6.已知电离常数:K(HCN)=5×10-10,HCO:K =4.3×10-7,K =5.6×10-11,下列离子方程式书写正确的是
a 2 3 a1 a2
A.向KCN(aq)中通入少量的CO 气体:CO+H O+2CN-=2HCN+CO
2 2 2
B.少量SO 通入Ca(ClO) 溶液中:SO +H O+Ca2++2ClO-=CaSO ↓+2HClO
2 2 2 2 3
C.氢氧化铁沉淀溶解于过量氢碘酸溶液中:2Fe(OH) +6H++2I-=2Fe2++6H O+I
3 2 2
D.向Ba(OH) 溶液中加入少量的NaHCO 溶液:2HCO +Ba2++2OH-=BaCO ↓+CO +2H O
2 3 3 2
【答案】C
【解析】A.由电离常数可知酸性HCO>HCN>HCO ,则反应的离子方程式为CN﹣+HO+CO=HCN+HCO ,故A错误;
2 3 2 2
B.将少量SO 通入Ca(ClO) 溶液中,二者发生氧化还原反应,正确的离子方程式为:Ca2++3ClO﹣
2 2
+HO+SO═CaSO↓+2HClO+Cl﹣,故B错误;C.Fe(OH) 溶于HI,后生成的Fe3+能将I﹣氧化为I,自身被还原为Fe2+,离子
2 2 4 3 2
方程式为2Fe(OH)+6H++2I﹣=2Fe2++I+6HO,故C正确;D.Ba(OH) 溶液中加入少量NaHCO 溶液,HCO 完全转化成
3 2 2 2 3
BaCO 沉淀,正确的离子方程式为:HCO +Ba2++OH﹣=BaCO↓+HO,故D错误;故选C。
3 3 2
7.下列化学用语表示正确的是
A. 的空间结构: (正四面体形)
B.甲烷的标准燃烧热 为 ,则甲烷燃烧的热化学方程式可表示为
C. 离子结构示意图:
D.NaHCO =Na++H++CO 2-
3 3
【答案】C
【解析】A. 中,C的价层电子对数为3+ =3+0=3,不含孤电子对,其空间结构为平面三角
形,故A不正确;B.燃烧热应生成液态水,B错误;C. 核电荷数为8,核外电子数为10,则离子
结构示意图为 ,故C正确;D.NaHCO 电离出钠离子和碳酸氢根:NaHCO =Na++HCO ,故D
3 3
不正确;故选C。
8.下列有关物质结构与性质的比较正确的是
学科网(北京)股份有限公司A.分子的极性: B.酸性:
C.键角: D.基态原子未成对电子数:Mn>Cr
【答案】C
【解析】A.O 是非极性分子,O 是极性分子,分子的极性: ,故A错误;B.F原子电负性大,
2 3
吸电子能力强,所以酸性: ,故B错误;C.氧的电负性大于氯,ClO中键合电
2
子对偏向氧;氟电负性强于氧,OF 中键合电子对偏向氟,两对键合电子对排斥小,键角就小键角,所以
2
键角 ,故C正确;D.基态原子Mn原子价电子排布式为3d74s2,未成对电子数为2;基态原子
Cr原子价电子排布式为3d54s1,未成对电子数为6,基态原子未成对电子数Mn