文档内容
2023-2024学年高三化学下学期开学摸底考(全国卷新教材)
(考试时间:50分钟 试卷满分:100分)
注意事项:
1.答卷前,考生务必将自己的姓名、准考证号等填写在答题卡和试卷指定位置上。
2.回答选择题时,选出每小题答案后,用铅笔把答题卡上对应题目的答案标号涂黑。如需改动,用橡皮
擦干净后,再选涂其他答案标号。回答非选择题时,将答案写在答题卡上。写在本试卷上无效。
3.考试结束后,将本试卷和答题卡一并交回。
4.测试范围:高考全部内容。
可能用到的相对原子质量:H 1 C 12 N 14 O 16 Na 23 S 32 Cl 35.5 Ti 48
一、选择题:本题共7小题,每小题6分,共42分。在每小题给出的四个选项中,只有一项是符合题目要
求的。
7.化学与生产、生活、科技密切相关。下列说法错误的是
A.用于火箭发动机的碳化硅陶瓷是一种新型无机非金属材料
B.船体上镶嵌的锌块是利用牺牲阳极法来避免船体遭受腐蚀
C.马家窑文化遗址出土的单刃青铜刀属于青铜制品,青铜是一种合金
D.“一带一路”是现代版的“丝绸之路”,丝绸的主要成分是纤维素
8.我国科学家研制出一种催化剂,能在室温下高效催化空气中甲醛的氧化,反应化学方程式为:
HCHO+O CO+H O。用N 表示阿伏伽德罗常数的值,下列有关说法正确的是
2 2 2 A
A.该反应为吸热反应
B.HCHO分子空间结构为平面正三角形
C.1 mol CO 分子中,碳原子的价层电子对数为2N
2 A
D.处理22.4 L HCHO转移电子数目为4N
A
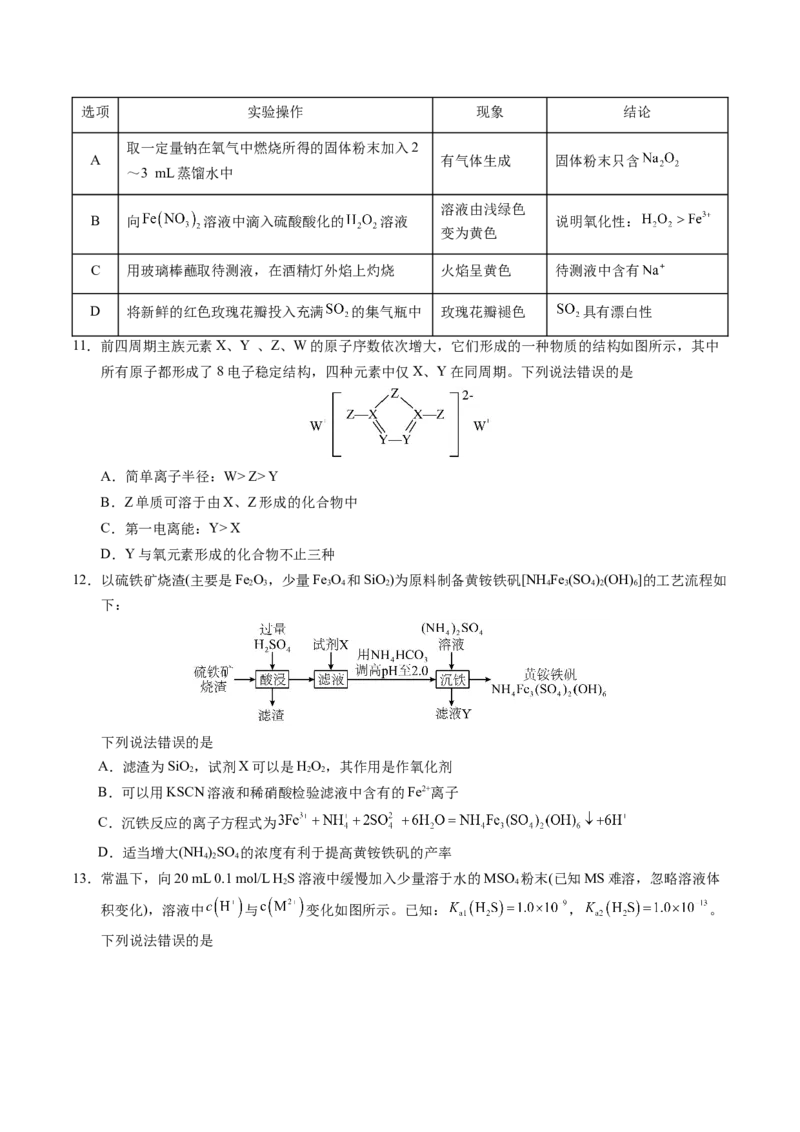
9.2023年1月18日,阿兹夫定片正式被纳入医保药品目录。阿兹夫定能更有效地针对变异的艾滋病病毒
发挥阻断作用,具有低耐药性和高疗效的显著优点,其结构简式如图所示。下列关于阿兹夫定的说法
不正确的是
A.五元环上有3种一氯代物
B.该有机物中C原子的杂化方式有2种
C.该有机物可以使酸性高锰酸钾溶液褪色
D.1 mol该有机物与足量的钠反应最多可产生2 mol H
2
10.根据下列实验操作、现象得出的结论正确的是
学科网(北京)股份有限公司选项 实验操作 现象 结论
取一定量钠在氧气中燃烧所得的固体粉末加入2
A 有气体生成 固体粉末只含
~3 mL蒸馏水中
溶液由浅绿色
B 向 溶液中滴入硫酸酸化的 溶液 说明氧化性:
变为黄色
C 用玻璃棒蘸取待测液,在酒精灯外焰上灼烧 火焰呈黄色 待测液中含有
D 将新鲜的红色玫瑰花瓣投入充满 的集气瓶中 玫瑰花瓣褪色 具有漂白性
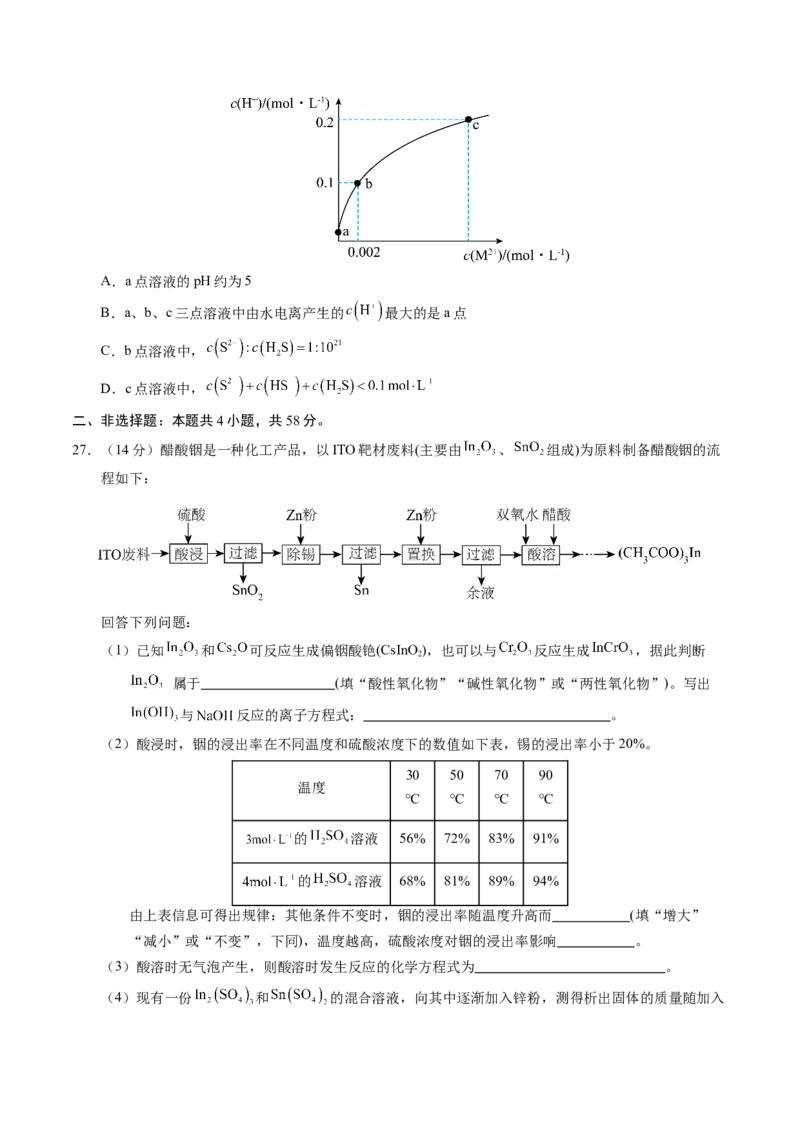
11.前四周期主族元素X、Y 、Z、W的原子序数依次增大,它们形成的一种物质的结构如图所示,其中
所有原子都形成了8电子稳定结构,四种元素中仅X、Y在同周期。下列说法错误的是
A.简单离子半径:W> Z> Y
B.Z单质可溶于由X、Z形成的化合物中
C.第一电离能:Y> X
D.Y与氧元素形成的化合物不止三种
12.以硫铁矿烧渣(主要是Fe O,少量Fe O 和SiO)为原料制备黄铵铁矾[NH Fe (SO )(OH) ]的工艺流程如
2 3 3 4 2 4 3 4 2 6
下:
下列说法错误的是
A.滤渣为SiO,试剂X可以是HO,其作用是作氧化剂
2 2 2
B.可以用KSCN溶液和稀硝酸检验滤液中含有的Fe2+离子
C.沉铁反应的离子方程式为
D.适当增大(NH )SO 的浓度有利于提高黄铵铁矾的产率
4 2 4
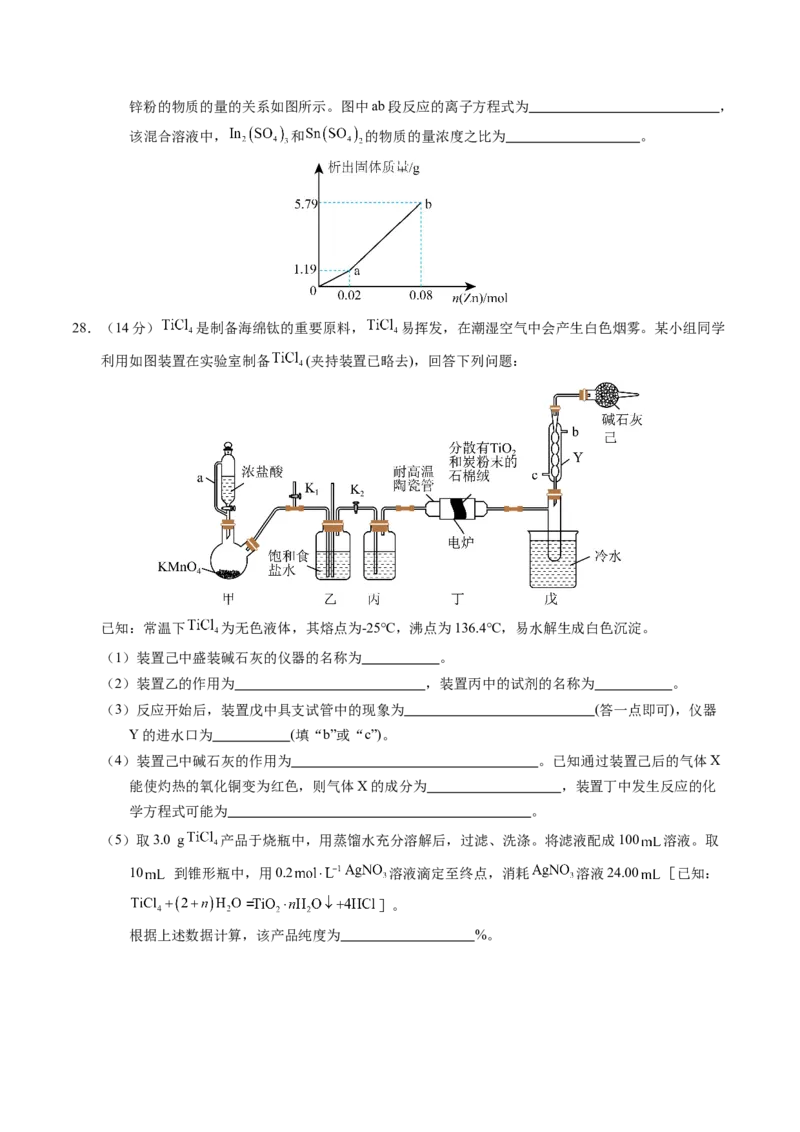
13.常温下,向20 mL 0.1 mol/L H S溶液中缓慢加入少量溶于水的MSO 粉末(已知MS难溶,忽略溶液体
2 4
积变化),溶液中 与 变化如图所示。已知: , 。
下列说法错误的是
学科网(北京)股份有限公司A.a点溶液的pH约为5
B.a、b、c三点溶液中由水电离产生的 最大的是a点
C.b点溶液中,
D.c点溶液中,
二、非选择题:本题共4小题,共58分。
27.(14分)醋酸铟是一种化工产品,以ITO靶材废料(主要由 、 组成)为原料制备醋酸铟的流
程如下:
回答下列问题:
(1)已知 和 可反应生成偏铟酸铯(CsInO ),也可以与 反应生成 ,据此判断
2
属于 (填“酸性氧化物”“碱性氧化物”或“两性氧化物”)。写出
与 反应的离子方程式: 。
(2)酸浸时,铟的浸出率在不同温度和硫酸浓度下的数值如下表,锡的浸出率小于20%。
30 50 70 90
温度
℃ ℃ ℃ ℃
的 溶液 56% 72% 83% 91%
的 溶液 68% 81% 89% 94%
由上表信息可得出规律:其他条件不变时,铟的浸出率随温度升高而 (填“增大”
“减小”或“不变”,下同),温度越高,硫酸浓度对铟的浸出率影响 。
(3)酸溶时无气泡产生,则酸溶时发生反应的化学方程式为 。
(4)现有一份 和 的混合溶液,向其中逐渐加入锌粉,测得析出固体的质量随加入
学科网(北京)股份有限公司锌粉的物质的量的关系如图所示。图中ab段反应的离子方程式为 ,
该混合溶液中, 和 的物质的量浓度之比为 。
28.(14分) 是制备海绵钛的重要原料, 易挥发,在潮湿空气中会产生白色烟雾。某小组同学
利用如图装置在实验室制备 (夹持装置已略去),回答下列问题:
已知:常温下 为无色液体,其熔点为-25℃,沸点为136.4℃,易水解生成白色沉淀。
(1)装置己中盛装碱石灰的仪器的名称为 。
(2)装置乙的作用为 ,装置丙中的试剂的名称为 。
(3)反应开始后,装置戊中具支试管中的现象为 (答一点即可),仪器
Y的进水口为 (填“b”或“c”)。
(4)装置己中碱石灰的作用为 。已知通过装置己后的气体X
能使灼热的氧化铜变为红色,则气体X的成分为 ,装置丁中发生反应的化
学方程式可能为 。
(5)取3.0 g 产品于烧瓶中,用蒸馏水充分溶解后,过滤、洗涤。将滤液配成100 溶液。取
10 到锥形瓶中,用0.2 溶液滴定至终点,消耗 溶液24.00 [已知:
]。
根据上述数据计算,该产品纯度为 %。
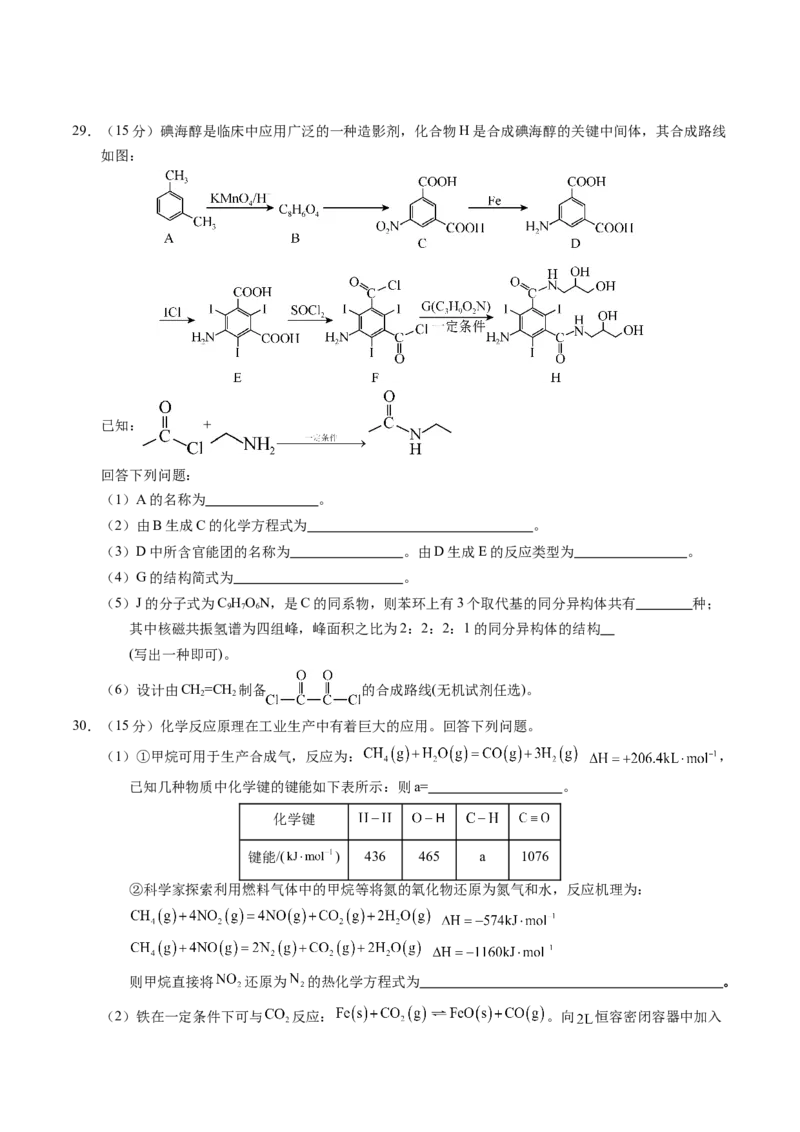
学科网(北京)股份有限公司29.(15分)碘海醇是临床中应用广泛的一种造影剂,化合物H是合成碘海醇的关键中间体,其合成路线
如图:
已知: +
回答下列问题:
(1)A的名称为 。
(2)由B生成C的化学方程式为 。
(3)D中所含官能团的名称为 。由D生成E的反应类型为 。
(4)G的结构简式为 。
(5)J的分子式为C HON,是C的同系物,则苯环上有3个取代基的同分异构体共有 种;
9 7 6
其中核磁共振氢谱为四组峰,峰面积之比为2:2:2:1的同分异构体的结构
(写出一种即可)。
(6)设计由CH=CH 制备 的合成路线(无机试剂任选)。
2 2
30.(15分)化学反应原理在工业生产中有着巨大的应用。回答下列问题。
(1)①甲烷可用于生产合成气,反应为: ,
已知几种物质中化学键的键能如下表所示:则a= 。
化学键
键能/( ) 436 465 a 1076
②科学家探索利用燃料气体中的甲烷等将氮的氧化物还原为氮气和水,反应机理为:
则甲烷直接将 还原为 的热化学方程式为 。
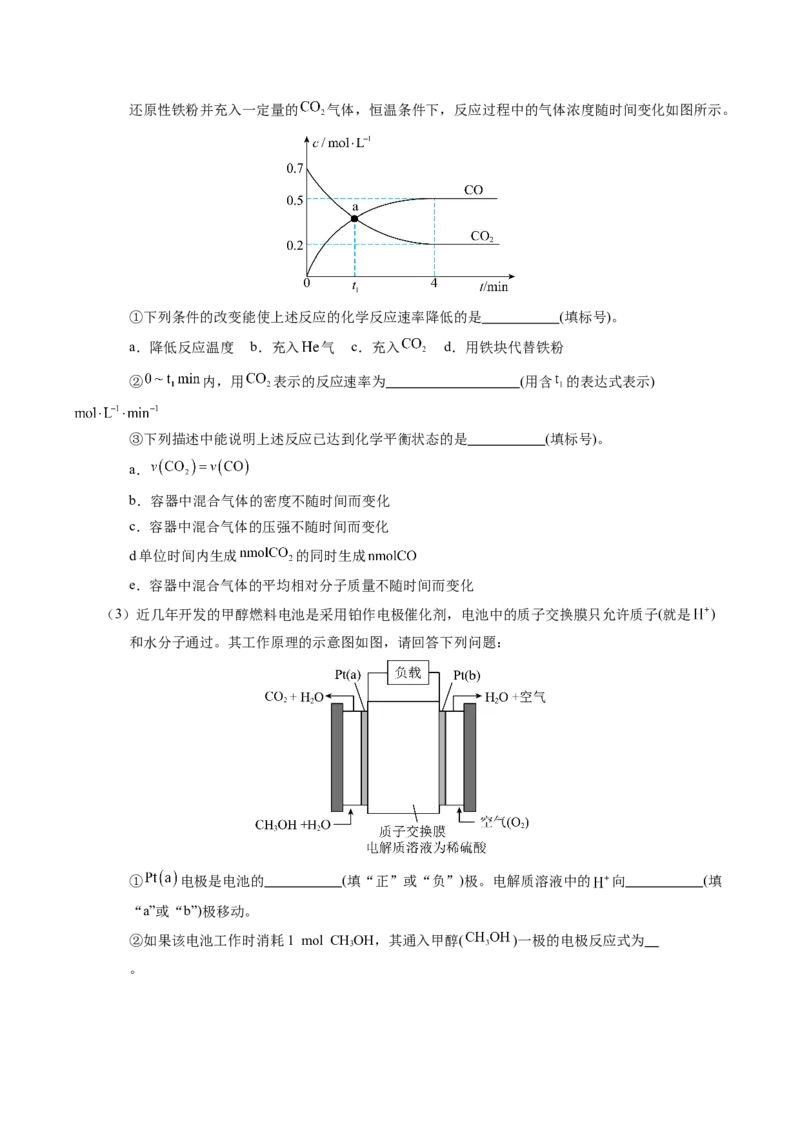
(2)铁在一定条件下可与 反应: 。向 恒容密闭容器中加入
学科网(北京)股份有限公司还原性铁粉并充入一定量的 气体,恒温条件下,反应过程中的气体浓度随时间变化如图所示。
①下列条件的改变能使上述反应的化学反应速率降低的是 (填标号)。
a.降低反应温度 b.充入 气 c.充入 d.用铁块代替铁粉
② 内,用 表示的反应速率为 (用含 的表达式表示)
③下列描述中能说明上述反应已达到化学平衡状态的是 (填标号)。
a.
b.容器中混合气体的密度不随时间而变化
c.容器中混合气体的压强不随时间而变化
d单位时间内生成 的同时生成
e.容器中混合气体的平均相对分子质量不随时间而变化
(3)近几年开发的甲醇燃料电池是采用铂作电极催化剂,电池中的质子交换膜只允许质子(就是 )
和水分子通过。其工作原理的示意图如图,请回答下列问题:
① 电极是电池的 (填“正”或“负”)极。电解质溶液中的 向 (填
“a”或“b”)极移动。
②如果该电池工作时消耗1 mol CHOH,其通入甲醇( )一极的电极反应式为
3
。
学科网(北京)股份有限公司