文档内容
2019年广西贵港市中考化学试卷
一、 选择题(每小题3分,共42分)
1.下列生产工艺中,不涉及化学变化的是( )
A.烧制生石灰 B.海水晒盐 C.冶炼生铁 D.海水制镁
2.人类的生命活动一刻也离不开水和氧气。下列关于水和氧气的叙述错误的是( )
A.水属于氧化物
B.氧气常用作氧化剂
C.氧气可供给呼吸
D.水是由两个氢原子和一个氧原子构成的
3.下列生活用品的主要材料属于有机合成材料的是( )
A.玻璃水杯 B.陶瓷碗 C.塑料脸盆 D.真皮手套
4.下列物质在空气中燃烧发出淡蓝色火焰的是( )
A.氢气 B.木炭 C.红磷 D.蜡烛
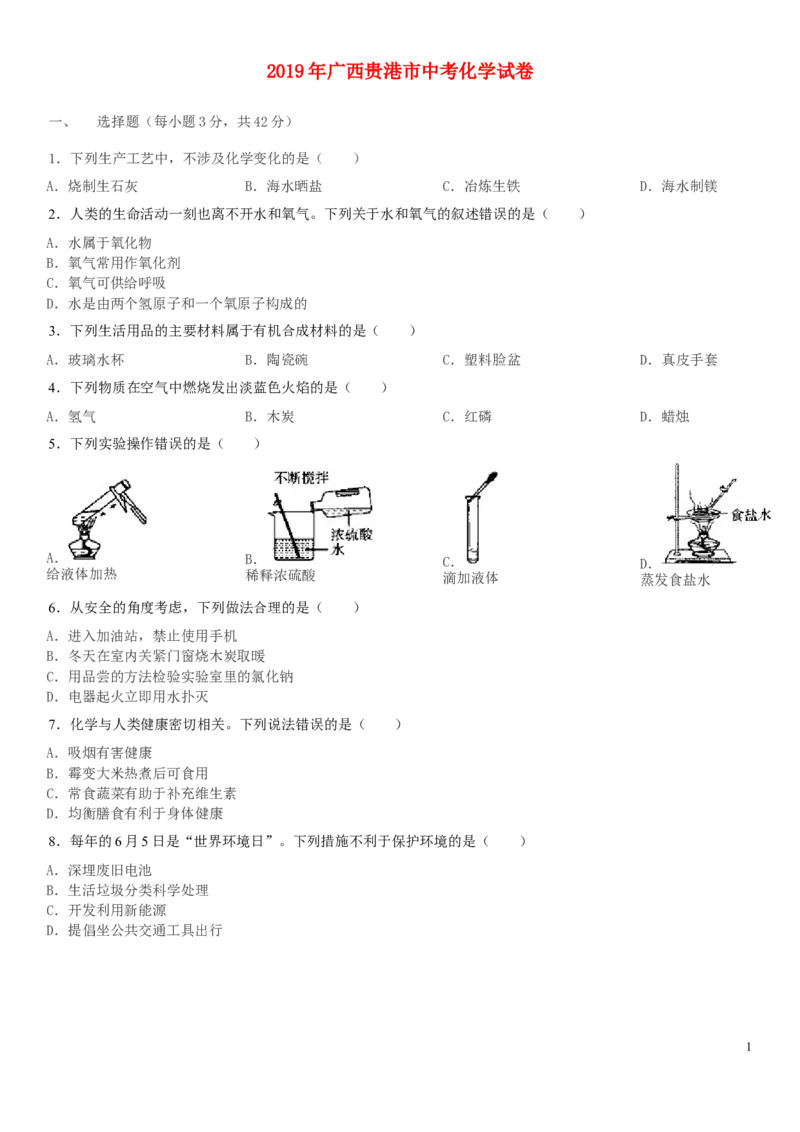
5.下列实验操作错误的是( )
A. B. C. D.
给液体加热 稀释浓硫酸 滴加液体 蒸发食盐水
6.从安全的角度考虑,下列做法合理的是( )
A.进入加油站,禁止使用手机
B.冬天在室内关紧门窗烧木炭取暖
C.用品尝的方法检验实验室里的氯化钠
D.电器起火立即用水扑灭
7.化学与人类健康密切相关。下列说法错误的是( )
A.吸烟有害健康
B.霉变大米热煮后可食用
C.常食蔬菜有助于补充维生素
D.均衡膳食有利于身体健康
8.每年的6月5日是“世界环境日”。下列措施不利于保护环境的是( )
A.深埋废旧电池
B.生活垃圾分类科学处理
C.开发利用新能源
D.提倡坐公共交通工具出行
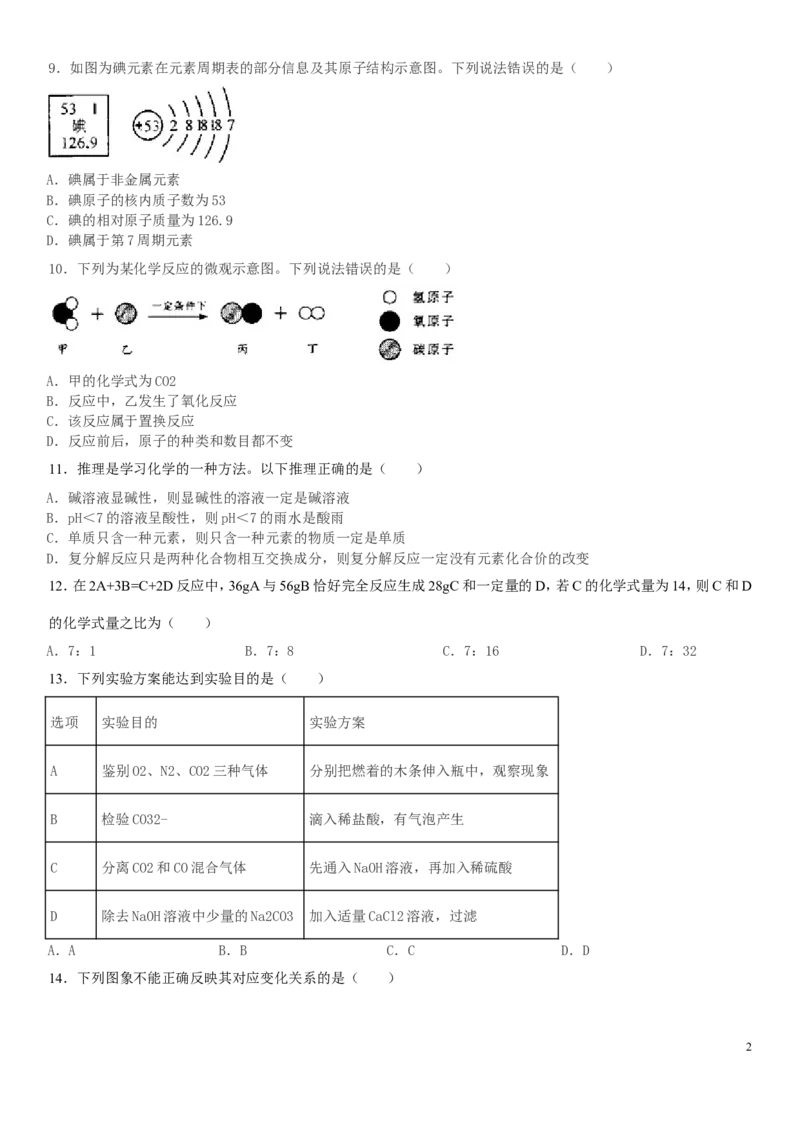
19.如图为碘元素在元素周期表的部分信息及其原子结构示意图。下列说法锆误的是( )
A.碘属于非金属元素
B.碘原子的核内质子数为53
C.碘的相对原子质量为126.9
D.碘属于第7周期元素
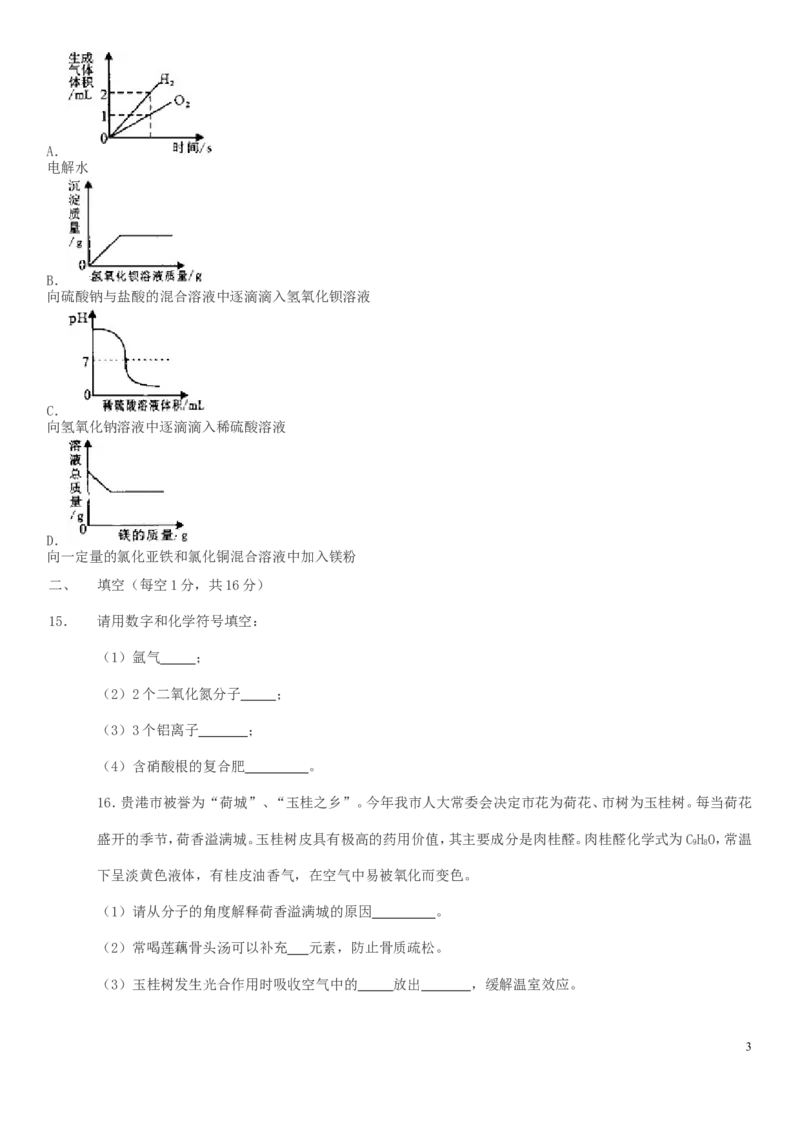
10.下列为某化学反应的微观示意图。下列说法错误的是( )
A.甲的化学式为CO2
B.反应中,乙发生了氧化反应
C.该反应属于置换反应
D.反应前后,原子的种类和数目都不变
11.推理是学习化学的一种方法。以下推理正确的是( )
A.碱溶液显碱性,则显碱性的溶液一定是碱溶液
B.pH<7的溶液呈酸性,则pH<7的雨水是酸雨
C.单质只含一种元素,则只含一种元素的物质一定是单质
D.复分解反应只是两种化合物相互交换成分,则复分解反应一定没有元素化合价的改变
12.在2A+3B=C+2D反应中,36gA与56gB恰好完全反应生成28gC和一定量的D,若C的化学式量为14,则C和D
的化学式量之比为( )
A.7:1 B.7:8 C.7:16 D.7:32
13.下列实验方案能达到实验目的是( )
选项 实验目的 实验方案
A 鉴别O2、N2、CO2三种气体 分别把燃着的木条伸入瓶中,观察现象
B 检验CO32- 滴入稀盐酸,有气泡产生
C 分离CO2和CO混合气体 先通入NaOH溶液,再加入稀硫酸
D 除去NaOH溶液中少量的Na2CO3 加入适量CaCl2溶液,过滤
A.A B.B C.C D.D
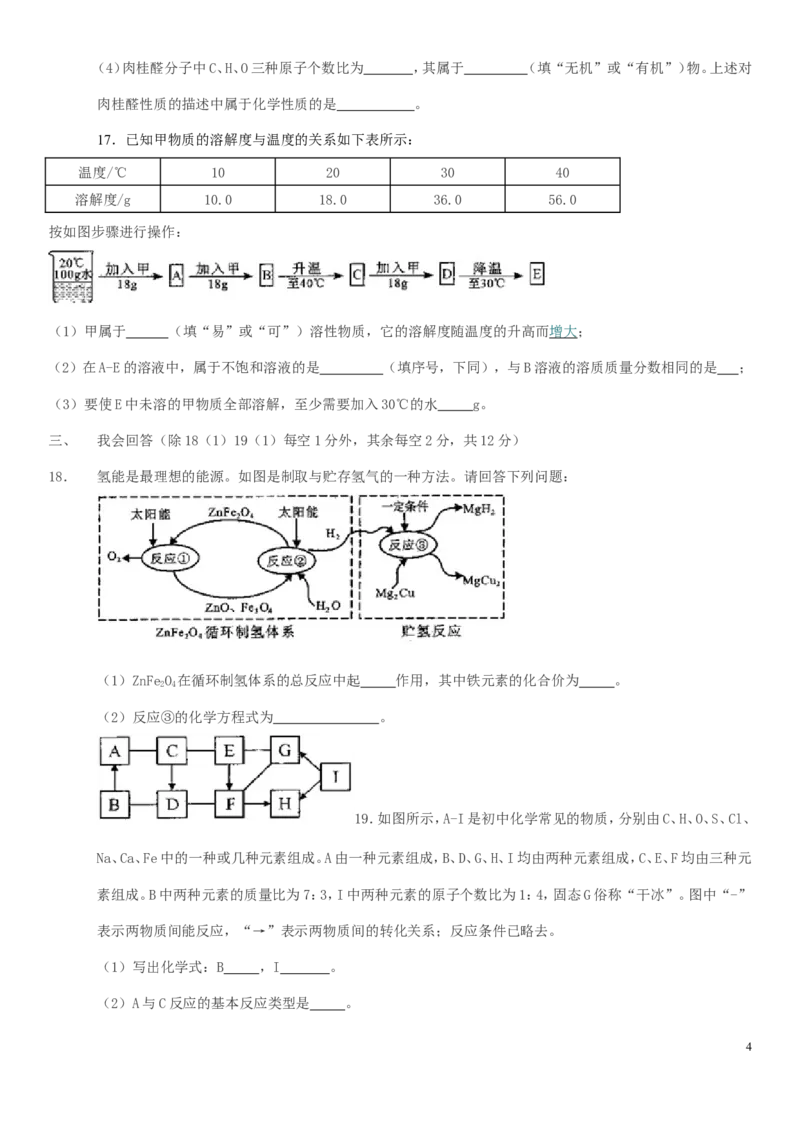
14.下列图象不能正确反映其对应变化关系的是( )
2A.
电解水
B.
向硫酸钠与盐酸的混合溶液中逐滴滴入氢氧化钡溶液
C.
向氢氧化钠溶液中逐滴滴入稀硫酸溶液
D.
向一定量的氯化亚铁和氯化铜混合溶液中加入镁粉
二、 填空(每空1分,共16分)
15. 请用数字和化学符号填空:
(1)氩气 ;
(2)2个二氧化氮分子 ;
(3)3个铝离子 ;
(4)含硝酸根的复合肥 。
16.贵港市被誉为“荷城”、“玉桂之乡”。今年我市人大常委会决定市花为荷花、市树为玉桂树。每当荷花
盛开的季节,荷香溢满城。玉桂树皮具有极高的药用价值,其主要成分是肉桂醛。肉桂醛化学式为CHO,常温
9 8
下呈淡黄色液体,有桂皮油香气,在空气中易被氧化而变色。
(1)请从分子的角度解释荷香溢满城的原因 。
(2)常喝莲藕骨头汤可以补充 元素,防止骨质疏松。
(3)玉桂树发生光合作用时吸收空气中的 放出 ,缓解温室效应。
3(4)肉桂醛分子中C、H、O三种原子个数比为 ,其属于 (填“无机”或“有机”)物。上述对
肉桂醛性质的描述中属于化学性质的是 。
17.已知甲物质的溶解度与温度的关系如下表所示:
温度/℃ 10 20 30 40
溶解度/g 10.0 18.0 36.0 56.0
按如图步骤进行操作:
(1)甲属于 (填“易”或“可”)溶性物质,它的溶解度随温度的升高而增大;
(2)在A-E的溶液中,属于不饱和溶液的是 (填序号,下同),与B溶液的溶质质量分数相同的是 ;
(3)要使E中未溶的甲物质全部溶解,至少需要加入30℃的水 g。
三、 我会回答(除18(1)19(1)每空1分外,其余每空2分,共12分)
18. 氢能是最理想的能源。如图是制取与贮存氢气的一种方法。请回答下列问题:
(1)ZnFeO 在循环制氢体系的总反应中起 作用,其中铁元素的化合价为 。
2 4
(2)反应③的化学方程式为 。
19.如图所示,A-I是初中化学常见的物质,分别由C、H、O、S、Cl、
Na、Ca、Fe中的一种或几种元素组成。A由一种元素组成,B、D、G、H、I均由两种元素组成,C、E、F均由三种元
素组成。B中两种元素的质量比为7:3,I中两种元素的原子个数比为1:4,固态G俗称“干冰”。图中“-”
表示两物质间能反应,“→”表示两物质间的转化关系;反应条件已略去。
(1)写出化学式:B ,I 。
(2)A与C反应的基本反应类型是 。
4(3)C→D的化学方程式为 。
(4)E→F的化学方程式为 。
四、 实验题(除第20(1)每空1分外,其余每空2分,共22分)
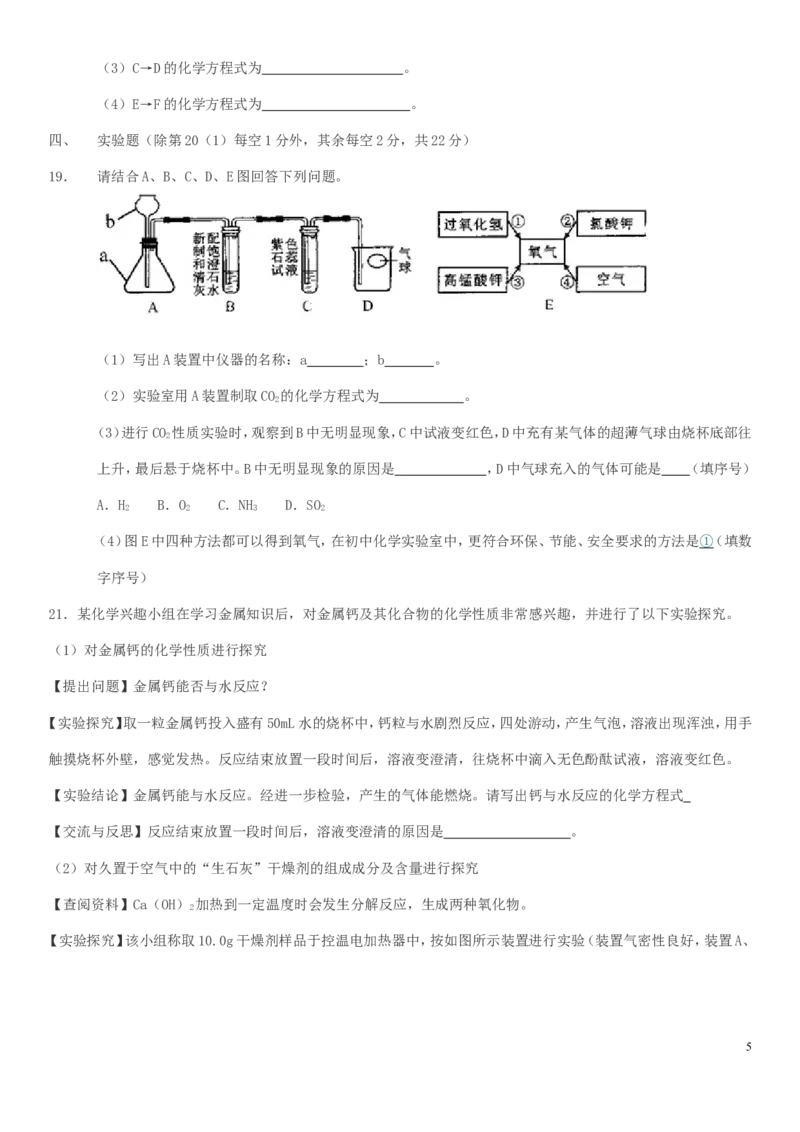
19. 请结合A、B、C、D、E图回答下列问题。
(1)写出A装置中仪器的名称:a ;b 。
(2)实验室用A装置制取CO 的化学方程式为 。
2
(3)进行CO 性质实验时,观察到B中无明显现象,C中试液变红色,D中充有某气体的超薄气球由烧杯底部往
2
上升,最后悬于烧杯中。B中无明显现象的原因是 ,D中气球充入的气体可能是 (填序号)
A.H B.O C.NH D.SO
2 2 3 2
(4)图E中四种方法都可以得到氧气,在初中化学实验室中,更符合环保、节能、安全要求的方法是①(填数
字序号)
21.某化学兴趣小组在学习金属知识后,对金属钙及其化合物的化学性质非常感兴趣,并进行了以下实验探究。
(1)对金属钙的化学性质进行探究
【提出问题】金属钙能否与水反应?
【实验探究】取一粒金属钙投入盛有50mL水的烧杯中,钙粒与水剧烈反应,四处游动,产生气泡,溶液出现浑浊,用手
触摸烧杯外壁,感觉发热。反应结束放置一段时间后,溶液变澄清,往烧杯中滴入无色酚酞试液,溶液变红色。
【实验结论】金属钙能与水反应。经进一步检验,产生的气体能燃烧。请写出钙与水反应的化学方程式
【交流与反思】反应结束放置一段时间后,溶液变澄清的原因是 。
(2)对久置于空气中的“生石灰”干燥剂的组成成分及含量进行探究
【查阅资料】Ca(OH) 加热到一定温度时会发生分解反应,生成两种氧化物。
2
【实验探究】该小组称取10.0g干燥剂样品于控温电加热器中,按如图所示装置进行实验(装置气密性良好,装置A、
5B、C中药品足量,实验操作正确)
【实验数据记录】充分反应后,产物被完全吸收,A装置增重0.9g,B装置增重2.2g
【分析与结论】该包干燥剂的成分有 (填化学式),其中Ca(OH) 的质量为 g。
2
【反思与拓展】
①停止加热后,需要通入N 一段时间的目的是 。
2
②若没有C装置,会导致含量测定结果偏小的成分是 。
五、 我会计算(共8分)
22.小红称取5.0g某品牌化肥(商标如图1)于烧杯中,加水完全溶解,滴入Ba(OH)溶液进行该化肥中(NH)SO 含
2 4 2 4
量的测定(杂质溶于水但不参加反应)。测定数据如表和图2所示。
滴入Ba(OH) 溶液质量/g 50 100 150 200
2
生成沉淀质量/g 2.33 4.66 6.99 m
已知:(NH)SO+Ba(OH)═BaSO↓+2NH↑+2HO
4 2 4 2 4 3 2
(1)表格中的m、坐标上的a数值分别为 、 ;
(2)该化肥属于 (填“合格”或“不合格”)产品
(3)计算所用Ba(OH) 溶液中溶质的质量分数(写出计算过程,结果精确至0.01%)。
2
参考答案:
1-14:BDC ADA BAD ADC CD
15: 故答案为:
(1)Ar;
6(2)2NO ;
2
(3)3Al3+;
(4)KNO 。
3
16: 解:(1)荷香溢满城是因为具有香味的分子是在不断的运动的,向四周扩散,使人们闻到荷香;故填:分
子在不断运动;
(2)骨头汤中含有的钙元素可以防止骨质疏松。故填:钙;
(3)玉桂树发生光合作用时吸收空气中的二氧化碳,放出氧气,缓解温室效应。故填:二氧化碳;氧气;
(4)由化学式可知,肉桂醛分子中C、H、O三种原子个数比为9:8:1,该物质是一种含碳元素的化合物,属于
有机物;化学性质是在化学变化中表现出来的性质,因此肉桂醛在空气中易被氧化而变色属于肉桂酸的化学
性质;故填:9:8:1;有机;在空气中易被氧化而变色。
17: 故答案为:(1)易,增大;
(2)A、C、D,A;
(3)50。
18: 故答案为:(1)催化,+3;
(2)3H +2Mg Cu
2 2
一
定 条
件
3MgH +MgCu 。
2 2
19: 故答案为:(1)Fe O ,CH ;
2 3 4
(2)置换反应;
(3)H SO +BaCl =BaSO ↓+2HCl;
2 4 2 4
(4)Ca(OH) +Na CO =CaCO ↓+2NaOH。
2 2 3 3
20: 故答案为:CaCO +2HCl=CaCl +H O+CO ↑;
3 2 2 2
(3)B中无明显现象的原因是:二氧化碳气体中混有氯化氢气体;D中气球充入的气体可能是:氢气、氧气、氨
气;故答案为:二氧化碳气体中混有氯化氢气体;ABC;
(4)在初中化学实验室中,更符合环保、节能、安全要求的方法是:用过氧化氢和二氧化锰制氧气;故答案为:
①;
21: 解:(1)【实验结论】
金属钙能与水反应。经进一步检验,产生的气体能燃烧,由质量守恒定律可知,该气体是氢气,因此钙与水反
应生成氢氧化钙和氢气,反应的化学方程式:Ca+2H O═H ↑+Ca(OH) 。
2 2 2
7故填:Ca+2H O═H ↑+Ca(OH) 。
2 2 2
【交流与反思】
反应结束放置一段时间后,溶液变澄清的原因是温度降低氢氧化钙溶解度增大,不能溶解的氢氧化钙全部溶
解。
故填:温度降低氢氧化钙溶解度增大,不能溶解的氢氧化钙全部溶解。
(2)【分析与结论】
A装置增重0.9g,B装置增重2.2g,说明氢氧化钙分解生成了0.9g水,碳酸钙分解生成了2.2g二氧化碳,反
应的化学方程式及其质量关系:
高温
Ca(OH)2=CaO+H2O
74 18
3.7g 0.9g
高温
CaCO =CaO+CO ↑,
3 2
100 44
5g 2.2g
干燥剂中氧化钙质量:10.0g-3.7g-5g=1.3g,
该包干燥剂的成分有CaO、Ca(OH) 、CaCO ,其中Ca(OH) 的质量为3.7g。
2 3 2
故填:CaO、Ca(OH) 、CaCO ;3.7。
2 3
【反思与拓展】
①停止加热后,需要通入N 一段时间的目的是使反应生成的水、二氧化碳全部被浓硫酸、氢氧化钠溶液吸收。
2
故填:使反应生成的水、二氧化碳全部被浓硫酸、氢氧化钠溶液吸收。
②若没有C装置,会导致空气中的部分二氧化碳进入B装置中,导致测定的二氧化碳质量偏大,由于氢氧化钙
的测定值不变,因此含量测定结果偏小的成分是氧化钙。
故填:氧化钙。
22: 故答案为:(1)6.99,1.02;
(2)不合格;
(3)3.42%。
89