文档内容
2021 浙江宁波化学
一、选择题
1. 2021年4月22日是第52个世界地球日,我国的主题是“珍爱地球—人与自然和谐共生”。下列行为符
合这一主题的是
A. 提倡使用含磷洗衣粉 B. 围海造田增加耕地面积
C. 空矿泉水瓶回收利用 D. 大量开采化石燃料缓解能源危机
【答案】C
【解析】
【详解】A、含磷洗衣粉的滥用可能会使得水体富营养化,会污染水体,不符合题意;
B、围海造田增加耕地面积会损害自然调节环境的能力、对动植物生长、繁衍不利,不符合题意;
C、空矿泉水瓶回收利用一方面减少了塑料污染,另一方面可以再循环利用矿泉水瓶的塑料组分,节约了
资源,符合题意;
D、化石能源的过度使用会污染环境,造成大气、水体等的污染,不符合题意。
故选C。
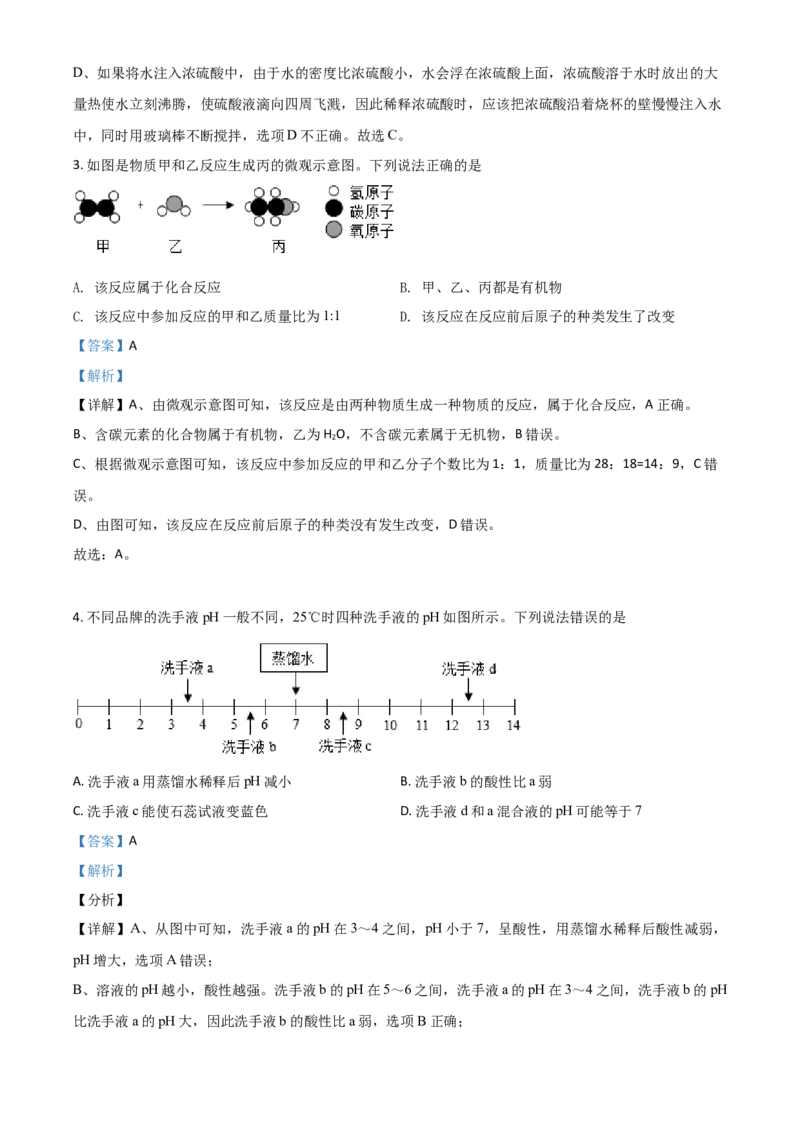
2. “操作千万条,安全第一条”。下列实验操作符合安全要求的是
A. 点燃酒精灯 B. 转移蒸发皿
C. 闻气味 D. 稀释浓硫酸
【答案】C
【解析】
【分析】
【详解】A、应该用火柴点燃酒精灯,绝对禁止用燃着的酒精灯引燃另一只酒精灯,以免发生火灾,选项
A不正确;
B、刚刚加热的蒸发皿温度很高,转移时应该用坩埚钳夹取,不能用手直接接触,选项B不正确;
C、因为有些气体对人体有害,所以闻气体的气味时应该采用“招气入鼻法”,选项C正确;D、如果将水注入浓硫酸中,由于水的密度比浓硫酸小,水会浮在浓硫酸上面,浓硫酸溶于水时放出的大
量热使水立刻沸腾,使硫酸液滴向四周飞溅,因此稀释浓硫酸时,应该把浓硫酸沿着烧杯的壁慢慢注入水
中,同时用玻璃棒不断搅拌,选项D不正确。故选C。
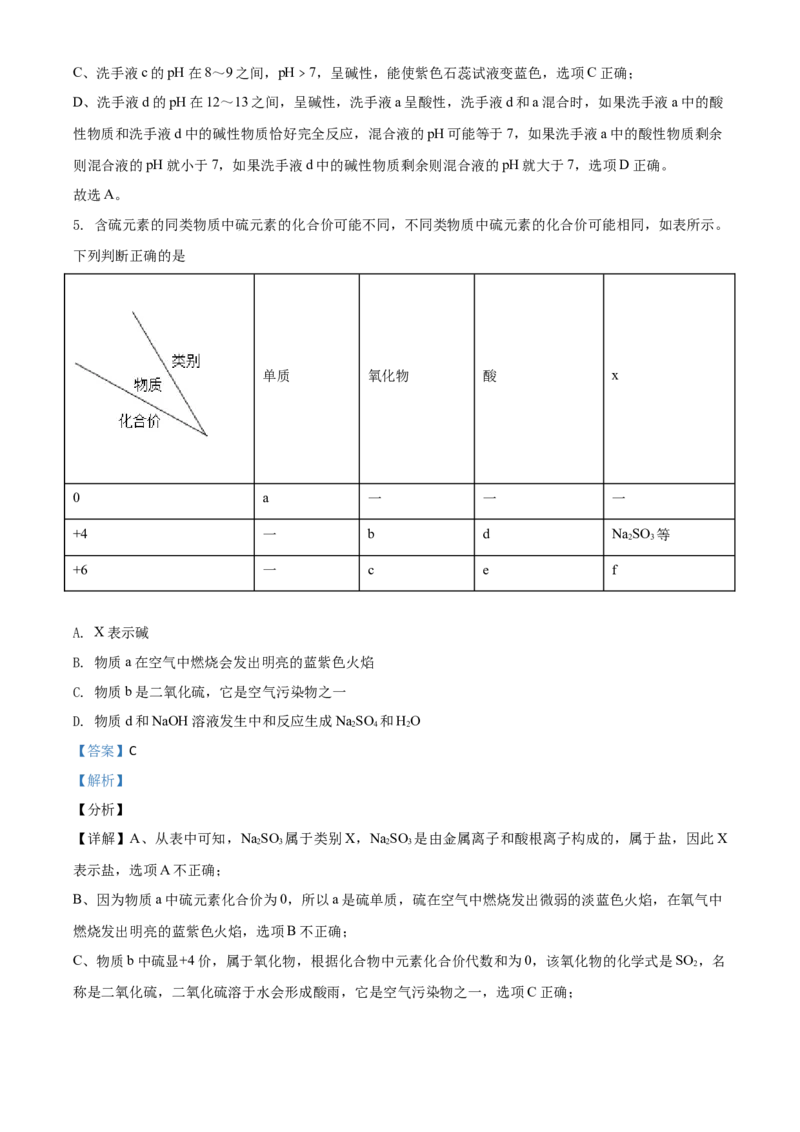
3. 如图是物质甲和乙反应生成丙的微观示意图。下列说法正确的是
A. 该反应属于化合反应 B. 甲、乙、丙都是有机物
C. 该反应中参加反应的甲和乙质量比为1:1 D. 该反应在反应前后原子的种类发生了改变
【答案】A
【解析】
【详解】A、由微观示意图可知,该反应是由两种物质生成一种物质的反应,属于化合反应,A正确。
B、含碳元素的化合物属于有机物,乙为H O,不含碳元素属于无机物,B错误。
2
C、根据微观示意图可知,该反应中参加反应的甲和乙分子个数比为1:1,质量比为28:18=14:9,C错
误。
D、由图可知,该反应在反应前后原子的种类没有发生改变,D错误。
故选:A。
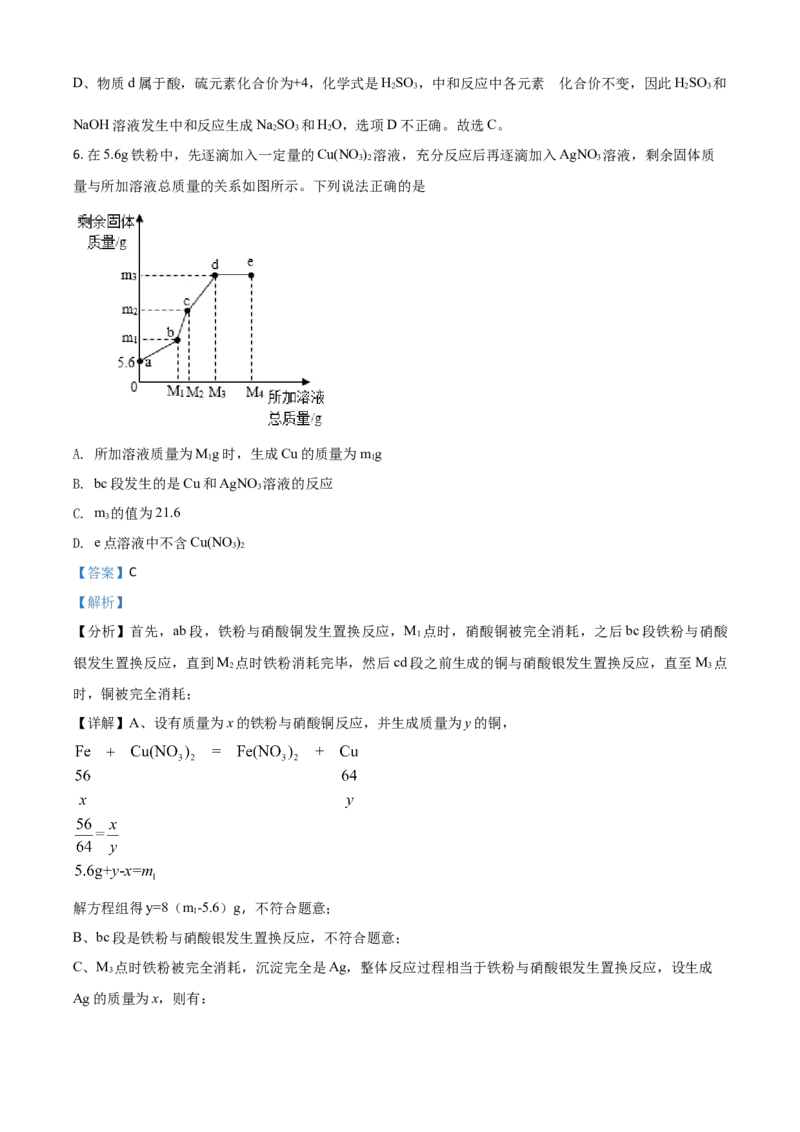
4. 不同品牌的洗手液pH一般不同,25℃时四种洗手液的pH如图所示。下列说法错误的是
A. 洗手液a用蒸馏水稀释后pH减小 B. 洗手液b的酸性比a弱
C. 洗手液c能使石蕊试液变蓝色 D. 洗手液d和a混合液的pH可能等于7
【答案】A
【解析】
【分析】
【详解】A、从图中可知,洗手液a的pH在3~4之间,pH小于7,呈酸性,用蒸馏水稀释后酸性减弱,
pH增大,选项A错误;
B、溶液的pH越小,酸性越强。洗手液b的pH在5~6之间,洗手液a的pH在3~4之间,洗手液b的pH
比洗手液a的pH大,因此洗手液b的酸性比a弱,选项B正确;C、洗手液c的pH在8~9之间,pH﹥7,呈碱性,能使紫色石蕊试液变蓝色,选项C正确;
D、洗手液d的pH在12~13之间,呈碱性,洗手液a呈酸性,洗手液d和a混合时,如果洗手液a中的酸
性物质和洗手液d中的碱性物质恰好完全反应,混合液的pH可能等于7,如果洗手液a中的酸性物质剩余
则混合液的pH就小于7,如果洗手液d中的碱性物质剩余则混合液的pH就大于7,选项D正确。
故选A。
5. 含硫元素的同类物质中硫元素的化合价可能不同,不同类物质中硫元素的化合价可能相同,如表所示。
下列判断正确的是
单质 氧化物 酸 x
0 a 一 一 一
+4 一 b d NaSO 等
2 3
+6 一 c e f
A. X表示碱
B. 物质a在空气中燃烧会发出明亮的蓝紫色火焰
C. 物质b是二氧化硫,它是空气污染物之一
D. 物质d和NaOH溶液发生中和反应生成NaSO 和HO
2 4 2
【答案】C
【解析】
【分析】
【详解】A、从表中可知,NaSO 属于类别X,NaSO 是由金属离子和酸根离子构成的,属于盐,因此X
2 3 2 3
表示盐,选项A不正确;
B、因为物质a中硫元素化合价为0,所以a是硫单质,硫在空气中燃烧发出微弱的淡蓝色火焰,在氧气中
燃烧发出明亮的蓝紫色火焰,选项B不正确;
C、物质b中硫显+4价,属于氧化物,根据化合物中元素化合价代数和为0,该氧化物的化学式是SO ,名
2
称是二氧化硫,二氧化硫溶于水会形成酸雨,它是空气污染物之一,选项C正确;的
D、物质d属于酸,硫元素化合价为+4,化学式是HSO ,中和反应中各元素 化合价不变,因此HSO 和
2 3 2 3
NaOH溶液发生中和反应生成NaSO 和HO,选项D不正确。故选C。
2 3 2
6. 在5.6g铁粉中,先逐滴加入一定量的Cu(NO ) 溶液,充分反应后再逐滴加入AgNO 溶液,剩余固体质
3 2 3
量与所加溶液总质量的关系如图所示。下列说法正确的是
A. 所加溶液质量为Mg时,生成Cu的质量为mg
1 1
B. bc段发生的是Cu和AgNO 溶液的反应
3
C. m 的值为21.6
3
D. e点溶液中不含Cu(NO )
3 2
【答案】C
【解析】
【分析】首先,ab段,铁粉与硝酸铜发生置换反应,M 点时,硝酸铜被完全消耗,之后bc段铁粉与硝酸
1
银发生置换反应,直到M 点时铁粉消耗完毕,然后cd段之前生成的铜与硝酸银发生置换反应,直至M 点
2 3
时,铜被完全消耗;
【详解】A、设有质量为x的铁粉与硝酸铜反应,并生成质量为y的铜,
解方程组得y=8(m-5.6)g,不符合题意;
1
B、bc段是铁粉与硝酸银发生置换反应,不符合题意;
C、M 点时铁粉被完全消耗,沉淀完全是Ag,整体反应过程相当于铁粉与硝酸银发生置换反应,设生成
3
Ag的质量为x,则有:解得x=21.6g,符合题意;
D、cd段之前生成的铜与硝酸银发生置换反应生成了银单质和硝酸铜溶液,后面在滴加硝酸银也不会与硝
酸铜反应,因此e点含有硝酸铜存在,不符合题意。
。
故选C
【点睛】bc的斜率大于cd的斜率,而相对原子质量是Ag>Cu>Fe,在结合题干和所学知识,可以得出b点
的转折是因为硝酸铜被完全消耗,而不是铁粉被完全消耗。
二、填空题
7. 2021年5月10日,成都市某小区电梯内发生一起电瓶车自燃事故。
(1)电瓶车自燃的原因很多,常见的是由于电源短路,形成大电流并产生大量的热。这一过程中,化学
能转化为电能,电能再转化为______能。
(2)针对上述电梯内电瓶车自燃隐患,宁波市未雨绸缪,早就采取了相应的措施,其中“阻车感应系
统”已在多个小区推行。如图所示是某阻车感应系统在电梯轿厢内的信息传递示意图,一旦电瓶车进入电
梯,就会被摄像头检测到,语音告警器将进行语音提示,同时电梯门不会关闭。这一信息传递过程与反射
弧类似,图中的______(填序号)类似于反射弧中的感受器。
(3)电动汽车一般由电池包供电。若电池包意外进水,可能引发电动汽车自燃,其机理如图:
这里的可燃性气体是______。
【答案】 ①. 内 ②. ① ③. 氢气(H)
2【解析】
【分析】
【详解】(1)电瓶车电源短路时,化学能转化为电能,形成大电流。大电流导致电源线路产生大量的热,
电能再转化为内能。
(2)阻车感应系统中的信息传递过程与反射弧类似,系统中电瓶车识别预警摄像头的作用是检测是否有
电瓶车进入电梯,相当于反射弧中接受信息的感受器。故填:①。
(3)水电解生成氢气和氧气,氢气具有可燃性,故引发电动汽车自燃的可燃性气体是氢气(H)。
2
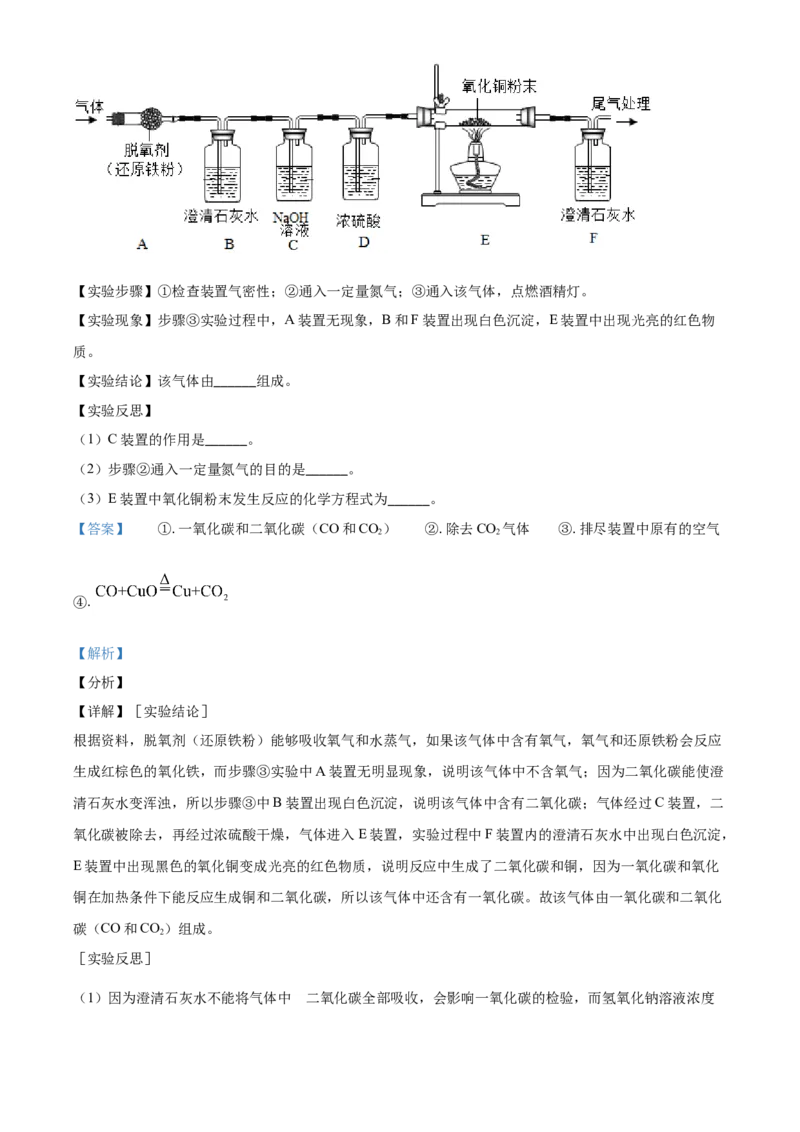
8. 有一包白色粉末,可能由BaCl 、NaOH、NaCO、NaSO 中的一种或几种组成。为确定其成分,某兴趣
2 2 3 2 4
小组做了如图所示实验。
则:(1)无色溶液A中一定含有的溶质是______。
(2)白色粉末的成分是______。
【答案】 ①. 氯化钠(NaC1) ②. 氯化钡和碳酸钠(BaCl 和NaCO)
2 2 3
【解析】
【分析】白色粉末加水生成白色沉淀,那么一定有氯化钡,碳酸钠和硫酸钠至少有一种没因为氯化钡和碳
酸钠可以生成碳酸钡沉淀和氯化钠,氯化钡和硫酸钠生成硫酸钡沉淀和氯化钠,硫酸钡沉淀不溶于酸,沉
淀加酸溶解说明白色粉末一定有碳酸钠和氯化钡,一定没有硫酸钠,无色溶液A,pH=7,说明溶液一定没
有氢氧化钠白色粉末一定没有氢氧化钠,故白色粉末一定有碳酸钠和氯化钡一定没有氢氧化钠和硫酸钠。
【详解】(1)白色粉末一定有碳酸钠和氯化钡一定没有氢氧化钠和硫酸钠,碳酸钠和氯化钡生成碳酸钡
沉淀和氯化钠,无色溶液A中一定有氯化钠,故填:氯化钠。
(2)由分析可知,白色粉末的成分氯化钡和碳酸钠,故填:氯化钡和碳酸钠。
三、实验探究题
9. 有一瓶气体,可能由O、CO、CO 中的一种或几种组成。为确定其组成,在老师的指导下,实验小组对
2 2
该瓶气体进行了如下探究:
【查阅资料】脱氧剂(还原铁粉)能够吸收氧气和水蒸气。
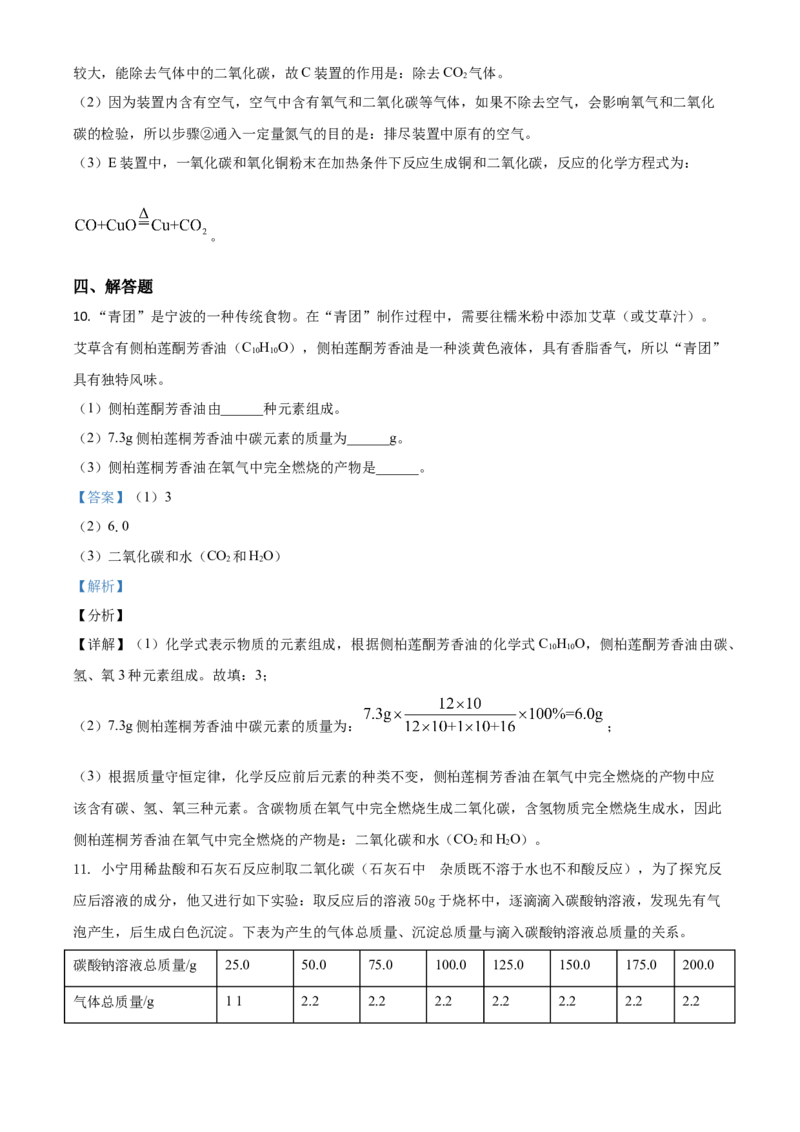
【实验设计】用如图所示的装置进行实验(已略去夹持装置)。【实验步骤】①检查装置气密性;②通入一定量氮气;③通入该气体,点燃酒精灯。
【实验现象】步骤③实验过程中,A装置无现象,B和F装置出现白色沉淀,E装置中出现光亮的红色物
质。
【实验结论】该气体由______组成。
【实验反思】
(1)C装置的作用是______。
(2)步骤②通入一定量氮气的目的是______。
(3)E装置中氧化铜粉末发生反应的化学方程式为______。
【答案】 ①. 一氧化碳和二氧化碳(CO和CO) ②. 除去CO 气体 ③. 排尽装置中原有的空气
2 2
④.
【解析】
【分析】
【详解】[实验结论]
根据资料,脱氧剂(还原铁粉)能够吸收氧气和水蒸气,如果该气体中含有氧气,氧气和还原铁粉会反应
生成红棕色的氧化铁,而步骤③实验中A装置无明显现象,说明该气体中不含氧气;因为二氧化碳能使澄
清石灰水变浑浊,所以步骤③中B装置出现白色沉淀,说明该气体中含有二氧化碳;气体经过C装置,二
氧化碳被除去,再经过浓硫酸干燥,气体进入E装置,实验过程中F装置内的澄清石灰水中出现白色沉淀,
E装置中出现黑色的氧化铜变成光亮的红色物质,说明反应中生成了二氧化碳和铜,因为一氧化碳和氧化
铜在加热条件下能反应生成铜和二氧化碳,所以该气体中还含有一氧化碳。故该气体由一氧化碳和二氧化
碳(CO和CO)组成。
2
[实验反思]
的
(1)因为澄清石灰水不能将气体中 二氧化碳全部吸收,会影响一氧化碳的检验,而氢氧化钠溶液浓度较大,能除去气体中的二氧化碳,故C装置的作用是:除去CO 气体。
2
(2)因为装置内含有空气,空气中含有氧气和二氧化碳等气体,如果不除去空气,会影响氧气和二氧化
碳的检验,所以步骤②通入一定量氮气的目的是:排尽装置中原有的空气。
(3)E装置中,一氧化碳和氧化铜粉末在加热条件下反应生成铜和二氧化碳,反应的化学方程式为:
。
四、解答题
10. “青团”是宁波的一种传统食物。在“青团”制作过程中,需要往糯米粉中添加艾草(或艾草汁)。
艾草含有侧柏莲酮芳香油(C H O),侧柏莲酮芳香油是一种淡黄色液体,具有香脂香气,所以“青团”
10 10
具有独特风味。
(1)侧柏莲酮芳香油由______种元素组成。
(2)7.3g侧柏莲桐芳香油中碳元素的质量为______g。
(3)侧柏莲桐芳香油在氧气中完全燃烧的产物是______。
【答案】(1)3
(2)6.0
(3)二氧化碳和水(CO 和HO)
2 2
【解析】
【分析】
【详解】(1)化学式表示物质的元素组成,根据侧柏莲酮芳香油的化学式C H O,侧柏莲酮芳香油由碳、
10 10
氢、氧3种元素组成。故填:3;
(2)7.3g侧柏莲桐芳香油中碳元素的质量为: ;
(3)根据质量守恒定律,化学反应前后元素的种类不变,侧柏莲桐芳香油在氧气中完全燃烧的产物中应
该含有碳、氢、氧三种元素。含碳物质在氧气中完全燃烧生成二氧化碳,含氢物质完全燃烧生成水,因此
侧柏莲桐芳香油在氧气中完全燃烧的产物是:二氧化碳和水(CO 和HO)。
2 2
11. 小宁用稀盐酸和石灰石反应制取二氧化碳(石灰石中 的杂质既不溶于水也不和酸反应),为了探究反
应后溶液的成分,他又进行如下实验:取反应后的溶液50g于烧杯中,逐滴滴入碳酸钠溶液,发现先有气
泡产生,后生成白色沉淀。下表为产生的气体总质量、沉淀总质量与滴入碳酸钠溶液总质量的关系。
碳酸钠溶液总质量/g 25.0 50.0 75.0 100.0 125.0 150.0 175.0 200.0
.
气体总质量/g 11 2.2 2.2 2.2 2.2 2.2 2.2 2.2沉淀总质量/g 0 0 2.5 5.0 m n 9.0 9.0
(1)表中n=______。
(2)所取的反应后50g溶液中溶质是______。
(3)所用碳酸钠溶液中溶质的质量分数是多少?
【答案】(1)9.0
(2)氯化钙和氯化氢CaCl 和HCl
2
(3)解:设所用碳酸钠溶液中溶质的质量分数为x
答:所用碳酸钠溶液中溶质的质量分数是10.6%。
【解析】
【分析】
【详解】(1)当碳酸钠溶液的总质量为50g时,沉淀质量为0g,为75g时,沉淀质量为2.5g,为100g时,
沉淀质量为5.0g,则125g时,沉淀质量m=7.5g,之后在增加至150g时,沉淀质量应为10g,观察碳酸钠
溶液为175g、200g时,沉淀质量保持9.0g,可知沉淀最大质量为9.0g,所以n=9.0g;
(2)盐酸与石灰水反应,溶质肯定有氯化钙存在,而当加入25g碳酸钠溶液时,有气体产生,这说明盐酸
过量,即此时反应液还有盐酸存在,所以所取的反应后50g溶液中溶质是氯化钙和氯化氢(CaCl 和
2
HCl);
(3)首先盐酸与石灰水反应生成氯化钙、水、二氧化碳,之后加入碳酸钠,因为有气体产生,说明之前
的盐酸是加入过量的,因此加入碳酸钠溶液后碳酸钠首先与盐酸反应,等盐酸被完全反应后,碳酸钠在于
氯化钙反应生成碳酸钙沉淀和氯化钠直至氯化钙被完全消耗,当加入碳酸钠溶液50g时,碳酸钠恰好与剩
余的盐酸反应。详见答案。