文档内容
定远育才学校 2025-2026 学年高一(上)12 月月考
化学试题
可能用到的相对原子质量:H-1 C-12 O-16 Na-23 S-32 Cl-35.5 K-39 Ca-40 Fe-56
一、选择题:本题共14小题,每小题3分,共42分.每小题只有一个选项符合题目要求.
1.下列物品所涉及的合金材料属于新型合金的是( )
A B C D
用生铁铸造的下水井 用不锈钢制造的地铁 用储氢合金装配的
用硬铝制造的飞机外壳
盖 列车车体 以H 为燃料的汽车
2
2.1868年,俄国化学家门捷列夫制作出了第一张元素周期表,揭示了化学元素间的内在联系,成
为化学史上的重要里程碑之一、下列有关元素周期表的说法不正确的是( )
A. 迄今人类发现的元素中,金属元素和非金属元素种数相近
B. 元素周期表有7个横行,18个纵行
C. 元素周期表有七个周期,分为短周期和长周期
D. 人们在周期表中金属与非金属的分界处可以找到半导体材料,如硅、锗等
3.宏观辨识与微观探析是化学学科核心素养之一。下列离子方程式书写正确的是( )
A.
氢氧化钡溶液与硫酸铜溶液混合:Ba2++SO2-
===BaSO↓
4 4
B. 石灰乳与CuSO 溶液制波尔多液:2OH-+Cu2+===Cu(OH)↓
4 2
C.
用小苏打治疗胃酸过多:HCO-
+H+===CO↑+HO
3 2 2
D. 钠和水反应:Na+HO===Na++H↑+OH-
2 2
4.化学创造美好生活,下列生产生活用途对应的化学知识说法错误的是( )
选项 生产生活用途 化学知识
月饼的包装袋内加入一小袋 铁粉能与氧气反应,作为脱
A
铁粉 氧剂
B 用Fe O 作涂料 Fe O 是碱性氧化物
2 3 2 3用漂白粉漂白棉、麻、纸张
C Ca(ClO) 具有强氧化性
等 2
小苏打可用作治疗胃酸过多
D 小苏打与酸能发生反应
的药物
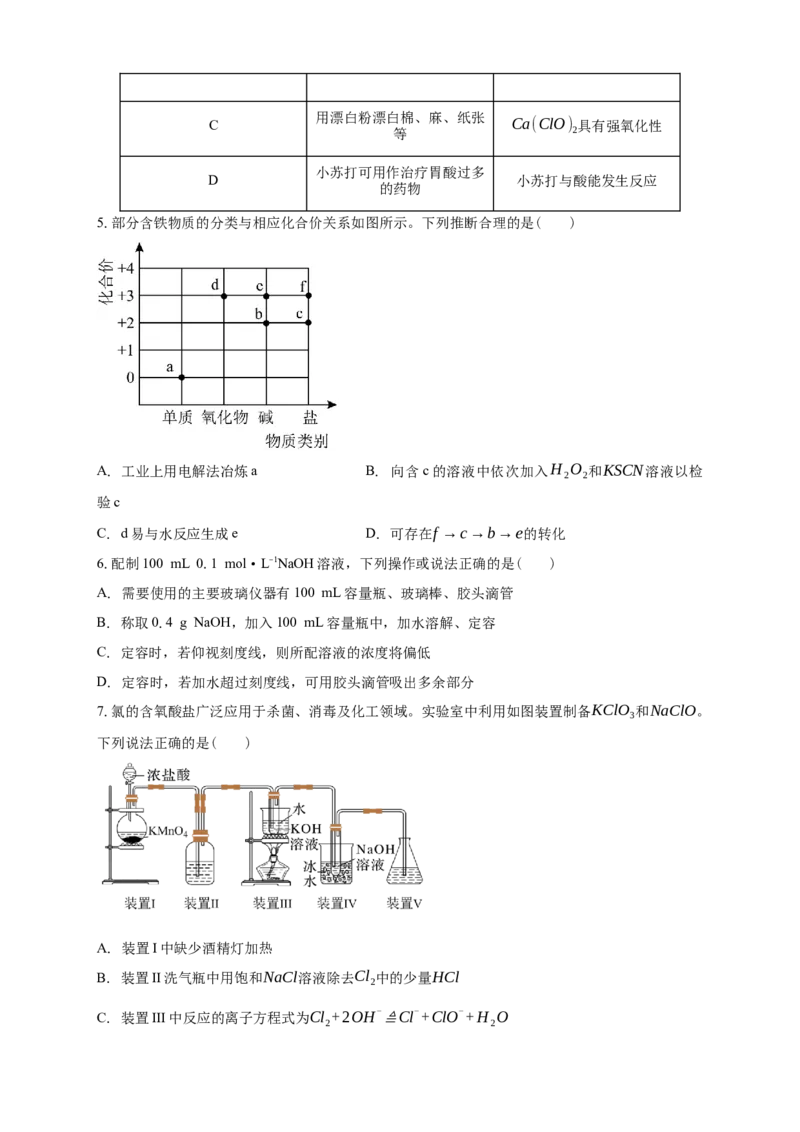
5.部分含铁物质的分类与相应化合价关系如图所示。下列推断合理的是( )
A. 工业上用电解法冶炼a B. 向含c的溶液中依次加入H O 和KSCN溶液以检
2 2
验c
C. d易与水反应生成e D. 可存在f →c→b→e的转化
6.配制100 mL 0.1 mol·L-1NaOH溶液,下列操作或说法正确的是( )
A. 需要使用的主要玻璃仪器有100 mL容量瓶、玻璃棒、胶头滴管
B. 称取0.4 g NaOH,加入100 mL容量瓶中,加水溶解、定容
C. 定容时,若仰视刻度线,则所配溶液的浓度将偏低
D. 定容时,若加水超过刻度线,可用胶头滴管吸出多余部分
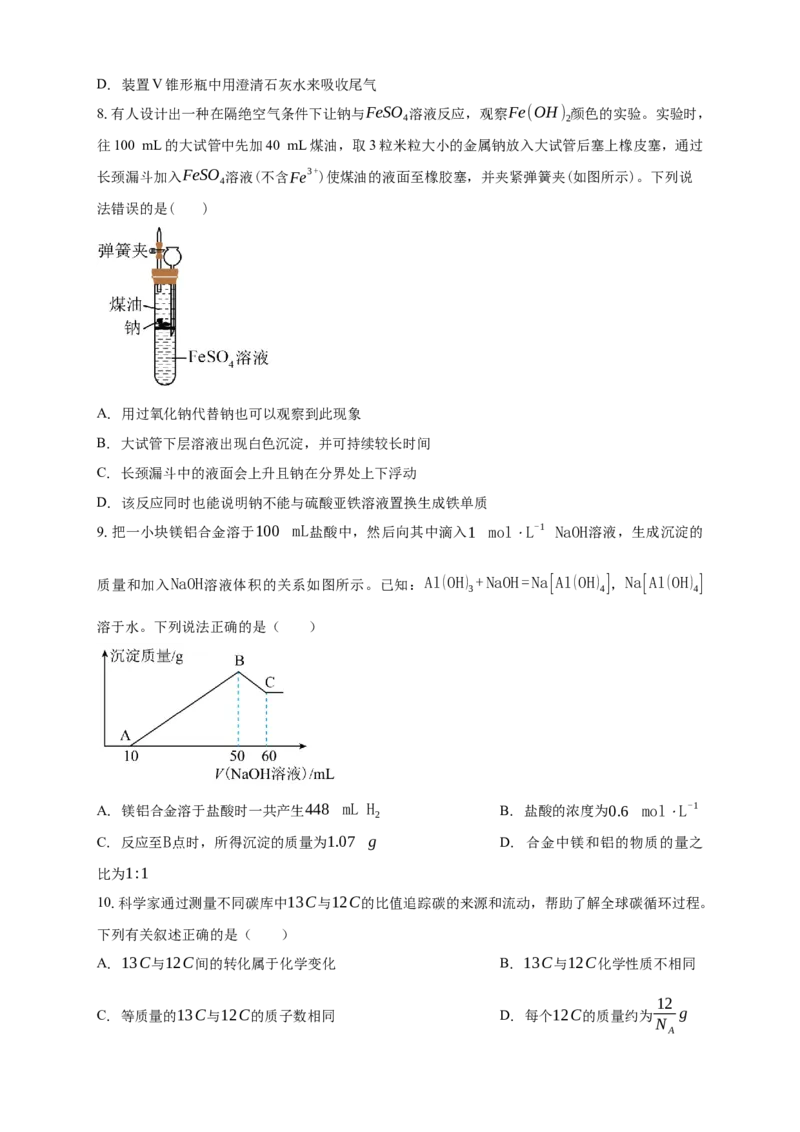
7.氯的含氧酸盐广泛应用于杀菌、消毒及化工领域。实验室中利用如图装置制备KClO 和NaClO。
3
下列说法正确的是( )
A. 装置I中缺少酒精灯加热
B. 装置II洗气瓶中用饱和NaCl溶液除去Cl 中的少量HCl
2
C. 装置III中反应的离子方程式为Cl +2OH- ≜Cl-+ClO-+H O
2 2D. 装置V锥形瓶中用澄清石灰水来吸收尾气
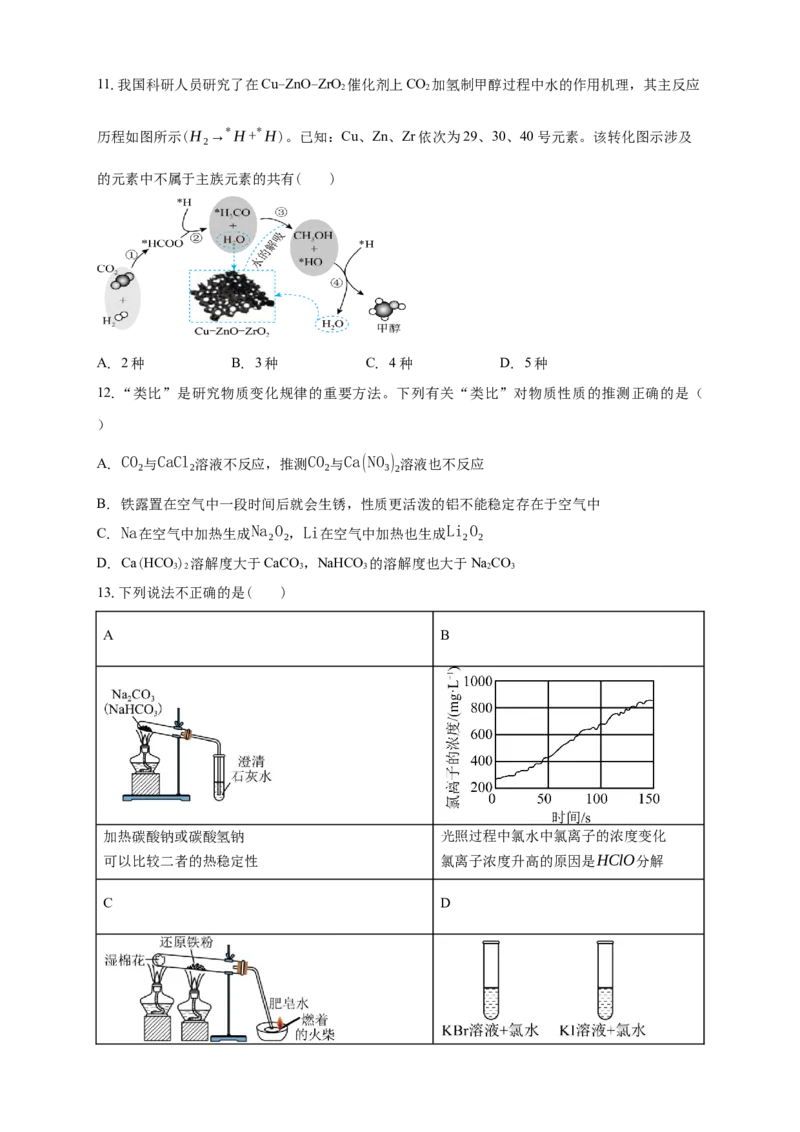
8.有人设计出一种在隔绝空气条件下让钠与FeSO 溶液反应,观察Fe(OH) 颜色的实验。实验时,
4 2
往100 mL的大试管中先加40 mL煤油,取3粒米粒大小的金属钠放入大试管后塞上橡皮塞,通过
长颈漏斗加入FeSO 溶液(不含Fe3+)使煤油的液面至橡胶塞,并夹紧弹簧夹(如图所示)。下列说
4
法错误的是( )
A. 用过氧化钠代替钠也可以观察到此现象
B. 大试管下层溶液出现白色沉淀,并可持续较长时间
C. 长颈漏斗中的液面会上升且钠在分界处上下浮动
D. 该反应同时也能说明钠不能与硫酸亚铁溶液置换生成铁单质
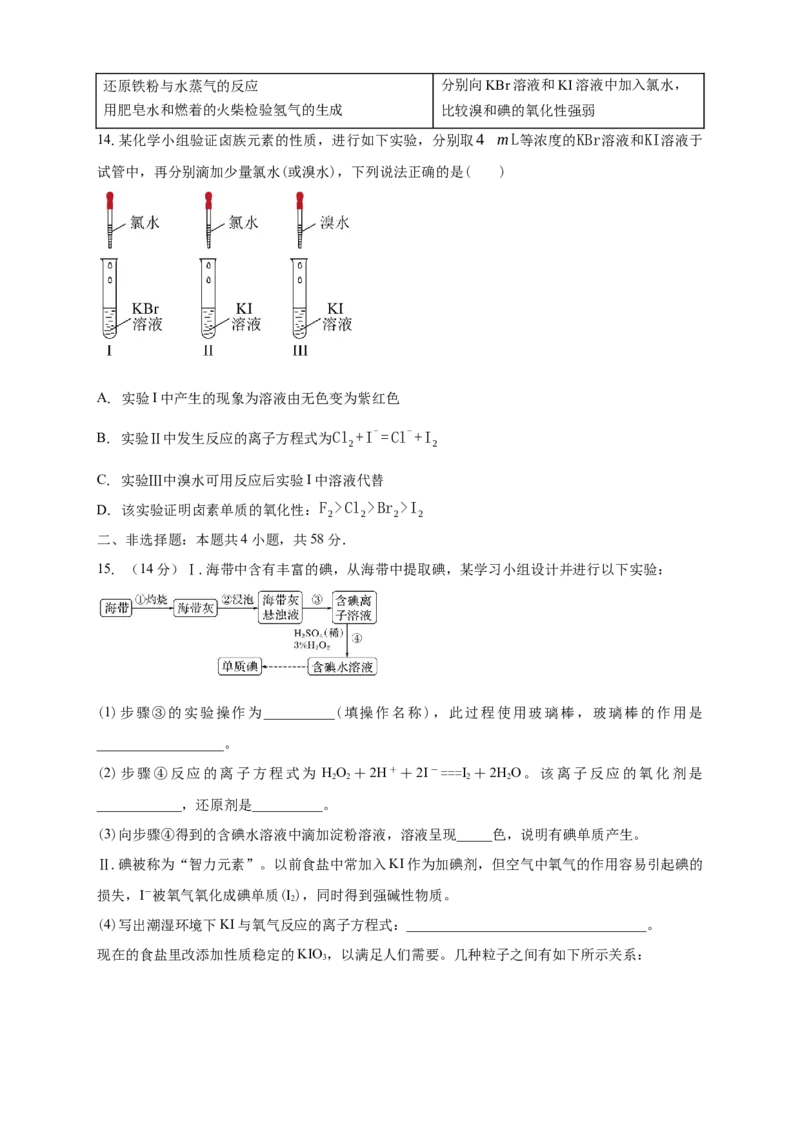
9.把一小块镁铝合金溶于100 mL盐酸中,然后向其中滴入1 mol⋅L-1 NaOH溶液,生成沉淀的
质量和加入NaOH溶液体积的关系如图所示。已知:Al(OH) +NaOH=Na[Al(OH) ],Na[Al(OH) ]
3 4 4
溶于水。下列说法正确的是( )
A. 镁铝合金溶于盐酸时一共产生448 mL H B. 盐酸的浓度为0.6 mol⋅L-1
2
C. 反应至B点时,所得沉淀的质量为1.07 g D. 合金中镁和铝的物质的量之
比为1:1
10.科学家通过测量不同碳库中13C与12C的比值追踪碳的来源和流动,帮助了解全球碳循环过程。
下列有关叙述正确的是( )
A. 13C与12C间的转化属于化学变化 B. 13C与12C化学性质不相同
12
C. 等质量的13C与12C的质子数相同 D. 每个12C的质量约为 g
N
A11.我国科研人员研究了在Cu-ZnO-ZrO 催化剂上CO 加氢制甲醇过程中水的作用机理,其主反应
2 2
历程如图所示(H →*H+*H)。已知:Cu、Zn、Zr依次为29、30、40号元素。该转化图示涉及
2
的元素中不属于主族元素的共有( )
A. 2种 B. 3种 C. 4种 D. 5种
12.“类比”是研究物质变化规律的重要方法。下列有关“类比”对物质性质的推测正确的是(
)
A. CO 与CaCl 溶液不反应,推测CO 与Ca(NO ) 溶液也不反应
2 2 2 3 2
B. 铁露置在空气中一段时间后就会生锈,性质更活泼的铝不能稳定存在于空气中
C. Na在空气中加热生成Na O ,Li在空气中加热也生成Li O
2 2 2 2
D. Ca(HCO ) 溶解度大于CaCO ,NaHCO 的溶解度也大于NaCO
3 2 3 3 2 3
13.下列说法不正确的是( )
A B
加热碳酸钠或碳酸氢钠 光照过程中氯水中氯离子的浓度变化
可以比较二者的热稳定性 氯离子浓度升高的原因是HClO分解
C D还原铁粉与水蒸气的反应 分别向KBr溶液和KI溶液中加入氯水,
用肥皂水和燃着的火柴检验氢气的生成 比较溴和碘的氧化性强弱
14.某化学小组验证卤族元素的性质,进行如下实验,分别取4 mL等浓度的KBr溶液和KI溶液于
试管中,再分别滴加少量氯水(或溴水),下列说法正确的是( )
A. 实验I中产生的现象为溶液由无色变为紫红色
B. 实验Ⅱ中发生反应的离子方程式为Cl +I-=Cl-+I
2 2
C. 实验Ⅲ中溴水可用反应后实验I中溶液代替
D. 该实验证明卤素单质的氧化性:F >Cl >Br >I
2 2 2 2
二、非选择题:本题共4小题,共58分.
15. (14分)Ⅰ.海带中含有丰富的碘,从海带中提取碘,某学习小组设计并进行以下实验:
(1)步骤③的实验操作为__________(填操作名称),此过程使用玻璃棒,玻璃棒的作用是
__________________。
(2)步骤④反应的离子方程式为 HO +2H++2I-===I +2HO。该离子反应的氧化剂是
2 2 2 2
____________,还原剂是__________。
(3)向步骤④得到的含碘水溶液中滴加淀粉溶液,溶液呈现_____色,说明有碘单质产生。
Ⅱ.碘被称为“智力元素”。以前食盐中常加入KI作为加碘剂,但空气中氧气的作用容易引起碘的
损失,I-被氧气氧化成碘单质(I),同时得到强碱性物质。
2
(4)写出潮湿环境下KI与氧气反应的离子方程式:__________________________________。
现在的食盐里改添加性质稳定的KIO ,以满足人们需要。几种粒子之间有如下所示关系:
3(5)四个途径中属于氧化还原反应的是____________(填序号)。
(6)碱性条件下碘酸钾能被氯气氧化为高碘酸钾(KIO ),反应的化学方程式为 Cl +KIO +
4 2 3
2KOH===2KCl+KIO +HO,写出该反应的离子方程式:___________________________。
4 2
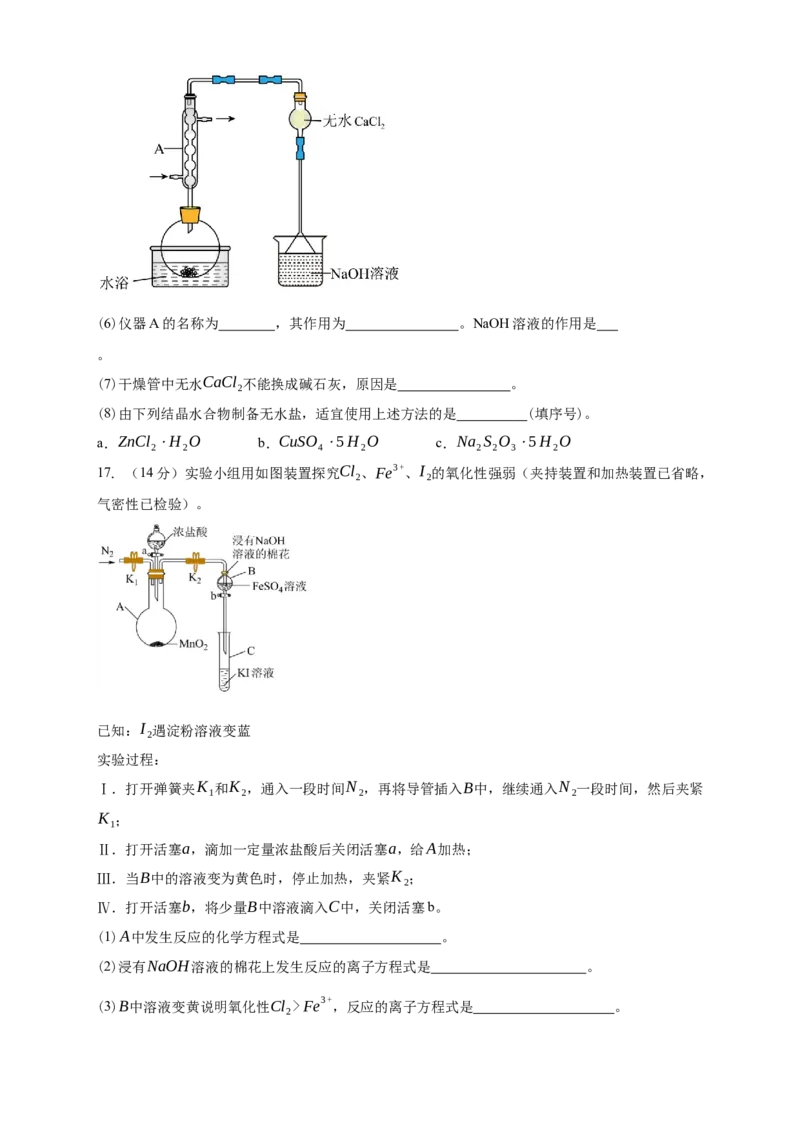
16. (14分)氯化铁是重要的化工原料。针对氯化铁的实验室制备方法,回答下列问题:
Ⅰ.FeCl ⋅6H O的制备
3 2
制备流程图如下:
(1)将废铁屑分批加入稀盐酸中,至盐酸反应完全。判断反应完全的现象为 。含
有少量铜的废铁屑比纯铁屑反应快,原因为
。
(2)操作①所必需的玻璃仪器中,除烧杯外还有 。
(3)检验FeCl 溶液中是否残留Fe2+的试剂是 。
3
(4)为增大FeCl 溶液的浓度,向稀FeCl 溶液中加入纯Fe粉后通入Cl 。此过程中发生的主要反应
3 3 2
的离子方程式为
。
(5)操作②为 。
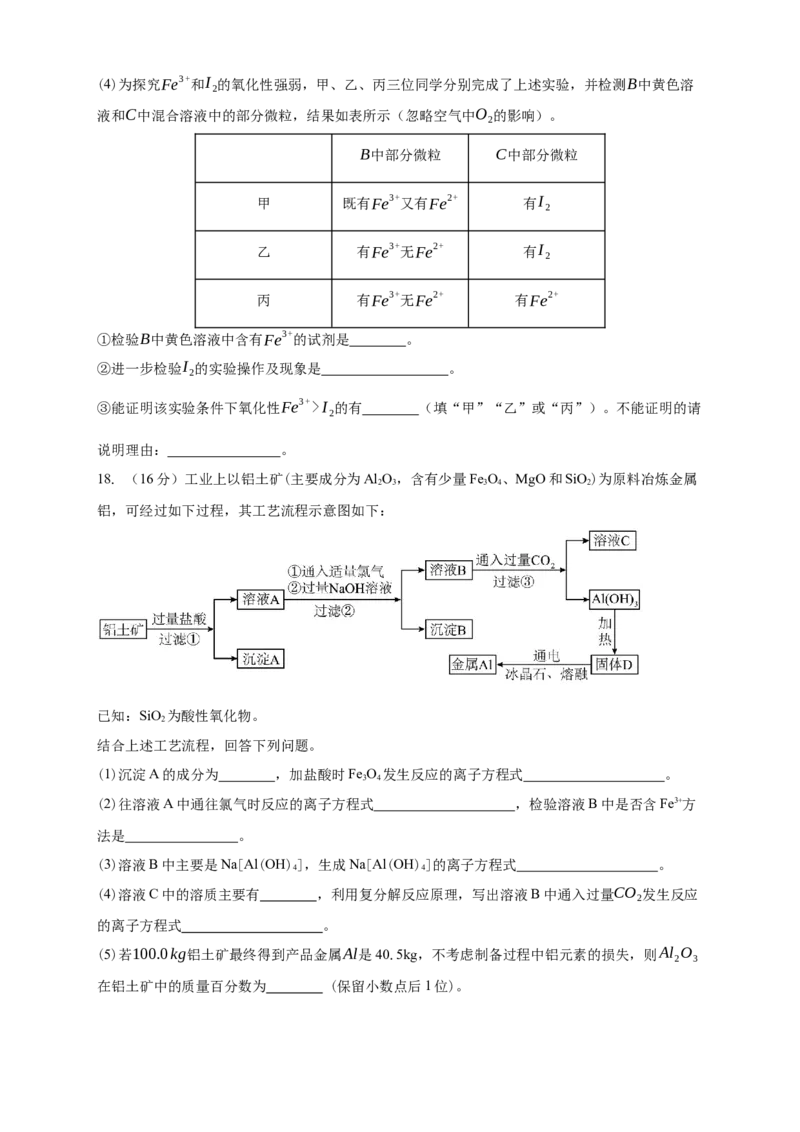
Ⅱ.由FeCl ⋅6H O制备无水FeCl
3 2 3
将FeCl ⋅6H O与液体SOCl 混合并加热,制得无水FeCl 。已知SOCl 沸点为77 ℃,反应方
3 2 2 3 2
Δ
程式为:FeCl 3 ⋅6H 2 O+6SOCl 2¿FeCl +6SO ¿ ↑+12HCl↑,装置如下图所示(夹持和加热装
3 2
¿
置略)。(6)仪器A的名称为 ,其作用为 。NaOH溶液的作用是
。
(7)干燥管中无水CaCl 不能换成碱石灰,原因是 。
2
(8)由下列结晶水合物制备无水盐,适宜使用上述方法的是 (填序号)。
a.ZnCl ⋅H O b.CuSO ⋅5H O c.Na S O ⋅5H O
2 2 4 2 2 2 3 2
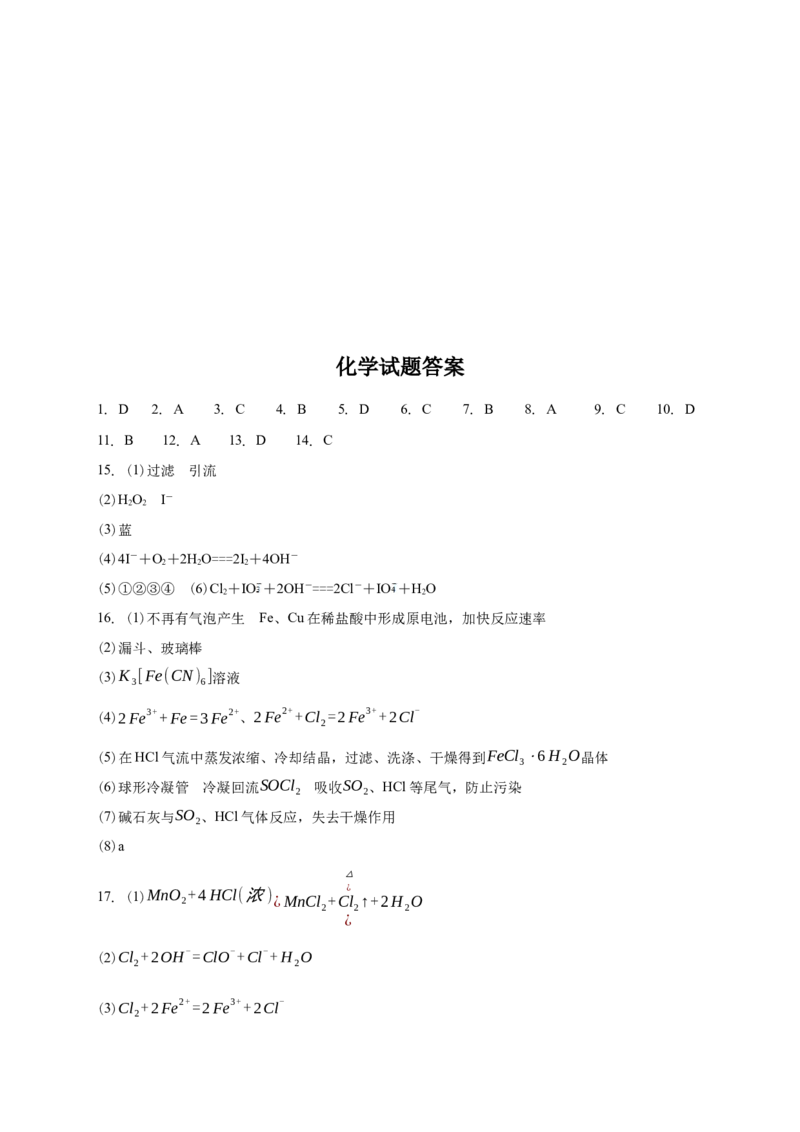
17. (14分)实验小组用如图装置探究Cl 、Fe3+、I 的氧化性强弱(夹持装置和加热装置已省略,
2 2
气密性已检验)。
已知:I 遇淀粉溶液变蓝
2
实验过程:
Ⅰ.打开弹簧夹K 和K ,通入一段时间N ,再将导管插入B中,继续通入N 一段时间,然后夹紧
1 2 2 2
K ;
1
Ⅱ.打开活塞a,滴加一定量浓盐酸后关闭活塞a,给A加热;
Ⅲ.当B中的溶液变为黄色时,停止加热,夹紧K ;
2
Ⅳ.打开活塞b,将少量B中溶液滴入C中,关闭活塞b。
(1)A中发生反应的化学方程式是 。
(2)浸有NaOH溶液的棉花上发生反应的离子方程式是 。
(3)B中溶液变黄说明氧化性Cl >Fe3+ ,反应的离子方程式是 。
2(4)为探究Fe3+和I 的氧化性强弱,甲、乙、丙三位同学分别完成了上述实验,并检测B中黄色溶
2
液和C中混合溶液中的部分微粒,结果如表所示(忽略空气中O 的影响)。
2
B中部分微粒 C中部分微粒
甲 既有Fe3+又有Fe2+ 有I
2
乙 有Fe3+无Fe2+ 有I
2
丙 有Fe3+无Fe2+ 有Fe2+
①检验B中黄色溶液中含有Fe3+的试剂是 。
②进一步检验I 的实验操作及现象是 。
2
③能证明该实验条件下氧化性Fe3+>I
的有 (填“甲”“乙”或“丙”)。不能证明的请
2
说明理由: 。
18. (16分)工业上以铝土矿(主要成分为Al O,含有少量Fe O、MgO和SiO)为原料冶炼金属
2 3 3 4 2
铝,可经过如下过程,其工艺流程示意图如下:
已知:SiO 为酸性氧化物。
2
结合上述工艺流程,回答下列问题。
(1)沉淀A的成分为 ,加盐酸时Fe O 发生反应的离子方程式 。
3 4
(2)往溶液A中通往氯气时反应的离子方程式 ,检验溶液B中是否含Fe3+方
法是 。
(3)溶液B中主要是Na[Al(OH)],生成Na[Al(OH)]的离子方程式 。
4 4
(4)溶液C中的溶质主要有 ,利用复分解反应原理,写出溶液B中通入过量CO 发生反应
2
的离子方程式 。
(5)若100.0kg铝土矿最终得到产品金属Al是40.5kg,不考虑制备过程中铝元素的损失,则Al O
2 3
在铝土矿中的质量百分数为 (保留小数点后1位)。化学试题答案
1. D 2. A 3. C 4. B 5. D 6. C 7. B 8. A 9. C 10. D
11. B 12. A 13. D 14. C
15. (1)过滤 引流
(2)HO I-
2 2
(3)蓝
(4)4I-+O+2HO===2I+4OH-
2 2 2
(5)①②③④ (6)Cl+IO +2OH-===2Cl-+IO +HO
2 2
16. (1)不再有气泡产生 Fe、Cu在稀盐酸中形成原电池,加快反应速率
(2)漏斗、玻璃棒
(3)K [Fe(CN) ]溶液
3 6
(4)2Fe3++Fe=3Fe2+、2Fe2++Cl =2Fe3++2Cl-
2
(5)在HCl气流中蒸发浓缩、冷却结晶,过滤、洗涤、干燥得到FeCl ⋅6H O晶体
3 2
(6)球形冷凝管 冷凝回流SOCl 吸收SO 、HCl等尾气,防止污染
2 2
(7)碱石灰与SO 、HCl气体反应,失去干燥作用
2
(8)a
△
17. (1)MnO 2 +4HCl(浓) ¿MnCl +C ¿ l ↑+2H O
2 2 2
¿
(2)Cl +2OH-=ClO-+Cl-+H O
2 2
(3)Cl +2Fe2+=2Fe3++2Cl-
2(4)KSCN溶液 取少量C中混合溶液于试管中,滴加淀粉溶液,溶液变蓝 甲、丙 乙中B溶液
不含Fe2+,则B溶液可能溶有过量的Cl ,Cl 和Fe3+均能将I-氧化为I ,C中有I 生成不能证明氧
2 2 2 2
化性Fe3+>I
2
18. (1)SiO Fe O+8H+===Fe2++2Fe3++4HO
2 3 4 2
(2)2Fe2++Cl===2Fe3++2Cl- 取少量B溶液,滴加KSCN溶液,若溶液不变红色,则无Fe3+
2
(3)Al(OH)+OH-===[Al(OH)]-或Al3++4OH-===[Al(OH)
]
-
3 4 4
(4)NaHCO
[Al(OH)]-+CO===Al(OH)↓+HCO-
3 4 2 3 3
(5)76.5%